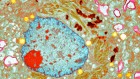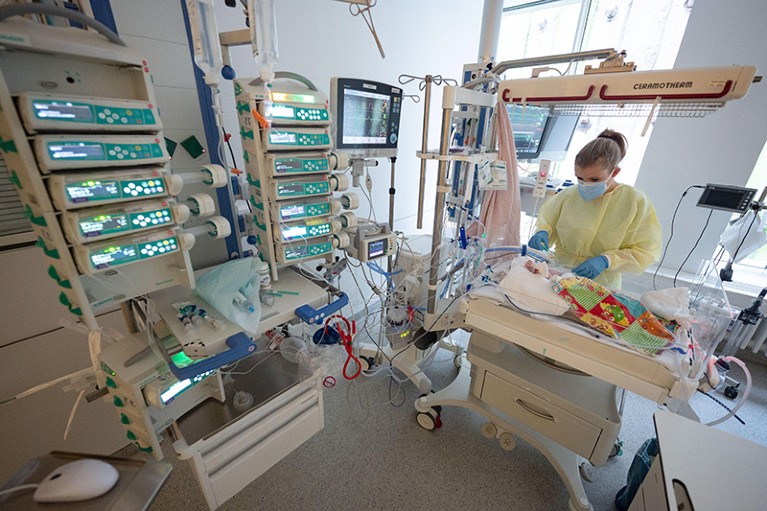
一个护士照顾一个孩子感染RSV的奥尔加医院的重症监护室斯图加特,德国。信贷:供品Murat / dpa /学生
在过去的几个月里,呼吸道合胞体病毒(RSV)已经发送5岁以下的儿童医院以惊人的速度在美国和欧洲。作为儿科单元填充能力之外,和医生面对一个的tripledemic RSV,流感和COVID-19,一些一直在打电话要宣布进入紧急状态。
为什么喉炎的飙升——科学家们有多担心?
RSV,煽动起肺部的最小的航空公司,是唯一的三个呼吸系统疾病尚未有任何批准的疫苗——但这可能很快就会改变。上周,辉瑞制药公司宣布美国食品和药物管理局(FDA)已同意审查RSV疫苗,是管理成人60岁以上的老人,作为一个优先级。如果得到批准——可能就会发生——这可能是第一个批准为RSV疫苗。同样的疫苗也显示出积极的结果在临床试验对RSV在怀孕的人,和辉瑞说它将寻求批准这一组由今年年底。
自然回头看着RSV疫苗出现了,和之前对他们是如何改变公共卫生环境。
RSV几十年来一直是一个问题。现在为什么疫苗只新兴吗?
努力开发一个RSV疫苗后被大幅倒退一个特别引人注目的失败在1960年代。研究人员已经开发了一个包含RSV疫苗微粒的化学灭活病毒无法复制。但当他们测试了在婴儿在临床试验中,它以悲剧告终:两名婴儿死亡。起初,婴儿容忍疫苗,杰森McLellan表示结构在奥斯汀的得克萨斯大学的生物学家。但在接下来的感冒和流感季节,80%的孩子挨了一枪,然后随后被RSV成为他们生病住院1。相比之下,只有5%的儿童接受了安慰剂,然后抓住RSV最终在医院。
故障停止努力开发一个RSV疫苗,作为科学家致力于理解发生了什么事。
研究人员如何克服这种失败?
而不是继续试图让疫苗灭活病毒,研究人员尝试蛋白质疫苗病毒的一个单独的组件,如表面蛋白,用于触发保护性免疫反应。重大突破是当科学家,包括McLellan特征不同构象的蛋白质F, RSV的表面上发现的一个分子。蛋白F有助于汇集病毒和宿主细胞的膜,所以,该病毒可以感染细胞。
流感和感冒卷土重来——为什么是现在?
蛋白F以两种形式存在:postfusion形式,这是高度稳定的,一种十二,不是。蛋白质需要在十二形式感染,病毒和宿主细胞聚在一起时,第二种形式一旦感染和转换。
十二F是“一个非常不稳定的蛋白质”,但“这就是完全活跃,引发最强大的免疫反应”,因此需要一个有效的疫苗,佩德罗毛孢子菌病说,休斯顿贝勒医学院的病毒学家,德州的研究侧重于减少婴儿呼吸道病毒引起的疾病负担。
McLellan特征和一些合作者最终十二的结构形式,然后研究出如何稳定2。这使疫苗研发,以及潜在的免疫抗体疗法打开大门。许多公司现在有RSV疫苗,辉瑞和葛兰素史克的版本最接近中国监管机构的批准。
这些疫苗会成功吗?
辉瑞公司,总部在纽约,宣布成功的第三阶段从两个试验结果在今年早些时候的候选疫苗。在一个试验中,该公司给怀孕的人提高疫苗抗体总数,这个想法是,这些抗体将会转移到他们的婴儿。
辉瑞在一份新闻稿中报道说,这一策略对严重病例的疗效81.8% RSV的婴儿在出生后的90天。

医疗设施如马塞诸斯州大学的纪念医疗中心在伍斯特操作能力高于正常因为tripledemic的疾病传播。信贷:苏珊娜他通过盖蒂/波士顿环球报
在美国,RSV通常发送平均58000 - 80000 5岁以下儿童每年去医院,据美国疾病控制和预防中心(CDC)。婴儿最有可能住院治疗RSV大约两个半月的年龄,当他们的肺还在发育,McLellan说。婴幼儿感染RSV的主要风险”有很大的关系有更小的航空公司”,海伦Chu说,西雅图华盛顿大学的传染病专家。
RSV也可以是危险的65岁以上的成年人,导致60000 - 120000年平均住院每年在美国,美国疾病控制和预防中心说。在其他辉瑞的三期临床试验,这种疫苗被报道有85.7%的功效在预防严重疾病在60岁以上的成年人。葛兰素史克公司的全球总部在伦敦,也报道成功的第三阶段测试结果对RSV疫苗在60岁以上成人,有94.1%在预防严重疾病的功效。
辉瑞、葛兰素史克将角逐批准;葛兰素史克公司上个月宣布FDA将疫苗优先审查。与辉瑞公司,最早可能在可能批准。
但疫苗是“不会让RSV消失”,警告巴尼·格雷厄姆,病毒学家和免疫学家Morehouse医学院在亚特兰大,乔治亚州,谁与McLellan十二f .疫苗将会做什么,他补充说,保护最弱势群体,包括非常年轻和老年人。
与此同时,其他治疗方法能遏制RSV吗?
在本月之前,只有一个应对RSV的药物。单克隆抗体palivizumab,最初由制药公司落实在盖瑟斯堡,马里兰州,可以作为预防性管理每月减少婴幼儿疾病的严重程度。考虑到成本,必要的频率必须注入剂量和事实,医生只给palivizumab高危婴儿和儿童。另一个单克隆抗体,称为nirsevimab和由公司阿斯利康在剑桥,英国,和赛诺菲安万特在巴黎,在今年早些时候完成了三期试验成功3。其优点是一剂提供了5个月的婴儿预防严重疾病。欧盟委员会(European Commission)上个月批准它,FDA正在审查。
许多工具可以很快可以帮助对抗疾病困扰父母几十年,格雷厄姆说。“这是一个重大突破。”

 流感在加拿大引起儿童住院大幅飙升
流感在加拿大引起儿童住院大幅飙升 为什么喉炎的飙升——科学家们有多担心?
为什么喉炎的飙升——科学家们有多担心? 感冒和流感季节COVID-19是如何改变
感冒和流感季节COVID-19是如何改变