文摘
最初的殖民新生儿肠道受到交付模式,喂养,母亲的微生物群,一系列环境因素。出生后,婴儿的微生物群的构成发生了一系列重大变化特别是在生命的最初几周和几个月的最终发展成一个更稳定和多样化的成人人口的童年。肠道失调是与疾病相关的肠道菌群的改变,似乎是常见的新生儿。肠道失调的后果是不确定的,但强烈的因果关系间接证据和有限的证据表明,生态失调在生命早期会影响婴儿的健康严重,以及对疾病的易感性。
介绍
肠道菌群由数万亿活微生物与宿主共存。细菌是最丰富的殖民者,但古细菌,真菌和病毒在健康个体也丰富。三合一的微生物群之间的相互作用的复杂性,环境因素和宿主的证据表明,这个庞大的微生物群落(1)争夺并生成营养,(2)影响和塑造了宿主先天和适应性系统,和(3)防止触发急性和慢性疾病。越来越多的证据进一步表明,肠道菌群影响粘液生产、成熟和连续性的上皮黏膜下层单层分离肠道流明,炎症反应的重要品质,和生理稳态(1]。肠道微生物之间的相互作用和发展中免疫系统似乎特别重要在生命早期(2]。
范例,肠道微生物容易适应限制类别如共生体或共生生物(包括主机和微生物从中受益共存),共生体(微生物的好处和主机是安然无恙),和病原体(细菌福利和主机受到伤害)的理解是合作的因素允许不致病的微生物殖民和主机共享受益本质类似于毒力因素驱动致病性(3,4]。因此,许多肠道微生物更精确地描述为pathobionts,造成伤害的能力在某些情况下,容忍别人的(甚至是有益的)。
肠道失调描述改变肠道微生物群与疾病有关。在某些情况下,组分变化和相关的表型变化可以归结于一个小的微生物。疾病的因果关系的这种变化可以通过展示传播性测试模型系统的宿主病表型与微生物群转移(5,6]。在其他情况下,一个协会更为微妙。措施失调通常无法证实因果作用的特定微生物模式在一个特定的疾病(7,8,9]。失调可能是疾病的结果,或者仅仅是重合的,而不是病因。此外,在新生儿反过来也许真的。不立即改变与病理相关可能带来深远的影响在儿童通过microbiome-immune交互。在这里,我们审查的重要性在新生儿肠道菌群发展和改变的后果在新生儿的这个复杂的微生物群落。
失调和发展
损伤器官形态发生过程中会有后果的器官恢复和发展,以及下游系统的函数依赖,器官。形成期的微生物包括生命的最初3年与年龄相关性变化主要类群受环境、饮食、药物(10,11,12]。肠道免疫系统的发展与影响孩子的微生物和微生物代谢的微生物的结构组件和产品(12,13,14]。早期的重要性在动物模型演示了微生物破坏早期生命窗口导致特异性免疫/健康改变不了触发中断时在一个成熟的年龄15,16]。
动物模型有助于分析肠道菌群发展的影响,尤其是实验动物在无菌条件下长大。微生物群的影响开始在子宫内可以观察到后代的无菌坝高代谢综合征的风险,即使在传统条件下(17]。老鼠在无菌条件贫困增长,减少重量和小肠粘膜表面区域,减少肠道蠕动,增加粘液,体积不断增加的盲肠和轻度腹泻18]。无菌鼠也证明改变神经发育缺陷的应力响应率,焦虑行为,社交能力,和认知19]。显然这种方法是完全的优雅与无菌动物的殖民与单一的微生物或特定的微生物群落(无菌的或“已知的微生物群”)和分析产生的表型。比较无菌,无菌的,和野生动物展示肠道菌群在肠道发展的重要性20.)和肠道失调的一个重要的因果作用在严重急性营养不良的21,肥胖22),非酒精性肝病23),阿尔茨海默病(24],colitis-associated结直肠癌(25),等等。
新生儿患病率肠道失调
解决问题的常见肠道失调发生在生命早期假设的理解婴儿的正常微生物群不幸的是缺乏。以下假设似乎合理的:(1)微生物群落动态和由宿主因素,环境因素,和有效养分,(2)肠道菌群的组成我们的祖先的新生儿是受到母亲的阴道,粪便,口交,和牛奶微生物群,通过营养物质可在母乳,通过水平传播家庭和小型社区中共享食物,餐具和个人卫生设施,和(3)引入现代卫生实践、抗生素、防腐剂,和其他药物,现代饮食等所谓的“西方”高脂肪、高糖饮食,和婴儿配方奶粉已经从根本上改变了人类的肠道微生物群与我们的祖先。
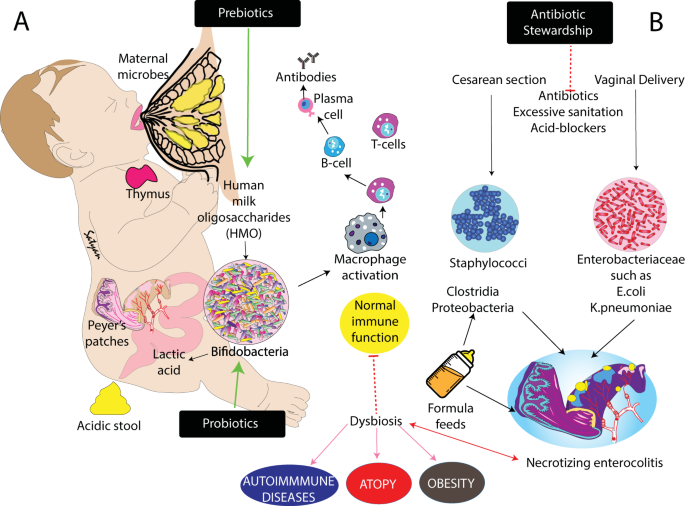
最早试图描述母乳喂养的婴儿的粪便微生物群被蒂塞尔(发表26和洛根27]。都描述了一个优势的革兰氏阳性、厌氧、y形的,不动的细菌在健康婴儿。这些细菌被认为是一个单一的物种,乳酸菌外直到1960年代,当多个物种被分组在一个属双歧杆菌属(家庭Bifidobacteriaceae、订单Bifidobacteriales门放线菌)。双歧杆菌属种选择性发酵碳水化合物;一些生产所需的糖苷酶消化植物低聚糖(例如,双歧杆菌adolescentis,b . longum无性系种群longum)和其他必要的糖苷酶来消化牛奶的低聚糖(例如,b . longum无性系种群对象的,b . bifidum和一些菌株的b .谕令)。这些差异在细菌基因组中编码和已确认的生化和分子特征的细菌糖苷酶和运输蛋白(28,29日,30.]。微生物能够消费牛奶组件有一个竞争优势在婴儿肠道。鉴于母乳充足的低聚糖,细菌的种类相对较少的消耗这些聚糖,如提到的双歧杆菌属属,可以繁殖及其丰度”花朵。“观察母亲的母乳寡糖产生大量巨大的结构多样性,不作为直接婴儿营养来源,考虑到他们缺乏必要的糖苷酶,说明要么共同进化的人类牛奶和有限数量的细菌物种几百万年前,还是一个非常聪明的设计,或者其中的一些。最终的结果是,母亲是塑造她的婴儿通过选择性的微生物群营养和抗菌素在她的牛奶(图。1)。
然而,这种古老的产妇对婴儿的影响机制通过母乳微生物群,可能削弱了现代实践。最近14个研究发表在1926年至2017年之间,其中包括超过300健康的母乳喂养的婴儿,记录这段时间的增加粪便pH值从5.0到6.5 (31日]。这pH值的变化是一致的降低Bifidobacteriaceae(产生乳酸,降低粪便pH值)和增加Clostridiaceae肠杆菌科(增加粪便pH值)。
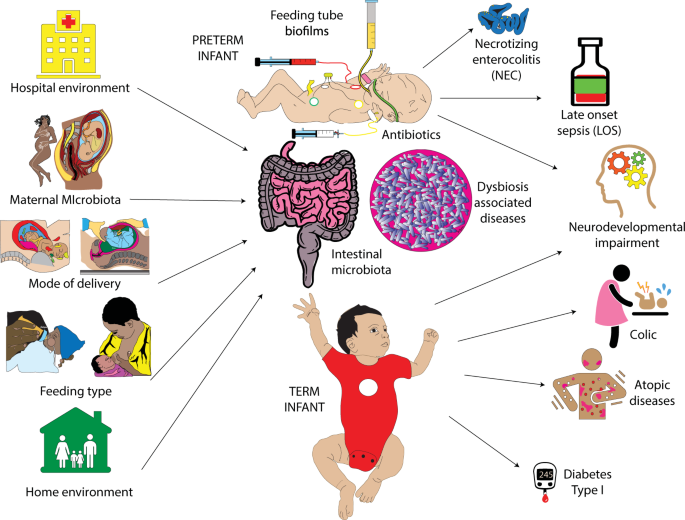
这种变化可以直接的健康后果(无花果。1,2)。例如,肠杆菌科提到(门变形菌门)革兰氏阴性兼性厌氧菌,包括两个物种是众所周知的新生儿学专家:大肠杆菌和肺炎克雷伯菌。毒性提供能动性因素包括鞭毛菌毛,允许对宿主细胞表面,干扰体内平衡和毒素。许多肠杆菌科触发宿主免疫应答通过微生物的识别模式,如脂多糖在细胞壁或鞭毛。大肠杆菌和k .肺炎尤其会导致毁灭性的公开的新生儿疾病。丰富的肠杆菌科被描述为一个生态失调的标志(32]。
健康的足月婴儿的粪便微生物群的研究表明可识别的模式虽然具有高程度的个体变异。现在新兴的广泛模式表明细菌殖民者的第一波影响的交付模式(肠杆菌科,阴道分娩婴儿和Staphylococcaceae通过剖腹产出生的婴儿)和第二波受到喂养类型(Bifidobacteriaceae在母乳喂养的婴儿和人工喂养的宝宝更多元化的人口包括Staphylococcaceae Clostridiaceae, Enterococcaceae, Bifidobacteriaceae,和类杆菌)(33]。在早产婴儿,模式更为复杂与高度的个体变异(再次):最初的殖民扩张与Staphylococcaceae其次是肠杆菌科和Clostrideaceae Bifidobacteriaceae和杆菌典型延迟或缺席34,35]。术语和早产儿,停止母乳喂养和引入补充食品开始稳步增加微生物多样性导致更复杂的微生物群,最终导致稳定社区成人的特点。
从广义上讲,存在低数量的Bifidobacteriaceae和高数量的肠杆菌科和Clostridiaceae可以作为一个合理的起点来定义失调在生命的最初几个月。这种模式是常见的在一些设置,包括早产婴儿,婴儿需要长期住院或抗生素,well-appearing婴儿在某些地理区域dysbiosis-associated疾病的风险增加(36]。微生物群组成“不成熟”是一个术语的延迟的微生物群的发展。它是儿童严重急性营养不良的特征(37),可能是另一个有用的定义失调在婴儿38,39,40]。
新生儿肠道失调的原因
如上所述,在足月婴儿,交付和喂养方式类型(母乳和配方比组合)显著影响婴儿微生物群的组成(41,42]。不同的婴儿微生物群与送货上门和医院交付已报告(43]。母亲的饮食和她牛奶中的微生物(通常类似于孕产妇皮肤和粪便的微生物群)也影响婴儿粪便微生物群虽然一般温和程度(44,45,46]。许多其他因素可以影响微生物群和一些可能造成生态失调。暴露在产时B组链球菌的抗生素预防败血症和/或由于剖腹产非常普遍和影响新生儿肠道菌群(47,48]。除了抗生素(49),其他药物通常为母亲和婴儿,改变肠道菌群包括酸阻断剂(50,51选择性5 -羟色胺再摄取抑制剂,二甲双胍和泻药52,53]。最近的示威活动改变了婴儿与暴露于环境毒素微生物群(54,55,母亲吸烟56),和接近毛茸茸的动物42,57)强调了许多因素影响这个社区。
早产儿是一个独特的人口,从进化的角度来看,“新”有长期住院(具有多个环境因素),经常暴露于抗生素,不成熟的先天和适应性免疫系统。在早产儿,肠道菌群的组成的主要决定因素是post-menstrual年龄和年龄在几周内(34,35),然而,多种其它因素也影响包括产前皮质类固醇、分娩方式,抗生素暴露,喂养类型,喂食管停留时间和生物膜,性别,和压力58,59,60,61年]。表1提出了几个例子婴儿粪便微生物群的改变与围产期暴露(43,47,48,49,56,57,60,62年,63年,64年,65年,66年,67年]。
失调指数
“生态失调指数”被描述为新发病小儿克罗恩病(CD)基于细菌的比例增加患者CD(肠杆菌科、Pasteurellacaea Veillonellaceae, Fusobacteriaceae,奈瑟氏菌科,和Gemellaceae)的细菌减少患者CD (Erysipelotrichales,细菌性的,梭菌属的,和Bifidobacteriaceae) (7,68年]。这与症状严重程度指数诊断有效性和相关但没有预测对治疗的反应。胃肠失调指数随后被描述不同中风的诊断和预后价值(69年),幽门螺杆菌感染(70年]。一个商用GA-map™失调测试(遗传分析,奥斯陆,挪威)确定的偏差程度的微生物群组成一个病人样本与健康的成年人口控制和生成一个失调指数得分与粪便calprotectin(肠道炎症的标志)8]。失调指数升高已经证明了这种产品的成人患者强直性脊柱炎(8),肠易激综合症,炎症性肠病(71年,干燥综合征(72年]。失调指数尚未描述疾病影响这个词或早产婴儿。鉴于上述讨论的微生物群的发展,生态失调指数为新生儿需要合并胎龄和年龄的粪便收集。
新生儿肠道失调的后果
与肠道失调相关疾病过程的列表很长,多样化的(表2提供了一些例子)。对于大多数人来说,肠道失调和dysbiosis-associated疾病之间的因果关系尚未建立,然而,对于一些因果关系和潜在机制。后者的例子包括1型糖尿病(73年,74年哮喘和过敏性疾病/ [75年,76年]。之间的关联研究抗生素暴露在子宫内或围产期和儿童肥胖的疾病和过敏性皮炎的三和弦,哮喘和过敏性鼻炎喜忧参半77年,78年,79年,80年]。在疾病的婴儿,一个引人注目的数据与肠道失调来自NEC的研究,晚发型败血症(LOS)和婴儿绞痛(无花果。2)。
NEC,仔细研究粪便微生物群疾病发作之前显示一个模式在门级的增加变形菌门和减少壁厚菌门和拟杆菌门81年]。更深入,增加肠杆菌科在家庭层面(82年),而克雷伯氏菌在属级报告以及增加fimbriae-expressing细菌(82年]。几项研究已经证明,经验治疗早产的婴儿用抗生素超过4天NEC(后来发展的风险增加83年,84年]。政府相关的抑酸剂早产儿也与大便失调(50和NEC的风险增加85年]。很可能失调住院婴儿是影响微生物在NICU的表面86年,87年),也许可以解释一些医院之间的NEC发生率差异很大。最近仔细分析演示了一个NICU“空间特定的微生物群”,是由婴儿肠道微生物88年]。
在洛杉矶,肠道失调疾病发病机理还不太清楚。最洛杉矶NICU归因于感染涉及皮肤微生物和中央导管。然而,最近的调查洛发现相同的有机体在婴儿的粪便和血液文化与洛杉矶,这表明易位的肠道微生物洛(可能是一个常见的原因89年]。在动物模型中,大量的特定的肠道微生物预防引起败血症,而他们的缺席是与疾病严重度增加有关90年]。在早产儿中,大量的双歧杆菌属似乎是保护物种,或标记的保护,对洛(89年,91年]。
最后,婴儿绞痛是常见的和相关的风险增加的长期学习和行为的挑战[92年]。几项研究已经证明肠道失调与婴儿绞痛,包括与严重性特定类群协会(93年]。
机制
机制的详细讨论肠道失调引发局部和全身性疾病是超出了本文的范围和被别人了94年,95年,96年,97年,98年,99年,One hundred.,101年,102年]。相反,我们将简要地讨论完善的机制和一些有前途的小说提出了详细的机制,然后再考虑益生菌产生的短链脂肪酸的作用和共生的细菌。关键的机械的示威活动,包括(1)肠道通透性的改变肠道微生物(103年),(2)改变肠道微生物的局部和全身炎症(例如,通过toll样受体和相关细胞因子的刺激和变化的T细胞和嗜中性粒细胞反应)(13,104年),(3)改变肠道成熟的肠道微生物及其代谢产物(105年,106年]。最近发现阐明机制影响肠道微生物宿主病易感性,包括(1)变更的肠道微生物的抗原从肠道流明到固有层通过杯状细胞相关的段落107年),(2)早期肠道微生物诱导的红细胞分化regulator-1 (Erdr1)细胞分化和生存的监管机构没有发现老鼠在无菌条件下或在无菌鼠殖民与粪便微生物群控制小鼠断奶,这表明有一个窗口在生命的早期发展的微生物群(直接或通过代谢物)可以诱导Erdr1改变肠道发育和再生修复能力(108年),和(3)刺激肠道微生物的宿主肠嗜铬细胞的细胞生产的5 -羟色胺,肠神经系统的主要神经递质(109年]。
短链脂肪酸(SCFAs,最常见的是乙酸,丙酸,丁酸)是发酵的产物膳食纤维的几种肠道细菌(表3)。SCFAs colonocytes的重要能量来源(32)和调节胰岛素敏感性,葡萄糖和脂质稳态,系统性炎症(110年,111年]。最近的一次大规模的基因型分析,粪便微生物群,成人和粪便短链脂肪酸分析证明因果关系增加粪便丁酸和改善胰岛素反应后口服糖耐量测试和减少粪便丙酸与2型糖尿病的风险增加(112年]。通过诱导肠道糖质新生[SCFAs影响葡萄糖代谢113年),然而,SCFAs在能量代谢的作用似乎更广泛报道SCFAs对食欲调节的影响和肠脑轴(114年]。在老鼠身上,SCFAs孕产妇肠道微生物产生的影响神经分化,小肠和胰腺细胞胚胎的胚胎通过激活G protein-coupled受体(17]。在兔子,盲肠的微生物群在从乳儿过渡到断奶早期改变导致增加产量的丁酸盐影响肠道通透性(105年]。
CD和溃疡性结肠炎患者SCFA-producing细菌数量较低,低水平的粪便SCFAs。机制SCFAs保护宿主免受炎症性肠病包括支持肠上皮细胞增殖、诱导紧密连接蛋白增加屏障功能,抗菌肽的感应,一系列的抗炎作用[115年]。
SCFAs和乳酸产生丰富的母乳时结合微生物可以食用母乳寡糖,等b . longumssp对象的导致减少粪便pH值和抑制的兼性厌氧菌如肠杆菌科116年]。不成熟的肠道可能比成熟的肠道SCFAs的反应是不一样的。虽然SCFAs证明抗炎作用对人类胎儿瀑样和胎鼠肠117年],丁酸似乎触发NEC-like病变无菌lactose-fed鹌鹑(118年),在小猪NEC模型中,包含发酵配方大肠杆菌有高水平的乙酸和丙酸与NEC-like病变(119年]。色氨酸在母乳被肠道微生物代谢,包括b . longumssp对象的indole-3-lactic酸,aryl-hydrocarbon受体结合在不成熟的肠道组织,抑制促炎细胞因子IL8 [120年]。
试图减弱新生儿肠道失调
抗生素的管理工作
在美国,30 - 35%的足月婴儿立即围产期暴露于抗生素,对B组链球菌预防或担忧孕产妇intra-amniotic感染(无花果。1)[121年]。然而,这种方法降低了婴儿死亡率的长期后果产生的肠道失调是不确定的。不幸的是,备受期待的孕产妇接种B组链球菌和关键的大肠杆菌(122年)没有出现迫在眉睫的但可能会导致降低抗生素暴露。减少不必要的抗生素暴露在生命的最初几个月也许有价值减少失调的风险及其相关疾病过程以及降低成本和抗生素耐药细菌的出现(123年]。回顾127年加利福尼亚nicu显示广泛的抗生素使用情况(从2.4到97.1%的patient-days)的中值24%的病人。抗生素的使用有相似率高的nicu记录感染的抗生素使用率较低的nicu [124年]建议减少抗生素管理的机会。同一组的后续研究显示在NICU抗生素使用从2013年到2016年下降22%(减少42960抗生素天)更大的下降在NICU建立抗生素管理计划(125年]。这些和其他的研究表明,进一步的好处可以获得抗生素管理(123年]。
益生元
生命起源以前的聚糖膳食补充剂,提供一个共生的细菌营养底物来刺激经济增长。母乳寡糖,上面所讨论的,是高选择性,只有有限数量的细菌可以利用它们作为的主要营养来源双歧杆菌属和拟杆菌物种)。相比之下,许多其他商业益生元被多种肠道微生物,从而可能刺激共生体和病原体的生长。母乳寡糖是非常宽容的热量,因此对巴氏灭菌(和丰富的捐赠母乳)。虽然母乳的好处与多种生物活性成分,有可能生命起源以前的复杂碳水化合物的影响至少部分负责观察减少NEC与母乳喂养。最近18随机安慰剂对照试验的荟萃分析显示减少败血症和死亡的发生率和住院时间管理生命起源以前的补充剂,但没有区别在NEC的发病率(126年]。
益生菌
益生菌是膳食补充剂含有活的微生物。受益于益生菌的证据管理也许是最引人注目的减少早产儿NEC和死亡。大量的随机安慰剂对照临床试验的益生菌在早产儿。几个荟萃分析这些试验已经证明在NEC明显降低,死亡和/或在早产儿住院时间与益生菌政府(127年,128年]。此外,荟萃分析的观察性队列研究益生菌政府早产儿,NEC显示类似的削减和死亡的临床试验(129年,130年]。最近的一项荟萃分析的随机对照试验的益生菌政府的母亲在怀孕期间减少过敏性湿疹,早产,NEC和死亡的后代(131年]。随机对照试验的荟萃分析在足月婴儿绞痛与益生菌表现出显著降低哭泣时间管理。> 50%的概率减少哭泣时间接近2倍(132年]。欧洲儿科胃肠病学和肝脏病学学会最近发布了一个条件建议益生菌用于早产儿预防NEC (133年]基于毒株特异性网络分析的临床试验(134年]。美国胃肠病协会最近的建议总结了有限的证据成人益生菌管理的好处和利益的令人信服的证据预防早产儿NEC (135年]。风险益生菌包括污染的益生菌产品136年从益生菌微生物)和脓毒症137年]。从益生菌政府看来,伤害对婴儿是一种罕见的并发症,NEC,败血症和死亡是等于或低于婴儿接受益生菌比接受安慰剂或在大多数研究没有益生菌。那些鼓吹对益生菌的常规管理早产儿注意的益生菌生产不足和监管问题仍对菌株的首选益生菌菌株或组合和最佳剂量(138年]。
结论
在过去的二十年里已经有一个虚拟的知识爆炸作用的殖民微生物群在调节宿主生理和维持体内平衡。不利的微生物群的构成的变化,生态失调,在某些情况下会导致明显的疾病,但往往有更多的微妙和阴险的后果。well-appearing术语婴儿在发达国家,肠道失调是常见的,可能是因为转移从母乳喂养,剖腹产,抗生素和其他药物,“西方”的饮食和现代卫生实践。在早产婴儿照顾在现代nicu,肠道失调似乎几乎普遍。婴幼儿肠道失调的后果是不确定的,但强烈的因果关系间接证据和有限的证据表明许多急性和慢性疾病,随着时间的推移越来越多有关肠道失调。早期干预措施,限制或反向孕产妇和婴儿肠道失调包括抗生素管理,增加母乳喂养支持,减少使用预防性抗生素和疫苗开发通知使用益生菌微生物和生命起源以前的聚糖在扭转这些趋势提供承诺。
引用
布莱塞Dominguez-Bello毫克,Godoy-Vitorino F,骑士R,乔丹。微生物在人类发展的作用。肠道。2019;68:1108-14。
Gensollen T,艾耶党卫军,Kasper DL,布隆伯格RS。殖民的微生物群在生命早期形状免疫系统。科学。2016;352:539-44。
艾尔斯JS。合作微生物宽容行为host-microbiota互利共生。细胞。2016;165:1323-31。
桑切斯KK,陈GY, Schieber AMP,雷德福,Shokhirev MN,尹浩然,勒布朗。合作代谢适应主机支持无症状感染和可以选择的减毒毒性肠病原体。细胞。2018;175:146 e15——58.。
索太,pam。Interbacterial殖民抵抗机制和策略病原体用来克服它们。粘膜Immunol。2019; 12:1-9。
Koh, Backhed f从协会到因果关系:肠道微生物群的作用及其对宿主代谢功能的产品。摩尔细胞。2020;78:584 - 96。
Gevers D, Kugathasan年代,Denson洛杉矶,Vazquez-Baeza Y, Van Treuren W,任B, et al。最近诊断为克罗恩病的首次治疗微生物。细胞。主机微生物。2014;15:382 - 92。
Klingberg E, Magnusson可Strid H,戴明,斯塔尔,Sundin J,等。不同的肠道微生物群组成强直性脊柱炎患者与粪便calprotectin水平上升有关。关节炎Res其他。2019;21:248。
王Falony G, Joossens M, Vieira-Silva年代,J, Darzi Y,浮士德K, et al .肠道微生物群体分析变异。科学。2016;352:560-4。
Yatsunenko扶轮基金会,Manary MJ, Trehan我Dominguez-Bello MG,孔特雷拉斯M,尹浩然,Magris。人类肠道微生物组在年龄和地理。自然2012;486:222-7。
李bitting K,赵C, Y,福特E,弗里德曼,倪J, et al .细菌殖民化重组新生儿肠道代谢组。Nat Microbiol。2020; 5:838-47。
Vangay P,病房T,戈贝尔JS,骑士d .抗生素,儿科失调,疾病。细胞。主机微生物。2015;17:553 - 64。
德斯穆克HS,刘Y, Menkiti或者梅J,戴N, O’leary) CE、et al .微生物群调节中性粒细胞内稳态和宿主抵抗大肠杆菌K1在新生儿败血症小鼠。Nat医学。2014;20:524-30。
白嘴鸦毫克,Garrett WS。的直觉。微生物群、代谢物、宿主免疫力。Nat Immunol牧师。2016;16:341-52。
Olszak T、D Zeissig年代,维拉MP,里希特J,因特网,et al。微生物在生命早期暴露持续对自然杀伤T细胞功能的影响。科学。2012;336:489 - 93。
考克斯LM Yamanishi年代,孙J, Alekseyenko AV,梁JM,我曹,et al。改变肠道微生物群在一个关键发展窗口有持久的代谢的影响。细胞。2014;158:705-21。
木村我,宫本茂J, Ohue-Kitano R,渡边K,山田T,尹浩然,Onuki。孕妇的肠道微生物群后代小鼠代谢表型的影响。科学。2020;367:eaaw8429。
戈登·哈,Pesti l .无菌的动物作为工具研究的主持人微生物的关系。Bacteriol。启35:390 1971;429年。
纽菲尔德Luczynski P,借债过度KA, Oriach CS,克拉克G, Dinan TG,克莱恩摩根富林明。成长在一个泡沫:使用无菌动物肠道微生物群的影响评估对大脑和行为。Int J Neuropsychopharmacol。2016; 19: pyw020。
威尔·m·细菌和早期人类发展。早期的嗡嗡声Dev。2007; 83:165 - 70。
马纳尔·格莱托,年代,Chang HW Hibberd MC,龚六世,程J, et al . microbiota-directed效应在无菌的动物的食物和营养不良的孩子。科学。2019;365:eaau4732。
Mahowald恩伯PJ,草地,妈,Magrini V,狂欢节,戈登霁。一个肥胖相关的肠道微生物与增加能源产量的能力。大自然。2006;444:1027-31。
Safari Z,杰拉德p .肠道微生物之间的联系和非酒精脂肪肝(NAFLD)。细胞。摩尔生命科学。2019;76:1541-58。
刘黄李江C、G, P, Z,赵b .肠道微生物群和阿尔茨海默氏症。J老年痴呆症说。2017;58:1-15。
李YP,赵CC,林TJ,西南,黄WC,赵CF, et al .无菌鼠monocolonization脆弱拟杆菌改善azoxymethane /葡聚糖硫酸酯钠诱导colitis-associated结肠直肠癌。Immunopharmacol Immunotoxicol。2019; 41:207-13。
蒂塞尔h .生物苏尔la凝花intestinale nourrissons。C R Mem Soc杂志。1899;51:943。
洛根的车手。婴儿和儿童的肠道菌群。分册。1913;18:527-51。
加里多D, Barile D,米尔斯哒。一个分子基础bifidobacterial浓缩的婴儿胃肠道。难以减轻。2012;3:415S-21S。
Ruiz-Moyano年代,托坦SM,加里多哒,Smilowitz JT,德国JB Lebrilla CB, et al。食用母乳寡糖的变化由内脏相关婴儿双歧杆菌菌株谕令。:环境Microbiol。2013; 79:6040-9。
转而经营,德国JB, Lebrilla CB,米尔斯哒。母乳glycobiome及其对婴儿的影响肠道微生物群。《美国国家科学院刊。2011,108 (1):4653 - 8。
甘伟鸿BM,赫顿AA,帕伦博MC, Casaburi G,米切尔RD,安德伍德,et al .粪便pH值升高表明母乳喂养的婴儿肠道微生物的深刻变化由于双歧杆菌减少,在过去的一个世纪。mSphere。2018;3:e00041-18。
Litvak Y, Byndloss MX, Tsolis RM, Baumler AJ。Dysbiotic变形菌门扩张:上皮功能障碍的微生物签名。当今Microbiol 2017; 39:1-6。
米拉尼C, Duranti年代,Bottacini F,凯西E, F Turroni,马赫尼J, et al。第一个人类肠道微生物殖民者:组成,活动,和健康的婴儿肠道微生物群的影响。Microbiol启杂志2017;81:e00036-17。
La Rosa PS,华纳BB,周Y,魏因斯托克通用,Sodergren E, Hall-Moore厘米,et al。图案的早产儿肠道细菌种群的发展。《美国国家科学院刊。2014;111:12522-7。
Korpela K, Blakstad电子战、Moltu SJ Strommen K, Nakstad B, Ronnestad AE、et al .肠道菌群发展和早产儿胎龄。Sci众议员2018;8:2453。
Vatanen T, Plichta博士、Somani J,蒙克PC,阿瑟·TD大厅AB, et al .基因组变异和毒株特异性功能适应在人类肠道微生物在早期的生活。Nat Microbiol。2019; 4:470-9。
拉曼,格莱托马纳尔年代,Chang HW, Hibberd MC,萨勃拉曼尼亚年代,et al .稀疏的共变单元描述健康受损的人类肠道微生物群发展。科学。2019;365:eaau4735。
永吉NE Newgard CB Cotten厘米,戈德堡RN, Muehlbauer MJ,贝恩JR, et al。扰乱了成熟的微生物群和代谢物在极度早产儿出生后生长失败。Sci众议员2019;9:8167。
冯刘J,李Y, Y,潘L,谢Z,燕Z, et al .花纹的肠道微生物群与坏死性小肠结肠炎和早产儿晚发型败血症:一个前瞻性研究中国新生儿重症监护室。PeerJ。2019;7:e7310。
Galazzo G, van最佳N, Bervoets L, Dapaah IO, Savelkoul PH值,Hornef MW, et al。微生物群的发展和对生育模式,饮食,和过敏性疾病在粪便样本的纵向分析,收集了从婴儿到幼儿。胃肠病学。2020;158:1584 - 96。
马丹JC,霍恩AG) Lundgren SN,大学生科幻,Cottingham KL,莫里森HG, et al。协会剖腹产和公式的补充与肠道微生物组6周大的婴儿。JAMA Pediatr。2016; 170:212-9。
斯图尔特CJ,贾米德新泽西州,O ' brien杰,哈钦森DS,史密斯DP,黄MC, et al。时间的肠道微生物组在儿童早期发展泰迪学习。大自然。2018;562:583-8。
Combellick杰,胫骨H,胫骨D, Cai Y, Hagan H, lach C,等。不同的粪便微生物群在家或在医院出生的新生儿。Sci众议员2018;8:15660。
Sordillo我野蛮JH, Lee-Sarwar KA,兰格NE,周Y,奥康纳GT,等。饮食在怀孕期间和婴儿和婴儿肠道微生物组。203:47 J Pediatr。2018; 54. - e4。
Lundgren SN,太太JC, Emond是的,莫里森HG,克里斯滕森公元前Karagas先生,等。怀孕期间孕妇饮食与婴儿粪便微生物相关交付mode-dependent方式。微生物。2018;6:109。
威廉姆斯我Carrothers JM,马屁精KA,比蒂NF,布鲁克SL,彼得森港元,et al .牛奶中存在很强的多元关系,口头和粪便微生物在前六个月产后母婴的一对。J减轻。2019;149:902-14。
Azad MB,科尼亚T, Persaud RR,格特曼DS,沙里河RS, CJ,等。影响产妇产时抗生素、分娩和母乳喂养的方法在人类肠道微生物群的第一年生活:前瞻性队列研究。Int。Gynaecol。2016; 123:983 - 93。
科克莫,霍恩AG,戴德E,朗格年代,李Z,黄广告,等。产时的特定类抗生素与成熟的婴儿肠道微生物群:前瞻性队列研究。Int。Gynaecol。2020; 127:217-27。
艾克,Rutten N, Singendonk MMJ, Rijkers GT, Savelkoul榜单Meijssen CB, et al。新生儿抗生素微生物群发展和早期生活的影响是由两个截然不同的沉降器类型。PloS ONE。2020;15:e0228133。
古普塔RW, Tran L Norori J,摩天乔丹、Eren,泰勒厘米,et al . Histamine-2受体阻滞剂改变粪便微生物群在早产儿。J Pediatr杂志减轻。2013;56:397 - 400。
黄平君DM,利维EI Vandenplas y .质子泵抑制剂的影响微生物的年幼的孩子。Acta Paediatr。2020; 109:1531-8。
Vich维拉,Collij V,桑娜年代,Sinha T, Imhann F, Bourgonje AR, et al。常用的药物对肠道微生物群的组成和代谢功能。Nat Commun。2020; 11:362。
杰克逊,威尔第,Maxan我,胫骨厘米,Zierer J,鲍耶远端控制设备,et al .肠道微生物群对常见疾病和人口基数的处方药。Nat Commun。2018; 9:2655。
Iszatt N,詹森,Lenters V,达尔C, Stigum H,骑士R, et al。环境毒物在挪威母亲的母乳和肠道细菌成分和代谢产物在婴儿1个月。微生物2019;比赛进行。
劳厄他Moroishi Y,杰克逊BP,起到TJ,马丹JC, Karagas Nutrient-toxic元素混合物先生和产后早期肠道微生物在美国纵向出生队列。环境Int。2020; 138:105613。
麦克莱恩C,小君,Kozyrskyj a母亲吸烟对婴儿肠道微生物群的影响及其与儿童肥胖:范围审查。世界J Pediatr。15:341-9。2019;
桶嗯,科尼亚T, Takaro TK,小溪JR,沙里河R, CJ, et al。接触家庭毛茸茸的宠物影响肠道微生物群在3 - 4个月的婴儿出生后各种场景。微生物。2017;40。
D 'Agata AL,吴J, Welandawe MKV,南美洲动宾,凯恩B, gro兆瓦。早期生活的影响NICU强调发展中肠道微生物组。Dev Psychobiol。2019; 61:650-60。
何鸿燊TTB gro兆瓦,凯恩B,绮,托雷斯英航,吉尔伯特是的,et AL .二分早产儿肠道微生物的发展。微生物。2018;6:157。
Parra-Llorca, Gormaz M,阿尔坎塔拉C, Cernada M, Nunez-Ramiro, Vento M, et al .早产儿肠道微生物组根据喂养类型:捐赠母乳的意义。Microbiol前面。2018;9:1376。
塔夫脱DH, Salinero路,Vongbhavit K, Kalanetra公里,Masarweh C, Yu, et al .细菌殖民化和抗菌素耐药性基因在新生儿喂养管。《生态。2019;95:fiz039。
Nogacka,萨拉查N,苏亚雷斯M,米拉尼C, Arboleya年代,索利斯G, et al。影响产时抗菌预防肠道菌群和抗生素抗性基因的流行阴道分娩的足月新生儿交付。微生物。2017;5:93。
gasparri AJ,园地TS,吉布森可,塔尔π,华纳BB Dantas本人交出密码g .抗生素早产婴儿肠道微生物和resistome的扰动。肠道微生物。2016;7:443-9。
吉布森可,王B,艾哈迈迪年代,伯纳姆CA,塔尔π,华纳BB, et al。早产婴儿肠道微生物群的发展动态和抗生素resistome。Nat Microbiol。2016; 1:16024。
刘黄Rutayisire E、K, Y,道f .交货方式会影响肠道微生物群的多样性和殖民模式在婴儿的第一年的生活:一个系统的复习。BMC杂志。2016;16:86。
达尔C, Stigum H, J的数值,Iszatt N, Lenters V, Peddada年代,et al .早产儿不同微生物没有解释的交付模式,母乳喂养持续时间或抗生素暴露。Int增加。2018;47:1658 - 69。
桶MH,桶嗯,Mahoney JJ,科尼亚结核病,格特曼DS,贝克尔AB. et al .产后接触家庭消毒剂,婴儿肠道微生物群和随后的儿童肥胖的风险。地中海Assoc j . 2018; 190: E1097-e107。
肖KA,贝莎M, Hofmekler T, Chopra P, Vatanen T, Srivatsa,等。生态失调、炎症,和对治疗的反应:纵向研究的儿科学科与新诊断炎症性肠病。基因组医学。2016;8:75。
高夏GH, C, XX,曾庆红XL,朱镕基JJ,徐肯塔基州,et al .中风失调指数(SDI)肠道微生物与中风的脑损伤和预后有关。前神经。2019;10:397。
张郭Y, Y,格哈德•M,高JJ, Mejias-Luque R, L, et al .效果幽门螺杆菌Linqu胃肠道微生物群:以人群为基础的研究,胃癌的高危区域。肠道》2019。https://doi.org/10.1136/gutjnl - 2019 - 319696。
Casen C, Vebo HC, Sekelja M, Hegge英尺,Karlsson可,Ciemniejewska E,等。在人类肠道微生物群偏差:一种新的诊断试验确定失调IBS患者或炎症性肠病。滋养Therap杂志》2015;42:71 - 83。
马歇尔Mandl T, J,奥尔森P, B欧胜,Andreasson k在原发性干燥综合征严重的肠道失调是普遍和与系统性疾病相关活动。关节炎Res其他。2017;19:237。
Vatanen T, Kostic广告,d 'Hennezel E, Siljander H, Franzosa EA,尹浩然,Yassour。有限合伙人微生物免疫原性变化导致人类自身免疫。细胞。2016;165:842-53。
Vatanen T, Franzosa EA, Schwager R,特里帕西年代,阿瑟·TD Vehik K, et al。人类肠道微生物在泰迪的早发性1型糖尿病的研究。大自然。2018;562:589 - 94。
蔡HH,周HC,东黄,蒋介石提单,廖CC,刘HH, et al .肠道失调具有丰富的瘤胃球菌属gnavus associates在婴儿过敏性疾病。胃肠病学。2018;154:154 - 67。
李·乔丹Kang MJ,李SY,李E、K金,赢得了年代,et al .扰动的肠道微生物与过敏性皮肤炎根据喂养婴儿的基因类型。J过敏Immunol。2018; 141:1310-9。
拉蒙特射频,穆勒Luef B, sten约根森j .儿童炎症和代谢疾病暴露于抗生素在怀孕后,产前、产时和新生地。F1000Res。2020;9:144。
Dowhower Karpa K,保罗•IM Leckie是的,Shung年代,Carkaci-Salli N, Vrana KE, et al .了回顾性的图表总结确定围产期因素与食物过敏有关。减轻j . 2012; 11:87。
梅茨TD, McKinney J, Allshouse AA, Knierim SD,凯里JC, Heyborne KD。暴露于B组链球菌抗生素预防和早期儿童身体质量指数在阴道出生队列。J Matern胎儿新生儿医学。2020;33:3318 - 3323。
沃尔DL、咖喱WJ Mauger D,米勒J, Tyrie k .产时抗生素和儿童特应性皮炎。J是地中海Fam。2015; 28:82-9。
Pammi M,应付J,塔尔π,华纳BB,明日,梅V, et AL。之前在早产儿肠道失调坏死性小肠结肠炎:系统回顾和荟萃分析。微生物。2017;31。
洞螈先生,Bhattacharya N, Crits-Christoph Firek英航,贝克R, y, et al .坏死性小肠结肠炎之前增加肠道细菌复制,克雷伯氏菌,fimbriae-encoding细菌。Sci放置2019;5:eaax5727。
Esmaeilizand R,沙PS, Seshia M,绮W, Yoon电子战,陶氏k .抗生素接触和发展在早产新生儿坏死性小肠结肠炎。Paediatr儿童健康。2018;23:e56-e61。
Esaiassen E, Fjalstad JW, Juvet路,van den安加约,克林根贝格c .抗生素暴露在新生儿和早期的不良结果:系统回顾和荟萃分析。J Antimicrob。Chemother。2017; 72:1858 - 70。
Guillet R,斯托尔BJ,厘米,Cotten Gantz M,麦当劳,普尔周,et al。h2受体疗法协会和更高的发病率极低出生体重婴儿的坏死性小肠结肠炎。儿科。2006;117:e137-42。
休伊特公里,Mannino FL,冈萨雷斯,追逐JH, Caporaso詹,骑士R, et al。细菌多样性两个新生儿重症监护病房(nicu)。PloS ONE。2013;8:e54703。
马Bokulich NA,米尔斯哒,安德伍德。表面微生物在新生儿重症监护室:与常规清洁和随时间的变化。中国Microbiol。2013; 51:2617-24。
布鲁克斯B洞螈先生,Firek英航,贝克R, Geller-McGrath D,老雷蒙,等。发展中早产儿肠道微生物组是一个主要因素形成的微生物组新生儿重症监护病房的房间。微生物。2018;6:112。
斯图尔特CJ, Embleton ND,马斯ECL,史密斯DP, Fofanova T,尼尔森,et al .纵向发展的早产儿肠道微生物组和代谢组与晚发型败血症和健康对照组。微生物。2017;5:75。
歌手小,超视距如Zindl CL,西尔伯格DJ, Conlan年代,Laufer VA,等。防止新生儿的失调小鼠肠道微生物预防迟发性败血症。Nat医学。2019;25:1772 - 82。
马西AC,斯图尔特CJ。早产儿肠道微生物的作用在脓毒症和坏死性小肠结肠炎。早期的嗡嗡声Dev。2019; 138:104854。
Hemmi MH,沃克D,施耐德美国之间的关联问题哭,睡觉和/或喂养儿童在婴儿期和长期行为的结果:一个荟萃分析。拱说孩子。2011;96:622-9。
Loughman,奎因T,国家ML,摘要,摩尔RJ, Van T,等。婴儿绞痛的微生物群:预测对哭泣和随后的儿童行为问题。J Dev源自健康2020:1-11说。https://doi.org/10.1017/S2040174420000227。
Huttenhower C, Kostic广告,泽维尔RJ。炎症性肠病微生物作为翻译的模型。免疫力。2014;40:843-54。
梅耶尔EA, Tillisch K,古普塔a .肠道/脑轴和微生物群。中国Investig。2015; 125:926-38。
本田K,利特曼博士适应性免疫内稳态和疾病的微生物群。大自然。2016;535:75 - 84。
施罗德BO, Backhed f信号从肠道微生物群遥远的器官生理学和疾病。Nat医学。2016;22:1079 - 89。
利维M, Kolodziejczyk AA,泰国人CA, Elinav大肠失调和免疫系统。Nat Immunol牧师。2017;17:219-32。
Maruvada P, V里昂,卡普兰LM, Chang EB。人类微生物组和肥胖:超越联想。细胞。主机微生物。2017;22:589 - 99。
巴赫摩根富林明。自身免疫的卫生假说:病原体和共生体的角色。Nat Immunol牧师。2018;18:105-20。
布朗JM,色度SL。微生物调制的心血管疾病。Nat启16:171 2018;81年。
Tilg H, Zmora N,阿道夫TE, Elinav大肠肠道菌群代谢炎症加剧。Nat Immunol牧师。2020;20:40-54。
Iacob年代,Iacob DG。传染病威胁、肠道屏障和特洛伊木马:生态失调。Microbiol前面。2019;10:1676。
Fouhse JM,杨K, More-Bayona J,高Y, Goruk年代,Plastow G, et al。新生儿接触阿莫西林改变长期免疫反应,尽管在仔猪肠道微生物群的瞬态影响。Immunol前面。2019;10:2059。
博蒙特M, Paes C, Mussard E,克努森C, Cauquil L, Aymard P, et al .肠道微生物群派生代谢物导致肠道屏障成熟suckling-to-weaning过渡。肠道微生物。2020;11:1268 - 86。
Suh SH, Choe K,香港SP, Jeong SH, Makinen T, Kim KS et al .肠道微生物群调节乳完整性通过诱导VEGF-C肠道绒毛巨噬细胞。EMBO众议员2019;20:e46927。
Kulkarni DH,麦当劳公斤、努KA Gustafsson JK,公里,科兹洛夫斯基和Hunstad哒,et al .杯状细胞相关抗原的段落中抑制鼠伤寒沙门氏菌感染,防止病原体传播和限制对饮食抗原的反应。粘膜Immunol。2018; 11:1103-13。
Abo血型H, Chassaing B, Harusato奎洛斯M,巴西JC,非政府组织六世,et al。红细胞分化regulator-1引起微生物群在生命早期肠道干细胞增殖和再生。Nat Commun。2020; 11:513。
Fung TC, Vuong他,卢娜CDG普罗诺沃斯特GN, Aleksandrova AA,莱利NG, et al .肠内5 -羟色胺和氟西汀曝光调节肠道内细菌殖民化。Nat Microbiol。2019; 4:2064 - 73。
Canfora EE、Meex RCR Venema K, Blaak EE。肠道微生物代谢物在肥胖、非酒精性脂肪肝和2型糖尿病。自然评论。内分泌学。2019;15:261 - 73。
刘西城,Vaziri ND。肠道微生物的短链脂肪酸和糖尿病的风险。Nat Nephrol牧师。2019;15:389 - 90。
桑娜年代,van Zuydam NR, Mahajan Kurilshikov, Vich维拉,他说U, et al .肠道微生物之间的因果关系,短链脂肪酸和代谢疾病。Nat麝猫。2019;51:600-5。
De vad F, Kovatcheva-Datchary P, Goncalves D, Vinera J, Zitoun C, Duchampt, et al . Microbiota-generated代谢物促进代谢好处通过肠脑的神经回路。细胞。2014;156:84 - 96。
Dalile B, Van Oudenhove L, Vervliet B,韦贝克k短链脂肪酸microbiota-gut-brain沟通的作用。Nat牧师杂志。2019;16:461 - 78。
Parada贝D·德·拉可Landskron G,冈萨雷斯MJ, Quera R, Dijkstra算法G, et al。短链脂肪酸(SCFAs)介导肠上皮和免疫调控和炎性肠道疾病的相关性。Immunol前面。2019;10:277。
Frese SA Hutton AA,孔特雷拉斯LN,肖CA,帕伦博MC, Casaburi G, et al .持久性的补充双歧杆菌longum无性系种群。对象的EVC001在母乳喂养婴儿。mSphere。2017;2:e00501-17。
郑N,高Y,朱W,孟D,沃克佤邦。殖民肠道共生的细菌产生的短链脂肪酸与表示母乳在人类未成熟的肠上皮细胞抗炎。PloS ONE。2020;15:e0229283。
Waligora-Dupriet AJ, Dugay Auzeil N, Nicolis我Rabot年代,Huerre先生,等。短链脂肪酸和多胺在坏死性小肠结肠炎的发病机理:动力学方面无菌的鹌鹑。厌氧菌。2009;15:138-44。
罗伊SK,孟Q, Sadowitz BD, Kollisch-Singule M, Yepuri N, Satalin J,等。在新生仔猪肠内细菌发酵配方管理:坏死性小肠结肠炎(NEC)的高保真模型。PloS ONE。2018;13:e0201172。
孟D, Sommella E,热血E, Campiglia P, Ganguli K, Djebali K, et al . Indole-3-lactic酸,色氨酸的代谢分泌双歧杆菌longum亚种对象是不成熟的肠道抗炎。Pediatr研究》2020。https://doi.org/10.1038/s41390 - 019 - 0740 - x。
Mukhopadhyay年代,韦德KC, Puopolo公里。药物预防和治疗新生儿败血症。Perinatol。2019; 46:327-47。
王Caballero-Flores G, Sakamoto K,曾庆红,Y,哈基姆J, Matus-Acuna V, et al .母体免疫授予保护后代对免疫球蛋白的附加和消除病原体通过交付母乳。细胞。主机微生物。2019;25:313 - 23. - e4。
Mukhopadhyay年代,森古普塔年代,Puopolo公里。挑战和机遇的早产儿中抗生素的管理工作。拱说孩子。2019;104:F327-f32。
舒尔曼J,迪曼德RJ,李HC,女仆问,贝内特MV,古尔德简森-巴顿。新生儿重症监护室的抗生素使用。儿科。2015;135:826-33。
舒尔曼J,利润J,李HC,女仆G,贝内特MV, Parucha J, et al .新生儿抗生素使用的变化。儿科。2018;142:e20180115。
李气C, N,购买C,太阳J,阴C .益生元对脓毒症的影响,坏死性小肠结肠炎,死亡率、喂养不耐受,时间全肠内喂养,住院时间、早产儿和大便频率:一个荟萃分析。欧元J减轻。2019;73:657 - 70。
太阳J, Marwah G, Westgarth M, N,购买埃尔伍德D,格雷博士益生菌对坏死性小肠结肠炎,败血症,脑室内出血,死亡率、住院时间、和体重早产儿:一个荟萃分析。难以减轻。2017;8:749 - 63。
Deshpande G, G开玩笑,饶,早产儿Patole S .益生菌的好处在低收入和中等收入国家:随机对照试验的系统评价。BMJ开放。2017;7:e017638。
王Dermyshi E, Y,燕C,香港W,邱G,龚X, et al .益生菌的“黄金时代”:系统回顾和荟萃分析的随机和观察性研究早产儿。新生儿学。2017;112:9-23。
奥尔森R, G云英岩,施罗德M, Brok j .预防早产儿益生菌:系统回顾和荟萃分析的观察性研究。新生儿学。2016;109:105-12。
旷L,江y在孕妇补充益生菌的影响:随机对照试验的荟萃分析。Br J减轻。2020;123:870 - 80。
简达Skonieczna-Zydecka K, K, Kaczmarczyk M, Marlicz W, Loniewski我Loniewska b .益生菌对症状的影响,肠道微生物群和炎症标记物在小儿疝气:系统回顾,随机对照试验的荟萃分析和多元回归。中国医学。2020;9:999。
van den ak CHP,范Goudoever JB,沙米尔R, Domellof M, Embleton ND, Hojsak我,et al .益生菌和早产儿:意见书由欧洲儿科胃肠病学学会肝脏病学和营养营养委员会和欧洲儿科胃肠病学学会肝脏病学和营养工作组益生菌和益生元。J Pediatr杂志减轻。2020;70:664 - 80。
van den ak CHP,范Goudoever JB, Szajewska H, Embleton ND, Hojsak我,里德D,早产儿et al .益生菌:一个毒株特异性系统回顾和网络荟萃分析。J Pediatr杂志减轻。2018;67:103-22。
苏GL, Ko CW Bercik P Falck-Ytter Y,苏丹,Weizman AV, et al . AGA临床实践指南在益生菌的作用在胃肠道功能紊乱的管理。胃肠病学》2020。https://doi.org/10.1053/j.gastro.2020.05.059。
刘易斯。沙尼G, Masarweh CF,瑞尔M, Frese SA塞拉哒,et al .验证bifidobacterial种和亚种的身份在商业益生菌产品。Pediatr杂志2016;79:445-52。
蒋介石MC,陈CL,冯Y,陈CC,留置权R,赵CH。乳杆菌脓毒症与极度早产婴儿益生菌疗法:发病机理和临床医生的检查。J Microbiol Immunol感染。2020。https://doi.org/10.1016/j.jmii.2020.03.029
佩尔LG、Loutet毫克,罗斯·德·谢尔曼点。反对益生菌预防NEC的日常管理。当今儿科2019;31:195 - 201。
确认
这项工作是由美国国立卫生研究院HD096241 (M.A.U.) HD088753(克里)HD072929 (S.L.) AI32738和AI125926 (C.L.B.)。
作者信息
作者和联系
相应的作者
道德声明
的利益冲突
作者宣称没有利益冲突。
额外的信息
出版商的注意施普林格自然保持中立在发表关于司法主权地图和所属机构。
权利和权限
关于这篇文章
引用这篇文章
安德伍德,硕士,Mukhopadhyay, S., Lakshminrusimha, S.et al。新生儿肠道失调。J Perinatol40,1597 - 1608 (2020)。https://doi.org/10.1038/s41372 - 020 - 00829 - 2
收到了:
修改后的:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41372 - 020 - 00829 - 2
本文引用的
动态的婴儿肠道微生物群在第一个18个月的生活:孕产妇艾滋病病毒感染和母乳喂养的影响
微生物组(2022)
儿童早期抗生素使用率婴儿新生儿重症监护单位解除
围产期学杂志》(2022)
孕产妇哮喘的影响早产儿肠道代谢组和微生物的研究(图)
科学报告(2022)
极早产儿的一系列益生菌:随机对照试验
儿科研究(2022)
的早期生活微生物宏基因组的印尼住院新生儿临床特点及其影响
科学报告(2022)