儿童急性淋巴细胞白血病(ALL)的治疗需要强化鞘内和全身治疗,以降低中枢神经系统(CNS)复发的风险。这种治疗与较高的神经毒性发生率有关,而且对患者和医疗保健系统都很繁重[1].改善中枢神经系统靶向治疗,需要了解在这种微环境中白血病存活的机制,并伴有更好的中枢神经系统白血病预后和预测性生物标志物。前者将有助于发现毒性较低的治疗方法,后者对于风险适应的中枢神经系统指导治疗的发展至关重要。
中枢神经系统中的白血病细胞位于软脑膜内,位于蛛网膜和脑膜间质层之间,沐浴在脑脊液(CSF)中。与血浆相比,脑脊液的营养成分相对较差,其蛋白质、脂类、葡萄糖和氧气含量较低。这与骨髓(BM)、脾脏和其他ALL细胞聚集的周围器官中高度细胞化和相对营养丰富的环境形成鲜明对比。中枢神经系统和外周神经系统的一个特殊区别在于胆固醇的生物利用度。胆固醇在整个中枢神经系统中相对丰富——主要存在于脑实质的有髓鞘神经鞘中——但在脑脊液中极其稀少[2].中枢神经系统中的胆固醇由一种特殊的亚型(24(S)-羟基胆固醇)组成,只在中枢神经系统中产生,主要由神经胶质神经元支持细胞产生,没有检测到“全身”胆固醇[3.].此外,通常在体循环中运输胆固醇的脂蛋白不在中枢神经系统中,而在脑脊液中检测到中枢神经系统特异性脂蛋白[3.].胆固醇及其中间体对细胞的维持、生存和生长至关重要,而胆固醇生物合成越来越被认为是癌症生物学中干扰的一个关键途径[4].
我们假设中枢神经系统中的白血病细胞对其独特的微环境进行代谢适应,这可能具有治疗利用价值。在体外实验中,我们发现CNS白血病细胞中胆固醇生物合成途径高度上调,抑制该途径会导致细胞活力降低和凋亡增加。我们提供的临床前证据表明,活跃的中枢神经系统白血病与脑脊液胆固醇水平降低有关,而上调的胆固醇合成基因特征可能确定白血病复发风险增加的患者,特别是中枢神经系统复发。
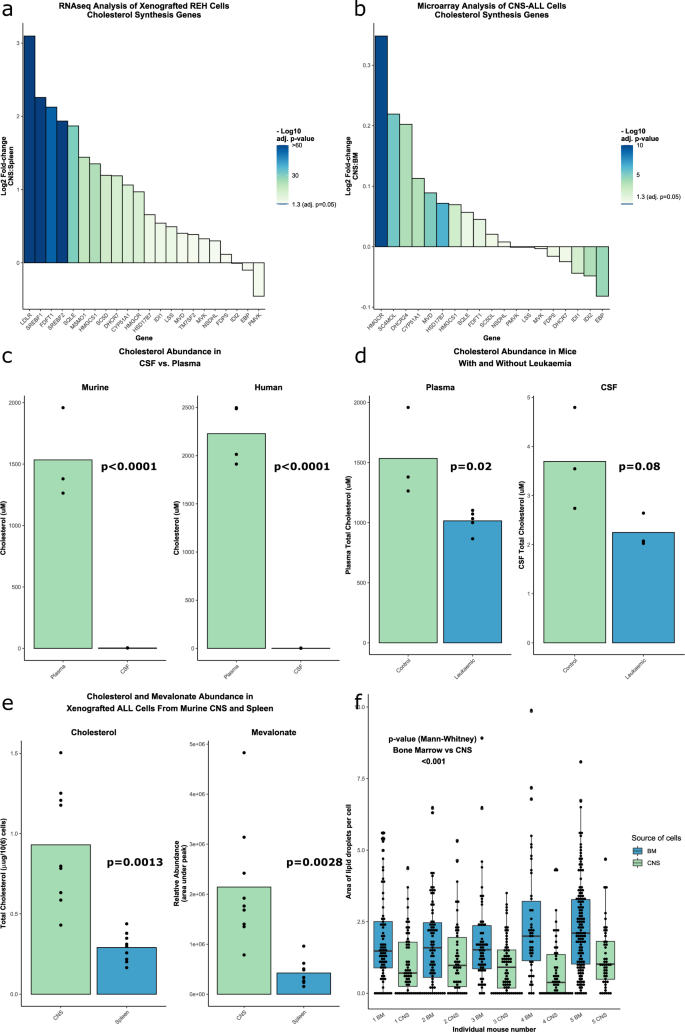
为了研究中枢神经系统微环境的转录适应性,我们从NSG (NOD-scid IL2Rg)的中枢神经系统和脾脏中提取白血病细胞零)小鼠移植两种人b细胞前体(BCP)白血病细胞系- sem和REH(详情见补充材料和方法).转录本最初与小鼠基因组进行比对,从任何污染的小鼠细胞中去除签名,然后进行基因集富集分析。低密度脂蛋白受体(LDLR)——控制胆固醇摄取的主要受体——和胆固醇生物合成途径的基因是中枢神经系统白血病细胞中相对于脾脏白血病细胞中高度上调的基因/过程。1补充图。1).为了进一步探索这种关联,我们检查了公开的人类数据集[5证实了ALL患者cns衍生细胞中胆固醇内稳态和生物合成基因的显著上调(图1)。1 b).
一个瀑布图显示从NSG小鼠的中枢神经系统和脾脏中提取的异种移植REH (BCP-ALL细胞系)细胞之间胆固醇生物合成途径基因的差异表达。n= 3个实验(每个实验3-4只老鼠)。b瀑布图显示了从CNS复发的儿童患者脑脊液中提取的人类BCP-ALL细胞与确诊时的BM或BM复发时的BM之间胆固醇生物合成途径基因的差异表达[5].一个,b调整p-使用Benjamini-Hochberg方法计算的值。c柱状图显示正常对照NSG小鼠和人血浆和脑脊液中胆固醇含量。老鼠:n= 3只(两组);人类:n= 4(等离子体),n= 5 (CSF)d条形图显示患有和未患白血病的NSG小鼠血浆和脑脊液中胆固醇含量。等离子体:n= 3(对照组),5(白血病);CSF:n= 3(两组)e柱状图显示从NSG小鼠的中枢神经系统和脾脏中提取的异种移植的SEM细胞内的细胞内胆固醇和甲戊酸的丰度。N = 9只(各组)。d- - - - - -fP-使用二尾学生计算的值t以及。f从NSG小鼠的中枢神经系统和骨髓中提取的异种移植的SEM细胞中脂滴面积的箱线图。n= 5只小鼠的658个细胞(385个骨髓/273个中枢神经系统)。P-值使用Wilcoxon秩和/Mann-Whitney U检验计算。
我们能够证实小鼠和人类脑脊液中的胆固醇水平非常低(图。1 c),并表明活动性白血病的存在与这些水平进一步降低的趋势相关(图。1 d补充图。2).胆固醇水平的降低可能是由于CNS白血病细胞从脑脊液主动摄取所致。为了支持这一观点,总胆固醇和胆固醇中间体甲戊酸盐的测量显示,从中枢神经系统提取的扫描电镜细胞中这些代谢物的水平高于从脾脏提取的细胞(图1)。1 e).与来自骨髓的扫描电镜细胞相比,来自中枢神经系统的扫描电镜细胞中脂滴减少。1 f).
为了研究胆固醇合成对ALL细胞存活是否重要,我们用HMGCoA还原酶抑制剂辛伐他汀体外处理SEM细胞。这导致细胞活力降低,凋亡增加(补充图。2 b).通过使用HMGCoA还原酶下游产物甲戊酸盐挽救表型证实了靶向效应(补充图)。2 b).有趣的是,补充胆固醇并不能挽救表型(补充图。2摄氏度),这表明白血病细胞需要甲丙酸和胆固醇之间的上游中间产物。与其他团体一样[6我们无法确定辛伐他汀治疗的异种移植小鼠体内白血病负担的降低(补充图。2 d, e).发现HMGCR基因基因敲除/敲除的SEM细胞在体外不可活(数据未显示)。
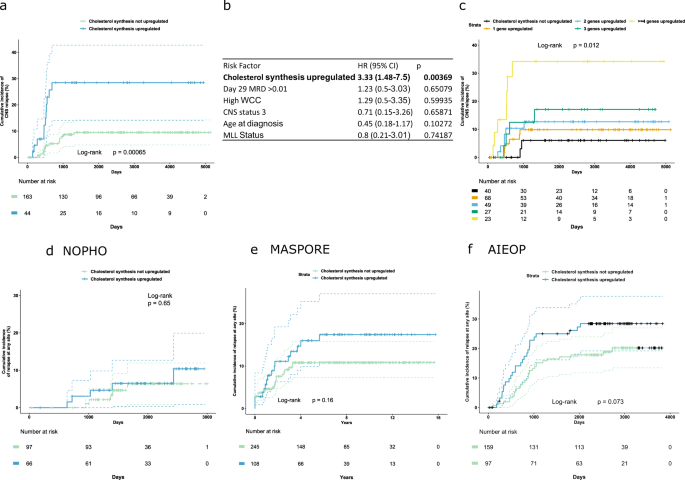
最后,我们研究了诊断性BM样本中ALL细胞中胆固醇合成信号上调是否与白血病复发风险增加有关。儿童肿瘤组(COG) P9906试验中接受高危ALL治疗的儿童的公开数据来自美国国家癌症研究所TARGET一期ALL项目(http://ocg.cancer.gov/programs/target)和NCBI地质数据集GSE GSE11877。使用21个胆固醇通路基因(详见补充方法),我们发现表达上调(Z评分为> 1.5的至少2个基因上调)与孤立中枢神经系统复发的风险相关(图。2 a, b),总生存率降低(补充图。3 b、d),但不会复发(补充图。3 a, c).此外,胆固醇基因上调(z评分> 1.2)以剂量依赖性的方式增加CNS复发风险(图。2摄氏度).这种增加的中枢神经系统复发风险与最小残留疾病(MRD)风险组无关,在本分析中,胆固醇合成基因的上调比第28天的MRD水平更能预测中枢神经系统复发(图。2 b).相比之下,MRD仍然是脑脊膜炎复发和总生存期最相关的危险因素(补充图。3模拟).P9906试验招募高危患者[7],因此有较高的CNS复发率。利用现有基因表达谱对其他国际队列的检查证实了胆固醇生物合成上调与白血病复发的关系(图。2 d-f),但没有足够的能力验证其对中枢神经系统复发率的独立影响(补充图。3 e, g,我).有降低总生存率的趋势,但这仅在3个数据集中的1个达到统计学意义(补充图。3 f、h、j).
一个Kaplan-Meier曲线显示,在TARGET数据集中,通过上调胆固醇生物合成基因,高危BCP-ALL儿童孤立中枢神经系统复发的累积发生率。虚线表示95%置信区间。b该数据集的Cox比例风险模型与传统风险因素(诱导治疗第29天MRD阳性>0.01%,WCC > 50 × 109/L, > 5个白细胞/μL脑脊液,发现ALL母细胞,>年龄10岁,发现MLL重排)和胆固醇合成基因上调。cKaplan-Meier曲线显示,随着胆固醇生物合成通路中基因数量的增加,孤立中枢神经系统复发的累积发生率升高(定义为基因表达z值≥1.2)。在国际数据集中,任何因胆固醇合成上调而复发的累积发生率(d) NOPHO, (e) MASPORE,和(f) AIEOP组。
在这项研究中,体外、体内和原始患者数据互补表明,胆固醇代谢上调与中枢神经系统白血病之间存在一致的关联。先前的报道表明,急性白血病的表现可能与血浆/血清胆固醇水平低有关[8],随后在治疗过程中升高[9].系统性低胆固醇血症的病因尚未得到证实,但可能是由于白血病细胞的摄取增强,或急性炎症刺激肝脏摄取[10].脑脊液中的胆固醇水平此前从未在此背景下被检测过,由于脑脊液缺乏来自外周的胆固醇运输,因此脑脊液作为中枢神经系统白血病的独立生物标志物具有特别的吸引力。我们的数据显示,中枢神经系统ALL细胞中脂滴的减少进一步证实了代谢适应的重要性,特别是脂代谢,如最近所描述的[11].
ALL细胞在中枢神经系统微环境中需要胆固醇有几个潜在的原因。我们的研究结果和提出的模型在补充图中以图形形式显示。4.胆固醇和其他甾醇对膜的完整性和流动性很重要。此外,胆固醇合成途径的中间产物参与许多重要的细胞过程。其中包括参与电子传输和细胞呼吸的泛素酮(辅酶Q);法尼基和香叶酰香叶酰类异戊二烯,Ras家族等蛋白质的共价结合所需;糖蛋白合成所需要的Dolichol;和异戊烯腺嘌呤,它对某些tRNA功能和蛋白质合成至关重要。在细胞应激条件下,对其中一个或多个过程的依赖增加,很可能是CNS ALL中观察到的通路上调的基础。一个有吸引力的候选者是胆固醇生物合成途径在Ras的法尼基化中的作用——Ras/Raf/MEK/ERK途径已知在CNS白血病中被激活,在低营养条件下尤其重要[12,13].selumetinib -一种MEK1/2抑制剂可根除患者异种移植瘤中的中枢神经系统白血病[13].另一种可能的机制是通过富含胆固醇的膜结构域调节受体信号——有实验证据表明,VEGFR刺激促进了FLT-1在ALL细胞系中这些富含胆固醇的膜结构域的定位[14].再次,增强的VEGF活性与CNS白血病有因果关系[15].细胞因子信号(如TNF信号)的作用在CNS ALL中已经被探索过了[16].细胞信号与细胞代谢之间存在着明显的密切联系,这一领域值得进一步研究。
他汀类药物在体内缺乏疗效可能反映血浆和脑脊液药物水平不足和/或代偿通路可能在体内起作用。我们的结果与Samuels的报告相似等他发现了耐药ALL中辛伐他汀的潜在脆弱性。他们证实,辛伐他汀的体外活性良好,但缺乏体内疗效,可能是由于最大耐受剂量达到较低的血浆水平[6].
中枢神经系统白血病仍然是一个临床挑战。特别是,缺乏足够的预后标记物表明中枢神经系统复发的风险,以及在轻脑膜中缺乏敏感的中枢神经系统浸润的生物标记物,阻碍了风险适应的中枢神经系统指导治疗的发展。我们的研究发现,脑脊液胆固醇水平低——可能是由于白血病细胞的细胞摄取——是CNS白血病存在的潜在临床生物标志物。此外,对患者预后数据的分析表明,上调的胆固醇生物合成特征与复发风险的增加相关,特别是在中枢神经系统。现在需要在大量前瞻性临床队列中进一步验证这些潜在的预后生物标志物。
数据可用性
这些异种移植实验的RNA-Seq数据可通过登录号GSE135115获得,标题为“从中枢神经系统和脾脏提取的ml - af4和TEL-AML1急性淋巴细胞白血病母细胞的基因表达谱”。该数据库有两个数据集,GSE135113“从中枢神经系统和脾脏提取的ml - af4急性淋巴细胞白血病母细胞的基因表达谱”和GSE135114“从中枢神经系统和脾脏提取的tell - aml1急性淋巴细胞白血病母细胞的基因表达谱”。该数据集的结果此前曾发表过[11].
参考文献
Pui CH, Howard SC.儿科白血病中中枢神经系统恶性疾病的当前管理和挑战。柳叶刀杂志。2008;9:257 - 68。
王晓燕,王晓燕。儿童和成人脑脊液中脂质的组成。J Neurochem。1971;18:769 - 76。
王晓燕,王晓燕。神经元和神经胶质细胞中胆固醇的内稳态。Semin Cell Dev Biol. 2005; 16:193-212。
Kuzu OF, Noory MA, Robertson GP。胆固醇在癌症中的作用。实用癌症杂志2016;76:2063 - 70。
van der Velden VH, de Launaij D, de Vries JF, de Haas V, Sonneveld E, Voerman JS等。诊断时新的细胞标志物与儿童b细胞前体急性淋巴母细胞白血病的孤立中枢神经系统复发相关。中华血液学杂志2016;172:769-81。
Samuels AL, Beesley AH, Yadav BD, Papa RA, Sutton R, Anderson D,等。小儿急性淋巴细胞白血病诱导治疗耐药的临床前模型。《血癌杂志》2014;4:e232。
康浩,陈林,Wilson CS, Bedrick EJ, Harvey RC, Atlas SR,等。无复发生存和最小残留疾病的基因表达分类器改善了儿童b前体急性淋巴细胞白血病的风险分类和预后预测。血。2010;115:1394 - 405。
Mogensen PR, Grell K, Schmiegelow K, Overgaard UM, Wolthers BO, Mogensen SS,等。儿童急性淋巴细胞白血病诊断中的血脂异常。《公共科学图书馆•综合》。2020;15:e0231209。
Moschovi M, Trimis G, Apostolakou F, Papassotiriou I, Tzortzatou-Stathopoulou F.儿童急性淋巴细胞白血病的血脂改变。J Pediatr内科杂志/杂志。2004; 26:289 - 93。
Pugliese L, Bernardini I, Pacifico N, Peverini M, Damaskopoulou E, Cataldi S,等。严重的低胆固醇血症在血液系统恶性肿瘤中常被忽视。中华癌症杂志2010;46:1735-43。
Savino AM, Fernandes SI, Olivares O, Zemlyansky A, Cousins A, markt EK,等。急性淋巴细胞白血病对中枢神经系统微环境的代谢适应依赖于硬脂酰辅酶a去饱和酶。Nat癌症。2020;1:998 - 1009。
Williams MT, Yousafzai Y, Cox C, Blair A, Carmody R, Sai S,等。白细胞介素-15在b前期急性淋巴细胞白血病中增强细胞增殖并上调CNS归巢分子。血。2014;123:3116-27。
欧文杰,马锡森E,敏托L,布莱尔H, Case M,哈尔西C,等。Ras通路突变在复发的儿童急性淋巴细胞白血病中普遍存在,并对MEK抑制具有敏感性。血。2014;124:3420-30。
Casalou C, Costa A, Carvalho T, Gomes AL,朱铮,吴燕,等。胆固醇调节急性白血病细胞中VEGFR-1 (FLT-1)的表达和信号转导。Mol Cancer Res. 2011; 9:215-24。
蒙克五,特伦丁L,赫齐格J,德米尔S,塞弗里德F,克劳斯JM,等。中枢神经系统参与急性淋巴细胞白血病是由血管内皮生长因子介导的。血。2017;130:643-54。
Jaime-Pérez JC, Gamboa-Alonso CM, Jiménez-Castillo RA, López-Silva LJ, Pinzón-Uresti MA, Gómez-De León A,等。CNS复发前急性淋巴细胞白血病患儿脑脊液中TNF-α增高。《血细胞分子杂志》2017;63:27-31。
确认
我们要感谢为这项研究中使用的基因组数据库提供样本的患者和家属。此外,我们感谢J. Goodfellow、H. Willison、S. Bhatti和YY在获得初级脑脊液样本方面的帮助,感谢NHS大格拉斯哥和克莱德生物库的对照血浆,感谢C. Orange和L. Stevenson在组织学方面的帮助。组织学切片由格拉斯哥大学伊丽莎白女王大学医院的切片扫描和图像分析服务机构扫描。RNA-seq是由格拉斯哥大学的格拉斯哥多元组学研究机构完成的。LC-MS代谢组学分析由格拉斯哥Beatson研究所代谢组学组的G MacKay、D Sumpton和N van der Broek进行。我们也感谢K. Keeshan和英国癌症研究中心比特森癌症研究所生物服务部的动物援助。本文的计算工作部分是在新加坡国家超级计算中心(https://www.nscc.sg).这项工作是丹麦全国研究计划儿童肿瘤网络靶向研究、组织和预期寿命(CONTROL)的一部分,并得到了丹麦癌症协会(R-257-A14720)和丹麦儿童癌症基金会(2019-5934和2020-5769)的支持。这项工作得到了首席科学家办公室(OO, PH, EG和CH,拨款ETM/374), Cariparo基金会,CRUK核心资金给CRUK Beatson研究所(A17196和A31287), CRUK格拉斯哥中心(A18076和A25142), CRUK职业发展奖学金(A17728) (JK),玫瑰树信托奖学金(M480) (GMcG), CRUK核心资金(A18278) (EG)和威廉和伊丽莎白戴维斯基金会(AC,临床研究奖学金)的支持。
作者信息
作者和联系
贡献
AC, OO, AM, EG和CH制定想法和计划实验。实验由AC、GMcG、OO、AM和XB在ST、DS和JK的帮助下进行。生物信息分析由AC进行,由EM和ph支持。国际数据访问和分析:NOPHO - MD, AC和KS, MASPORE-ZL, AEY, AIEOP-DS, MGV, GtK。这封信是AC起草的,所有作者都投稿了。所有作者审阅并接受文章内容。
相应的作者
道德声明
相互竞争的利益
作者声明没有竞争利益。
额外的信息
出版商的注意施普林格自然对出版的地图和机构附属的管辖权要求保持中立。
权利和权限
开放获取本文遵循创作共用署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),该协议允许在任何媒体或格式中使用、分享、改编、分发和复制,只要您给予原作者和来源适当的署名,提供创作共用许可协议的链接,并说明是否有更改。本文中的图片或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果材料不包含在文章的创作共用许可中,并且您的预期用途不被法律法规允许或超出了允许的使用范围,您将需要直接从版权所有者那里获得许可。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于这篇文章
引用这篇文章
考辛斯,A.;奥利瓦雷斯,O.;et al。儿童急性淋巴细胞白血病的中枢神经系统参与与胆固醇生物合成途径的上调有关。白血病(2022)。https://doi.org/10.1038/s41375-022-01722-x
收到了:
修改后的:
接受:
发表:
DOI:https://doi.org/10.1038/s41375-022-01722-x