文摘
防御病原体如SarCoV2哺乳动物包括免疫功能之间的相互作用和代谢途径消除感染,同时防止hyperinflammation。氨基酸代谢途径代表与其他抗菌剂治疗策略的潜在目标。iNOS-mediated生产不涉及从Arg天生的炎症反应的病原体,没有生产过剩可以诱导hyperinflammation。两个参数——和Trp-catabolising酶__arg1 IDO1减少hyperinflammation的免疫抑制效应通过Arg饥饿(__arg1)或通过免疫调节活动的Trp-derived代谢物Kyn (IDO1)。为了应对氨基酸丰富mTOR激活宿主蛋白质翻译和冠状病毒使用这个机器为自己的蛋白质合成和复制。GCN2相比,氨基酸饥饿的传感器,激活通路限制炎症和病毒复制。Gln损耗改变更加抑制免疫反应,通过支持调节性T表型而不是Th1表型。增殖激活免疫细胞是高度依赖于爵士,T细胞的活化和分化需要足够的爵士和饮食Ser限制可以抑制其增殖。半胱氨酸对t细胞增殖的严格要求,因为他们不能满足转化为半胱氨酸。限制了抑制病毒RNA帽甲基化和复制和感染细胞的增殖增加满足要求。 Phe catabolism produces antimicrobial metabolites resulting in the inhibition of microbial growth and an immunosuppressive activity towards T lymphocytes.
介绍
宿主防御病原体入侵,包括SarCoV2等的细菌或病毒,包括哺乳动物中初始先天免疫和根除感染的保护性反应,通过直接作用于病原体和本地诱发炎症,随后由不同的免疫调节机制平衡和疾病预防次生有害hyperinflammation宽容。这些过程包括一系列的一部分复杂的免疫功能之间的相互作用和代谢途径造成的趋同进化的两个系统1,2]。尤其说明了战略利用更高的生物响应病原体感染使用氨基酸代谢和信号通路限制病原体入侵和调节免疫反应的时间进程。哺乳动物控制免疫反应和细胞内的氨基酸通过不同的机制包括当地的分解代谢增加和生产氨基acid-derived代谢物与抗菌细胞毒性和免疫调节活动。有趣的是,它已经表明,这些机制不仅导致病原体的饥饿和控制感染,但也参与调节潜在有害hyperinflammatory反应(3]。在这种情况下,氨基酸消耗或饱食,和/或针对不同的氨基酸代谢和信号通路可以表示,在协会与其他抗菌药物潜在的治疗策略对微生物病原体(表1)。
精氨酸和arginine-catabolizing酶伊诺和__arg1
精氨酸(Arg)是一种非必需氨基酸,健康人类参与蛋白质的合成和尿素循环和不同分子作为前体包括谷氨酸(Glu),瓜氨酸(Cit)和一氧化氮(NO),一个重要的生物活性分子与心血管,免疫,神经信号功能,抗菌细胞毒性活动(4]。在人类中,参数是由内源性合成提供的饮食和收益的两个主要步骤,与肠上皮细胞的初始转换饮食脯氨酸(Pro)、Glu、和谷氨酰胺(Gln)鸟氨酸(内在的)和Cit, Cit的和随后的转换参数在近端肾小管,在免疫细胞的合成没有作为免疫反应的信号分子(5]。Arg的吸收和运输到细胞溶质载体家庭7 (SLC7)和阳离子氨基酸转运蛋白(cat 1、CAT-2 CAT-3)。cat 1由大多数组织表达的观察,而CAT-2在小鼠树突状细胞(dc)是调节视黄酸,在巨噬细胞和Th1、th2型细胞因子,增加相关参数发生分解代谢酶活性和Arg-derived生物活性代谢产物的生产6,7]。
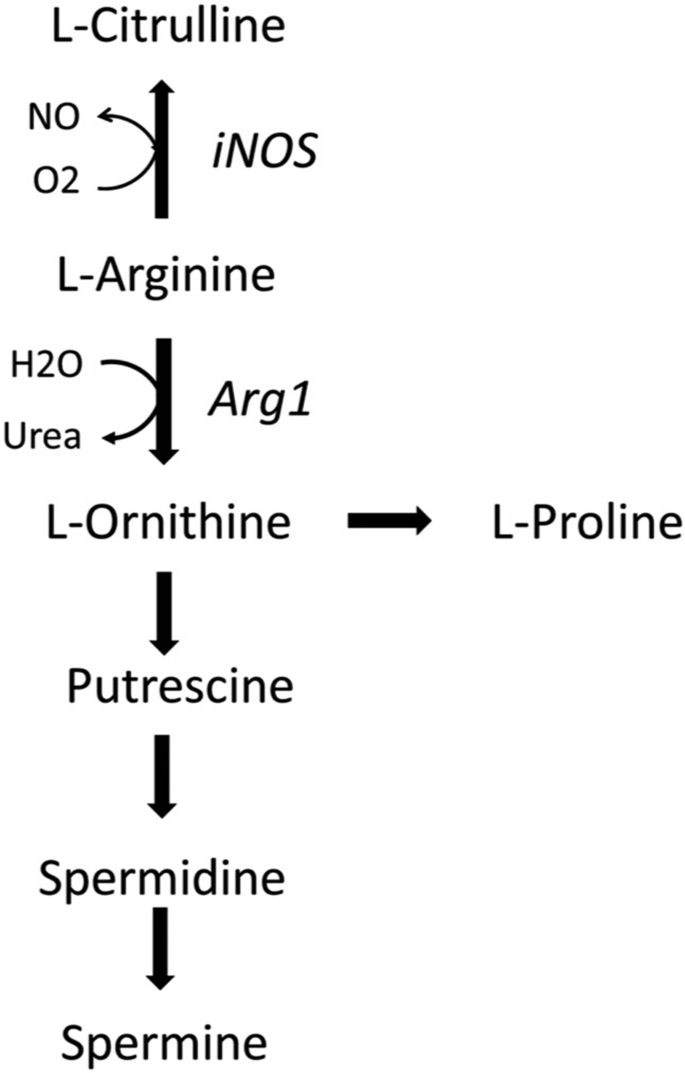
Arg分解代谢涉及在哺乳动物四种酶包括一氧化氮合酶(NOS1, NOS2 NOS3)、精氨酸酶(__arg1、最长),精氨酸脱羧酶(ADC)和精氨酸甘氨酸amidinotransferase(阿加特设计局)[8]。三号同功酶生产没有和cit从参数称为神经元(NOS1或nNOS),诱导(NOS2或间接宾语)和内皮(NOS3,或以挪士)酶(9]。NOS1和NOS3本构酶,而NOS2(间接宾语)引起的促炎细胞因子(包括IFN-g和IL-1b)和microbial-associated产品(脂多糖(LPS)。精氨酸酶水解参数为尿素和内在的和参与鸟氨酸循环和在生产过程中,酶的鸟氨酸脱羧酶和鸟氨酸氨基转移酶、Glu、Pro, Cit和具有生物活性的多胺(腐胺、亚精胺和精胺)参与细胞增殖,细胞修复、炎症的调制。精氨酸酶表达的免疫细胞,参与一些免疫反应(10,11]。两个异构体__arg1和最长有不同的组织分布和细胞本地化。__arg1是巨噬细胞的胞质酶表达、myeloid-derived抑制细胞(MDSCs)、DCs和先天淋巴细胞组2 th2型细胞因子(il - 4, IL-13) [10,12,13),和其他病原体感染的信号相关的因素(10,14]。在人类中,__arg1存在于粒细胞的颗粒间健康受试者(15,16),在外周血单核细胞在受伤后受试者在激活单核细胞在自身免疫性疾病患者(17]。
这两个参数的相对表达异化酶伊诺和__arg1、和生产相关的Arg-derived代谢物,巨噬细胞分化的内在规定,相关函数,和激活状态,概要文件和时间进程对病毒和细菌病原体的免疫反应(无花果。1)[18]。除了参数外,其他氨基酸参与了巨噬细胞分化,如Gln或丝氨酸,进入三羧酸循环和一个碳代谢中的作用,分别为(3]。
参数是没有参与的衬底iNOS-mediated生产初始先天炎症免疫反应的病毒感染(19]。在这个对病原体的先天免疫反应的初始阶段iNOS-expressing巨噬细胞主导促炎细胞因子和细菌有限合伙人和无参数的刺激炎症免疫反应和细胞毒性,抑制细胞生长的活动来消除病原体。在实验动物模型中,严重的流感病毒感染诱发没有生产过剩和肺hyperinflammation因果相关发病率(20.]。COVID-19严重病例也以没有生产过剩,肺hyperinflammation和地方组织损伤(21]。Arg消耗使用Arg-depleting酶是一种有前途的治疗患者的抗病毒方法SARSCoV-2感染。减少等离子体参数水平可能会限制生产没有伊诺和hyperinflammatory响应的程度,与ADI-PEG20如前所观察到的肝细胞癌患者和丙型肝炎病毒感染(22]。几个发达arginine-metabolising酶可以降低等离子体参数和NO-dependant COVID-19 hyperinflammatory反应和其它病毒性疾病(23]。
此外,Arg损耗可能直接影响SARSCoV-2生命周期。参数出现的关键氨基酸病毒复制的DNA和RNA病毒和几个步骤SARSCoV-2复制依赖与守恒的Arg残留病毒蛋白质。Arg损耗可能抑制SARS-CoV-2复制和包装如前所观察到的其他病毒的家庭Herpesviridae和Adenoviridae [23,24]。体外数据显示Arg-depleting酶pegzilarginase抑制SARS-CoV-2复制在维洛细胞(23]。此外,Arg残留在407位置和S1 / S2现场SARS-CoV-2的突起蛋白可能参与绑定病毒宿主细胞受体的血管紧张素转换酶2和融合的病毒膜与宿主细胞膜(25,26,27]。
在第二阶段的病原体感染的免疫反应,Arg1-expressing巨噬细胞主导th2型细胞因子和提供专业和多胺,参与调节hyperinflammation和组织修复(18]。然而,病毒和宿主争夺多胺参与宿主组织修复但也包装病毒基因组和病毒的关键酶活性。因此,任何药物抗病毒策略目标参数和多胺生产应该支持主机而限制使用病毒复制的多胺(28]。
色氨酸和tryptophan-catabolizing酶IDO1
必需氨基酸色氨酸(Trp)的前体的合成蛋白质和几个分子参与多样化的生物过程的规定,包括氨基酸犬尿氨酸(Kyn),河畔,血清素和褪黑激素(29日]。在哺乳动物中,Kyn通路是Trp分解代谢的主要途径之一,而较低的金额通过methoxyindole catabolised通路。转换的Kyn涉及两种酶,indoleamine-2, 3 -加双氧酶1 (IDO1)和tryptophan-2 3-dioxygenase (TDO)(图。2)。IDO1是单体的,haem-containing酶催化作用初始,退化的病原反应一步进L-Kyn [30.,31日]。或者,可以转换Trp色氨酸hydroxylase-1 5-hydroxytryptophan,前兆的途径合成血清素和褪黑激素(32]。
酶IDO1,主要由DCs表示,参与免疫调节免疫抑制急性炎症的控制效果与异化的活动,从而诱导迅速变化的和Kyn水平导致Trp剥夺微环境和代immunoactive Kyn代谢物(33]。Kyn是芳基碳氢化合物受体的内源性配体(AhR)影响免疫细胞和癌细胞的生物学34]。的Kyn-derived分解代谢物如喹啉酸和3-hydroxyanthranilic酸具有不同的生物活性,作为免疫抑制因素和抑制t细胞增殖35,36]。细胞因子γ-IFN激活强烈短期IDO1-competent DCs T淋巴细胞介导的免疫抑制活动,包括抑制增殖、凋亡和分化向监管表型Treg [37]。缺陷IDO1催化活性的主要作用是低一代的Kyn-type AhR的配体和Treg细胞(37,38]。有缺陷的活动IDO1以前所示自身免疫性和慢性炎症性疾病39,40]。
识别机制控制的功能和命运IDO1打开新战略IDO1药物控制的功能及其免疫调节作用和调节IDO1催化活性是一种很有前途的治疗方法调节的免疫反应在不同的步骤中病原体感染的免疫反应。对于某些病毒感染高IDO1活动代表一个免疫反应迟钝在最初的免疫反应的主要原因,旨在消除病原体的差别,对这些短期的免疫抑制监管IDO1应该改善这种短期的免疫反应的影响。相比之下,在第二阶段的反应,移植和增加IDO1可以参与的活动,防止有害hyperinflammation。
参数之间的十字路口,Trp新陈代谢和监管的影响,这两个酶__arg1和IDO1参与急性hyperinflammation相关的次级控制病原体感染的免疫调节免疫抑制效应通过氨基酸消耗(至于__arg1)或通过免疫调节的结合影响Kyn和信号活动(至于IDO1) [3,32]。然而,这两个途径可能有独立功能根据不同的环境条件和可以互补相关的治疗方法。有趣的是,一个IL4-dominated细胞环境促进__arg1表达式(主要是巨噬细胞/ MDSCs) [14),而一个γ-IFN-dominated细胞环境促进IDO1 (DCs)表达式41]。参数之间的交互和Trp代谢免疫调节过程中也说明了亚精胺,激活相关的分子途径的激活IDO1和授予DCs耐受性表型(42]。
谷氨酰胺和主机防御
免疫细胞快速增殖细胞,包括一些,需要提供一些氨基酸如Gln和移植提供这些氨基酸代谢途径,和这些过程可以作为抗感染治疗靶点[43]。氨基酸Gln是一种非必需氨基酸,可以成为有条件的基本生理应激或在关键时期疾病和损伤(44]。Gln对细胞增殖至关重要,包括淋巴细胞、胸腺细胞,和colonocytes,积极应用于几个重要的代谢过程。Gln参与蛋白质的合成,是核苷酸和氨基酸糖的前体,由谷氨酰胺酶降解Glu,进一步代谢不同的产品包括g-amino丁酸,谷胱甘肽,和叶酸,是能源的主要来源,提供中间体三羧酸循环的组件。Gln是人类肌肉中含量最丰富的游离氨基酸在高利率和等离子体,利用快速分裂的细胞,包括白细胞、提供能源和核苷酸生物合成。几个基因的表达在免疫系统细胞在很大程度上是依赖Gln的可用性。
Gln的退化导致NH的形成3和天冬氨酸的合成嘌呤和嘧啶核苷酸参与DNA和RNA的合成。Gln作为氮捐赠者的快速分裂的细胞,淋巴细胞,等它核苷酸合成和能源生产的关键45),这严重影响免疫细胞反应的效率46]。谷氨酰胺酶催化的水解脱氨基Gln Glu和北半球3在哺乳动物中谷氨酰胺酶是高度表达的淋巴细胞和巨噬细胞的淋巴器官,增加对炎症刺激反应(47]。Gln充当能量底物为白细胞和中扮演着重要的角色在细胞增殖,组织修复过程活动和细胞内途径与病原体识别(48]。M2的柠檬酸循环巨噬细胞没有底物的代谢途径通量偏差而M1巨噬细胞(LPS)处理衬底流量偏差有两个点,一个发生在异柠檬酸脱氢酶一步反应和另一个帖子琥珀酸的形成。这导致柠檬酸循环中间体的积累(如琥珀酸,a-ketoglutarate、柠檬酸和itaconate),调节LPS激活巨噬细胞。Itaconate有消炎的作用通过核转录因子的激活红细胞2两个相关因素通过Kelch-like ECH-associated蛋白质1烷基化。
天真的T淋巴细胞迅速激活后病原体入侵和Gln至关重要的扩散和生物合成的活动需要高能源供应增加了吸收和使用Gln [49,50,51]。在T淋巴细胞的活化Gln转运蛋白包括ASCT2调节诱导迅速Gln吸收当这些转运蛋白的减少活动损害这些免疫细胞功能50,52,53]。Gln参与免疫系统细胞扩散的控制通过ERK和物等激活蛋白激酶。两种蛋白质作用于转录因子的激活物和AP-1等,导致细胞扩散基因的转录。适当Gln浓度导致关键的淋巴细胞的表达细胞表面标记,如CD25、CD45RO、CD71,和细胞因子的产生,如IFN-g TNF-a, il - 6。Gln促进激活人类T淋巴细胞的增殖,刺激PBMCs,这些细胞的产生和分泌-γ-IFN和IL - 2, Gln损耗抑制T淋巴细胞增殖,降低IL - 2和干扰素-γ生产(50,54,55]。除了作为燃料,Gln调节immuno-inflammatory反应和抗氧化状态。政府Gln调节肠道炎症,饥饿的56]。Gln和其他氨基酸也可能通过免疫细胞的氧化还原调控发挥他们的作用,调节许多细胞功能。Gln(通过谷氨酸),半胱氨酸,甘氨酸的合成谷胱甘肽的前体氨基酸。然而,这三种氨基酸中,谷氨酸可能代表了第一个和最重要的限制步骤合成谷胱甘肽中间化合物(57]。反过来,谷氨酸合成依赖于Gln胞内的可用性。因此,更高的Gln /谷氨酸比率强化谷胱甘肽合成的底物的可用性。
Gln损耗改变的平衡变得更加抑制免疫反应,通过支持调节性T表型而不是Th1表型,甚至在一个环境诱导Th1表型、细胞因子与干扰素-γ分泌的抑制(49]。Gln互补显示抗病毒活性对疱疹病毒(58,59)和补充将锌、维生素D和Gln显示一个潜在的辅助和协同治疗潜力通过γ-IFN信号在调制抗病毒免疫防御功能治疗COVID - 19 (60]。然而,由于病毒感染宿主细胞Gln利用率的增加,开发针对Gln的抗病毒策略必须耗尽Gln在病毒感染宿主细胞的环境有利于Gln利用率由宿主免疫细胞系统(61年]。
其他氨基酸代谢和信号通路
氨基酸充分性不足和氨基酸和蛋白质的新陈代谢由氨基酸传感控制通路mTOR GCN2和两个通道之间的串扰(62年]。针对氨基酸丰富mTOR激活宿主蛋白质翻译和冠状病毒利用这个细胞机制为自己的蛋白质合成和复制(63年]。患者的高危肥胖有害hyperinflammatory与SARS-CoV-2感染发病率可能相关的一部分多余的氨基酸和mTOR hyperactivation作出有利于环境使用主机的冠状病毒包括SARS-CoV-2转化为病毒复制机器。相比之下,观察到在应对氨基酸饥饿氨基酸传感器GCN2激活下游通路限制炎症和病毒复制(64年,65年,66年]。激活GCN2期间显示限制病毒入侵等病毒感染登革病毒感染,upregulation自噬,抑制促炎细胞因子IL-1β和肠道炎症,降低hyperinflammation和细胞因子风暴64年,65年,66年]。在这种背景下,利用生物活性药物分子激活氨基酸饥饿传感器GCN2可以减少病毒感染和hyperinflammation参与SARS-CoV-2感染患者(66年]。
另一个例子是丝氨酸(Ser)也需要在大量快速增长的细胞(67年,68年,69年]。Ser提供通过吸收细胞的细胞外环境,并通过甘氨酸转氨作用产生的新创或葡萄糖和Glu [70年]。Ser都是跨细胞膜通过sodium-independent中性氨基酸换热器(SLC7A10 / SLC3A2)主要表达在神经细胞膜,或sodium-dependent中性氨基酸交换机SLC1A4 / SLC1A5表示在其他组织。增殖激活免疫细胞是高度依赖于爵士,T细胞的活化和分化需要足够的爵士和饮食Ser限制可以抑制其增殖(68年,71年]。SLC1A5不足会损害辅助T 1的分化(Th1)和Th17细胞和减弱炎症反应通过抑制T细胞receptor-activated mTORC1 [52]。Ser可以从头合成甘氨酸转氨作用的丝氨酸hydroxymethyltransferase (SHMT1/2)或从3 -磷酸甘油酸(3 pg)、一个中间的糖酵解72年]。Ser直接调节适应性免疫通过控制T细胞增殖能力通过提供一个碳单位新创核苷酸生物合成在T细胞增殖71年)和山姆维持一个高代的山姆:S-adenosyl-homocysteine比支持的表观遗传组蛋白的甲基化和一些免疫细胞因子的生产,包括IL-1β。山姆看起来必不可少的炎性巨噬细胞,减少山姆一代具有抗炎效果(73年,74年]。有趣的是,巴尔病毒感染诱发感染细胞NADPH的控制水平维持细胞内Ser水平增加一个碳通量对B细胞增殖(75年]。
以同样的方式,两个加压法氨基酸,必需氨基酸蛋氨酸(满足)和具有氨基酸半胱氨酸(半胱氨酸),也参与免疫调节。半胱氨酸对T细胞增殖的严格要求,因为T细胞缺乏酶转换开会半胱氨酸和必须进口半胱氨酸通过他们的交通系统76年]。半胱氨酸的可用性是至关重要的t细胞功能,与细胞提供(作为抗原递呈细胞”情况)或隔离(尤其是MDSCs)这种氨基酸,分别导致刺激或抑制效应。半胱氨酸加双氧酶(CDO) catabolises半胱氨酸半胱氨酸亚磺酸,并进一步hypotaurine和牛磺酸、或丙酮酸和亚硫酸盐。因此,CDO不仅删除多余半胱氨酸细胞毒性,但也是必要的生产hypotaurine硫酸/牛磺酸和亚硫酸盐/从半胱氨酸77年]。铜的结合,n -乙酰半胱氨酸常秋水仙碱,目前没有相关的实验使用抗病毒药物,已被建议作为一个潜在的治疗SARSCOV-2-infected患者(78年]。此外,帽冠状病毒RNA的结构是由两个病毒甲基转移酶甲基化转移甲基提供S-adenosylmethionine (SAM)。病毒的适当的甲基化水平取决于可用性在主机形成山姆和它提出了限制了可用性治疗Covid-19患者口服重组methioninase [79年]。限制了不仅可以抑制病毒复制,这取决于病毒RNA帽甲基化,但还能抑制感染细胞的增殖,具有增加满足要求。最重要的是,病毒诱导t细胞——macrophage-mediated细胞因子风暴,发病的一个重要原因,也可以被损耗,由于t细胞和巨噬细胞的激活需要的满足。
此外,白介素4-inducible 1酶分泌或局部在溶酶体中,催化作用板式换热器分解代谢主要板式换热器的损耗和生产a-ketoacid phenylpyruvate,过氧化氢和抗菌毒性作用会使相关的生产NH3和碱化的媒介76年,80年]。这些过程导致微生物细菌生长的抑制作用和对T淋巴细胞免疫抑制活动(81年]。
结论
氨基酸代谢和信号流程参与病原体感染的控制和调节炎症激活引起的先天,自适应和调节免疫反应。之间的串扰氨基酸的分解代谢和免疫系统代表了一个重要的免疫反应过程优化和减少hyperinflammation相关感染的免疫反应。氨基酸中,参数可用性和降解酶伊诺参与炎症通过生产没有先天反应,而参数和Trp可用性,两个分解代谢的相关酶__arg1 IDO1,代表参与调节免疫反应和分解代谢过程施加监管影响炎症和适应性免疫反应。此外,氨基酸Gln,爵士,半胱氨酸,满足,和板式换热器也被视为氨基酸参与病原体发展和平衡的免疫反应性。总的来说,多余的氨基酸和mTOR hyperactivation显示为一个环境有利于病毒入侵,而氨基酸饥饿和GCN2激活限制病毒入侵。这些不同的机制代表hyperinflammatory响应相关的潜在治疗靶点控制感染和因果相关病原体引起的发病率和死亡率,包括冠状病毒。
改变历史
2021年7月08
这篇论文已经发表的校正:https://doi.org/10.1038/s41387 - 021 - 00167 - y
引用
格GS。炎症,metaflammation和immunometabolic紊乱。大自然。2017;542:177 - 85。
费AW Jr .)巨噬细胞,脂肪和immunometabolism的出现。中国Investig。2013; 123:4992-3。
Grohmann U, Mondanelli G,颠茄ML, Orabona C,帕太,Iacono, et al .氨基酸传感和降解途径的免疫调节。细胞因子生长因子启2017;35:37-45。
吴G,莫里斯SM Jr .精氨酸代谢:一氧化氮。生化j . 1998; 336:1-17。
小量,Brasse-Lagnel C, Fairand Renouf年代,Lavoinne A Argininosuccinate合成酶从尿素循环citrulline-NO周期。欧元。2003;270:1887 - 99。
Yeramian,马丁·L Serrat N, Arpa L, C太阳系,伯J, et al .精氨酸运输通过阳离子氨基酸转运蛋白2起着至关重要的监管作用,古典或替代激活巨噬细胞。J Immunol。2006; 176:5918-24。
Chang J, Thangamani年代,Kim MH Ulrich B,莫里斯SM Jr .)金CH。视黄酸的发展促进Arg1-expressing树突细胞调节t细胞的分化。J Immunol欧元。2013;43:967 - 78。
Gogoi M,小百货,威尔逊KT Chakravortty d .精氨酸代谢建立发病机制的双重作用。当今Microbiol 2016; 29:43-8。
Bogdan c .一氧化氮和免疫应答。Nat Immunol。2001; 2:907-16。
Dzik JM。进化根精氨酸酶的表达和调控。Immunol前面。2014;5:544。
Munder m .精氨酸酶:一个新兴的关键球员在哺乳动物的免疫系统。Br J杂志。2009;158:638-51。
Saenz Monticelli洛杉矶,巴克博士Flamar l, SA Wojno, Yudanin NA, et al。精氨酸酶1是一个天生的lymphoid-cell-intrinsic代谢检查点2型控制炎症。Nat Immunol。2016; 17:656 - 65。
灰色的乔丹,Poljakovic M, Kepka-Lenhart D,莫里斯SM Jr .感应的精氨酸酶转录DNA通过il - 4需要复合STAT6和C / EBPβ响应元素。基因。2005;353:98 - 106。
勃朗特V, Zanovello p .精氨酸代谢调节免疫反应。Nat Immunol牧师。2005;5:641-54。
雅各布森LC, Theilgaard-Monch K,克里斯滕森EI, Borregaard n .精氨酸酶1表达在白明胶酶中幼粒细胞/晚幼粒细胞和本地化人类中性粒细胞的颗粒。血。2007;109:3084-7。
Rotondo R, Bertolotto M, Barisione G, Astigiano年代,Mandruzzato年代,Ottonello L, et al .胞外分泌嗜苯胺蓝的和精氨酸酶第一颗粒由多形核中性粒细胞激活需要抑制T淋巴细胞增殖。J Leukoc杂志。2011;89:721-7。
Rouzaut Subira毫升,De Miguel C Domingo-de-Miguel E,冈萨雷斯,圣地亚哥E, et al . Co-expression诱导一氧化氮合酶和精氨酸酶在不同的人类单核细胞的子集。细胞凋亡受内生不。Biochim et Biophys学报。1999;1451:319-33。
基尔M,霍夫曼M,不仅仅Schabbauer g蛋白构建块:燃料macrophagepolarization氨基酸及相关代谢途径。2021年2月j。https://doi.org/10.1111/febs.15715。Epub提前打印。PMID: 33460504。
Ricciardolo FL,迪斯蒂法诺、萨巴蒂F, g Folkerts活性氮物种在呼吸道。欧元J杂志。2006;533:240-52。
Perrone洛杉矶,贝尔瑟JA, Wadford哒,Katz JM,汤佩使TM。诱导一氧化氮导致病毒高致病性流感病毒感染小鼠后发病。J感染说。2013;207:1576 - 84。
徐Z, L,王Y,张J,黄L, C, et al .病理发现COVID-19与急性呼吸窘迫综合征有关。柳叶刀》和医学。2020;8:420-2。
Izzo F,蒙特拉M,奥兰多美联社,Nasti G, Beneduce G,加莱G, et al。聚乙二醇精氨酸deiminase降低丙型肝炎病毒滴度和抑制一氧化氮合成。J杂志。2007;22:86 - 91。
Grimes JM,汗,Badeaux M,饶RM,罗林森SW Carvajal RD。精氨酸损耗作为COVID-19患者的治疗方法。Int J感染说。2021;102:566 - 70。
麦克布莱德R, Van Zyl M,菲尔丁的冠状病毒核衣壳是一种多功能蛋白。病毒。2014;6:2991 - 3018。
萨哈P, Banerjee AK,特里帕西PP,斯利瓦斯塔瓦AK,雷,一个已经病毒的病毒:氨基酸突变在印度分离冠状病毒S蛋白COVID-19可能影响受体结合,因此,传染性。Biosci众议员2020;40:BSR20201312。
汗汗,咱,贝格MH,艾哈迈德,法鲁克a e,歌曲YG,等。比较基因组分析新型冠状病毒(SARS-CoV-2)从不同的地理位置和突变的影响主要目标蛋白质:一个在硅片的见解。《公共科学图书馆•综合》。2020;15:e0238344。
霍夫曼M, Kleine-Weber H, Pohlmann s multibasic突起蛋白的裂解位点SARS-CoV-2人类肺细胞的感染是至关重要的。摩尔细胞。2020;78:779 - 84。e5。
Firpo先生,Mounce BC。不同功能的多胺在病毒感染。生物分子。2020;10:628。
Oxenkrug GF。基因和激素调节tryptophan-kynurenine新陈代谢:对血管性认知障碍的影响,重度抑郁症,老化。安n Y科学。2007;1122:35-49。
施瓦茨r .色氨酸犬尿氨酸通路的退化作为药物的目标。当今药物杂志。2004;4:12-7。
Fallarino F Grohmann U, Puccetti p吲哚胺2,3-dioxygenase:从催化剂信号功能。J Immunol欧元。2012;42:1932-7。
Grohmann U,勃朗特诉由氨基酸代谢的控制免疫反应。Immunol启236:243 2010;64年。
百花大教堂,默里PJ。色氨酸和吲哚在免疫调节新陈代谢。当今Immunol 2021; 70:7-14。
Opitz CA, Litzenburger嗯,Sahm F,奥特M, Tritschler我,特朗普年代,et al。一个内生异人类芳基碳氢化合物的配体受体。大自然。2011;478:197 - 203。
Frumento G, Rotondo R, Tonetti M, Damonte G, Benatti U,费拉拉GB。Tryptophan-derived分解代谢物负责抑制T细胞和自然杀伤细胞增殖诱导吲哚胺2,3-dioxygenase。J Exp。2002; 196:459 - 68。
Fallarino F, Grohmann U,黄千瓦Orabona C, Vacca C,比安奇R, et al。调制的色氨酸通过调节性T细胞分解代谢。Nat Immunol。2003; 4:1206-12。
Grohmann U, Puccetti p的共同进化IDO1气道高反应性和在哺乳动物的调控t细胞的出现。Immunol前面。2015;58。
帕洛塔Bessede, Gargaro M MT, Matino D, Servillo G, Brunacci C, et al。芳基碳氢化合物受体疾病控制的公差防御通路。大自然。2014;511:184 - 90。
Boasso, Herbeuval j],哈代啊,安德森SA,多兰MJ, Fuchs D, et al .艾滋病毒抑制CD4 + t细胞增殖诱导吲哚胺2,3-dioxygenase在血浆树突细胞。血。2007;109:3351-9。
Grohmann U, Fallarino F,比安奇R, Orabona C, Vacca C, Fioretti MC, et al。一个缺陷在色氨酸分解代谢损害宽容nonobese糖尿病老鼠。J Exp。2003; 198:153-60。
Grohmann U, Fallarino F, Puccetti p .宽容、DCs和色氨酸:我忙。趋势Immunol。2003; 24:242-8。
帕洛塔Mondanelli G,比安奇R MT, Orabona C, Albini E, Iacono, et al .精氨酸和色氨酸代谢之间的传递途径给予树突细胞免疫抑制特性。免疫力。2017;46:233-44。
奥特曼BJ,斯坦泽,见鬼的简历。从克雷布斯到诊所:谷氨酰胺代谢癌症治疗。Nat牧师癌症。2016;16:619。
凯利D, Wischmeyer PE。谷酰胺在关键的疾病:新见解。当今中国减轻金属底座护理。2003;6:217-22。
王K, Hoshino Y, Dowdell K, Bosch-Marce M,迈尔斯TG,尹浩然,Sarmiento补充谷氨酰胺抑制单纯疱疹病毒再活化。中国Investig。2017; 127:2626-30。
Ananieva大肠瞄准肿瘤生长的氨基酸代谢和抗肿瘤免疫反应。世界生物化学杂志。2015;6:281。
Newsholme EA,考尔德电脑。谷氨酰胺的作用提出一些细胞免疫系统的整个动物和投机的后果。营养。1997;13:728-30。
Cruzat V,马赛Rogero M,诺尔基恩K, Curi R, Newsholme p .谷氨酰胺:代谢和免疫功能、补充和临床翻译。营养。2018;10:1564。
罗伯特•PA Klysz D, Tai X,米特尼克拿出M, Cretenet G, Oburoglu L, et al . Glutamine-dependentα-ketoglutarate调节生产1 T辅助细胞之间的平衡和调节性T细胞生成。Sci信号。2015;8:ra97-ra。
卡尔埃尔,凯尔曼吴GS Gopaul R, Senkevitch E, Aghvanyan, et al .谷氨酰胺吸收和代谢协调调控ERK / MAPK在T淋巴细胞激活。J Immunol。2010; 185:1037-44。
施王R,狄龙CP, LZ, Milasta年代,卡特R,芬克尔斯坦D, et al。转录因子Myc在T淋巴细胞激活控制代谢重编程。免疫力。2011;35:871 - 82。
肖Nakaya M, Y,周X, Chang陶宏根,Chang M,程X, et al。炎症T细胞反应依赖于氨基酸转运ASCT2谷氨酰胺吸收的便利化和mTORC1激酶激活。免疫力。2014;40:692 - 705。
辛克莱LV, Rolf J,埃姆斯里E,这,泰勒点,卡佩尔哒。坐标控制氨基酸运输抗原受体代谢重编程的T细胞分化。Nat Immunol。2013; 14:500-8。
Chang W-K、杨KD、Shaio M-F。谷氨酰胺对Th1、Th2细胞因子的影响人类外周血单核细胞的反应。Immunol。1999; 93:294 - 301。
Horig H, Spagnoli GC, Filgueira L Babst R, Gallati H,更难F, et al .外源性谷氨酸盐的要求是局限于T细胞激活的事件。学生物化学J细胞。1993;53:343-51。
Kudsk KA。路线和营养类型对intestine-derived炎症反应。2003 J Surg.; 185:16-21。
吴G,方- z,杨年代,勒普顿JR,特纳ND。最近的进步营养Sciences-Glutathione新陈代谢及其对健康的影响。J减轻。2004;134:489 - 92。
Lee H-K Uyangaa E, Eo SK。谷氨酰胺和亮氨酸提供增强的保护性免疫粘膜感染单纯疱疹病毒1型。免疫Netw。2012; 12:196。
Bringhurst RM, Dominguez AA,谢弗。谷氨酰胺不足导致增强电镀效率的单纯疱疹病毒1型ICP0-null突变。J微生物学报。2008;82:11472-5。
名字JJ,塞·伐斯冈萨雷斯,他Souza ACR, Favaro WJ。维生素D,锌和谷氨酰胺:协同行动与OncoTherad免疫调制剂在干扰素信号和COVID - 19所示。Int J摩尔。2021;47:11。
Hirabara SM, Gorjao R, Levada-Pires AC,马西LN, Hatanaka E, Cury-Boaventura MF, et al .宿主细胞谷氨酰胺代谢作为一个潜在的抗病毒药物的目标。中国科学。2021;135:305-25。
伊莉斯Rødland G, Tvegard T, Boye E, Grallert b Tor和Gcn2通路之间的串扰响应不同的压力。细胞周期。2014;13:453 - 61。
肥胖和COVID-19 Bolourian, Mojtahedi z: mTOR通路可能是罪魁祸首的证据。ob启2020;21:e13084。
打脚,Afroz年代,Giddaluru J,纳兹,黄W, Khumukcham党卫军,et al .氨基酸饥饿传感挫伤IL-1β生产通过激活riboclustering和自噬。公共科学图书馆杂志。2018;16:e2005317。
Afroz年代,打脚,Giddaluru J,汗n登革热病毒诱导cox - 2信号通过营养传感器GCN2监管。Immunol前面。2020;11:1831。
飞利浦,汗n .氨基酸感应途径:主要检查在肥胖的发病机理和COVID-19。ob启2021;22:e13221。
杨M, Vousden KH。丝氨酸在癌症和一个碳代谢。Nat癌症。2016年,牧师16:650 - 62。
Jain M,尼尔森R,沙玛,Madhusudhan N, Kitami T, Souza, et AL .代谢物分析标识一个甘氨酸在快速癌症细胞增殖的关键作用。科学。2012;336:1040-4。
吴问,陈X,李江,太阳丝氨酸和代谢调节:一个新颖的机制在抗肿瘤免疫和衰老。衰老说。2020;11:1640。
Kalhan SC,汉森RW光碟。丝氨酸的复兴:一个常被忽视但必需氨基酸。生物化学杂志。2012;287:19786 - 91。
马呃,Bantug G,偶联T, Condotta年代,约翰逊RM, Samborska B, et al。丝氨酸是一个重要的效应T细胞扩张的代谢物。细胞金属底座。2017;25:345-57。
Kalhan SC, Uppal穆斯林杰,贝内特C, Gruca噢,Parimi PS, et al .代谢和基因响应限制等热量的蛋白质饮食的老鼠。生物化学杂志。2011;286:5266 - 77。
于W、王Z,张K,气Z,徐T,江D, et al。一个碳代谢支持S-adenosylmethionine和组蛋白甲基化开炎性巨噬细胞。摩尔细胞。2019;75:1147-60。e5。
《瓦尔登湖》,田L,罗斯RL,图片嗯,伯恩DP,赫斯基EL, et al .代谢控制BRISC-SHMT2装配调节免疫的信号。大自然。2019;570:194-9。
王LW,沈H、L诺人我,保罗JA,特鲁多年代,et al。Epstein-Barr-virus-induced一个碳代谢驱动B细胞转变。细胞金属底座。2019;30:539-55。e11。
黄McGaha TL, L, Lemos H,梅斯R, Mautino M, Prendergast GC, et al。氨基酸分解代谢:天然免疫与适应性免疫的关键调节器。Immunol启2012;249:135-57。
植木Stipanuk M,我,Dominy J,西蒙斯C, Hirschberger l半胱氨酸加双氧酶:一个健壮的系统调节细胞半胱氨酸的水平。氨基酸。2009;37:55 - 63。
Andreou撰写,Trantza年代,Filippou D, Sipsas N, Tsiodras S COVID-19:铜和防治作用的潜在作用(NAC)的候选人对SARS-CoV-2抗病毒治疗。体内。2020;34:1567 - 88。
霍夫曼RM,汉族问:口服methioninase Covid-19 methionine-restriction疗法。体内。2020;34:1593-6。
Boulland马丁,Marquet J, Molinier-Frenkel V,穆勒P, Guiter C, Lasoudris F, et al。人类IL4I1分泌L-phenylalanine氧化酶表达的成熟的树突细胞,抑制t淋巴球增生。血。2007;110:220-7。
Puiffe马丁,Lachaise我Molinier-Frenkel V,可以见到效果f .抗菌性能的哺乳动物L-amino酸氧化酶IL4I1。《公共科学图书馆•综合》。2013;8:e54589。
作者信息
作者和联系
相应的作者
道德声明
相互竞争的利益
作者宣称没有利益冲突。
额外的信息
出版商的注意施普林格自然保持中立在发表关于司法主权地图和所属机构。
权利和权限
开放获取本文是基于知识共享署名4.0国际许可,允许使用、共享、适应、分布和繁殖在任何媒介或格式,只要你给予适当的信贷原始作者(年代)和来源,提供一个链接到Creative Commons许可,并指出如果变化。本文中的图片或其他第三方材料都包含在本文的创作共用许可,除非另有说明在一个信用额度的材料。如果材料不包括在本文的创作共用许可证和用途是不允许按法定规定或超过允许的使用,您将需要获得直接从版权所有者的许可。查看本许可证的副本,访问http://creativecommons.org/licenses/by/4.0/。
关于这篇文章
引用这篇文章
多美,d氨基酸代谢和信号通路:在控制感染和免疫的潜在目标。减轻。糖尿病11,20 (2021)。https://doi.org/10.1038/s41387 - 021 - 00164 - 1
收到了:
修改后的:
接受:
发表:
DOI:https://doi.org/10.1038/s41387 - 021 - 00164 - 1