血栓是COVID-19患者死亡率的主要原因。血栓,包括肺栓塞(PE)和深静脉血栓形成(DVT),范围从轻微后遗症SARS-CoV-2感染致命的并发症(1]。有病史的人更容易患血栓和差的结果2]。指南从专业社会使用纤溶治疗(英尺)在COVID-19不一致(3]。英国《金融时报》对ARDS的结果(急性呼吸窘迫综合征)与COVID-19迄今尚未阐明。我们已经总结了105 COVID-19患者溶栓(tPA)。tPA应用溶栓(纤溶,一般肝素)失败后,救助(救助重病患者),或预防性治疗那些有潜在血栓形成(4]。我们比较了发病率,死亡率、并发症,实验室检测COVID-19 ARDS患者和那些没有ARDS (non-ARDS),和纤溶治疗的不良事件。
方法
这个池研究旨在总结纤溶治疗COVID-19的所有报告病例系列。IRB和知情同意不需要批准。所有105个病例的临床特征提出了在桌子上1,和其他的细节都显示在在线补充。结果ICU承认,放电一般病房,住院死亡,或出院回家。单向方差分析连续变量和χ2测试分类变量进行了使用R (v4.0.3)和棱镜9双边层次的意义P< 0.05。结果使用ggplot2包画。
结果
接受来自11个国家和代表多个种族。平均年龄为58.7±14.1年。有一个微不足道的ARDS和non-ARDS团体之间的年龄和性别差异。更多的ARDS组呼吸道疾病被报道。相比之下,没有其他并发症两组(表之间是不同的1)。体育与ARDS患者是tPA的主要迹象,而缺氧中风和心肌梗死non-ARDS non-ARDS集团。tPA的总剂量和频率用于抢救治疗ARDS和non-ARDS团体之间的无关紧要。一些不良事件报告。
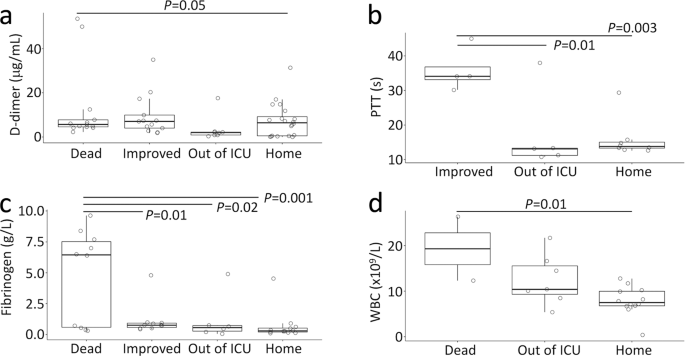
等离子体肺动脉栓塞和纤维蛋白原水平的病人死于高于那些幸存下来的人。ICU患者更高的PTT(表1)。白细胞,PTT、纤维蛋白原和LDH水平升高与non-ARDS相比ARDS患者的三倍。进一步,白细胞计数较低的患者(图中恢复过来。1)。在ARDS患者死亡率高,ICU护理的必要性。减少ARDS患者出院回家。整体开发PE患者的死亡率高得多(39.7%),感染性休克(63.6%),急性肾损伤(75.0%)、财政部(85.7%),心脏骤停和心脏衰竭(72.7%)。ARDS患者中,42%有多个肺栓塞或血栓。急性肾损伤的发生率、呼吸衰竭、和心动过速/颤是ARDS患者更大。
肺动脉栓塞(一个)、PTT (b)、纤维蛋白原(c),白细胞(d纤溶治疗前)水平比较四所有病人的结果。结果没有足够的患者(n< 3)被PTT (c),白细胞(d)。表中描述的缩写的全称1。
讨论
tPA是管理一般在抗凝治疗的失败,包括肝素钠、阿司匹林、伊诺肝素。抗病毒药物、抗生素和支持性护理各种剂量,持续时间、路线和组合应用到一些病人根据自己的条件。高死亡率的发现和ICU护理的必要性COVID-19-associated ARDS可能与预先存在的呼吸道疾病和炎症(5]。COVID-19的致命的并发症,包括体育、休克、心脏衰竭、肾损伤,和财政部,进一步降低存活率。除了白细胞,增加血浆PTT和纤维蛋白原水平可能预示预后不良。考虑一些与纤溶治疗相关的不良事件,早期和tPA的本地应用程序和其他(即。,uPA, plasminogen, plasmin) combined with precisely anti-inflammation interventions to target case-dependent cytokines and chemokines could improve the survival of COVID-19 patients with critically ARDS. By comparison, fibrinolytic therapy for COVID-19 patients without ARDS or other severe complications significantly improves the outcomes [2]。回顾性研究的主要局限是缺乏随机对照组织和标准化的实验室测试程序,临床读数和纤溶治疗。随机对照试验设计测试的好处正在招募患者纤溶治疗。然而,这集中研究分层和预后的影响COVID-19-associated ARDS。
引用
顾顾SX, Tyagi T, Jain K,大众,李SH,华JM, et al .血小板病和endotheliopathy:关键贡献者COVID-19 thromboinflammation。Nat牧师心功能杂志。2021;18:194 - 209。
霁霍奇金淋巴瘤,赵R, Matalon年代,Matthay MA。血纤维蛋白溶酶升高(ogen) COVID-19易感性的一个共同的危险因素。杂志启100:1065 2020;75年。
怀特CS,明日GB,米切尔JL Chowdary P,帽子新泽西。纤溶异常在急性呼吸窘迫综合征(ARDS)和多功能性的溶栓药物治疗COVID-19。J Thromb Haemost。2020; 18:1548-55。
杜安DJ, Shaefi年代,布兰诺SK,古普塔年代,公园,赖特FL,等。组织纤溶酶原激活物与COVID-19危重成人。安Thorac Soc。2021; 18:1917-21。https://doi.org/10.1513/annalsats.202102 - 202127 - rl。
赵R,苏Z, Komissarov AA,刘SL, G, Idell年代,et al .协会承认的肺动脉栓塞和COVID-19病人的临床特征:系统回顾,荟萃分析,多元回归。Immunol前面。2021;12:691249。
确认
这项研究是由国家卫生研究院授予HL134828。
作者信息
作者和联系
贡献
HLJ完全访问所有数据的研究,负责数据的完整性和数据分析的准确性。概念和设计:HLJ。数据的采集、分析或解释:RZ码,HLJ。起草的手稿:RZ, HLJ。关键的修订手稿的重要知识内容:RZ, HLJ。统计分析:HLJ码。获得资助:HLJ和RZ。行政、技术或材料支持:RZ码,HLJ。监督:HLJ。
相应的作者
道德声明
相互竞争的利益
作者宣称没有利益冲突。
权利和权限
关于这篇文章
引用这篇文章
霁,霍奇金淋巴瘤。,Dai, Y. & Zhao, R. Fibrinolytic therapy for COVID-19: a review of case series.学报杂志罪43,2168 - 2170 (2022)。https://doi.org/10.1038/s41401 - 021 - 00827 - w
收到了:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41401 - 021 - 00827 - w