摘要
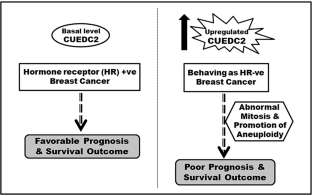
激素受体阳性(HR+ve)亚型内分泌抵抗的发展以及三阴性亚型挑战乳腺癌治疗缺乏明确靶点。促成这种内分泌抵抗的是一种叫做CUEDC2的蛋白质。它能降解激素受体,雌激素受体-α (ERα)和孕酮受体。ERα+ve乳腺癌CUEDC2水平越高,疾病预后越差。它还影响有丝分裂的进程。然而,这两种cuedc2驱动的功能在乳腺癌结局中的相互作用仍然难以捉摸。我们发现CUEDC2在有丝分裂过程中利用有丝分裂泛素化机制降解ERα。我们阐明了CUEDC2有丝分裂特异性磷酸化在这一过程中的重要性。此外,上调的CUEDC2覆盖了有丝分裂阻滞,增加了非整倍体。最后,我们招募了一个乳腺癌的前瞻性队列,发现在HR-ve病例中CUEDC2显著上调。 Moreover, individuals with higher CUEDC2 levels showed a poorer progression-free-survival. Together, our data confirmed that CUEDC2 up-regulation renders ERα+ve malignancies to behave essentially as HR-ve tumors with the prevalence of aneuploidy. This study finds CUEDC2 as a potential prognostic marker and a therapeutic target in the clinical management of breast cancer.
这是订阅内容的预览,通过你所在的机构访问
访问选项
订阅这本杂志
收到12个印刷问题和在线访问
每年259美元
每期只要21.58美元
租或购买这篇文章
只要这篇文章,只要你需要它
39.95美元
价格可能受当地税收的影响,在结账时计算




参考文献
王晓明,王晓明,王晓明,等。2020年全球癌症统计:全球185个国家的36种癌症的发病率和死亡率。中华癌症杂志。2021;71:209-49。
Pandit P, Patil R, Palwe V, Gandhe S, Patil R, Nagarkar R.乳腺癌分子亚型的患病率:2062例患者的单一机构经验。《欧洲乳房健康》,2020;16:39-43。
Saha Roy S, Vadlamudi RK。雌激素受体信号在乳腺癌转移中的作用。国际乳腺癌杂志。2012;2012:654698。
库马尔N,古拉提HK,夏尔马A,希尔S,贾萨尔AK,阿劳拉L,等。最近针对雌激素受体α治疗乳腺癌的策略。Mol Divers. 2021;25:6 3 - 24。
Belachew EB, Sewasew DT。雌激素阳性乳腺癌内分泌抵抗的分子机制。前内分泌(洛桑)。2021; 12:599586。
潘旭,周涛,邰玉华,王超,赵杰,曹颖,等。CUEDC2蛋白表达升高与乳腺癌内分泌抵抗有关。医学杂志,2011;17:708-14。
施宗强,马志强,马志强,王志强,王志强。泛素结合基序在分子内单泛素化反应中的作用。Embo j . 2003; 22:1273-81。
满俊,张晓霞。CUEDC2:炎症和肿瘤发生中一个新兴的关键人物。蛋白质细胞。2011;2:699-703。
高玉峰,李涛,常勇,王一波,张文文,李文华,等。cdk1磷酸化的CUEDC2促进纺锤体检查点失活和染色体不稳定。中国生物医学工程学报。2011;13:924-33。
林春春,李志强,李志强,李志强,等。乳腺癌细胞中雌激素受体α靶基因及反应元件的发现。基因组生物学,2004;5:R66。
王晓燕,王晓燕,王晓燕,等。雌激素诱导细胞周期蛋白D1启动子的研究进展。美国国家科学研究院。1999; 96:11217-22。
王c, Mayer JA, Mazumdar A, Fertuck K, Kim H, Brown M,等。雌激素通过雌激素受体和AP-1转录因子激活的上游增强子诱导c-myc基因表达。《Mol Endocrinol》2011;25:1527-38。
贾凡·莫哈丹,魏华,韩文杰,韩文杰。雌激素受体α具有细胞周期调节作用,并以配体依赖的方式调节细胞周期。细胞周期。2016;15:1579-90。
纺锤体毒素与细胞命运:两种途径的故事。Mol Inter, 2011; 11:41 - 50。
Elmaci, Altinoz MA, Sari R, Bolukbasi FH。磷酸化组蛋白H3 (PHH3)作为脑膜肿瘤的一种新的细胞增殖标志物和预后指标:一篇简短的综述。中华免疫组织化学杂志,2018;26:627-31。
沃森ER,布朗NG,彼得斯JM,斯塔克H,舒尔曼BA。APC/C E3泛素连接酶在细胞分裂中的调控作用。细胞生物学,2019;29:117-34。
Musacchio A, Salmon ED,时空中的纺锤装配检查点。中国生物医学工程学报。2007;8:379-93。
周震,何敏,沙亚安,万艳。APC/C的研究进展:从细胞功能到疾病和治疗。Cell Div. 2016;11:9。
encaracion CA, Ciocca DR, McGuire WL, Clark GM, Fuqua SA, Osborne CK。他莫昔芬治疗乳腺癌患者类固醇激素受体的测定。乳腺癌治疗。1993;26:237-46。
石磊,董斌,李震,卢勇,欧阳涛,李俊,等。ER-{α}36的表达,雌激素受体{α}的一种新变体,以及乳腺癌对他莫西芬治疗的耐药性。中华医学杂志。2009;27:34 - 9。
Musgrove EA, Sutherland RL。乳腺癌内分泌抵抗的生物学决定因素。癌症杂志2009;9:631-43。
Masoud V, page G.乳腺癌靶向治疗:对抗耐药性的新挑战。世界临床肿瘤学杂志,2017;8:120-34。
李志强,李志强,李志强。激素受体阳性乳腺癌的内分泌抵抗机制及治疗方法。前内分泌(洛桑)。2019; 10:245。
李文杰,李志强,李志强,等。雄激素受体过表达诱导人乳腺癌细胞对他莫西芬耐药。乳腺癌治疗。2010;121:1-11。
CJ勋爵,Ashworth A. BRCAness重访。癌症,2016;16:110-20。
Vagia E, Mahalingam D, Cristofanilli M. TNBC靶向治疗的前景。癌症(巴塞尔)。2020; 12:916。
周强,Atadja P, Davidson NE。组蛋白去乙酰酶抑制剂LBH589重新激活沉默的雌激素受体α (ER)基因表达,而不丢失DNA高甲基化。癌症生物学杂志2007;6:64-9。
Brinkman JA, El-Ashry D. ER阴性乳腺癌的ER再表达和内分泌治疗的再敏化。中华肿瘤学杂志。2009;14:67-78。
Saxena NK, Sharma D.雌激素受体的表观遗传再激活:恢复内分泌治疗反应的有希望的工具。生物化学学报。2010;2:191-202。
维苏娜,李ok A,金布尔B, Domek J, Kato Y, van der Groep P,等。Twist通过下调雌激素受体α来促进乳腺癌的激素抵抗。致癌基因2012;31:3223-34。
萨卡尔,高希,班纳吉,梅提,达斯,拉尔森,等。CCN5/WISP-2在正常和肿瘤乳腺细胞中恢复ER-比例变异,并使三阴性乳腺癌细胞对他莫西芬敏感。瘤形成2017;6:e340。
杨晓明,李志强,李志强,李志强,等。乳腺癌患者雌激素受体阴性表型的逆转及抗雌激素反应的恢复。临床癌症杂志2007;13:7029-36。
张培军,赵军,李海燕,满建华,何坤,周涛,等。CUE结构域2调控泛素-蛋白酶体对孕激素受体的降解。Embo j . 2007; 26:1831-42。
瓦苏德万A,舒肯KM,索斯维尔EL,吉里什V,阿德班博OA,谢尔策JM。非整倍体作为恶性生长的启动子和抑制子。癌症,2021;21:89-103。
Ben-David U, Amon A.环境决定一切:癌症中的非整倍体。Nat Rev Genet, 2020; 21:44-62。
卡罗尔JS。雌激素受体(ER)基因在乳腺癌中的调控机制。中国内分泌杂志,2016;17:R41-9。
赵志华,尹淑娟,具杰比,金玉生,李克勤,李志华,等。孕酮受体作为转录因子,在8- br - camp诱导的子宫内膜基质细胞脱基过程中,通过独立激活蛋白激酶a和Ras调节磷脂酶D1的表达。生物化学学报,2011;
确认
我们感谢Gopal C. Kundu博士,NCCS,浦那,和Tanya Das教授,Bose研究所,加尔各答,细胞培养相关的支持。
资金
本研究由科学与工程研究委员会(SERB)部门早期职业奖支持。印度政府科学技术(DST)(文件编号:。ECR/2015/000206)和西孟加拉邦政府科学技术和生物技术部(DSTBT)赠款(FST/P/S&T/9G-21/2016),授予SN。研究项目由大学教育资助委员会资助-初级研究奖学金(教资会编号::771/ csir-ugc net-2017)。SR是ICMR名誉科学家奖学金的获得者。
作者信息
作者及隶属关系
贡献
StR, SS, SR和SN对研究进行了概念化。StR、SS、PC、KSR、CM进行了实验。AG和SB提供临床样本和资料。AR进行组织学评估。StR, SS, CM, SN对数据进行分析。StR和SN根据所有作者的意见撰写了手稿。
相应的作者
道德声明
利益冲突
作者声明没有利益竞争。
伦理批准并同意参与
该研究由印度医学研究委员会(ICMR)监管下的机构伦理委员会(IEC SGCCRI REF NO- 2016/3/4/SN/NON-REG/05/02)批准。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
权利和权限
关于本文
引用本文
罗伊,S,萨哈,S,达尔,D。et al。CUEDC2和ERα之间的分子串扰通过调节乳腺癌有丝分裂影响临床结局。癌症基因Ther29, 1697-1706(2022)。https://doi.org/10.1038/s41417-022-00494-x
收到了:
修改后的:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41417-022-00494-x
