摘要
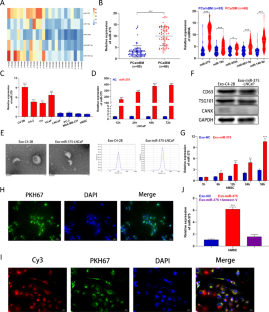
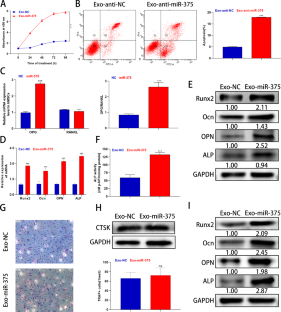
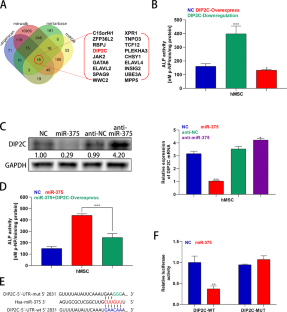
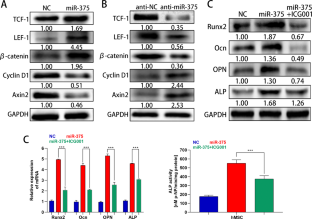
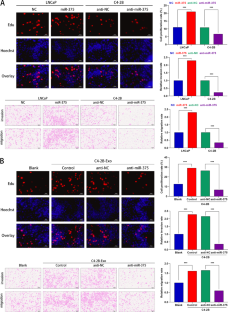
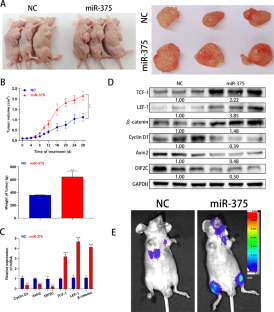
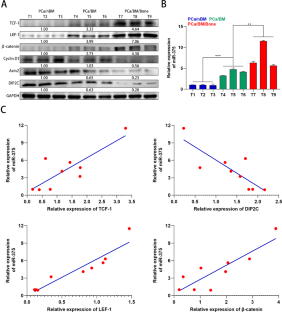
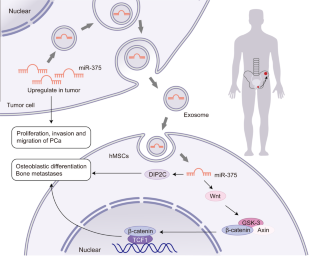
骨转移是导致晚期前列腺癌(PCa)死亡的最常见并发症。然而,前列腺癌骨转移的确切机制尚不清楚。在此,我们探讨了外泌体miR-375在前列腺癌骨转移和肿瘤进展中的作用及其潜在机制。本研究显示,miR-375在骨转移的晚期PCa和转移性PCa细胞系中表达显著上调。此外,miR-375在pc来源的外泌体中表现出高表达,并可通过外泌体传递到人间充质干细胞(hMSCs)。在机制上,miR-375直接靶向DIP2C并上调Wnt信号通路,从而促进hMSCs的成骨细胞分化。此外,miR-375在体外促进PCa细胞的增殖、侵袭和迁移,在体内促进肿瘤进展和成骨细胞转移。值得注意的是,miR-375、TCF-1、LEF-1和β-catenin在有骨转移的PCa组织中的表达高于无骨转移的PCa组织,并呈持续升高的趋势,而DIP2C、cyclin D1和Axin2的表达则相反。总之,我们的研究表明,癌症来源的外泌体miR-375靶向DIP2C,激活Wnt信号通路,促进成骨细胞转移和PCa进展。
这是订阅内容的预览,通过你所在的机构访问
访问选项
订阅期刊
获得1年的完整期刊访问权限
119.00美元
每期只要9.92美元
所有价格均为净价格。
增值税稍后将在结帐时添加。
税务计算将在结账时完成。
买条
在ReadCube上获得时间限制或全文访问。
32.00美元
所有价格均为净价格。
数据可用性
本研究中包括的所有数据均可通过联系通讯作者获得。
参考文献
张晓明,陈晓明,陈晓明。2008年全球癌症负担的预测:全球癌症研究,2008。国际癌症杂志,2010;
Siegel RL, Miller KD, Jemal A.癌症统计,2020。中国癌症杂志。2020;70:7-30。
张晓东,张志强,张志强,等。去势抵抗性前列腺癌的新疗法:疗效和安全性。欧洲,2011;60:279-90。
Suzman DL, Boikos SA, Carducci MA。前列腺癌的骨靶向药物。癌症转移,2014;33:619-28。
桥本K, ohchi H, Sunamura S, Kosaka N, Mabuchi Y, Fukuda T,等。癌症分泌的hsa-miR-940通过靶向ARHGAP1和FAM134A在骨转移微环境中诱导成骨细胞表型。美国国家科学研究院。2018; 115:2204-9。
Dolloff NG, Shulby SS, Nelson AV, Stearns ME, Johannes GJ, Thomas JD,等。人类前列腺癌细胞的骨转移潜能与α血小板衍生生长因子受体激活的Akt/PKB相关。致癌基因。2005;24:6848-54。
戴娟,北川勇,张娟,姚震,米津上A,程晟,等。血管内皮生长因子参与骨形态发生蛋白介导的前列腺癌诱导成骨细胞分化。癌症决议2004;64:994-9。
尹俊杰,Mohammad KS, Kakonen SM, Harris S, Wu-Wong JR, Wessale JL,等。内皮素-1在成骨细胞骨转移发病机制中的作用。美国国家科学研究院。2003; 100:10954-9。
张志刚,张志刚,张志刚,张志刚,等。人骨髓瘤细胞表达的核因子- kappab配体受体激活剂在体外介导破骨细胞形成,并与体内骨破坏相关。癌症决议2003;63:5438-45。
张志刚,张志刚,张志刚,张志刚,等。血小板源性溶血磷脂酸支持乳腺癌骨溶解性骨转移的进展。中国科学(d辑),2004;
Johnstone RM, Adam M, Hammond JR, Orr L, Turbide C.网织细胞成熟过程中的囊泡形成。质膜活性与释放的囊泡(外泌体)的关系。生物化学杂志,1987;
宋永华,张伟,张军。外泌体在肿瘤诊断中的应用。癌症。2017;九8。
叶勇,李世林,马云云,刁玉杰,杨林,苏明明,等。外泌体miR-141-3p调节成骨细胞活性促进前列腺癌成骨细胞转移Oncotarget。2017;8:94834-49。
Hassan MQ, Maeda Y, Taipaleenmaki H, Zhang W, Jafferji M, Gordon JA,等。miR-218指导Wnt信号通路促进成骨细胞分化和转移性癌细胞的骨模拟。中国生物医学工程学报。2012;
段勇,谭志,杨敏,李娟,刘超,王超,等。pc -3衍生的外泌体通过下调miR-214和阻断NF-kappaB信号通路抑制破骨细胞分化。生物医学杂志2019;2019:8650846。
吴小刚,周长峰,张玉梅,闫瑞敏,魏文峰,陈晓军,等。癌源性外泌体miR-221-3p通过靶向THBS2促进宫颈鳞状细胞癌血管生成。血管生成。2019;22:397 - 410。
李少林,安宁,刘波,王淑云,王俊杰,叶艳。LNCaP细胞外泌体通过miR-375转移促进成骨细胞活性。《科学通报》2019;17:4463-73。
刘华,李培文,杨文杰,米华,潘建林,黄玉春,等。从血清外泌体microRNAs鉴定慢性萎缩性胃炎的非侵入性生物标志物。BMC癌症杂志2019;19:129。
车勇,石旭,石勇,姜旭,艾强,石勇,等。过表达mir -143的MSCs衍生的外泌体通过下调TFF3抑制人前列腺癌细胞的迁移和侵袭。《分子科学》2019;18:232-44。
王晓峰,张玉凯,于志生,周建林。血清RANKL/OPG比值在老年患者转子间骨折愈合中的作用Mol Med 2013; 7:1169-72。
于磊,隋波,范伟,雷磊,周林,杨林,等。来自成骨肿瘤的外泌体通过转移col1a1靶向miRNA-92a-1-5p激活破骨细胞分化并同时抑制成骨。中国生物医学工程学报。2021;10:e12056。
Yoneda T, Williams PJ, Hiraga T, Niewolna M, Nishimura R.在体内和体外,寻骨克隆与MDA-MB-231亲本人乳腺癌细胞和寻脑克隆表现出不同的生物学特性。中华骨科学杂志,2001;16:1486-95。
WNT信号在前列腺癌中的表达。地理学报。2017;14:683-96。
Pickl JM, Tichy D, Kuryshev VY,托尔斯泰Y, Falkenstein M, Schuler J,等。Ago-RIP-Seq鉴定Polycomb抑止复合物I成员CBX7是miR-375在前列腺癌进展中的主要靶点。Oncotarget。2016;7:59589 - 603。
甘tq,陈文杰,秦宏,黄森,杨丽华,方悠悠,等。microRNA-375在肺腺癌中的临床价值和潜在通路信号:基于癌症基因组图谱(TCGA)、基因表达综合(GEO)和生物信息学分析的研究医学科学通报,2017;23:2453-64。
叶小明,朱海燕,白卫东,王涛,王林,陈勇,等。miR-375的表观遗传沉默通过靶向IGF1R在her2阳性乳腺癌中诱导曲妥珠单抗耐药。BMC癌症杂志2014;14:134
冢本Y,中田C,野口T,谷川M,阮lt,内田T,等。MicroRNA-375在胃癌中下调,并通过靶向PDK1和14-3-3zeta调节细胞存活。癌症决议2010;70:2339-49。
王艳,Lieberman R,潘杰,张强,杜敏,张鹏,等。miR-375通过靶向SEC23A和YAP1诱导前列腺癌多西紫杉醇耐药。Mol Cancer, 2016;15:70。
塞尔斯LA,达斯R,汤利SL,库蒂尼奥I,汉森AR, Centenera MM,等。ZEB1-miR-375-YAP1通路调控前列腺癌上皮可塑性致癌基因。2017;36:24-34。
崔妮,朴杰,李俊杰,约杰,朴志勇,金e,等。miR-93/miR-106b/ mir -375- cm - crabp1在前列腺癌进展中的新调控轴。Oncotarget。2015;6:23533-47。
Costa-Pinheiro P, Ramalho-Carvalho J, Vieira FQ, Torres-Ferreira J, Oliveira J, Goncalves CS,等。MicroRNA-375在前列腺癌发生中发挥双重作用。临床表观遗传学。2015;7:42。
傅志强,李志强,李志强,等。外泌体和非外泌体泌尿mirna。前列腺癌检测预后。2017;77:573-83。
高勇,郭勇,王智,戴智,徐勇,张伟,等。分析循环miRNAs 21和375作为早期诊断前列腺癌的潜在生物标志物。赘生物。2016;63:623-8。
王志强,王志强,王志强,等。miR-375和尿激酶纤溶酶原激活物受体的联合血清水平被认为是前列腺癌的诊断和预后的生物标志物。国际癌症杂志。2015;137:1406-16。
李志强,李志强,李志强,等。通过深度测序比较肿瘤分期增加的前列腺癌的microRNA分析。Mol Cancer res 2014; 12:250-63。
郑洪辉,裴志强,陈志强,陈志强,等。循环microRNA分析鉴定了一个转移性前列腺癌患者的亚群,并有癌症相关缺氧的证据。科学通报,2013;8:e69239。
胡文娜,刘志强,张志强,等。锌(II)离子处理前列腺癌细胞系中的MicroRNAs和锌代谢相关基因表达中华医学杂志,2012;
Iorio MV, Croce CM。癌症中的MicroRNA失调:诊断、监测和治疗。全面的审查。EMBO Mol Med. 2012; 4:143-59。
McDonald AC, Vira M, Shen J, Sanda M, Raman JD, Liao J,等。血浆中循环的microRNAs作为前列腺癌早期检测的潜在生物标志物。前列腺癌。2018;78:411-8。
Kachakova D, Mitkova A, Popov E, Popov I, Vlahova A, Dikov T,等。血清前列腺特异性抗原和let-7c、miR-30c、miR-141和miR-375血浆表达水平的组合作为前列腺癌潜在的更好的诊断生物标志物。中国生物医学工程学报,2015;
韩玲,林伟东,孙勇。肿瘤微环境中的细胞外囊泡:老故事,但新故事。《Mol Cancer》2019;18:59。
焦欣,Wood LD, Lindman M, Jones S, Buckhaults P, Polyak K,等。Notch、NF-KB、PIK3CA和Hedgehog通路在人乳腺癌中的体细胞突变中华癌症杂志,2012;
李娟,平吉林,马波,陈良,李丽强。DIP2C在乳腺癌中的表达及其临床意义Pathol Res Pr 2017; 213:1394-9。
王晓明,王志强,王志强,王志强,王志强。RKO细胞中DIP2C缺失对DNA甲基化和上皮-间充质转化的影响。BMC癌症杂志,2017;17:487。
资金
本研究由南方医科大学南方医院总统基金资助[批准号:2020B025]。
作者信息
作者及隶属关系
贡献
HSH:概念化;LY与YCM:方法论;HSH:验证;LY、YCM、CSS、LWH:调查;YCM和CSS:资源;YCM:写作——初稿;CSS和LJY:写作-审阅&编辑;CSS和LJY:可视化;LY和LJY:监督;HJL:项目管理; HJL and HSH: Funding acquisition.
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
伦理认可和同意参与
所有小鼠实验均经南方医院动物伦理委员会批准(批准号:;nfyy - 2019 - 1227)。
发表同意书
这篇文章是原创的,还没有在期刊上发表过,目前也没有被其他期刊考虑。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
权利和权限
根据与作者或其他权利持有人签订的出版协议,自然或其许可方(例如,社会或其他合作伙伴)对本文拥有排他性权利;作者对这篇文章接受的手稿版本的自我存档仅受此类出版协议的条款和适用法律的约束。
关于本文
引用本文
刘勇,杨超,陈森,刘勇。et al。癌症来源的外泌体miR-375靶向DIP2C,并通过调节Wnt信号通路促进成骨细胞转移和前列腺癌进展。癌症基因Ther(2022)。https://doi.org/10.1038/s41417-022-00563-1
收到了:
修改后的:
接受:
发表:
DOI:https://doi.org/10.1038/s41417-022-00563-1
