摘要
背景及目标
便秘是最常见的胃肠疾病之一,尤其是在老年人中。本研究旨在评估选定的多菌株益生菌对生活在养老院的老年人的功能性便秘和实验室血液参数的有效性和安全性。
研究对象与方法
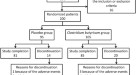
60名符合资格标准的功能性便秘患者(42名女性,18名男性),年龄77.9±8.84岁,完成了研究。在双盲、安慰剂对照、平行设计中,每个参与者随机接受所选的益生菌混合物(N= 28)或安慰剂(N作为他们日常饮食和药物的辅助治疗,持续12周。该液体益生菌配方含有双歧杆菌animalis无性系种群。lactisBLC1,嗜酸乳杆菌LA3和干酪乳杆菌首次对BGP93进行了测试。
结果
与安慰剂相比,补充选定的益生菌导致累积大便频率轻微但不显著增加。然而,在治疗的第71天之后,益生菌组的累积大便数显著增加(P当排除泻药的影响时,< 0.05)。两组之间的差异在益生菌干预1周后开始增加,这表明益生菌的影响是长期的。在27项实验室血液参数测试中,治疗和时间对大多数参数没有显著的依赖或独立影响。
结论
多菌种益生菌补充被发现是有效的,安全的和耐受性良好的老年人功能性便秘。
简介
便秘是老年人中最常见的慢性疾病之一。它的患病率随着年龄的增长而上升,在女性中更常见。在一些自我报告便秘的研究中,65岁或以上的女性中有26%和男性中有16%认为自己便秘,而在84岁的患者亚组中,受影响的比例在女性中增加到34%,在男性中增加到26% [1].便秘在养老院居民中更为常见。多项描述性研究显示,约半数居民患有慢性便秘,其中56-75%定期服用泻药[2].慢性疾病数量多、多药率高与便秘显著相关。此外,长者身体虚弱,常与行动不便、进食不足及脱水有关,亦会引致便秘[3.].慢性便秘对健康相关的生活质量有不利影响,精神和身体状况显著下降。它还对患者和国家卫生服务构成经济负担[4].
功能性便秘的病理生理学是多因素的,包括饮食、结肠运动和吸收、肛肠运动和感觉功能以及行为和心理因素[5].尽管越来越多的循证研究证明了各种疗法的有效性,但仍有近一半的患者对其症状的改善不满意,并担心安全性、不良反应、不便和味道[6,7].在这种背景下,在过去的十年中,益生菌治疗便秘的有效性的调查已经被注意到。最近对15个随机对照试验的荟萃分析表明,益生菌,如双歧杆菌属,乳酸菌而且链球菌菌株,减轻功能性便秘在成人增加大便频率,肠转运时间和粪便的一致性。多菌种益生菌被发现对便秘症状的有益作用比单一菌种益生菌更显著[8].因此,用特定的益生菌菌株改变肠道腔内环境可能会影响肠道的运动和分泌,并为功能性便秘患者提供益处[9].此外,最近的证据表明,肠道菌群在慢性低度炎症中起着关键作用,是年龄老化和各种年龄相关疾病最一致的生物学特征之一。在对健康老年人与住院或住院的老年患者进行比较的研究中,发现了肠道菌群组成谱的差异[10].益生菌的临床疗效已被发现取决于微生物菌株。它们的混合物似乎比单一菌株益生菌的效率更高,因为多菌种益生菌的作用可能是互补或协同的[11,12,13].
综上所述,本随机对照试验旨在评价多菌种益生菌对养老院老年人功能性便秘和实验室血液参数的疗效和安全性。这项研究的假设是益生菌对患有慢性便秘的老年人的排便频率有有益的影响。在本研究中,我们首次使用了含有双歧杆菌animalis无性系种群。lactisBLC1,嗜酸乳杆菌LA3和干酪乳杆菌BGP93。
研究对象与方法
研究参与者
共有67名65岁或以上的老年养老院居民,根据罗马IV标准定义功能性便秘,并能够理解该程序,符合纳入研究的条件。有梗阻性肠梗阻诊断或病史、怀疑或确诊结肠易激综合征、溃疡性结肠炎、克罗恩病或恶性消化道疾病、近一个月内任何原因的腹泻、近一个月内未使用抗生素治疗的急性感染性疾病以及药物治疗中使用阿片类镇痛药物的受试者被排除在研究之外。患有功能性便秘并符合纳入研究条件的居住家庭用户被参考协议细节。在向他们解释了研究的目标和潜在的好处和风险后,他们签署了知情同意书,确认了他们的自愿参与。
补充配方组成
含有益生菌制剂嗜酸乳杆菌La3 (1 × 109CFU / g),双歧杆菌animalis无性系种群。lactisBLC1 (1.5 x 109CFU / g)干酪乳杆菌Bgp93 (2 × 109CFU/g)为液体口服制剂,便于随食物口服9滴。它是由制药有限公司生产的。在克罗地亚萨格勒布(克罗地亚市场上以PROBalans SENIOR drops的名称出售),从未在任何患者队列中进行过正式研究。安慰剂治疗含有中链甘油三酯油,从椰子油或棕榈油中提取的分馏油,其有效含量为辛酸(C8)和癸酸(C10)甘油三酯+二氧化硅,外观、药物形式和给药途径与主动治疗相同。
每日九滴的剂量不少于1 × 109益生菌在生产日期的CFU。根据安全性和有效性报告中列出的研究,该剂量已显示出对人体肠道的积极影响。为了确保产品在整个保质期内的稳定性,制造时的起始剂量接近6.25 × 109CFU/9滴(基于每种益生菌的使用量及其在制造材料中的声明强度)。由于本品是悬浮在油基中的粉末,保证每日推荐用量不小于1 × 109CFU,根据所制备悬液的密度和制药有限公司在制造本产品时使用的瓶子组件,选择9滴作为日剂量。
研究设计和方案
2018年12月至2019年2月,在克罗地亚Vrbovec的Saint Camillus de Lellis养老院进行了一项单中心、随机、双盲、安慰剂对照试验。第一个研究阶段是招募期,在此期间对受试者进行监测,主要是为了确定排便频率和一般健康状况,没有进行额外的治疗。4周后,他们重新评估纳入和排除标准,并向符合条件的患者提供了研究过程的详细信息。符合纳入标准的患者进入第二阶段,并随机分为安慰剂组(N= 32)或益生菌(N=研究的一部分。采用计算机生成的算法进行随机干预。由于编码和液体配方的模糊性,参与者、调查人员和统计人员对益生菌和安慰剂的身份一无所知。
参与者被指示在接下来的12周内,除了目前的治疗外,每天一次(在正餐之前)服用9滴液体口服配方。选择12周的研究时间主要是基于我们之前对测试产品的经验,这些经验表明,治疗几周后就会产生初步效果,而大约10周后就会产生完全效果。每天监测和记录每位受访者的粪便频率,包括额外的一周,以评估益生菌干预的长期效果。主要反应变量是每个受试者在研究期间的累计大便次数。所有其他变量都被认为是次要的。参与者在基线和干预12周后进行了两次静脉血取样。对采集的血液样本进行表中所列27项实验室血液参数分析2:高敏c反应蛋白(hsCRP)、葡萄糖(Glu)、维生素B12 (B12)、叶酸(Fol)、甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)、天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、γ谷氨酰转移酶(GGT)、碱性磷酸酶(ALP);及在补充表格内S3:白细胞(WBC)、红细胞(RBC)、血红蛋白(hbg)、红细胞压积(HCT)、平均红细胞体积(MCV)、平均红细胞血红蛋白(MCH)、平均红细胞浓度(MCHC)、血小板(PLT)、红细胞分布宽度(RDW)、平均血小板体积(MPV)、中性粒细胞百分比(Neuts)、淋巴细胞百分比(lymphos)、单核细胞百分比(Monos)、嗜酸性粒细胞百分比(Eos)和嗜碱性粒细胞百分比(Baso)。监测如此大量的血液参数的基本原理是评估安全性,即,我们想确认测试产品不会对血液参数造成重大干扰。
数据收集
研究小组由三名学术成员、一名全科医生、一名护士和一名社区药剂师研究员组成,负责开展工作,并根据纳入标准检查参与研究的每个受试者是否符合纳入标准。通过查阅入院文件、医疗记录和采访居民和家庭医务人员来检索居民数据。由社区药剂师研究员收集每位居民的标准人口统计学和人体测量学特征、当前和过去的病史、常规处方和非处方药物、药物过敏史和药物不良反应、血清生化参数、肾功能和血压。研究期间保持了参与者的生活习惯(饮食习惯、体育活动和液体摄入)和泻药bisacodyl。疗养院的营养学家决定所吃食物的数量和种类。由于参与者的个人偏好和各种伴随疾病,存在个体差异。然而,这两个研究小组在饮食方面完全具有可比性。护理人员和社区药剂师研究员在第二天早上记录益生菌组和安慰剂组中每个个体受访者的每日粪便数量。在护理之家的救护车上夜间禁食10-12小时后采集静脉血样本,并在萨格勒布杜布拉瓦临床医院实验室诊断科进行分析。
统计分析
样本量软件(2017年,NCSS, LLC,美国犹他州凯斯维尔,ncss.com/software/pass)用于样本量计算分析。最初的计算是基于在同一疗养院进行试验的初步研究。试点研究包括两组8名居民,他们分别接受安慰剂或verum制剂,最终目的是比较90天试验期后的累积大便数量。使用alpha=0.05和幂(1 - beta)为0.90的参数,估计所需的最终样本量为每组21人。
使用Statistica软件包(TIBCO software Inc., 2018)分析从研究中获得的数据。由于进行了大量的分析,应用了对多重性的校正,统计显著性水平设置为0.01。对于连续变量,采用Kolmogorov-Smirnov检验检验其分布的正态性,并采用相应的参数或非参数检验。使用独立样本的t检验比较人口统计学结果和参与者特征。结果以参加者人数(N),中位数(IQR),在P< 0.05。使用Mann-Whitney U检验检测两个研究组之间每天的累积大便量。P附属表的数值S1而且S2显示这些测试的结果。
结果
参与者的基线特征
最初,67名居民接受了资格评估并参加了这项研究。在研究期间,7名参与者去世,并被排除在进一步分析之外。没有一例死亡可归因于整个研究过程中提供的补充剂。60名参与者(42名女性,18名男性),年龄78岁(65-98岁),患有功能性便秘,符合资格标准,完成了这项研究。他们毫无困难地遵循了研究方案,并报告在食用益生菌或安慰剂后没有任何副作用。基线参数分析显示,两组在所有人口统计学和人体计量学参数上相似(表2)1).
益生菌对功能性便秘的作用
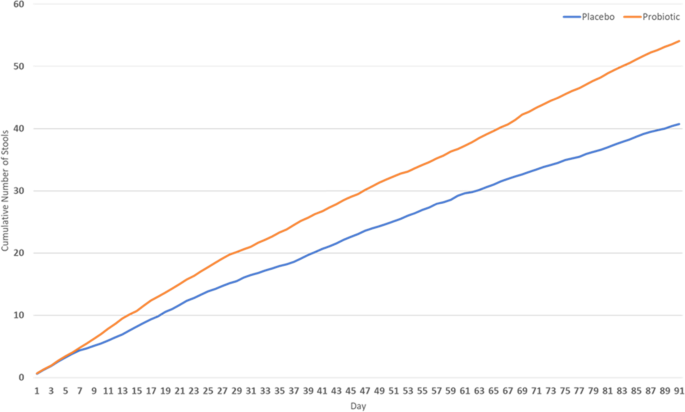
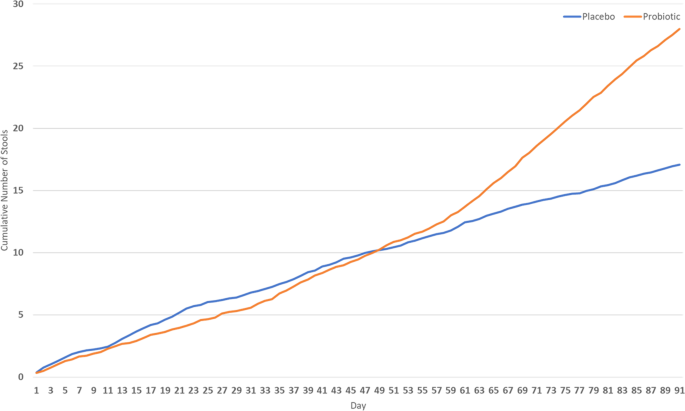
累计排便次数在益生菌组之间具有可比性(平均消耗48;31-70次,累计排便次数54次)和安慰剂(平均消耗38次;29-53,累积排便数41)组,在91天的研究(图。1).第一周后,与安慰剂组相比,益生菌组的大便数量持续增加,但两组之间没有显著差异。然而,两组之间的差异有增加的趋势。P数值范围从0.994(第一周)到0.090(上周)。两组受试者服用的泻药数量相似,安慰剂组的平均摄入量为16(9-28)(泻药数量为33),益生菌组的平均摄入量为18(9-33)(泻药数量为29)(P= 0.665)。Bisacodyl通常用于治疗便秘,其他泻药很少使用。在排除了参与者服用泻药的数据后,再次比较了两组的累计大便次数。结果如图所示。2,前6周观察到两组粪便数累积值相似。两组之间的差异开始增加,有利于益生菌,并在治疗的第71天后达到统计学意义(P< 0.05)。完整的资料P数值见补充资料(补充表格)S1而且S2).
益生菌对实验室血液参数的影响
共处理了27项实验室血液参数。评估了益生菌组和安慰剂组在治疗内和治疗间的所有血液参数的差异。表格2列示12个选定参数的值,其他参数见补充表S3.两种干预措施的实验室参数值在基线时无显著差异。在大多数情况下,治疗和时间对血液参数变化没有显著的依赖和独立影响。在使用益生菌期间,在治疗中发现葡萄糖(P= 0.018)和B12 (P= 0.019),以及胆固醇(P= 0.032)和LDL (P= 0.043)S3).
安全性和耐受性
在研究期间,安慰剂组和益生菌组在血液学或生化安全参数上没有显著差异(表2)2及补充表S3).干预前后平均值均在临床参考范围内。两组均未观察到不良事件。耐受性非常好,在整个研究过程中,两组样本的测试率均为100%,没有因服用益生菌或安慰剂而退出。
讨论
据我们所知,这是第一个临床试验,以证明有效性和安全性的液体益生菌配方含有双歧杆菌animalis无性系种群。lactisBLC1,嗜酸乳杆菌LA3和干酪乳杆菌BGP93。这种多菌种益生菌组合显示出增加养老院老人排便频率的趋势,尽管没有统计学意义。我们的主要结果是检查所选益生菌菌株对累积粪便数量的影响。虽然两组之间没有显著差异,但益生菌组的累积大便数始终高于安慰剂组P从第二周到干预期结束,各指标有逐渐下降的趋势。此外,当两组之间的累积粪便数进行比较时,排除了受访者使用泻药时的数据,在治疗的第10周达到了统计学上的显著差异。在益生菌干预一周后,两组之间的差异呈增加趋势,表明益生菌干预的效果延长。我们的研究结果表明,需要长期摄入这些益生菌才能对便秘症状产生显著效果,同时使用泻药可能会降低益生菌的效果。这与最近的研究结果一致,即益生菌和泻药的联合治疗对功能性慢性便秘儿童没有任何加性作用[14].虽然我们的主要目标是在不改变生活习惯(如规律饮食和泻药摄入)的情况下,在现实生活实验中评估选定的益生菌混合物如何影响功能性便秘,但重要的是要强调便秘可能受到膳食纤维摄入的显著影响。在最近的一项荟萃分析中,高纤维饮食与较低的便秘患病率有关[15].另一项荟萃分析发现,短链β-果聚糖补充剂显著增加了排便频率[16,17,18].
最近的证据支持肠道菌群在功能性便秘的发病机制和治疗中的作用。双歧杆菌和乳酸菌的水平下降,而双歧杆菌和乳酸菌的数量增加拟杆菌门便秘的受试者与健康对照组相比15,19].然而,之前的临床试验对益生菌对功能性便秘的影响给出了不同的结果,这可能部分是由于益生菌的不同菌株和剂量,参与者的临床异质性,以及试验的设计和持续时间。用BB-12和GCL2505菌株进行的研究双歧杆菌animalis无性系种群。lactis(syn。双歧杆菌lactis)对增加人体肠道中双歧杆菌总数具有临床相关益处[14],以及排便频率低的健康受试者的排便频率和腹部不适[20.,21].的剂量反应效应双歧杆菌lactisHN019对成人全肠转运时间和功能性胃肠症状的影响[15],但在另一项研究中未得到证实[22].最近的随机临床试验表明,补充双歧杆菌lactisNCC2818并没有显著缩短整个肠道转运时间,也没有影响其他便秘相关的结果和成人粪便微生物群的变化[23].饮用含有益生菌的饮料干酪乳杆菌Shirota可显著改善慢性便秘患者自我报告的便秘严重程度和大便一致性[24].由不同菌株的双歧杆菌和乳酸菌组成的一些配方也已被纳入临床试验。虽然无统计学意义,但多菌种益生菌混合组成嗜酸乳杆菌DDS-1,双歧杆菌animalis无性系种群。lactisUABla-12,双歧杆菌longumUABl-14和双歧杆菌bifidumUABb-10比安慰剂更早地帮助调节肠道功能,相应的转变为更多的纤维溶菌群[25,26].此外,含有聚葡萄糖的酸奶产品,双歧杆菌lactisHN019和嗜酸乳杆菌与对照组相比,NCFM显著缩短了结肠转运时间[24].
我们的研究最初假设,在慢性便秘的老年人中观察到的益生菌的有益作用与调节与年龄相关的肠道菌群失衡和改善免疫反应有关,这是次要结果。衰老的一个共同特征是先天和后天免疫功能下降,随后血液中典型促炎介质浓度增加,如急性期蛋白、细胞因子和粘附分子('炎症')[27].这种现象是老年人发病和死亡的一个高度重要的危险因素。低级别炎症的许多可能的触发因素已经被提出,从功能失调的线粒体和随之而来的氧化应激到肠道菌群的不平衡。通过选择性地改变有益与有害的微生物种类来治疗肠道细菌,可以逆转炎症反应并恢复粘膜稳态[7,27,28].hsCRP被认为是一种非常敏感的炎症、感染和组织损伤的系统标记物。许多研究表明血清hsCRP水平升高与衰老及衰老相关疾病有关[29,30.].我们的研究还表明,大多数受访者的血清hsCRP水平升高(>3 mg/L),表明存在慢性低度炎症。尽管与安慰剂组相比,益生菌组的hsCRP水平有所下降,但这在统计学上并不显著。这些发现并不完全符合最近一项荟萃分析的结果,该分析表明益生菌显著降低了血清中hsCRP和促炎细胞因子的浓度[31].相反,一些研究报告说,补充益生菌对血清hsCRP水平没有显著影响[32].
维生素B12缺乏症的患病率随着年龄的增长而增加,特别是在体弱多病和住院治疗的受试者中,但由于其临床表现很微妙,因此往往不被认识到。这可能很严重,特别是从神经精神病学和血液学的角度来看[33,34].益生菌,大多属于属乳酸菌而且双歧杆菌属,为宿主提供多种健康益处,包括维生素B的产生[35].考虑到这一点,益生菌组和安慰剂组进行了比较,在接受测试的多菌株益生菌治疗12周后,发现B12水平显著增加(P= 0.019)。相比之下,叶酸作为晚年生活中最常见的维生素缺乏症也没有治疗效果(表2).
从以往的研究中可知,食用某些益生菌菌株可以改善各种疾病和状况的脂质代谢[36,37].我们的益生菌干预没有影响TC、LDL和HDL胆固醇水平,这与其他一些研究的结果一致[38,39].最近的荟萃分析表明,益生菌干预降低了高胆固醇血症成人的TC和LDL水平,但没有发现益生菌对甘油三酯和HDL水平的显著影响。亚组分析表明,益生菌的功效因菌株而异[40].
双歧杆菌和乳酸菌对高血糖患者代谢控制的积极影响已被报道[41,42].一项荟萃分析表明,补充益生菌可能有助于降低高基线水平(≥7 mmol/L)的成年人的空腹血糖(FBG),多物种益生菌可能比单一物种益生菌对FBG的影响更大[43].因此,我们的研究显示,补充益生菌后FBG水平有轻微但显著的降低(P= 0.019)。
根据血液学、生化和不良事件的情况,本研究测试的益生菌混合物在12周的治疗期间表现出良好的耐受性和安全食用,这与其他研究人员此前报道的数据一致[12,25,44].
在这项研究的局限性中,最重要的一个是所包括的受试者数量有限,这是单中心设计的结果。尽管这个设计有缺点,但我们还是选择了它,因为我们希望在年龄、性别、习惯、病史和其他相关参数方面有尽可能同质的人群。日常护理方案、饮食和伴随药物消费的差异是支持单中心设计而不是多中心方法的其他理由。虽然这意味着所包括的受试者数量是有限的,但我们认为受试者数量和人口同质性之间的权衡平衡了这一决定。我们还受到这样一个事实的指导,即比较两组间的累积大便次数是可能的,因为两个研究组的规模、服用泻药的总量和研究的持续时间在两个研究组之间是可比较的。
我们的研究结果表明,选择多菌株益生菌可以作为一种辅助治疗工具,以治疗老年养老院居民的功能性便秘。本文的结果与其他支持多菌株益生菌补充剂对便秘症状优于单一益生菌的研究结果一致,这可能归因于具有不同活性的不同菌株之间的协同相互作用[8].补充一种新的和原始的液体配方含有动物双歧杆菌亚种。lactisBLC1,嗜酸乳杆菌LA3和干酪乳杆菌BGP93有效、安全、耐受性好。通过对两个研究组的累积大便数进行统计分析,证实了试验的初始假设。主要的兴趣分析是比较受试者在不服用泻药的日子里大便的次数。的P在补充材料(补充表)中列出的值S2)清楚地证实了组间差异的统计学意义。然而,还需要进一步的长期、多中心、随机、对照研究来阐明所选益生菌对老年人功能性便秘患者的大便频率和转运时间,以及肠道菌群和轻度炎症的影响。
数据可用性
数据可以在已发表的文章及其补充文件中找到。索取资料请发邮件至KFŠ。
参考文献
Gallegos-Orozco JF, fox - orenstein AE, Sterler SM, Stoa JM。老年人慢性便秘。美国胃肠病学杂志,2012;107:18-26。https://doi.org/10.1038/ajg.2011.349.
罗克MV,波拉斯EP。老年患者慢性便秘的流行病学和管理。中国医学杂志。2015;10:919-30。https://doi.org/10.2147/CIA.S54304.
De Giorgio R, Ruggeri E, Stanghellini V, Eusebi LH, Bazzoli F, Chiarioni G.老年人慢性便秘:胃肠病学家的入门。BMC Gastroenterol. 2015;15:130。https://doi.org/10.1186/s12876-015-0366-3.
弗拉赫J,郭克斯M,范德华MB,克拉森E,拉尔森a。老年机构慢性便秘患者补充益生菌的经济潜力。PharmaNutrition。2018; 6:198 - 206。https://doi.org/10.1016/j.phanu.2018.10.001.
Basilisco G, Coletta M.慢性便秘:综述。《挖掘肝脏》2013;45:89 - 93。https://doi.org/10.1016/j.dld.2013.03.016.
Dimidi E, Christodoulides S, Fragkos KC, Scott SM, Whelan K.益生菌对成人功能性便秘的影响:随机对照试验的系统综述和荟萃分析。中华临床医学杂志,2014;30(4):366 - 366。https://doi.org/10.3945/ajcn.114.089151.
李志强,李志强,李志强,等。慢性便秘文献综述。医学(巴尔的摩)。2018; 97: e10631。https://doi.org/10.1097/MD.0000000000010631.
张C,江J,田F,赵J,郝主任H、翟Q,等。益生菌对成人功能性便秘影响的随机对照试验的meta分析临床营养学杂志,2020;39:2963-9。https://doi.org/10.1016/j.clnu.2020.01.005.
Dimidi E, Christodoulides S, Scott SM, Whelan K.益生菌和胃肠道微生物群对肠道运动和便秘的作用机制。Adv Nutr, 2017; 8:484-94。https://doi.org/10.3945/an.116.014407.
布福德太瓦。相信你的肠道:与年龄相关的炎症、健康和疾病中的肠道微生物组。微生物。2017;5:80。https://doi.org/10.1186/s40168-017-0296-0.
老年人使用益生菌的微生物区系和有效性综述。世界临床病例杂志。2015;3:156。https://doi.org/10.12998/wjcc.v3.i2.156.
Martínez-Martínez MI, Calabuig-Tolsá R, Cauli O.益生菌治疗老年人便秘的效果:一项系统综述。老年医学杂志,2017;71:142-9。https://doi.org/10.1016/j.archger.2017.04.004.
Ohkusa T, Koido S, Nishikawa Y, Sato N.肠道菌群与慢性便秘:综述与更新。Front Med. 2019;6:19。https://doi.org/10.3389/fmed.2019.00019.
久保田M,伊藤K,富本K,金崎M,筑山K,久保田A,等。这种乳酸菌DSM 17938和氧化镁在功能性慢性便秘儿童中的作用:一项双盲和随机临床试验。营养。2020;12:225。https://doi.org/10.3390/nu12010225.
陈震,彭勇,史强,陈勇,曹林,贾静,等。中国罗马标准功能性便秘患病率及危险因素:系统回顾和荟萃分析front Med. 2022;9:815156。https://doi.org/10.3389/fmed.2022.815156.
李志刚,李志刚,李志刚。β-果聚糖对肠道功能的影响:系统综述和meta分析。营养。2019;11:91。https://doi.org/10.3390/nu11010091.
帕塔萨拉斯,陈杰,陈旭,贾宁,Connor HM, Wolf PG,等。女性慢性便秘患者结肠黏膜菌群与粪便、症状、结肠转运和甲烷产生的关系胃肠病学。2016;150:367 - 79。https://doi.org/10.1053/j.gastro.2015.10.005.
Anzawa D, Mawatari T, Tanaka Y, Yamamoto M, Genda T,高桥S,等。含合生素的效果双歧杆菌animalis无性系种群。lactisGCL2505和菊粉对肠道双歧杆菌的影响:一项随机、安慰剂对照、交叉研究。食品科学,2019;7:1828-37。https://doi.org/10.1002/fsn3.1033.
Dimidi E, Mark Scott S, Whelan K.益生菌与便秘:作用机制,患者和医疗保健专业人员有效性和利用的证据。Proc Nutr Soc 2020; 79:147-57。https://doi.org/10.1017/S0029665119000934.
Eskesen D, Jespersen L, Michelsen B, Whorwell PJ, Müller-Lissner S, Morberg CM。益生菌菌株的作用双歧杆菌animalis无性系种群。lactis, BB-12®对排便频率低且腹部不适的健康受试者排便频率的影响:一项随机、双盲、安慰剂对照、平行组试验中国生物医学工程学报,2015;https://doi.org/10.1017/S0007114515003347.
Waller PA, Gopal PK, Leyer GJ, Ouwehand AC, Reifer C, Stewart ME,等。的剂量反应效应双歧杆菌lactisHN019对成人全肠转运时间和功能性胃肠症状的影响Scand J Gastroenterol. 2011;46:10 - 57。https://doi.org/10.3109/00365521.2011.584895.
Ibarra A, Latreille-Barbier M, Donazzolo Y, Pelletier X, Ouwehand AC。28天疗效双歧杆菌animalis无性系种群。lactis补充HN019对功能性便秘成人结肠转运时间和胃肠道症状的影响:一项双盲、随机、安慰剂对照和剂量范围试验肠道微生物,2018;9:236-51。https://doi.org/10.1080/19490976.2017.1412908.
Dimidi E, Zdanaviciene A, Christodoulides S, Taheri S, Louis P, Duncan PI,等。随机临床试验:双歧杆菌lactisNCC2818益生菌vs安慰剂,以及对慢性便秘患者肠道转运时间、症状和肠道微生物的影响。中国医药科学。2019;49:251-64。https://doi.org/10.1111/apt.15073.
Koebnick C, Wagner I, Leitzmann P, Stern U, Zunft HJF。含益生菌饮料干酪乳杆菌Shirota可改善慢性便秘患者的胃肠道症状。《胃肠病学杂志》2003;17:655-9。https://doi.org/10.1155/2003/654907.
Martoni CJ, Evans M, Chow CET, Chan LS, Leyer G.益生菌产品对功能性便秘患者排便习惯和微生物特征的影响:一项随机对照试验。J Dig Dis 2019; 20:45 - 46。https://doi.org/10.1111/1751-2980.12797.
Magro DO, De Oliveira LMR, Bernasconi I, De Souza Ruela M, Credidio L, Barcelos IK,等。含聚葡萄糖的酸奶,嗜酸乳杆菌NCFM和双歧杆菌lactisHN019:一项针对慢性便秘的随机、双盲对照研究。张勇,2014;13:7 7。https://doi.org/10.1186/1475-2891-13-75.
李志强,李志强,李志强,杨志强,Doré,等。衰老中低度炎症(炎症)的改变和营养的作用的健康相关性。老龄化决议Rev. 2017; 40:95-119。https://doi.org/10.1016/j.arr.2017.09.001.
胡珀LV,利特曼DR,麦克弗森AJ。微生物群和免疫系统之间的相互作用。科学。2012;336:1268 - 73。https://doi.org/10.1126/science.1223490.
Jayedi A, Rahimi K, Bautista LE, Nazarzadeh M, Zargar MS, Shab-Bidar S.炎症标志物与发生高血压的风险:队列研究的荟萃分析。心。2019;105:686 - 92。https://doi.org/10.1136/heartjnl-2018-314216.
裴克特A,凯泽K,梅尔兹J,曼哈特L, Schäfer I, Hilgendorf I,等。冠心病的残余炎症风险:真实世界队列中高敏感CRP升高的发生率临床研究。2020;109:315-23。https://doi.org/10.1007/s00392-019-01511-0.
Milajerdi A, Mousavi SM, Sadeghi A, Salari-Moghaddam A, parhan M, Larijani B,等。益生菌对炎症生物标志物的影响:随机临床试验的荟萃分析欧洲营养学杂志,2020;59:633-49。https://doi.org/10.1007/s00394-019-01931-8.
Mazidi M, Rezaie P, Ferns GA, Vatanparast H.益生菌对血清c反应蛋白浓度的影响:随机对照试验的系统回顾和荟萃分析。营养。2017;9点。https://doi.org/10.3390/nu9010020.
Marchi G, Busti F, Zidanes AL, Vianello A, Girelli D.老年人钴胺素缺乏。地中海血液病感染杂志2020;12:2020043。https://doi.org/10.4084/MJHID.2020.043.
田中平,李志强,李志强。B族维生素缺乏的临床意义。中华临床生化杂志,2020;https://doi.org/10.3164/jcbn.20-56.
罗茜,李丽娟,李丽娟。益生菌生产叶酸的研究进展。营养。2011;3:118-34。https://doi.org/10.3390/nu3010118.
López-Moreno A, Suárez A, Avanzi C, Monteoliva-Sánchez M, Aguilera M.调节肥胖相关微生物菌群失调的益生菌菌株和干预总剂量:系统综述和荟萃分析。营养。2020;12:1-29。https://doi.org/10.3390/nu12071921.
Koutnikova H, Genser B, Monteiro-Sepulveda M, Faurie J-M, Rizkalla S, Schrezenmeir J,等。细菌益生菌对肥胖、糖尿病和非酒精性脂肪肝相关变量的影响:随机对照试验的系统回顾和荟萃分析英国医学杂志2019;9:e017995。https://doi.org/10.1136/bmjopen-2017-017995.
艾维KL,霍奇森JM,科尔DA,汤普森PL,斯托切斯基B,王子RL。酸奶及其益生菌对血压和血脂的影响随机对照试验。中华心血管病杂志2015;25:46-51。https://doi.org/10.1016/j.numecd.2014.07.012.
李y, Ba Z, Roberts RF, Rogers CJ, Fleming JA,孟H,等。的影响双歧杆菌animalis无性系种群。lactisBB-12®对健康年轻人血脂/脂蛋白谱和短链脂肪酸的影响:一项随机对照试验2017;16:39。https://doi.org/10.1186/s12937-017-0261-6.
莫锐,张旭,杨艳。益生菌对高胆固醇血症成人血脂谱的影响:随机对照试验的荟萃分析。医学临床(Barc)。2019; 152:473 - 81。https://doi.org/10.1016/j.medcli.2018.09.007.
Kocsis T, Molnár B, Németh D, Hegyi P, Szakács Z, Bálint A,等。益生菌对2型糖尿病患者有有益的代谢作用:一项随机临床试验的荟萃分析科学通报2020;10:11787。https://doi.org/10.1038/s41598-020-68440-1.
Łagowska K, Malinowska AM, Zawieja B, Zawieja E.通过补充益生菌改善孕妇葡萄糖代谢取决于妊娠糖尿病状况:荟萃分析。科学通报2020;10:1-17。https://doi.org/10.1038/s41598-020-74773-8.
Nikbakht E, Khalesi S, Singh I, Williams LT, West NP, Colson N.益生菌和合生素对血糖的影响:对照试验的系统回顾和荟萃分析。中国营养学杂志,2018;57:95-106。https://doi.org/10.1007/s00394-016-1300-3.
Mego M, Holec V, Drgona L, Hainova K, Ciernikova S, Zajac V.接受化疗和放疗的癌症患者中的益生菌。补充Ther Med 2013; 21:712-23。https://doi.org/10.1012/j.ctim.2013.08.018.
确认
作者要感谢Vladimir Trkulja教授博士在设计研究时的帮助,以及Jerko jakiich, MPharm,对本试验中使用的益生菌的技术支持和捐赠。
作者信息
作者及隶属关系
贡献
KFŠ对研究的概念化和设计、数据分析和展示做出了贡献,并进行了研究。SV-K对结果的解释做出了贡献,并起草和编辑了手稿。PH有助于数据分析和解释以及结果的呈现。IM对数据分析和演示做出了贡献。LS对手稿的关键修改做出了贡献。DV对研究的概念化和设计、结果的解释和对手稿的批判性修改做出了贡献。所有作者都同意提交最终的文章版本。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
伦理批准
该研究方案由Saint Camillus de Lellis机构的伦理委员会和萨格勒布大学药学和生物化学系伦理委员会批准(文献编号:643-03/17-01/01)。这项研究遵循了赫尔辛基宣言和东京宣言的指导方针。该试验在ClinicalTrials.gov上注册为NCT04506801。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
Šola, K.F., vladimir - knezevich, S., hrabatec, P.;et al。多菌株益生菌对老年人功能性便秘的影响:一项随机对照试验。Eur J clinin Nutr76, 1675-1681(2022)。https://doi.org/10.1038/s41430-022-01189-0
收到了:
修改后的:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41430-022-01189-0