摘要
帮助家庭沟通遗传性癌症风险的干预措施有可能改善家庭癌症结局。本综述旨在评估在遗传学诊所中采用的先证者介导的干预措施的有效性,以增加对高危亲属的遗传风险披露。检索MEDLINE、Embase、CINAHL、PubMed和PsycINFO在1990-2020年间的出版物。对研究质量进行评估。从回顾的5605份记录中,9项研究(4项随机对照试验和5项队列研究)纳入了患有糖尿病的家庭BRCA1, BRCA2以及林奇综合症。干预提供模式包括遗传咨询与额外的电话或亲自随访、信件、视频和决策辅助。高危亲属的比例通知在干预组和家庭调解组,先证者的风险范围为54.0% ~ 95.5%。在知情的人中,24.4-60.0%联系遗传学诊所和22.8 - -76.2%在基因诊所接受咨询后进行基因检测.一项研究报告了干预组和对照组在所有三项结果上的显著差异,另一项研究报告了与亲属联系遗传学诊所的差异。这些研究表明,有针对性的遗传咨询加上额外的随访,可以增加知情亲属和联系遗传诊所的亲属的比例,但并不是最终的结果。随着种系检测的增加,干预措施需要考虑到家庭沟通过程,并通过与先验者和亲属的接触来解决披露后变量(例如,亲属的看法、情绪反应),以最大限度地提高识别家族中遗传癌症风险的公共卫生效益。

简介
在鉴定广泛遗传性疾病的病因方面,特别是关于癌症易感生殖系致病变异方面,已经取得了迅速的进展。虽然可变,但传统上估计癌症的遗传贡献为5-10%,然而,最近的数据表明,由于常见和罕见的变异,它可能高达33% (95% CI, 30-37%) [1].致病变异的发现影响了临床实践和结果,为个人提供个性化的癌症风险评估,并建议加强监测或降低风险的策略,以提高生存率。
在无症状个体中检测致病变异有可能挽救生命。然而,由于致病性变异在一般人群中的总体患病率较低,在一般人群中对所有种系变异进行普遍检测是不可行的,而且成本过高[2].因此,级联检测,即直接检测已知致病变异的亲属,是临床遗传服务采用的主要方法[2].在对亲属进行检测之前,必须向家人披露遗传结果。然而,这可能会产生问题,因为信息的传播往往留给先证者(家庭中接受遗传咨询和/或基因检测的第一个人),他通常被要求将基因检测的可用性告知其有风险的亲属。风险亲属基于遗传亲缘关系分为一级亲缘关系(与特定个体有50%相同DNA的亲属;父母、子女和兄弟姐妹)或二级(有25%相同DNA的亲戚;祖父母、孙子孙女、姨妈/叔叔、同父异母兄弟姐妹和侄女/侄子)或第三级亲属(DNA相同12.5%的亲属;近亲)。
先证者在披露时会遇到许多挑战。常见的障碍包括由于移民、分居、死亡或冲突而与一些家庭成员失去联系[3.].先证者也可能面临情感障碍,如内疚、焦虑、担心给亲人造成负担或害怕关系破裂[3.,4].其他障碍则与缺乏语言技能、受教育程度低、先证者误解及知识不足,或依赖其他亲属承担传播责任有关[5].尽管报告的披露率从中等到较高不等[6,7,8,9,10],随后对知情亲属进行的基因检测仍不理想。在一项已知乳腺癌致病变异家族的传播研究中(乳腺癌易感基因1或BRCA2),整体披露率为90%,但其后亲属的测试率为57% [11].BRCA检测率较低的亲属的一些特征包括:年轻亲属、男性亲属、父系亲属,包括二级或三级亲属[11].
帮助先证者提供有关年轻、男性和有风险的远方亲属的风险的信息和教育,可能会解决一些障碍。
通过克服先证者面临的挑战,遗传学诊所与有风险的亲属直接接触的直接介导方法(DMA)似乎在传播信息方面是有效的[12].然而,仍然存在隐私和机密性障碍,阻碍DMA的广泛实现。因此,许多遗传中心目前并没有法律权力凌驾于患者传播其遗传结果的自主权之上[13]及/或指引并未强制要求披露[14].此外,许多国家没有立法支持来维持遗传登记,而这是确保全面和有效地进行DMA所必需的。因此,先证者仍有责任向家庭通报遗传风险。鉴于这种情况,重要的是综合关于先证者介导的干预措施的现有数据,这些干预措施解决了障碍,并支持先证者与亲属就遗传结果进行沟通,以更好地支持他们完成这一艰巨的任务。
因此,本文的目的是回顾先证者介导的干预对增加风险亲属遗传风险披露的有效性,与三个主要结果相关:
有风险的亲属告知其风险的比例
高危亲属联系基因诊所的比例
高危亲属在基因诊所接受咨询后进行基因检测的比例
材料与方法
数据库搜索过程
数据库(MEDLINE, Embase, CINAHL, PubMed和PsycINFO)在标题和摘要中使用适当的MeSH术语和关键词进行搜索,使用以下术语:[干预或((决策或沟通)和(辅助或工具或仪器)]和家庭和[癌症或肿瘤或遗传学]。我们将搜索结果导出到EndNote X9 (Thomson Reuters)进行筛选。最终搜索于2020年11月进行,之后对所有纳入的研究进行了滚雪球式的搜索(包括通过参考文献列表向后检索,以及通过谷歌Scholar索引的引用向前检索)。评审遵循系统评审和元分析的首选报告项目指南[15](补充档案1).
纳入和排除标准
如涉及下列事项,则列入:
- 1.
家庭沟通:先证者与高危亲属之间关于亲属癌症遗传风险和/或生殖系基因检测的沟通。
- 2.
干预:临床可实施的干预,至少有一个组成部分集中在改善家庭披露或教育先证者与亲属谈论遗传性癌症。干预措施包括教育资源(决策辅助、网站)和/或遗传咨询策略。
- 3.
研究设计随机对照试验(rct)、单臂和非随机对照试验。
- 4.
遗传条件:遗传性乳腺癌(乳腺癌易感基因1或BRCA2)和遗传性非息肉病性结直肠癌(HNPCC;林奇综合征)
- 5.
结果:重点关注干预后的三个结果:1)被告知风险的风险亲属的数量,2)联系遗传诊所的风险亲属的数量,3)在遗传诊所咨询后进行基因检测的风险亲属的数量
- 6.
在1990年至2020年期间发表在同行评审的期刊上,以寻找DNA检测引入临床实践后的相关论文。
下列条款被排除:
- 1.
处理与配偶和亲属的一般通信。
- 2.
没有涉及生殖系基因检测。
- 3.
是一种医疗干预,其目的不在于协助先证者与亲属沟通。
- 4.
是会议记录、评论或评论。
- 5.
研究是否包括旨在改善家庭沟通的干预措施,但仅提供定性结果数据或提供无法提取先证者特定数据的总分。
数据提取
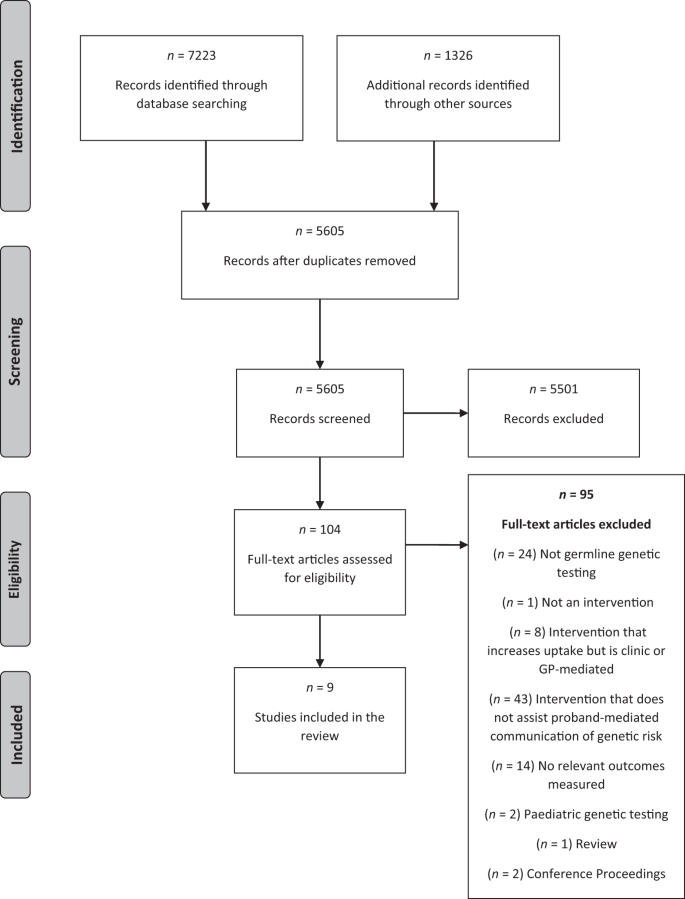
去除重复后,我们鉴定出5605篇文章(图。1).两名作者(A.L.Y.和M.J.S.)根据收录标准独立筛选了标题和摘要(评分者之间的一致性为91%),讨论后解决了分歧。审查了105篇全文文章,最终9篇文章符合纳入标准。其中两人是通过滚雪球式的搜索找到的。三位审稿人(A.L.Y, m.j.s., A.I.)独立地从这九项研究中提取数据,并交叉检查提取结果以确认其可靠性。提取研究设计、样本特征(干预组和对照组),包括先证者告知、联系遗传学诊所、随后进行基因检测的高危亲属的比例和统计差异。对于有多种疾病的文章,我们联系了作者,以获得更多的数据和分析BRCA或林奇综合征的风险。将研究干预特征制成表格,并根据回顾目标中的三个结局类别对数据进行比较。
质量分析
唐斯和布莱克[16两名审稿人(A.L.Y, M.J.S.)独立使用了随机和非随机医疗干预研究的检查表,以评估研究的方法学报告质量。差异通过讨论解决(Cohen’s Kappa = 0.91)。各研究的质量评分列于表中1并被定义为:有限(<50%),足够(50-70%),良好(71-80%),或强(>评分80%)。
结果
在本综述中纳入的9项研究中(图。1)有4项随机对照试验和5项非随机研究。7项研究专门评估先证者的干预措施BRCA一项研究评估了对Lynch综合征患者的干预。其余两项研究包括BRCA以及伴有其他遗传疾病的Lynch综合征,这些都没有包括在最终分析中。研究特征和结果总结于表中1.与研究问题相关的三个主要结果测量结果载于表中2- - - - - -4和如下所述。平均质量分数[16]的比例为65%(范围为41-89%)。从质量评分超过70%的研究中得出的结果和结论被认为更有分量[17,18,19,20.].
干预组件
所描述的大多数干预措施涉及一两次基因咨询预约[21,22]或预约额外的电话遗传谘询[17,18]或披露后的延长会议[19].具体的沟通技巧包括动机性访谈[17]和罗伯特·巴克曼的[23]六步“突发坏消息”模式[19,20.].两项研究采用了多成分干预(面对面遗传咨询、书面资源和电话支持)[20.,24].两项研究是书面决策辅助,要么使用“直面癌症风险”(FORCE)资源,要么使用“共享风险信息工具”[2,25].两项研究比较了基因诊所与高危亲属直接接触(DCA)与家庭介导方法(FMA;先证者发起联络)[21,22].为了本综述的目的,FMA数据是所报告的干预成分和结果的重点。
结果1:被告知患病风险的高危亲属人数
六项研究提供了干预后知情亲属数量的衡量(表2)2).四项研究的干预措施包括增加/或加强基因咨询[17,19,20.,24]和两项研究评估了书面决策辅助[2,25].五项研究进行了标准的遗传咨询控制[2,19,20.,24,25]另一组没有接受心理咨询,作为对照组[17].干预组知情亲属的报告百分比为54.0-95.5%。一项研究[24]报告了显著的干预效果。福雷斯特等人。24]发现,当先证者得到强化的遗传咨询(具体的谱系讨论,在结果披露后2-4周致电索引患者,提供如何与亲属联系的指导,并提出直接或通过索引患者向亲属分发信件),以鼓励家庭沟通有关疾病的信息时,更大比例的风险亲属得到了通知BRCA和/或Lynch综合征的风险,与对照组相比(分别为75%和34%,Pearsonχ2(1) = 18.0,p< 0.001)。
结果2:接触遗传学诊所的高危亲属数量
三项研究报告了干预后与遗传学诊所联系的高危亲属的数量(表2)3.).三种干预措施各不相同,其中包括两种侧重于披露的遗传学诊所预约[22],并增设三次电话遗传辅导[18]或多成分干预[24].据报道,干预组中亲属联系遗传学诊所的比例为24.4%至60.0%。一项研究有显著的结果[24].福雷斯特等人。24报告称,更大比例的高危亲属联系诊所寻求帮助BRCA干预组在干预后24个月与对照组相比(分别为60.0%对29.8%;皮尔森χ2(1) = 9.7,p= 0.002)。
结果3:遗传咨询后进行基因检测的高危亲属人数
六项研究提供了干预后基因检测摄取的测量(表4).
干预措施包括一两次基因咨询预约[21,22],并增设电话遗传谘询服务[18]、两份书面决策辅助文件[2,25],或多成分干预[24].据报道,在遗传学诊所接受咨询并随后进行预测性基因检测的高危亲属的百分比在22.8%至76.2%之间(不包括异常值)。有两项研究是异常值。Sermijn等人[22有53%(47/89)的亲属在先证法介导的情况下主动寻求预测性遗传咨询,98%(46/47)的患者进行了预测性基因检测。辅导。加西亚等人。[2]在肿瘤外展访问中招募患者,提供关于家庭沟通的书面材料,尽管所有22例患者都与亲属进行了沟通,但只有1名亲属在6个月后进行了后续检测(1/22;4.5%)。福雷斯特等人。24在排除州际转诊的亲属后,干预组的亲属检测率高于对照组(53.3%对25.5%,Pearsonχ2(1) = 18.0,p< 0.001)。
讨论
本综述的目的是检验先证者介导的干预对改善高危亲属遗传风险披露的有效性。干预效果的三个主要结果被考虑:有风险的亲属被告知的数量,联系遗传学诊所的数量,以及在遗传学诊所接受咨询后进行基因检测的数量。在符合纳入标准的九项研究中,只有四项研究质量良好[17,18,19,20.只有一项研究[24]报告了所有三个结果变量的显著差异,另有一项研究[18]报告遗传学诊所就诊的重要发现。这些发现强调需要进行更多高质量的研究来衡量医疗保健干预的结果,以支持先证沟通,以提高风险亲属对基因检测的认识、沟通和接受。
四项确定的研究为随机对照试验,采用干预措施,由医疗保健专业人员(即遗传咨询师、专科护士或训练有素的心理社会工作者)提供以家庭沟通为重点的遗传咨询。两项研究使用了“突发坏消息”[23模型[19,20.],或在最初的基因辅导课程中作为独立的干预措施[19]或由护士额外访视,并辅以一套其他资料(例如小册子、录像带、病历副本及家谱)[20.].另外两项研究提供电话咨询,一项作为标准咨询研究的辅助,分三个时间点进行(增加剂量)[18],或在两个时间点上,首先根据患者的总结信,探讨已分享的内容,其次,如果存在障碍,则进行头脑风暴解决方案[17].
没有一项随机对照试验报告有显著增加的风险亲属的信息披露和接受检测BRCA及林奇综合症[18].基线披露率[2,17]及披露的动机[19,20.,24]在一些研究中较高,这可能会影响纳入研究的干预措施增加价值的能力。另一种可能是干预的组成部分与标准护理没有足够的不同,特别是如果干预包括增加咨询的剂量[19),这就很难证明差异。
由Forrest等人进行的一项回顾性队列研究[24],在所有三种结果中都有显著的结果,评估了与对照组接受的咨询明显不同的干预措施。干预措施包括详细的、有意的遗传咨询,包括谱系审查、记录和尚未通知的亲属的讨论,讨论沟通障碍和潜在解决方案,以及在两个时间点进行电话随访。根据先证者联系风险亲属的程度,在最后的随访时间点,先证者可选择向亲属提供一封致亲属的信,或直接向亲属提供一封。虽然参与率很低,但研究结果表明,有意提供咨询以提高知情和接受测试的亲属比例是有效的。然而,鉴于该研究的样本量较小[24],需要进一步的研究来重复这些发现。
进行谱系审查和解决家庭沟通障碍的技能是遗传顾问的技能,这些技能很容易适用于标准的遗传咨询预约[13].需要进一步的研究来探索与遗传顾问以外的医疗保健专业人员进行干预的可行性。心理学家、护士、社会工作者也可以为遗传学诊所提供额外的支持,使先证者具备与亲属沟通的技能,特别是在主流化越来越普遍的情况下[26].
福雷斯特等人。24研究还表明,总结重要遗传结果的信件可能会有所帮助,特别是当先证者对自己清楚准确地传达这些结果的能力缺乏信心时。重要的是,需要对遗传学诊所(DCA)通过信件直接接触的研究与Forrest等人使用的家庭介导方法(FMA)进行区分。比较这两种方法的研究[21]发现DCA和FMA实践在心理困扰方面没有差异,而且使用DCA方案的基因检测的使用率更高[22].然而,这些研究中使用的DCA协议最初依赖于先证者在从遗传学诊所发送信件之前联系亲属[21,22],这是一个模拟FMA协议所遵循的协议的过程[24].事实上,遗传学诊所必须遵守有关是否使用纯DCA方案的立法和指南[13,14].
在已确定的研究中存在一些局限性,需要在未来的研究中加以解决。首先,考虑到只有四项研究是随机对照试验,需要更严格的研究,有足够的能力来检验假设,以确定提高披露率的最佳实践。其次,需要考虑首选的主要结果。目前一些研究的主要结果包括遗传风险知识、自我效能、风险感知和动机。虽然这些都是重要的过程变量,但使用审计和调查数据衡量客观结果(如本次综述评估的三个结果变量)也很重要[24].第三,需要很好地描述对照条件(特别是涉及标准遗传咨询的条件),以便识别干预组和对照组之间的关键差异[2,17,24].第四,考虑到一些纳入的研究报告了较高的基线披露率,针对面临沟通困难的家庭进行招募可能会增加发现干预效果的可能性。我们理解上的这种差距可能会发现干预措施缺乏的领域,包括但不限于考虑亲属的看法、假设和经验。从家庭交流文献中,我们知道先证者在得知他们的测试结果时的情绪反应,以及他们随后的预防决定,有时会描绘出一幅黯淡的未来图景,而他们的孩子不希望遵循这一图景[3.].分享感言和家庭小组会议可以让亲戚们考虑其他人的经历。此外,干预措施可以针对已知检测率较低的某些高危亲属群体,例如父母血统中的亲属和男性亲属。可以通过像胡子月基金会(the Movember Foundation) (https://movember.com)以及参与视觉和社交媒体平台。
目前审查的局限性也需要考虑。所提供内容的可变性,特别是标准护理程序、对照组/对照组、随访频率、结果和已确定研究中高危亲属的定义,不允许对试验结果进行定量综合。知情的风险亲属的百分比是基于先证者的自我报告,它提供了真实知情数量的代理,因为直接接触亲属是不道德的。此外,亲属被告知的百分比取决于先证者被告知的百分比。非英语进行的研究被排除在外,因此一些相关论文可能被省略。
总之,有限数量的干预措施已经衡量了改善向家庭成员披露遗传风险的干预措施的有效性。有意的遗传咨询实践,包括谱系审查和改善沟通的策略,以及额外的随访,可以提高患有遗传性遗传病的家庭的披露率BRCA以及林奇综合症。然而,这方面的发现很少,没有随机对照试验显示出显著的结果。鉴于许多研究报告了较高的披露率,但亲属之间的检测吸收率较低,未来的研究应侧重于检查披露后变量(例如,亲属对检测结果的感知和理解,对其家庭成员的决定的情绪反应),以确定这些是否对高危家庭成员的基因检测构成障碍。使用流程模型,如Lafrenière等人开发的流程模型。[27]提供了一个框架,以了解基因检测结果传达给家庭成员的过程。有针对性的干预可以借鉴定性研究,在干预前发展阶段使用模型,不仅关注先证者的披露内容,还关注先证者所传达的情绪或情绪、决策过程和亲属的反应。随着基因检测的增加以及对遗传学诊所解决家庭沟通问题的需求,这仍然是进一步研究的关键领域。
数据可用性
数据共享不适用于本文,因为在本研究中没有创建或分析新的数据。
代码的可用性
在这项研究中产生或分析的数据可以在已发表的文章及其补充文件中找到,以及作者的请求。
参考文献
Mucci LA, Hjelmborg JB, Harris JR, Czene K, Havelick DJ, Scheike T,等。北欧国家双胞胎癌症的家族风险和遗传性。《美国医学协会杂志》上。2016; 315:68 - 76。https://doi.org/10.1001/jama.2015.17703
Garcia C, Sullivan MW, Lothamer H, Harrison KM, Chatfield L, Thomas MH,等。增加遗传性乳腺癌和卵巢癌级联检测的机制:在遗传咨询中引入标准化沟通辅助的影响。《妇产科杂志》2020;46:1835-41。
Young AL, Butow PN, Rhodes P, Tucker KM, Williams R, Healey E,等。跨代谈话:关于BRCA1和BRCA2基因癌症风险的家庭沟通。《热内法典》2019;28:516-32。https://doi.org/10.1002/jgc4.1055
McGarragle KM, Hare C, Holter S, Facey DA, McShane K, Gallinger S,等。调查家庭成员间结直肠癌风险状况的沟通和亲属对结肠镜检查的反应:一项定性研究。癌症临床实践2019;17:16https://doi.org/10.1186/s13053-019-0114-8
希利E,泰勒N,格林宁S,韦克菲尔德CE,沃里克L,威廉姆斯R,等。在澳大利亚BRCA家庭中,量化家庭传播和识别风险信息沟通的障碍。Genet Med. 2017; 19:1323-31。https://doi.org/10.1038/gim.2017.52
张EL, Olson AD, Yu TM, Han PZ, Beattie MS. 1103例高危女性BRCA结果和家庭检测的交流。癌症流行病学生物标记,2010;19:2211-9。https://doi.org/10.1158/1055-9965.EPI-10-0325
Aktan-Collan KI, Kääriäinen HA, Kolttola EM, Pylvänäinen K, Järvinen HJ, Haukkala AH,等。与下一代分享遗传风险:突变阳性父母与Lynch综合征后代的沟通。2011; 10:43-50。https://doi.org/10.1007/s10689-010-9386-x
Pentz RD, Peterson SK, Watts B, Vernon SW, Lynch PM, Koehly LM,等。遗传性非息肉病性结直肠癌家庭成员对告知义务的认识和卫生专业人员在传播遗传信息中的作用Gen Test, 2005; 9:261-8。
石井N,新井M,小山Y,上野M,山口T,风间K,等。鼓励Lynch综合征患者家属寻求医疗评估的影响因素癌症杂志,2011;10:649-54。
李志强,李志强,李志强,等。癌症基因检测的患者沟通结果在不同的人群中。交通行为医学。2018;8:85-94。https://doi.org/10.1093/tbm/ibx010
芬利E, Stopfer JE, Burlingame E, Evans KG, Nathanson KL, Weber BL,等。在已知BRCA1/2突变的家庭中决定结果传播和接受基因检测的因素。Gen Test, 2008; 12:81-91。https://doi.org/10.1089/gte.2007.0037
孟科,李志强,李志强,等。遗传性乳腺癌和Lynch综合征的症状前基因检测:文献的系统回顾和临床实践的意义。2018; 18:127-35。https://doi.org/10.1007/s10689-018-0089-z
Young AL, Butow PN, Tucker KM, Wakefield CE, Healey E, Williams R.什么时候发布消息,谁负责?一项关于卫生专业人员关于BRCA遗传癌症风险披露的观点的横断面定性研究。英国医学公开赛2020;10:e033127https://doi.org/10.1136/bmjopen-2019-033127
Dheensa S, Fenwick A, Shkedi-Rafid S, Crawford G, Lucassen A.遗传医学中医疗保健专业人员对患者亲属的责任:实证研究的系统回顾和综合。Genet Med. 2016; 18:290-301。
Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD,等。PRISMA 2020声明:报告系统评价的最新指南。BMJ。2021; 372: n71。
Downs SH, Black N.为评估卫生保健干预的随机和非随机研究的方法学质量创建检查表的可行性。流行病学与社区卫生杂志,1998;52:377-84。https://doi.org/10.1136/jech.52.6.377
Eijzenga W, de Geus E, Aalfs CM, Menko FH, Sijmons RH, de Haes HCJM,等。如何支持癌症遗传学顾问告知有风险的亲属?随机对照试验的经验教训。患者教育计数2018;101:1611-9。https://doi.org/10.1016/j.pec.2018.05.009
Hodgson J, Metcalfe S, Gaff C, Donath S, Delatycki MB, Winship I,等。一项旨在改善家庭沟通的复杂遗传咨询干预的随机对照试验结果。《欧洲学报》,2016;24:356-60。https://doi.org/10.1038/ejhg.2015.122
Montgomery SV, Barsevick AM, Egleston BL, Bingler R, Ruth K, Miller SM,等。准备个人沟通基因检测结果的亲属:一项随机对照试验的报告。2013; 12:537-46。https://doi.org/10.1007/s10689-013-9609-z
Roshanai AH, Rosenquist R, Lampic C, Nordin K.在癌症遗传咨询中增强信息是否能提高咨询师对风险亲属的知识、风险感知、信息满意度和协商?一项随机研究。学报学报。2009;48:499 - 1009。https://doi.org/10.1080/02841860903104137
Aktan-Collan K, Haukkala A, Pylvänäinen K, Järvinen HJ, Aaltonen LA, Peltomäki P,等。直接接触邀请遗传性结肠癌家族的高危成员进行遗传咨询和DNA测试。中华医学杂志2007;44:732-8。https://doi.org/10.1136/jmg.2007.051581
张志刚,张志刚,张志刚,张志刚,等。BRCA1/2基因突变家庭介入咨询程序的影响:有效性和安全性。癌症。2016;15:155-62。https://doi.org/10.1007/s10689-015-9854-4
巴克曼R.如何宣布坏消息。多伦多:多伦多大学出版社;2017.
福雷斯特·勒,伯克·J,巴克·S,阿莫尔·DJ。增加遗传咨询支持可以改善家庭遗传信息的交流。Genet Med. 2008; 10:167-72。https://doi.org/10.1097/GIM.0b013e318164540b
卡戴珊A, Fehniger J, Creasman J,张E, Beattie MS.遗传性乳腺癌和卵巢癌综合征家庭共享风险信息工具(ShaRIT)的初步研究。中华癌症杂志2012;10:4https://doi.org/10.1186/1897-4287-10-4
观点:从遗传咨询到基因组咨询的进化。欧洲医学杂志2019;62:288-9。https://doi.org/10.1016/j.ejmg.2019.04.010
Lafrenière D, Bouchard K, Godard B, Simard J, Dorval M. BRCA1/2基因检测后的家庭沟通:仔细观察过程。《热内计数》,2013;22:323-35。https://doi.org/10.1007/s10897-012-9559-x
确认
感谢对他们的数据进行重新分析的作者:Jan Hodgson, Jo Burke和David Amor。
资金
这项研究没有获得任何财政资助。开放获取基金由CAUL及其成员机构支持和组织。
作者信息
作者及隶属关系
贡献
概念化:ALY, PB, KT;数据策划:ALY、AI、MJS、JH、LF;形式分析:ALY, AI, MJS, JH, LF;考察:ALY、AI、MJS、KT、CW、RW、PB;资源:阿里;可视化:AI, MJS;写作-初稿:ALY、AI;撰稿编辑:ALY, AI, MJS, KT, CW, RW, PB, JH, LF。
相应的作者
道德声明
相互竞争的利益
作者声明,与所描述的工作没有竞争的经济利益。只有一名作者与披露存在利益冲突,瑞秋·威廉姆斯(Rachel Williams)曾代表阿斯利康(AstraZeneca)向患者倡导组织展示,但没有宣传他们的产品。
伦理批准
进行系统评价不需要伦理批准。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
杨,a.l.,伊姆兰,A,斯波尔玛,M.J.et al。proband介导的干预增加BRCA或Lynch综合征家庭的遗传风险披露:一项系统综述。Eur J Hum Genet31, 18-34(2023)。https://doi.org/10.1038/s41431-022-01200-z
收到了:
修改后的:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41431-022-01200-z
这篇文章被引用
新的一年,新的基因
欧洲人类遗传学杂志(2023)