文摘
早产的风险增加心血管疾病(CVD)是公认的在系统性红斑狼疮(SLE)。异常类型I-Interferon(干扰素)中性粒细胞的交互有助于增强心血管疾病风险。在狼疮动物模型,Janus激酶(激酶)抑制剂tofacitinib改善临床特征,免疫调节异常和血管功能障碍。我们进行了一项随机、双盲、安慰剂对照的临床试验tofacitinib系统性红斑狼疮学科(ClinicalTrials.gov NCT02535689)。在这项研究中,30个受试者被随机分配到tofacitinib(5毫克每日两次)或安慰剂在2:1块中。本研究的主要结果是tofacitinib的安全性和耐受性。二次结果包括临床反应和机械的研究。在系统性红斑狼疮tofacitinib被发现是安全会议研究的主要终点。我们还表明,tofacitinib改善代谢疾病和免疫参数与系统性红斑狼疮的过早动脉粥样硬化有关。Tofacitinib提高高密度脂蛋白胆固醇水平(p= 0.0006,95% CI: 4.12, 13.32)和粒子数(p= 0.0008,95% CI: 1.58, 5.33);卵磷脂胆固醇酰基转移酶浓度(p= 0.024,95% CI: 1.1−26.5),胆固醇流出容量(p= 0.08,95% CI: 0.01−0.24),改善动脉硬化和endothelium-dependent血管舒张和I型干扰素基因签名,减少低密度粒细胞和循环网。这些改进的一些更强大的主题STAT4风险等位基因。
介绍
系统性红斑狼疮(SLE)的发病机制涉及多个先天和适应性免疫通路的失调1。先天免疫系统的作用,特别是I型干扰素,低密度,中性粒细胞和嗜中性粒细胞胞外陷阱(网),现在被认为是一个潜在的基本在系统性红斑狼疮发病机制及其相关的血管损伤2。心血管疾病(CVD)的风险和过早动脉粥样硬化是系统性红斑狼疮显著增加,尤其是在年轻女性3,4。努力调节系统性红斑狼疮血管病变、动脉粥样硬化的发展和发展努力均告失败5。
免疫失调的特点提出了系统性红斑狼疮扮演突出角色在推动过早动脉粥样硬化6。具体来说,I-Interferon类型(干扰素)中性粒细胞的途径和不同的子集称为低密度粒细胞(爬)显示增强的能力形成中性粒细胞胞外陷阱(网)直接参与血管损伤,动脉粥样硬化斑块的形成,和心血管疾病进展7,8。
Janus激酶/转录信号传感器和催化剂(JAK / STAT)通路是一项基本信号级联使用细胞应对多种细胞因子和生长因子9。许多炎性细胞因子与系统性红斑狼疮发病机理,包括I型和II型干扰素(ifn),信号通过JAK-STAT通路10,11。激酶抑制剂(jakinibs)在各种狼疮小鼠模型显示效果12。使用jakinibs临床试验显示,轻度到中度系统性红斑狼疮患者关节炎临床疗效13,14。此外,tofacitinib调节中性粒细胞和I型干扰素反应特异表达,内皮功能障碍,在狼疮鼠脂蛋白12。
我们假设减轻木菠萝的异常激活先天免疫途径抑制剂会导致代谢疾病的改善参数和免疫失调与不成熟的血管损害系统性红斑狼疮有关。为此,我们进行了阶段Ib /活动花絮,双盲,安慰剂对照的临床试验在系统性红斑狼疮tofacitinib科目有轻度到中度的疾病。的存在STAT4风险等位基因(rs7574865)与更严重的临床表型和系统性红斑狼疮血管疾病的风险明显增加,而且由于I型干扰素激活STAT4,我们将被试基于存在(+)或缺席(−)STAT4风险等位基因已建议增加和敏感I型干扰素的生产在系统性红斑狼疮患者外周血单核细胞,探讨这些单的效果(s)的临床和tofacitinib免疫反应15,16,17。
在这里,我们表明,tofacitinib主题是安全的和良好的耐受性有轻度到中度的系统性红斑狼疮。没有意外的不良事件或恶化的系统性红斑狼疮疾病活动,没有严重的不良事件,机会性感染,或者使用tofacitinib血栓栓塞事件。tofacitinib治疗能提高高密度脂蛋白胆固醇水平和粒子数,卵磷脂,胆固醇酰基转移酶浓度和胆固醇流出的能力。它也提高了动脉硬化和endothelium-dependent血管舒张。tofacitinib使用显著减少了I型干扰素基因签名,水平的低密度粒细胞和循环网。这些变化是更健壮的系统性红斑狼疮的主题STAT4风险等位基因。还需要长期的研究来确定tofacitinib在心血管疾病预防系统性红斑狼疮的疗效。
结果
安全与疾病活动
三十系统性红斑狼疮患者注册,所有完成这项研究,包括在分析中。基线人口统计学和临床特点分层的主题STAT4风险等位基因状态如表所示1和补充图。1。有更多的非裔美国人的主题STAT4风险allele-negative群tofacitinib和安慰剂组(P= 0.002)。研究对象与STAT4风险等位基因是年轻,主要是西班牙裔,但这些差异没有统计学意义。有71个不良事件:43 tofacitinib组和28在安慰剂组,没有严肃的AEs tofacitinib组;AE的差异没有统计学意义(表2)。大多数的AEs tofacitinib组中观察到的是轻度(16/43)、中度(5/43)上呼吸道感染后self-resolved或口服抗生素治疗。没有带状疱疹复活、BK病毒血症或静脉血栓栓塞事件记录。没有临床或统计上显著的变化观察tofacitinib组基线测量和安慰剂组相比,在其他实验室安全参数(表3)。tofacitinib组与安慰剂相比,血红蛋白变化差异分数−0.33 (95% CI 0.33−−0.88) 56天,−0.20(95%可信区间,0.81−0.40)在84年的一天;白细胞计数差异变化分数−0.63 (95% CI 0.63−−1.46) 56天,−0.52(95%可信区间,1.35−0.30)在84年的一天;绝对中性粒细胞计数差异变化分数−0.58 (95% CI 0.58−−1.35) 56天,−0.21(95%可信区间,0.85−0.43)在84年的一天;血小板计数变化的差异分数−15.36 (95% CI 15.36−−35.79) 56天,5.3(95%可信区间,12.33−22.93)在84年的一天;血清AST差异变化分数为0.71 (95% CI, 0.71−5.14) 56天,−13.8(95%可信区间,34.91−7.31)在84年的一天;和血清ALT差异变化分数为1.58 (95% CI, 1.58−4.55) 56天,−2.15(95%可信区间,8.86−4.56)84(表3)。这些差异在统计学上意义重大。所有的患者在两组符合疾病爆发的标准试验过程中,并没有新的BILAG 2004 A或B的分数。基线是咽部菌2 K tofacitinib组的得分为5.1±2.2均值±标准差,在安慰剂组相比,5.5±3.7;变化的差异分数(tofacitinib比安慰剂)为0.04(95%置信区间CI:−1.04, 1.11), 56天,−0.72(95%置信区间CI:−1.98, 0.53)在84天。基线意味着BILAG 2004 tofacitinib组的得分是7.6±4.6均值±标准差,在安慰剂组相比,9.3±4.3;变化的差异分数(tofacitinib比安慰剂)为1.56(95%置信区间CI:−1.86, 4.98), 56天,−2.04(95%置信区间CI:−4.96, 0.89)在84天。基线是指PGA tofacitinib组的得分为0.8±0.8(平均值±标准偏差),1.2±0.9相比安慰剂组;分数的差异变化(tofacitinib比安慰剂)为0.18(95%置信区间CI:−0.28, 0.64), 56和0.23(95%置信区间CI:−0.30, 0.76)在84天。这些差异在统计学上意义重大。 The SLE serological disease activity (complement C3 and C4 levels) and the patient-reported outcomes (SF-36) were similar at baseline visit and did not have a significant difference in change scores at day 56 or day 84 (Table4)。有一个数值增加anti-ds-DNA抗体滴度在两组在研究过程中,但这些增长未达到统计上的显著水平。这项研究没有动力来评估临床疗效。
尽管随机化,有一些差异tofacitinib和安慰剂组在基线的访问。服用安慰剂的受试者报告显著更高程度的疲劳,在基线以MD-Fatigue规模,显著改善疲劳研究中。服用安慰剂的受试者基线DAS-28-ESR较高和较低的基线anti-ds-DNA水平相比tofacitinib组,但这些并没有显著差异(表4)。受试者的安全和疾病活动数据tofacitinib和安慰剂分层基于存在与否STAT4风险等位基因显示非统计性之间的显著差异在某些变量组(如上所述其他地方除外);这些差异的临床意义是不确定的,需要进一步探索一个更大的样本(补充表1和2)。
Tofacitinib调制I型干扰素基因签名和pSTAT水平
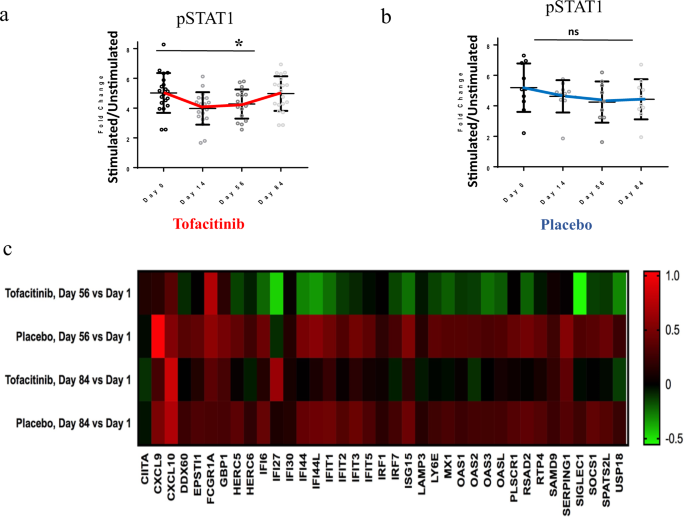
评估目标参与对象接收tofacitinib,我们测量STAT1的磷酸化STAT3和STAT5。Tofacitinib使用导致显著抑制pSTAT1 CD4+T细胞在试验(14天、56P= 0.023;无花果。1)。还有一个趋势观察对无意义的抑制pSTAT1主题在一个意义不明的安慰剂,没有任何已知的生物学解释。相比之下,pSTAT3、pSTAT5 pSTAT1 CD8水平没有显著不同+T细胞,CD20+B细胞或CD14+单核细胞之间tofacitinib或安慰剂治疗患者(无花果。1 b和补充图。2 a, b)。评估这些参数停药后一个月后表明,影响pSTAT1在停止用药后没有坚持。
一个显著抑制pSTAT1患者tofacitinib 56天(P= 0.023)回到基线的第84天n= 20生物独立样本。数据平均值+ /−SEM。混合线性模型使用了重复的措施。b没有明显的变化在病人安慰剂。n= 10生物独立样本。数据平均值+ /−SEM。混合线性模型使用了重复的措施。cTofacitinib降低了I型干扰素基因签名,在外周血基因表达Nanostring:热图显示干扰素刺激基因表达在外周血Nanostring: Log2意味着折叠干扰素刺激基因的表达变化从基线到天56和84 Tofacitinib科目(n= 20生物独立样本)和安慰剂(n= 10生物独立样本)。源数据作为源数据文件提供。结果显示为褶皱的变化刺激与如果细胞群。混合线性模型使用了重复的措施。未配对的双尾,t测试在适当的地方使用。没有调整为多个比较。
我们下一个评估基因表达组间基线,天56和84年由全血RNAseq。总共90个基因被发现是两个不同的(22和68年下降),方差分析比较tofacitinib和安慰剂治疗56天。明显的68个基因表达下调tofacitinib小组56天,19日是干扰素刺激基因(研究小组)。84天,其中大部分的水平19 isg回到预处理的水平,但一些基因仍显著下调(无花果。1 c和补充图。3)。Nanostring被用来验证tofacitinib影响干扰素签名(无花果。1 c)。干扰素反应基因得分没有显著不同的学科之间的基线tofacitinib和安慰剂。在56天,受试者tofacitinib水平显著减少的isg相比安慰剂(P一天= 0.01),它仍然重要,84年访问(P= 0.02)(补充图。4)18。
Tofacitinib调制提供中性粒细胞反应
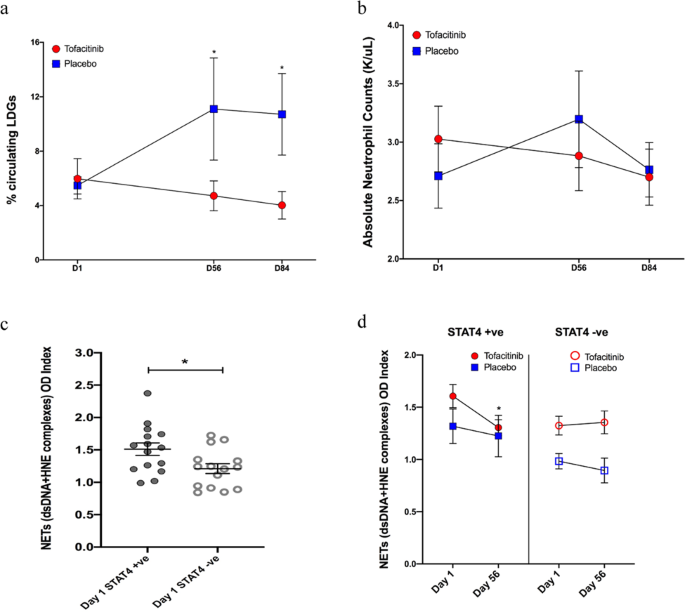
JAK / STAT通路,在中性粒细胞生物学同源细胞因子是至关重要的19。我们检查的影响tofacitinib爬(系统性红斑狼疮的促炎的中性粒细胞升高的不同子集)和合成网的能力。我们发现有一个显著减少的百分比爬在系统性红斑狼疮科目tofacitinib相比安慰剂在56天(P= 0.048),减少持续84天(P= 0.014;无花果。2),而总中性粒细胞在积极治疗没有显著减少(图2 b和表4)。也有随之而来的爬在安慰剂组部分解释了这个统计上的显著差异。网的作用在促进炎症和血管损伤在系统性红斑狼疮前所述体外和体内的效果STAT4净形成风险等位基因是未知的7。我们发现系统性红斑狼疮的主题STAT4风险等位基因的水平明显高于有循环净复合物基线相比STAT4风险allele-negative科目(P= 0.02)(图2摄氏度)。循环净复合物的水平明显降低基线相比STAT4风险allele-positive受试者接受tofacitinib (P= 0.037)(图二维)。相比之下,受试者接受安慰剂或接收tofacitinib这些学科STAT4风险allele-negative没有显示减少循环净复合物(无花果。二维)。总的来说,这些结果表明STAT4风险allele-positive主题显示更高水平的循环网和tofacitinib修改特征SLE-associated中性粒细胞失调在主题积极遗传风险单体型7。然而,尽管这些差异显著,但有一个群体之间的重叠和也有较低的净表达在安慰剂受试者基线。
一个结果代表的百分比变化循环爬:受试者接受tofacitinib与安慰剂。显著降低tofacitinib组爬下P= 0.048在56天P使用未配对= 0.014天84t测试。b绝对中性粒细胞计数的变化。c循环净在基线水平:个人阳性STAT4风险等位基因(每个主题由封闭的圆圈代表)增强循环净水平(评估人类嗜中性粒细胞弹性蛋白酶(HNE) -dsDNA复合物)然后受试者STAT4风险等位基因负(每个主题由开放圈)P= 0.02使用未配对t测试。d循环净水平变化在研究:患者STAT4积极风险等位基因和接收tofacitinib显示显著降低循环净复合物P= 0.037使用未配对t测试。源数据作为源数据文件提供。所有数据代表的意思是±SEM、*P< 0.05,是基于tofacitinibn= 20,安慰剂n= 10。未配对的双尾,t测试被用于所有的结果。没有调整为多个比较。
改善代谢疾病和血管功能参数
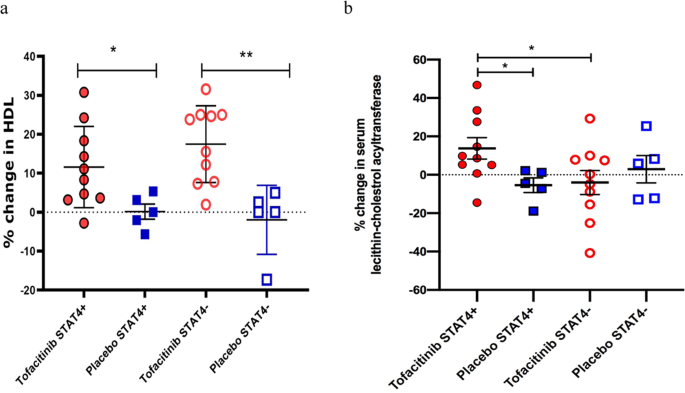
自从tofacitinib改进的I型干扰素信号和嗜中性粒细胞异常与过早心血管疾病相关,我们决定如果tofacitinib治疗血浆脂蛋白水平和功能的影响。有显著增加高密度脂蛋白胆固醇各科tofacitinib组完成的研究药物阶段(56天)与基线相比(P不管他们的= 0.006)STAT4风险等位基因状态(图。3和补充图。5 b)。低密度脂蛋白和甘油三酯水平没有影响(补充图。5模拟)。Tofacitinib水平也显著提高高密度脂蛋白颗粒大,而其他脂蛋白小分支变化不显著(表4)。在56天,显著增加Lecithin-cholesterol酰基转移酶(LCAT)浓度检测系统性红斑狼疮学科tofacitinib上STAT4风险allele-positive (P= 0.024,95% CI: 1.1—-26.5)相比STAT4安慰剂或风险allele-positive小组主题为阴性tofacitinib这种风险等位基因(P= 0.04,95%置信区间CI:−18.2, 10.2)(图3 b)。此外,在56天,有统计上显著的增加胆固醇流出容量治疗系统性红斑狼疮学科tofacitinib (P= 0.002,95% CI: 0.04—-0.16)和一个无意义的趋势相比安慰剂(P= 0.08,95%置信区间CI:−0.01, 0.24)(补充图。5 e)。这种效应并不依赖于主体的STAT4风险等位基因状态。没有在统计上有显著差异的胰岛素抵抗,以HOMA-IR来衡量,发现与安慰剂tofacitinib-treated组(P= 0.51,95% CI: 0.93−0.48)(表3)。tofacitinib组相比,安慰剂组有降低胆固醇和甘油三酯值的基线,但是这些差异没有统计学意义,在研究(表基本上保持不变3)。
一个在血清高密度脂蛋白胆固醇变化百分比相比,56天1的基础上STAT4风险等位基因状态(每个圆和正方形代表个人主题):结果代表*P= 0.037的区别STAT4风险allele-positive科目tofacitinib vs安慰剂和* *P= 0.002STAT4风险allele-negative科目tofacitinib vs安慰剂。未配对t测试使用。b变化百分比Lecithin-cholesterol酰基转移酶(LCAT)浓度相比,56天1的基础上STAT4风险等位基因状态(每个圆和正方形代表个人主题):结果代表*P= 0.033的区别STAT4风险allele-positive科目tofacitinib vs安慰剂和*P= 0.044的区别STAT4风险allele-positive科目tofacitinib vsSTAT4风险allele-negative tofacitinib科目。克鲁斯卡尔-沃利斯检验(未配对,非参数)。源数据作为源数据文件提供。所有的结果都是意味着±SEM, *P< 0.05 * *P< 0.01,是基于tofacitinibn= 20,安慰剂n= 10。双尾测试是在适当的地方使用。没有调整为多个比较。
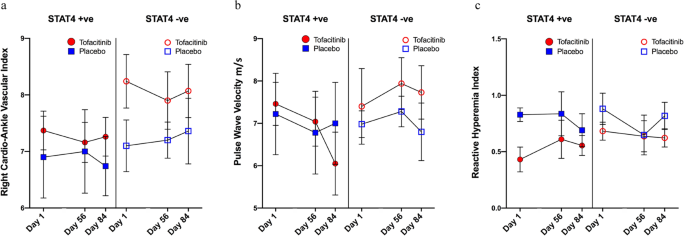
增强动脉硬化和损伤endothelium-dependent血管舒张描述与血管病变和亚临床动脉粥样硬化在系统性红斑狼疮20.,21。与之前的研究一致,各项指标的基线值的动脉硬化和损伤内皮功能障碍在系统性红斑狼疮患者高于年龄组(表引用值1)22,23。病人在tofacitinib臂临床显著降低动脉硬化(以CAVI和采集和改善endothelium-dependent血管舒张(以EndoPAT奥镁)。具体地说,病人在tofacitinib减少CAVI平均值±标准误差的均值在56天−0.28±0.14,0.14±0.19−在第84天(无花果。4)。采集只在下降STAT4风险allele-positive科目tofacitinib−0.42 m / s 56±0.58天,和−1.41 m / s 84±0.92天,分别从基线(图。4 b)。同样,奥镁的改善,STAT4风险allele-positive tofacitinib科目,在56天0.18±0.17,0.23 + 0.09天84(无花果。4摄氏度)。相比之下,没有安慰剂组中观察到的改进。整体而言,这些结果表明,系统性红斑狼疮科目短期tofacitinib治疗表现出改善代谢疾病和血管参数之前与简历相关风险的系统性红斑狼疮患者和一般人群。重要的是,其中的一些在受试者的保护作用更明显STAT4风险等位基因。
一个对cardioankle血管指数(CAVI):结果代表CAVI变化在主题tofacitinib vs安慰剂STAT4在审判allele-positive风险和负面的科目。b脉搏波速度(采集):结果代表变化在受试者采集tofacitinib vs安慰剂STAT4在审判allele-positive风险和负面的科目。c反应性充血指数(开展):结果代表的变化在主题开展tofacitinib vs安慰剂STAT4在审判allele-positive风险和负面的科目。源数据作为源数据文件提供。所有的结果都是意味着±SEM和基于tofacitinibn= 20,安慰剂n= 10。的配对t测试,Mann-WhitneyU,在适当的地方或方差分析被用于比较基于常态分布。双尾测试是在适当的地方使用。没有调整为多个比较。
讨论
在这项研究中,短期使用tofacitinib科目有轻度到中度的系统性红斑狼疮是总体安全,同时,没有意想不到的AEs,血栓栓塞事件或机会性感染。我们探索性分析表明,tofacitinib导致重大积极调制相关的代谢疾病和免疫参数之前增加了冠状动脉粥样硬化性斑块,血管炎症和血管功能异常在狼疮和一般人群24,25。过早动脉粥样硬化和血管病变导致心血管事件大大有助于增强的发病率和死亡率在系统性红斑狼疮,这种现象不是用传统的心血管危险因素来解释6,24。jakinibs可能有作用的观察调制系统性红斑狼疮血管病变和潜在的减少心血管危险因素可能在这个病人的人口具有重要意义。
先前的工作从我们的小组和其他涉及一个病理生理的联盟之间的I型干扰素,爬下,和增强网络形成机制,促进对系统性红斑狼疮过早动脉粥样硬化和血管病变7,26,27,28,29日。Tofacitinib显著减少了I型干扰素基因签名在循环免疫细胞和有选择地调制循环爬下的数字,但不是总中性粒细胞,与水平显著降低循环网。tofacitinib的机制导致爬下有待进一步减少特征和cytokine-specific作用可能与抑制这些细胞在骨髓或组织,可能通过细胞凋亡促进他们的死。感兴趣的,我们发现个人携带STAT4风险等位基因有更高水平的循环网,表明某些多态性与风险增强自身免疫可能促进增强网的形成,为其他自身免疫风险snp现象最近报道30.,31日。
虽然已经预计到对I型干扰素的影响,目前尚不清楚为什么爬下被tofacitinib优先目标,为什么有关净抑制增强应对毒品的存在STAT4风险等位基因。一个场景是,由于I型干扰素激活STAT4,相关科目STAT4风险等位基因增加中性粒细胞的启动导致增加网络的形成。我们目前的数据是一致的这一观点,看来tofacitinib可能优先阻止这个启动主体风险等位基因32。虽然tofacitinib受影响的I型干扰素反应和标记的嗜中性粒细胞失调,影响观察其他免疫细胞类型或主题有轻度到中度的系统性红斑狼疮的临床活动并不重要。I型干扰素的确切作用在SLE的发病机制仍在定义和废除这个途径可能不会导致减少疾病表现,从最近的临床试验证据使用干扰素受体阻滞剂Anifrolumab和血浆树突细胞特定受体抗体BIIB05933,34。未来的研究的影响tofacitinib在较大的患者组,由遗传风险分层和更大的活动性疾病,需要评估变更先天和适应性免疫参数,和临床疾病活动。
系统性红斑狼疮高密度脂蛋白被描述与降低胆固醇流出小颗粒大小和容量和LCAT活性驱动至少部分通过氧化增强网络的形成7,35,36,37。在这里,我们表明,短期使用tofacitinib系统性红斑狼疮导致的水平得到显著提升,高密度脂蛋白的大小和功能。重要的是,tofacitinib导致动脉合规和内皮功能的改善,逆转的SLE-associated加速血管老化。改善主动脉合规的采集保存在冲刷阶段可能由于调节tofacitinib对内皮细胞的影响38。尽管这些变化尚不具备统计学意义(可能是由于小样本大小)然而在短时间内改变的程度令人印象深刻,需要进一步探索。这一发现机制的短期tofacitinib暴露导致动脉合规和内皮功能的改善仍然投机。更高的患病率STAT4风险等位基因与心血管风险有关的系统性红斑狼疮患者和动脉粥样硬化动物模型16,39。在这项研究中,高密度脂蛋白功能(以LCAT活性),动脉硬化,endothelium-dependent血管舒张改善个人tofacitinib阳性STAT4风险等位基因。
未来临床试验需要确定对血管功能的积极作用jakinibs特定疾病或可概括的其他自身免疫性疾病,也许,甚至普通人群。事实上,解决CV风险non-autoimmune疾病人群中通过使用抗炎药物(canakinumab)据报道才能成功25。
有一个无意义的趋势降低tofacitinib绝对中性粒细胞计数对象。正如预期的那样,有更多的轻度和中度感染(主要是上呼吸道感染)tofacitinib组比安慰剂。当前研究的局限性包括短期和少量的科目有轻度到中度的疾病。作为一个早期阶段探索性研究,调整为多个比较。此外,还有在基线差异组和安慰剂组中观察到的变化可能是部分负责结果中观察到的一些次要的这项研究的结果。没有允许,因此伴随免疫抑制药物的安全性存在额外的药物还有待特征。然而,使用药物,具有良好的安全性,促进有益影响系统性炎症、疾病表现和CV风险防范是一个高度期望的目标系统性红斑狼疮等自身免疫性疾病。
总之,我们的研究的上下文中使用个性化的方法系统性红斑狼疮患者根据STAT4风险等位基因。从目前的试验结果显示木菠萝的影响抑制在受试者更健壮STAT4相关风险等位基因,这是一个更严重的系统性红斑狼疮,和心血管事件的风险增加15,16。JAK-STAT通路参与了多种细胞因子的细胞内信号;因此,需要额外的机械的研究来更好地描述通路研究的成果负责。随访可以更好地评估如果更大规模的研究这种个性化医疗方法的分层遗传风险等位基因导致发病率和死亡率的改善。
方法
研究设计和主题
批准的这项研究是美国国家卫生研究院(NIH) IRB (ClinicalTrials.govNCT02535689)。研究设计和行为符合有关规定对人类研究参与者的使用和按照规定的标准进行了赫尔辛基宣言》是由美国国立卫生研究院办公室授权的人类课题研究。书面知情同意和决心的资格后,受试者被随机分配到tofacitinib(5毫克每日两次)或安慰剂在2:1。三十成人系统性红斑狼疮科目符合美国风湿病学院(ACR)修订标准系统性红斑狼疮和有轻微到严重疾病活动的分类(系统性红斑狼疮疾病活动指数2000(咽部菌2 K)评分2至14)参加一个门诊临床研究设置40。每组中,有一半的受试者纯合或杂合的STAT4风险等位基因。受试者tofacitinib或安慰剂8周,随访4额外的几周之后(补充图。1)。合格的受试者在稳定剂量的抗疟药(前12周检查访问)和/或口服糖皮质激素(筛选访问前4周)(强的松或同等< 20毫克/天)但没有免疫抑制剂被允许。系统性红斑狼疮疾病活动决心使用咽部菌2 K, BILAG 2004年疾病活动得分28-Erythrocyte沉降率(DAS-28-ESR),医生(PGA)的全球评估(李克特量表0 - 3)和patient-reported结果(SF-36、多维疲劳评估问卷)41,42,43,44,45,46。不良事件的利率(AEs,由美国国家癌症研究所(NCI)定义的,常见的术语标准不良事件(CTCAE),版本4.0)每周记录。这项研究的主要结果是定义为比较的不良事件率和利率之间的系统性红斑狼疮疾病耀斑tofacitinib组和安慰剂组。系统性红斑狼疮疾病爆发被定义为增加咽部菌2 K得分≥3或增加PGA > 1。二级结果包括评估的临床反应,影响生活质量的措施,一些探索性机械的研究来评估药物的效果免疫失调和代谢疾病签名与过早心血管疾病的发展(原协议,最终协议,和总结的变化提供补充文件)的一部分。
免疫和血液参数
每个主题都有STAT4风险等位基因的基因筛查之前使用商用TaqMan访问®单核苷酸多态性基因型。详细的试剂和方法PBMC隔离,刺激,荧光条码方法用于染色和多路复用phosphoflow分析中描述的补充方法和其他地方47。路径分析和基因注释完成使用Toppgene (toppgene.cchmc.org)。结果证实了使用NanoString(参见补充的方法)。爬下被列为CD10+,CD15+,CD14罗48。人类中性粒细胞弹性蛋白酶(HNE) dna净复合物以等离子体,所述49。提供的细节补充的方法。
心血管危险因素和血管功能的测量
内稳态模型评估胰岛素抵抗(HOMA-IR)指数=空腹血糖(更易/ l)×空腹胰岛素(μU /毫升)/ 22.5)被用来评估胰岛素抵抗50。隔夜空腹血脂水平进行中央NIH临床中心实验室。脂蛋白粒子浓度和直径测量使用一个自动化的核磁共振光谱(NMR)。高密度脂蛋白(HDL)胆固醇流出容量测量使用方法和巨噬细胞细胞系J774出版51。人类血清lecithin-cholesterol酰基转移酶(LCAT)浓度是由ELISA量化(BioVendor;Ashville NC)。无创性血管功能的研究包括cardioankle血管指数(CAVI)、外周动脉张力测定法(帕特;反应性充血指数(开展),脉搏波速度(采集)7。提供的细节补充的方法。
统计分析
选择的样本大小是基于什么样的通常被使用在类似的研究和与我们的经验在早期阶段安全性研究一致52,53。没有正式的权力进行了计算。数据从所有随机受试者包括在分析中。综述了不良事件的频率为每个治疗组计数和百分比。评价治疗效果的变化从基线到治疗结束的时期(56天),一个线性mixed-effects符合纵向数据模型的方法是利用连续的安全参数和临床结果。模型包括基线值STAT4风险等位基因状态,治疗组,明确的时间点,时间交互作为固定的治疗效果。一个非结构化variance-covariance矩阵被用来占重复措施之间的相关性。变量只在基线评估和天56治疗期间,采用协方差分析(ANOCA)模型包括基线,治疗,和STAT4风险等位基因作为协变量。此外,配对t测试,Mann-WhitneyU在适当的地方,或方差分析被用于比较基于常态分布。改变分数从基线到第84天使用ANCOVA模型分别进行了分析。没有对调整为多个比较P由于探索性的分析值。第一个病人是参加2016年7月28日,最后一个病人参加9月18日,2017年。所有与SAS统计分析软件(版本9.4)。
核糖核酸测序分析
基因表达值计算与Partek基因组学套件6.6,也是用于主成分分析(PCA)和单向方差分析。方差分析是进行log2转换RPKM 0, 1抵消。
NanoString数据分析
运行的质量评估是(补充方法)完成的。数据联合、规范化和分析在Microsoft Excel(微软公司;雷蒙德,佤邦)。JMP 14版本被用于进一步的统计分析和策划(SAS公司;卡里,NC)。合成DNA寡核苷酸的37 isg和4看家基因被用作校准用标准检查运行和试剂很多一致性。
报告总结
进一步研究信息设计是可用的自然研究报告摘要与这篇文章有关。
改变历史
2021年6月24日
在本文的原始版本中,给定的和家庭的名字作者约翰·j·奥谢被错误地标记,导致不正确的索引。这个错误已经被修正。PDF和HTML版本显示正确的名字发表的时候。
引用
Tsokos, g . c .系统性红斑狼疮。心血管病。j .地中海。365年,2110 - 2121 (2011)。
Weidenbusch, M。,Kulkarni, O. P. & Anders, H. J. The innate immune system in human systemic lupus erythematosus.中国。科学。131年625 - 34。(2017)。
曼齐,等。不同年龄组女性心肌梗死和心绞痛的发病率与系统性红斑狼疮:与弗雷明汉的研究进行比较。点。j .论文。145年,408 - 415 (1997)。
Giannelou, m & Mavragani c . p .心血管疾病在系统性红斑狼疮:全面更新。j . Autoimmun。82年1 - 12 (2017)。
桑切斯,P。,Toro-Trujillo, E., Muñoz-Velandia, O. M., García, A. A. & Fernández-Ávila, D. G. Therapeutic Impact of Statins on the Lipid Profile and Cardiovascular Risk in Patients With Systemic Lupus Erythematosus: Systematic Review of the Literature and a Meta-analysis.Reumatol中国。15e86-e91 2019。
刘,y &卡普兰,m . j .心血管疾病在系统性红斑狼疮:一个更新。咕咕叫。当今。Rheumatol。30.,441 - 448 (2018)。
卡卢奇、p . m . et al .中性粒细胞子集和他们的基因签名与血管炎症和冠状动脉粥样硬化在红斑狼疮。江森自控的洞察力3e99276 (2018)。
高尔,r·r·卡普兰和m . j .致命捕捞:中性粒细胞在自身免疫细胞外的陷阱。咕咕叫。当今。Rheumatol。2,64 - 70 (2019)。
奥谢,J·J。,Holland, S. M. & Staudt, L. M. JAKs and STATs in immunity, immunodeficiency, and cancer.心血管病。j .地中海。368年,161 - 170 (2013)。
院长,g S。,Tyrrell-Price, J., Crawley, E. & Isenberg, D. A. Cytokines and systemic lupus erythematosus.安。感冒。说。59,243 - 251 (2000)。
Alunno,。,P一个djen, I., Fanouriakis, A. & Boumpas, D. T. Pathogenic and therapeutic relevance of JAK/STAT signaling in systemic lupus erythematosus: integration of distinct inflammatory pathways and the prospect of their inhibition with an oral agent.细胞8898 (2019)。
Furumoto, y . et al . Tofacitinib改善小鼠狼疮及其相关的血管功能障碍。关节炎Rheumatol。69年,148 - 160 (2017)。
你,h . et al。成功治疗关节炎和皮疹tofacitinib系统性红斑狼疮:从单一中心的经验。安。感冒。说。78年,1441 - 1443 (2019)。
华莱士,d . j . et al . Baricitinib系统性红斑狼疮:一项双盲,随机,安慰剂对照,第二阶段试验。《柳叶刀》392年,222 - 31所示。(2018)。
泰勒,k . e . et al .特异性STAT4遗传协会的严重疾病表现的系统性红斑狼疮。公共科学图书馆麝猫。4e1000084 (2008)。
Svenungsson、大肠等。STAT4风险等位基因与缺血性脑血管事件和anti-phospholipid抗体在系统性红斑狼疮。安。感冒。说。69年,834 - 840 (2010)。
Kariuki, s . n . et al .前沿:自身免疫性疾病风险的变体STAT4授予在狼疮患者体内IFN-alpha敏感性增加。j . Immunol。182年,品种马非常(2009)。
富里,r . et al . Anifrolumab anti-interferon-alpha受体单克隆抗体,在严重系统性红斑狼疮。关节炎Rheumatol。69年,376 - 86。(2017)。
Futosi, K。,Fodor, S. & Mocsai, A. Neutrophil cell surface receptors and their intracellular signal transduction pathways.Immunopharmacol Int。17,638 - 650 (2013)。
Taraborelli, m . et al。早期的系统性红斑狼疮患者的内皮功能障碍和控制没有以前的心血管事件。关节炎保健Res。70年,1277 - 1283 (2018)。
Tziomalos, k . et al .动脉硬化和外周动脉疾病患者的系统性红斑狼疮。Rheumatol。Int。37,293 - 298 (2017)。
Wohlfahrt, p . et al .参考cardio-ankle血管指数的值在一个白人人口的一个随机样本。j . Hypertens。35,2238 - 44 (2017)。
Mendoza-Pinto, c . et al .内皮功能障碍和系统性红斑狼疮患者的动脉硬化:系统回顾和荟萃分析。动脉粥样硬化297年55 - 63 (2020)。
布鲁斯,i n“不但…而且”:因素有助于加速动脉粥样硬化和冠心病过早在系统性红斑狼疮。风湿病学44,1492 - 1502 (2005)。
Ridker, p . m . et al .抗炎治疗动脉粥样硬化疾病的canakinumab。心血管病。j .地中海。377年1119 - 31 (2017)。
骑士,j . s . et al . Peptidylarginine deiminase抑制减少血管损伤和调节先天免疫反应在动脉粥样硬化小鼠模型。循环Res。114年,947 - 956 (2014)。
骑士,j . s . et al . Peptidylarginine deiminase抑制免疫调节和vasculoprotective鼠狼疮。j .中国。Investig。123年,2981 - 2993 (2013)。
查克,s . g . et al . I型干扰素调节血管功能,修复,血栓形成和血小板在狼疮小鼠模型和动脉粥样硬化进展。关节炎感冒。64年,2975 - 2985 (2012)。
Carmona-Rivera C。赵,W。,Yalavarthi, S. & Kaplan, M. J. Neutrophil extracellular traps induce endothelial dysfunction in systemic lupus erythematosus through the activation of matrix metalloproteinase-2.安。感冒。说。74年,1417 - 1424 (2015)。
常,H . H。,Dwivedi, N., Nicholas, A. P. & Ho, I. C. The W620 polymorphism in PTPN22 disrupts its interaction with peptidylarginine deiminase type 4 and enhances citrullination and NETosis.关节炎Rheumatol。67年,2323 - 2334 (2015)。
Odqvist, l . et al .基因变异在A20 citrullination配音域提供了一个遗传关联,中性粒细胞在系统性红斑狼疮细胞外的陷阱。安。感冒。说。78年,1363 - 70。(2019)。
Garcia-Romo g . s . et al .网中性粒细胞是I型干扰素生产的主要诱发儿童系统性红斑狼疮。科学。Transl。地中海。373 ra20 (2011)。
面前退却,e . f . et al . anifrolumab的审判活动的系统性红斑狼疮。心血管病。j .地中海。382年,211 - 21 (2020)。
富里,r . et al .单克隆抗体针对BDCA2改善皮肤损伤在系统性红斑狼疮。j .中国。Investig。129年,1359 - 71 (2019)。
Purmalek, m . m . et al .脂蛋白小分支协会和糖蛋白乙酰化与冠状动脉斑块在系统性红斑狼疮的负担。狼疮科学。地中海。6e000332 (2019)。
麦克马洪,m . et al .功能失调的促炎的高密度脂蛋白赋予女性增加动脉粥样硬化的风险和系统性红斑狼疮。关节炎感冒。60,2428 - 2437 (2009)。
史密斯,c . k . et al .狼疮高密度脂蛋白诱发巨噬细胞的促炎反应绑定lectin-like氧化低密度脂蛋白受体1和未能促进激活转录因子3活动。安。感冒。说。76年602 - 11 (2017)。
杨,X。,Wan, M., Cheng, Z., Wang, Z. & Wu, Q. Tofacitinib inhibits ox-LDL-induced adhesion of THP-1 monocytes to endothelial cells.Artif。细胞纳米级。Biotechnol。47,2775 - 82 (2019)。
Taghavie-Moghadam, p . l . et al . STAT4调节CD8(+)调节性T细胞/ T辅助滤泡细胞轴和促进动脉粥样化形成在胰岛素抵抗Ldlr(−−)老鼠。j . Immunol。199年,3453 - 65 (2017)。
业务,m . c .更新美国风湿病学院修订标准的分类系统性红斑狼疮。关节炎感冒。401725 (1997)。
平卡斯,T。,Swearingen, C. & Wolfe, F. Toward a multidimensional Health Assessment Questionnaire (MDHAQ): assessment of advanced activities of daily living and psychological status in the patient-friendly health assessment questionnaire format.关节炎感冒。42,2220 - 2230 (1999)。
龚珀兹,P。,Harwood, R., Ebrahim, S. & Dickinson, E. Validating the SF-36.BMJ(中国。研究》。)305年,645 - 646 (1992)。
最终,D D。,Ibanez, D. & Urowitz, M. B. Systemic lupus erythematosus disease activity index 2000.j . Rheumatol。29日,288 - 91 (2002)。
愚笨d . a . et al .评估患者的疾病爆发的系统性红斑狼疮:比较BILAG 2004和赛琳娜的耀斑版本。安。感冒。说。70年54-59 (2011)。
Aranow, c,一个试点研究,以确定最优的时间医生全球评估(PGA)在系统性红斑狼疮患者。Immunol。Res。63年,167 - 169 (2015)。
Villaverde,诉等。活动指数在类风湿性关节炎。j . Rheumatol。27,2576 - 2581 (2000)。
蔡,w . l . et al .高吞吐量pSTAT信号分析的荧光细胞条码和计算分析。j . Immunol。方法477年112667 (2020)。
丹尼,m . f . et al .不同子集的促炎的中性粒细胞与系统性红斑狼疮患者诱发血管损伤和综合I型干扰素。j . Immunol。184年,3284 - 3297 (2010)。
洪水,c . et al .中性粒细胞胞外陷阱富含线粒体DNA氧化interferogenic和导致lupus-like疾病。Nat,地中海。22,146 - 153 (2016)。
马修斯,d . r . et al .稳态模型评估:胰岛素抵抗和β细胞功能在人空腹血浆葡萄糖和胰岛素浓度。Diabetologia28,412 - 419 (1985)。
梅赫塔n n . et al .异常脂蛋白颗粒和胆固醇流出牛皮癣患者的能力。动脉粥样硬化224年,218 - 221 (2012)。
Hasni, s . et al . omalizumab的安全性和耐受性:随机临床试验的人性化ige单克隆抗体在系统性红斑狼疮。关节炎Rheumatol。71年,1135 - 1140 (2019)。
哈特曼,s . et al。人口临床药代动力学/药效学模型BIIB059,单克隆抗体治疗系统性和皮肤红斑狼疮。j . Pharmacokinet。Pharmacodyn。47,255 - 266 (2020)。
蔡,w . l . et al .高吞吐量pSTAT信号分析的荧光细胞条码和计算分析。j . Immunol。方法477年112667 (2020)。
确认
这项研究得到了校内研究项目,国家关节炎和肌肉骨骼和皮肤疾病研究所(National Institutes of Health)。辉瑞公司提供研究药物和安慰剂试验。审判由校内研究项目,NIAMS /国家卫生研究院。辉瑞公司提供的药物和安慰剂通过研究者发起的研究资助。辉瑞的作用仅限于提供研究药物和安慰剂,他们没有参与设计或研究的进行,报告的结果,或手稿准备。
资金
开放获取的资金由美国国立卫生研究院(NIH)。
作者信息
作者和联系
贡献
S.A.H.:study concept, design, protocol development, conduct, analyses, and manuscript draft. S.G.: study design, protocol development, conduct, analyses, and manuscript review. M.D.: study conduct and manuscript review. E.P.: study conduct and manuscript review. Y.T-O.: study conduct and manuscript review. P.M.C.: performed experimental studies and manuscript review. X.W.: performed experimental studies and manuscript review. M.N.: performed experimental studies, results analyses, and manuscript review. M.P.P.: performed experimental studies and manuscript review. R.R.G.: performed experimental studies and manuscript review. X.L.: performed statistical analyses. A.J.B.: study conduct and manuscript review. I.O.-N.: study conduct. Z.M.: data management and manuscript review. Y.S.: study conduct. D.T.: study conduct and manuscript review. J.C.: performed experimental studies. A.B.: performed experimental studies and manuscript review. R.A.: performed experimental studies and manuscript review. F.C.: performed experimental studies and manuscript review. Y.K.: performed experimental studies and manuscript review. A.L.B.: performed experimental studies and manuscript review. H.Z.: performed experimental studies and manuscript review. R.S.: performed experimental studies and manuscript review. K.S.: performed experimental studies and manuscript review. W. L.T.: performed experimental studies. L.V.: performed experimental studies. N.G.: performed experimental studies. V.G.: performed experimental studies. S.L.: performed experimental studies, analyses, and manuscript review. S.R.B.: performed experimental studies, analyses, and manuscript review. M.M.: study design and manuscript review. P.G.: study design, performed experimental studies, and manuscript review. N.N.M.: performed experimental studies and manuscript review. A.T.R.: performed experimental studies, analyses, and manuscript review. B.D.: study concept, design, and manuscript review. J.J.O.: study concept, design, and manuscript review. M.G.: study conduct, analyses, and manuscript review. M.J.K.: study concept, design, conduct, analyses, manuscript draft, and review.
相应的作者
道德声明
相互竞争的利益
美国国立卫生研究院和J.J.O.S.专利相关激酶抑制剂和收到版税。NIH和J.J.O.S.有合作协议,开发奖(CRADA)和辉瑞属于木菠萝抑制和tofacitinib。美国国立卫生研究院和J.J.O.S. CRADA进行新的木菠萝抑制剂。其余作者声明没有利益冲突。
额外的信息
同行审查的信息自然通讯由于Amit Saxena,西蒙弧拱,另一个匿名的评论家(s)为他们的贡献的同行评审工作。同行审查报告。
出版商的注意施普林格自然保持中立在发表关于司法主权地图和所属机构。
源数据
权利和权限
开放获取本文是基于知识共享署名4.0国际许可,允许使用、共享、适应、分布和繁殖在任何媒介或格式,只要你给予适当的信贷原始作者(年代)和来源,提供一个链接到Creative Commons许可,并指出如果变化。本文中的图片或其他第三方材料都包含在本文的创作共用许可,除非另有说明在一个信用额度的材料。如果材料不包括在本文的创作共用许可证和用途是不允许按法定规定或超过允许的使用,您将需要获得直接从版权所有者的许可。查看本许可证的副本,访问http://creativecommons.org/licenses/by/4.0/。
关于这篇文章
引用这篇文章
Hasni, S.A.古普塔,S。戴维斯分校M。et al。第一阶段的双盲随机安全试验Janus激酶抑制剂tofacitinib系统性红斑狼疮。Nat Commun123391 (2021)。https://doi.org/10.1038/s41467 - 021 - 23361 - z
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41467 - 021 - 23361 - z
本文引用的
治疗狼疮肾炎:共识,证据和观点
自然评论风湿病学(2023)
心血管风险Janus激酶抑制剂:凝视外面的黑盒
临床风湿病学(2023)
狼疮肾炎:新的和新兴生物和靶向治疗
BioDrugs(2023)
系统性红斑狼疮:药物靶向小分子的管道
药物(2023)
转录表达CXCL10 STAT1的狼疮肾炎和triptolide的干预效果
临床风湿病学(2023)