摘要gydF4y2Ba
CO的电化学还原gydF4y2Ba2gydF4y2Ba多碳产品(CgydF4y2Ba2 +gydF4y2Ba),当使用可再生电力时,提供了一条获取有价值的化学品和燃料的途径。在传统的中性介质CO中gydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2 +gydF4y2Ba设备,高达70%的输入COgydF4y2Ba2gydF4y2Ba穿过电池,与阳极产生的氧气混合。回收有限公司gydF4y2Ba2gydF4y2Ba从这个流增加了一个显著的能量惩罚。在这里,我们证明了使用液体到液体的阳极过程可以回收交叉的COgydF4y2Ba2gydF4y2Ba通过简单的气液分离,无需额外的能量输入:阳极尾气直接进入阴极输入,与新鲜CO一起gydF4y2Ba2gydF4y2Ba原料。我们报告了一种全电池低电压1.9 V的系统,总碳效率为48%,可实现262 GJ/吨乙烯,与最先进的单级CO相比,能源强度降低了46%gydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2 +gydF4y2Ba设备。该策略与当今效率最高的电解槽和CO兼容gydF4y2Ba2gydF4y2Ba在中性和碱性电解质中发挥最佳作用的催化剂。gydF4y2Ba
简介gydF4y2Ba
CO的电化学转化gydF4y2Ba2gydF4y2Ba(有限公司gydF4y2Ba2gydF4y2BaRR)转化为多碳(CgydF4y2Ba2 +gydF4y2Ba)产品是一种很有前途的降低净CO的方法gydF4y2Ba2gydF4y2Ba排放gydF4y2Ba1gydF4y2Ba.现有最好的COgydF4y2Ba2gydF4y2BaRR流池系统gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3 gydF4y2Ba零间隙膜电极组装(MEA)系统gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba实现CgydF4y2Ba2 +gydF4y2Ba法拉第效率(FEs) 70%和CgydF4y2Ba2 +gydF4y2Ba局部电流密度超过1acmgydF4y2Ba−2gydF4y2Ba在流式电池和超过100毫安厘米gydF4y2Ba−2gydF4y2Ba在多边环境。这些生产力水平与工业应用有关gydF4y2Ba7gydF4y2Ba.gydF4y2Ba
然而,当今CO的总能量gydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2 +gydF4y2Ba电解的能量太高——例如,当以乙烯为目标时,当今的电合成系统生产乙烯所需的能量比产品本身所含的能量足足多8倍gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba.主要的能源成本发生在电解槽和下游分离步骤(见方法:能源评估和补充说明)gydF4y2Ba1gydF4y2Ba在SI)gydF4y2Ba7gydF4y2Ba,gydF4y2Ba9gydF4y2Ba.已建立的降低电解能量需求的方法包括增加目标产物的选择性gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba并加入替代阳极反应gydF4y2Ba1gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba.与下游CO分离相关的主要能源和经济惩罚gydF4y2Ba2gydF4y2Ba保持挑战gydF4y2Ba14gydF4y2Ba.gydF4y2Ba
下游分离需要分离产品和回收未转化的COgydF4y2Ba2gydF4y2Ba从产品流和电解质gydF4y2Ba9gydF4y2Ba.回收有限公司gydF4y2Ba2gydF4y2Ba成本特别高,在中性和碱性介质CO的情况下,需要总能量输入的25%和70%gydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2 +gydF4y2Ba电解槽分别gydF4y2Ba8gydF4y2Ba,gydF4y2Ba15gydF4y2Ba.现在的公司gydF4y2Ba2gydF4y2BaRR催化剂在局部高碱性条件下(pH为> 12)催化CgydF4y2Ba2 +gydF4y2Ba阴极产生gydF4y2Ba2gydF4y2Ba.然而,形成碳酸盐的副反应(COgydF4y2Ba2gydF4y2Ba+哦gydF4y2Ba−gydF4y2Ba→公司gydF4y2Ba3 gydF4y2Ba2−gydF4y2Ba或HCOgydF4y2Ba3 gydF4y2Ba−gydF4y2Ba)在碱性条件下更受青睐,消耗大部分COgydF4y2Ba2gydF4y2Ba注射gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba15gydF4y2Ba.gydF4y2Ba
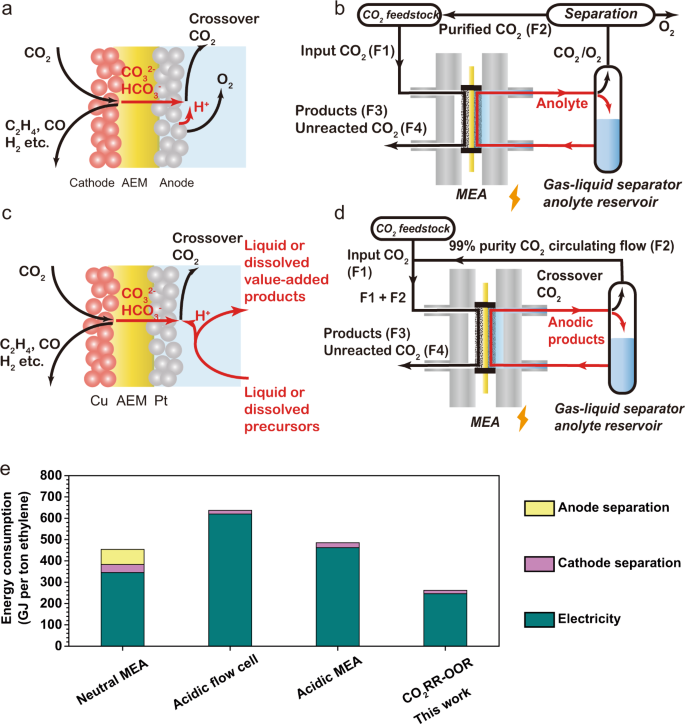
使用中性电解质(如KHCO)操作gydF4y2Ba3 gydF4y2Ba)在膜电极组装单元中减缓COgydF4y2Ba2gydF4y2Ba的损失。然而,大量CO的输入gydF4y2Ba2gydF4y2Ba(比转化为C的部分多3倍gydF4y2Ba2 +gydF4y2Ba)穿过阴离子交换膜(AEM),以碳酸盐/碳酸氢盐的形式到达阳极,与阳极反应产生的质子结合,并转化回COgydF4y2Ba2gydF4y2Ba(无花果。gydF4y2Ba1gydF4y2Ba)gydF4y2Ba4gydF4y2Ba,gydF4y2Ba15gydF4y2Ba.gydF4y2Ba
一个gydF4y2Ba常规CO中电化学过程的质量平衡gydF4y2Ba2gydF4y2BaRR-OER电解槽。gydF4y2BabgydF4y2Ba常规CO的工作原理gydF4y2Ba2gydF4y2BaRR-OER电解。F1 F2 F3 F4是COgydF4y2Ba2gydF4y2Ba分别是输入,交叉,转化为生成物和未反应。gydF4y2BacgydF4y2BaCO中电化学过程的质量平衡gydF4y2Ba2gydF4y2BaRR-OOR MEA电解器。mea型电解槽采用负载cu的气体扩散电极作为阴极,负载Pt/C的亲水碳布作为阳极,阴离子交换膜(AEM)作为固态电解质。在阴极,有一些COgydF4y2Ba2gydF4y2Ba电化学转化为COgydF4y2Ba2gydF4y2BaRR产物和CO的显著比例gydF4y2Ba2gydF4y2Ba由于局部ph值高,碳酸盐/碳酸氢盐离子转化为碳酸盐/碳酸氢盐离子,然后通过AEM迁移到阳极。有机前驱体在近中性电解质中被电化学氧化为增值产品,并在阳极产生质子。质子与碳酸盐/碳酸氢盐离子结合,重新生成COgydF4y2Ba2gydF4y2Ba作为阳极产物流中唯一的气相产物。gydF4y2BadgydF4y2Ba本公司的运作原则gydF4y2Ba2gydF4y2Bar - oor电解系统在CO中结合了低能量输入和高碳利用gydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2 +gydF4y2Ba转换。该系统使用由kco组成的阳极液gydF4y2Ba3 gydF4y2Ba还有液态有机前体。阴极腔内注入加湿的COgydF4y2Ba2gydF4y2Ba.质量平衡表见表gydF4y2BaS1gydF4y2Ba.gydF4y2BaegydF4y2Ba来自文献的乙烯生产基准系统的能量强度(中性MEAgydF4y2Ba4gydF4y2Ba;酸性流池gydF4y2Ba14gydF4y2Ba;酸是gydF4y2Ba21gydF4y2Ba)和这项工作。gydF4y2Ba
在阳极,交叉COgydF4y2Ba2gydF4y2Ba与O结合gydF4y2Ba2gydF4y2Ba通过析氧反应(OER)产生60-80% CO的气体混合物gydF4y2Ba2gydF4y2Ba20-40% OgydF4y2Ba2gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba.这种混合物不能直接循环到阴极中,因为氧还原将在阴极中占主导地位gydF4y2Ba18gydF4y2Ba.结果,CO分离gydF4y2Ba2gydF4y2Ba是阳极下游所需要的,每生产一吨乙烯会增加50-100 GJ的能量损失(见补充注gydF4y2Ba1gydF4y2Ba)——能源成本大于石化乙烯生产的能源消耗(67.5 GJ吨)gydF4y2Ba−1gydF4y2Ba)gydF4y2Ba19gydF4y2Ba.gydF4y2Ba
最近的能源和技术经济评估表明,这种分离惩罚水平与阳极CO有关gydF4y2Ba2gydF4y2Ba恢复是令人望而却步的gydF4y2Ba9gydF4y2Ba,gydF4y2Ba15gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba.在酸性条件下工作gydF4y2Ba14gydF4y2Ba,gydF4y2Ba21gydF4y2Ba,gydF4y2Ba22gydF4y2Ba提出了一种消除CO的新策略gydF4y2Ba2gydF4y2Ba交叉和相关的阳极分离能。然而,至少就目前而言,这种方法在与高全电池电压和低C相关的电解步骤中会产生较高的能源成本gydF4y2Ba2 +gydF4y2Ba酸性环境中的FE(图。gydF4y2Ba1 egydF4y2Ba、表gydF4y2Ba1gydF4y2Ba):目前在酸性CO中生产乙烯的能量强度gydF4y2Ba2gydF4y2BaRR型电解液比传统的aem型电解液(图。gydF4y2Ba1 egydF4y2Ba、表gydF4y2Ba1gydF4y2Ba).进一步的努力需要致力于开发新的催化剂和系统,以解决由酸性环境引起的电压、选择性和稳定性问题。gydF4y2Ba
我们采取了一种能够直接回收CO的策略gydF4y2Ba2gydF4y2Ba从无能量惩罚的阳极气流。与之前的工作一样,MEA电解器的阴极室持续供应COgydF4y2Ba2gydF4y2Ba.阳极室采用近中性阳极液(例如1 M KHCO)gydF4y2Ba3 gydF4y2Ba)含有一种液相前体,可被电化学氧化。AEM分离了阴极和阳极,为CO提供了有利的局部碱性条件gydF4y2Ba2gydF4y2BaRR。在这个系统中,一些输入COgydF4y2Ba2gydF4y2Ba(流速:F1 mol sgydF4y2Ba−1gydF4y2Ba)穿过到阳极;一部分转化为生成物(F3);部分产品通过了MEA (F4)。该系统的一个关键特征是,阳极出口气体可以再循环(F2)作为阴极的入口气体。碳效率定义为:gydF4y2Ba14gydF4y2Ba
在一个普通的基于aem的零间隙COgydF4y2Ba2gydF4y2Bar - oer电解槽(图;gydF4y2Ba1 a, bgydF4y2Ba),输入碳的很大一部分(F2,大约是F3的三倍gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba)从阴极穿过到阳极,并与阳极过程中的质子结合,生成气态COgydF4y2Ba2gydF4y2Ba.在不进行再循环的情况下,该系统的碳效率(<30%)接近于普通的MEA电解槽。gydF4y2Ba
我们注意到,如果阳极反应在本质上是全液态的,也就是说,如果它避免OgydF4y2Ba2gydF4y2Ba进化-那么这种方法就避免了这种CO的污染gydF4y2Ba2gydF4y2Ba含氧流gydF4y2Ba2gydF4y2Ba.回收的COgydF4y2Ba2gydF4y2Ba是高纯度(>99%),可以直接回收到阴极(图。gydF4y2Ba1 dgydF4y2Ba),也就是说,gydF4y2BaF1gydF4y2Ba=gydF4y2BaF3gydF4y2Ba+gydF4y2BaF4gydF4y2Ba.这样的系统打破了25%的COgydF4y2Ba2gydF4y2Ba利用极限gydF4y2Ba15gydF4y2Ba在基于aem的电解槽中,避免了与阳极气体分离相关的全部能量损失,并且这样做不会导致全电池电压或乙烯选择性的损失gydF4y2Ba7gydF4y2Ba.gydF4y2Ba
该方法需要全液相阳极过程,产生质子(或消耗氢氧化物),并在接近中性的介质中运行。候选阳极反应包括水-过氧化氢gydF4y2Ba23gydF4y2Ba,gydF4y2Ba24gydF4y2Ba, chloride-to-hypochloritegydF4y2Ba25gydF4y2Ba,以及广泛的有机氧化反应(OORs)gydF4y2Ba13gydF4y2Ba,gydF4y2Ba26gydF4y2Ba,gydF4y2Ba27gydF4y2Ba.然而,先前发表的过氧化氢和次氯酸盐生产催化剂导致气态副产物gydF4y2Ba23gydF4y2Ba,gydF4y2Ba24gydF4y2Ba,gydF4y2Ba25gydF4y2Ba.gydF4y2Ba
这里我们采用阳极有机氧化反应。最近的技术经济分析gydF4y2Ba1gydF4y2Ba,gydF4y2Ba27gydF4y2Ba建议用OOR代替OER,作为降低全电池电压并从电池两侧生产可销售产品的机会。候选的OOR反应包括葡萄糖的氧化gydF4y2Ba1gydF4y2Ba、甘油gydF4y2Ba1gydF4y2Ba,糠醛gydF4y2Ba27gydF4y2Ba, 5-hydroxymethylfurfuralgydF4y2Ba28gydF4y2Ba、醇gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba或任何其他生物质多元醇和单糖。CO的耦合gydF4y2Ba2gydF4y2BaRR和有机物的氧化已在h细胞中得到证实gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba28gydF4y2Ba,gydF4y2Ba29gydF4y2Ba,液养怜槽gydF4y2Ba30.gydF4y2Ba,气馈流式电池gydF4y2Ba1gydF4y2Ba,gydF4y2Ba13gydF4y2Ba,以及MEA电解器gydF4y2Ba31gydF4y2Ba.电化学CO还原与OOR的耦合最近已在MEA电解槽中得到证实gydF4y2Ba8gydF4y2Ba.然而,先前采用OOR作为阳极过程的系统并没有关注整体碳效率:最近的气体- cogydF4y2Ba2gydF4y2Ba美联储有限公司gydF4y2Ba2gydF4y2Ba在强碱性电解质(pH值> 14)中运行的ror - oor系统gydF4y2Ba1gydF4y2Ba,gydF4y2Ba13gydF4y2Ba,gydF4y2Ba31gydF4y2Ba,导致严重的能量损失,与(bi)碳酸盐再生回碱性和CO有关gydF4y2Ba2gydF4y2Ba.gydF4y2Ba
葡萄糖丰富的生物质,平均市场价格为400-500美元吨gydF4y2Ba−1gydF4y2Ba32gydF4y2Ba主要由淀粉制成。2017年,美国生产了超过500万吨葡萄糖(gydF4y2Bahttps://www.statista.com/statistics/496485/glucose-production-in-the-us/gydF4y2Ba).葡萄糖的电化学氧化产生葡萄糖酸盐,葡萄糖醛酸盐和葡萄糖酸盐(图。gydF4y2BaS1gydF4y2Ba)gydF4y2Ba33gydF4y2Ba,gydF4y2Ba34gydF4y2Ba,这些都是生产生物聚合物的原料gydF4y2Ba35gydF4y2Ba和药品gydF4y2Ba36gydF4y2Ba.葡萄糖酸的市场价格为700-1600美元/吨gydF4y2Ba32gydF4y2Ba,gydF4y2Ba37gydF4y2Ba,gydF4y2Ba38gydF4y2Ba.预计葡萄糖酸的市场规模为8000万美元gydF4y2Ba39gydF4y2Ba(2024)。最近的技术经济评估估计了这一点gydF4y2Ba32gydF4y2Ba,gydF4y2Ba40gydF4y2Ba可再生能源驱动的葡萄糖电化学氧化反应在经济上是可行的。在中性和近中性电解质的工业相关反应速率上,GOR优于OERgydF4y2Ba41gydF4y2Ba.GOR还提供电解节能,热力学电位为0.05 VgydF4y2Ba1gydF4y2Ba,显著低于OER (1.23 V)。gydF4y2Ba
在这项工作中,我们将CO配对gydF4y2Ba2gydF4y2Ba研究了葡萄糖氧化反应(GOR)的液相阳极氧化工艺策略。该系统的全电池电压为1.9 V,总碳效率为48%,可产生262 GJ/吨乙烯,与目前最先进的单级CO相比,能源强度降低了46%gydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2 +gydF4y2Ba设备。gydF4y2Ba
结果gydF4y2Ba
催化剂表征gydF4y2Ba
执行COgydF4y2Ba2gydF4y2Ba将纳米铜粒子和全氟磺酸(PFSA)离子沉积在疏水多孔聚四氟乙烯(PTFE)气体扩散电极上。PTFE气体扩散电极预溅射200 nm厚的多晶Cu以提高导电性(详见方法)。扫描和透射电子显微镜(分别为SEM和TEM)图像显示了由几十纳米厚的PFSA离聚体薄膜结合的铜纳米颗粒组成的表面形貌(图2)。gydF4y2Ba2gydF4y2Ba).阳极电极由Pt/C纳米颗粒和PFSA离聚物均匀混合在亲水和高度多孔的碳纤维布基板上(详情见方法)。SEM图像证实,阳极由大孔碳纤维组成(图2)。gydF4y2Ba2 bgydF4y2Ba)均被Pt/C纳米颗粒和PFSA复合材料覆盖(如图所示)。gydF4y2Ba2 bgydF4y2Ba).图中TEM图像gydF4y2Ba2摄氏度gydF4y2Ba结果表明,铂纳米颗粒的直径在5 ~ 10 nm之间。能量色散x射线能谱(EDS)元素作图显示Pt均匀分布在C纳米颗粒表面(图2)。gydF4y2Ba2e和ggydF4y2Ba).gydF4y2Ba
一个gydF4y2Ba扫描电子显微镜(SEM)和透射电子显微镜(TEM,插入)图像的阴极催化剂:铜纳米颗粒/PFSA复合材料。gydF4y2BabgydF4y2Ba阳极催化剂的SEM图像:Pt/C负载在亲水碳纤维上。gydF4y2BacgydF4y2BaPt/C催化剂的SEM图像。gydF4y2BadgydF4y2Ba- - - - - -gydF4y2BaggydF4y2Ba扫描透射电子显微镜图像(gydF4y2BadgydF4y2Ba)和相应的碳元素能谱(EDS)映射(gydF4y2BaegydF4y2Ba)、白金(gydF4y2BafgydF4y2Ba)和重叠(gydF4y2BaggydF4y2Ba)用于Pt/C催化剂。gydF4y2Ba
CO的电化学表征gydF4y2Ba2gydF4y2BaRR-GOR系统gydF4y2Ba
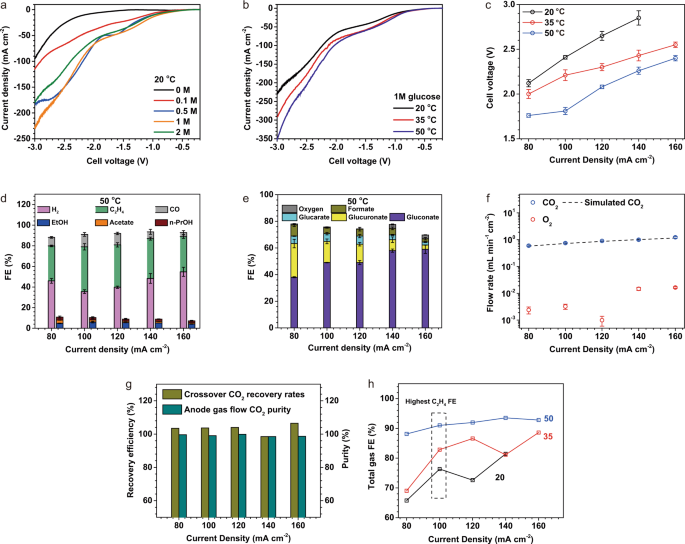
我们进行了线性扫描伏安法(LSV)测量来研究CO的电化学响应gydF4y2Ba2gydF4y2BaRR-GOR系统,阴极Cu负载为0.5 mg cmgydF4y2Ba−2gydF4y2Ba阳极铂负载为2毫克厘米gydF4y2Ba−2gydF4y2Ba(无花果。gydF4y2Ba3a及bgydF4y2Ba).当我们不添加葡萄糖到阳极液(COgydF4y2Ba2gydF4y2Bar - oer),电解槽的电流密度为94 mA cmgydF4y2Ba−2gydF4y2Ba全电池电压为3v。100ma cmgydF4y2Ba−2gydF4y2Ba,当我们引入葡萄糖,将其在阳极液中的浓度从0.1增加到0.5 M和1 M时,全电池电压从2.90下降到2.18 V和2.23 V。葡萄糖浓度0.5 M和1 M时的全电池电压相当接近:我们将此归因于阳极的电动动力学限制gydF4y2Ba42gydF4y2Ba:在0.5 M时,葡萄糖分子饱和了Pt催化剂的活性位点,因此,将浓度增加到1 M并不能使电池电压进一步降低。葡萄糖浓度进一步增加到2 M,全电池电压增加,即在100 mA cm时增加2.40 VgydF4y2Ba−2gydF4y2Ba因为Pt被葡萄糖和氧化中间体过量覆盖gydF4y2Ba43gydF4y2Ba.因此,我们采用1 M葡萄糖进行性能调查。gydF4y2Ba
一个gydF4y2Ba,gydF4y2BabgydF4y2BaCO的线性扫描伏安法(LSV)gydF4y2Ba2gydF4y2Ba不同葡萄糖浓度(0 M为CO)的rr - gore电解体系gydF4y2Ba2gydF4y2Ba高表面积IrO上的RR-OERgydF4y2BaxgydF4y2Ba-Ti催化剂)20gydF4y2BaogydF4y2BaC (gydF4y2Ba一个gydF4y2Ba)及(gydF4y2BabgydF4y2Ba)在不同温度下加入1m葡萄糖。在5 mV s的扫描速率下记录所有的剖面gydF4y2Ba−1gydF4y2Ba三次伏安扫描后立即进行。gydF4y2BacgydF4y2BaCO的全细胞电位gydF4y2Ba2gydF4y2Ba在不同温度下的RR-GOR,通过施加恒定电流来测量。gydF4y2BadgydF4y2Ba有限公司gydF4y2Ba2gydF4y2BaRR FE分布在50gydF4y2BaogydF4y2BaC和一些不同的电流密度。液态fe是基于从阴极+阳极液出口检测到的产物的总和。gydF4y2BaegydF4y2Ba不同电流密度下GOR液体产物的FE分布(用NMR和GC测量)gydF4y2BaogydF4y2BaC.用高效液相色谱法对戈尔产物进行定量,见图。gydF4y2Ba向gydF4y2Ba.gydF4y2BafgydF4y2Ba的有限公司gydF4y2Ba2gydF4y2Ba和OgydF4y2Ba2gydF4y2Ba流速(由电极几何面积归一化)在阳极气流50gydF4y2BaogydF4y2BaC.模拟COgydF4y2Ba2gydF4y2Ba是通过生成OHgydF4y2Ba-gydF4y2Ba和转移电子,假设COgydF4y2Ba2gydF4y2Ba转化为COgydF4y2Ba3 gydF4y2Ba2 -gydF4y2Ba.gydF4y2BaggydF4y2BaCO的回收率和纯度gydF4y2Ba2gydF4y2Ba在不同电流密度和50的阳极产物流中gydF4y2BaogydF4y2BaC.采收率由CO除以来定义gydF4y2Ba2gydF4y2Ba流量由测量得到,由预测得到。gydF4y2BahgydF4y2BaCO气体产物的FE分布gydF4y2Ba2gydF4y2Ba在不同温度和电流密度下的RR。gydF4y2Ba
通过LSV和计时电位测量,我们研究了不同温度下的电压-电流密度依赖性(图2)。gydF4y2Ba3b及cgydF4y2Ba).将操作温度从20提高到35gydF4y2BaogydF4y2BaC降低全电池电压0.1-0.3 V在广泛的电流密度从80到160毫安厘米gydF4y2Ba−2gydF4y2Ba(无花果。gydF4y2Ba3b及cgydF4y2Ba),归因于加速电化学动力学。当操作温度从35增加到50时,观察到类似的全电池电压降低gydF4y2BaogydF4y2BaC。gydF4y2Ba
同时实现高乙烯FE和低氧FEgydF4y2Ba
保持低OER FE对于确保高GOR效率和回收CO的足够纯度至关重要gydF4y2Ba2gydF4y2Ba.在现行条例中gydF4y2Ba2gydF4y2Ba在RR-GOR系统中,我们发现阴极和阳极催化剂需要精心设计才能实现COgydF4y2Ba2gydF4y2Ba恢复策略。gydF4y2Ba
在之前的研究中,阴极Cu (COgydF4y2Ba2gydF4y2BaRR)和阳极Pt (GOR)为1 mg cmgydF4y2Ba−2gydF4y2Ba6gydF4y2Ba,gydF4y2Ba44gydF4y2Ba0.5毫克厘米gydF4y2Ba−2gydF4y2Ba8gydF4y2Ba.当我们在CO中使用这些构型时gydF4y2Ba2gydF4y2BaRR-GOR系统,当寻求在100 mA cm以上工作时,我们获得了>3.4 V的高全单元电压gydF4y2Ba−2gydF4y2Ba,无花果。gydF4y2BaS5agydF4y2Ba,与CO相比优势不大gydF4y2Ba2gydF4y2BaRR-OER系统(图。gydF4y2BaS3gydF4y2Ba).高的全电池电压降低了GOR相对于OER的选择性,导致阳极OgydF4y2Ba2gydF4y2Ba>8%的FE(图;gydF4y2BaS5bgydF4y2Ba).gydF4y2Ba
重新检查Pt负载对于将全电池电压降低到<2.4 V是必要的(图2)。gydF4y2BaS5agydF4y2Ba),因此是OgydF4y2Ba2gydF4y2BaFE至<1%(图;gydF4y2BaS5bgydF4y2Ba)电流密度为120ma cmgydF4y2Ba−2gydF4y2Ba.然而,在这个电流密度下,COgydF4y2Ba2gydF4y2BaRR对乙烯的选择性约为30%。gydF4y2BaS5c dgydF4y2Ba),显著低于Cu的40-45%基准gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba.为了达到这一基准,系统必须运行在200毫安厘米gydF4y2Ba−2gydF4y2Ba(无花果。gydF4y2BaS5dgydF4y2Ba),全电池电压为3.23 V和OgydF4y2Ba2gydF4y2BaFE为7%(图;gydF4y2BaS5a bgydF4y2Ba).这并不是通过进一步增加铂负载来克服的。gydF4y2BaS5agydF4y2Ba),如图所示。gydF4y2BaS5gydF4y2Ba.调整铜负载改变所需的电流密度,以最大限度地提高乙烯FE。因此,我们对0.5毫克厘米gydF4y2Ba−2gydF4y2Ba铜阴极与2毫克厘米gydF4y2Ba−2gydF4y2BaPt阳极,在工业相关电流密度下同时实现最大乙烯FE和低氧FE。gydF4y2Ba
当运行在100毫安厘米gydF4y2Ba−2gydF4y2Ba和50gydF4y2BaogydF4y2BaC, COgydF4y2Ba2gydF4y2BaRR-GOR系统的全电池电压为1.8±0.1 V,比传统CO低1.6 VgydF4y2Ba2gydF4y2Ba在相同电流密度和温度下的r - oer系统gydF4y2Ba4gydF4y2Ba.我们将这种低的全电池电压归因于GOR比OER低的热力学势(0.05 vs. 1.23 V)和阳极催化剂对GOR的高活性。如此低的全电池电势显著降低了电力需求(表gydF4y2Ba1gydF4y2Ba).100ma cmgydF4y2Ba−2gydF4y2Ba时,系统在2时提供42%、48%和44%的乙烯fegydF4y2BaogydF4y2BaC, 35gydF4y2BaogydF4y2BaC,和50gydF4y2BaogydF4y2BaC(无花果。S7,gydF4y2Ba3 dgydF4y2Ba、表gydF4y2BaS5gydF4y2Ba,gydF4y2BaS6gydF4y2Ba而且gydF4y2BaS8gydF4y2Ba).cu溅射在PTFE GDE上不太可能参与COgydF4y2Ba2gydF4y2BaRR:我们观察到在疏水性碳素纸上喷涂铜纳米颗粒时的类似性能。gydF4y2BaS4gydF4y2Ba).gydF4y2Ba
我们研究了在较宽的电流密度范围内(80 ~ 160 mA cm) GOR的选择性gydF4y2Ba−2gydF4y2Ba)和工作温度(图;gydF4y2Ba3 egydF4y2Ba、表gydF4y2BaS7gydF4y2Ba而且gydF4y2BaS9gydF4y2Ba).温度从20度上升到50度gydF4y2BaogydF4y2BaC,我们检测到阳极液pH略有增加(从pH 7.9到8.3,图。gydF4y2BaS10gydF4y2Ba),这是由于CO的溶解度较低gydF4y2Ba2gydF4y2Ba在温暖的阳极液中。我们检测到葡萄糖酸盐是GOR的主要产物(>49% FE),在140 mA cm时达到58%的平台gydF4y2Ba−2gydF4y2Ba.GOR产品的完整分析如图所示。gydF4y2BaS12gydF4y2Ba而且gydF4y2Ba向gydF4y2Ba.在80 mA和160 mA cm的电流密度下,向氧方向的fe保持在<3%gydF4y2Ba−2gydF4y2Ba(在100ma cm时<1%gydF4y2Ba−2gydF4y2Ba全电池电压为1.80 V),这是由于OER动力学迟滞(图。gydF4y2Ba3gydF4y2Ba).gydF4y2Ba
回收有限公司gydF4y2Ba2gydF4y2Ba
的有限公司gydF4y2Ba2gydF4y2Ba回收策略需要高COgydF4y2Ba2gydF4y2Ba回收效率,在本工作中定义为:gydF4y2Ba
在哪里gydF4y2Ba我gydF4y2Ba指电流和gydF4y2BaFgydF4y2Ba法拉第常数。这里是COgydF4y2Ba2gydF4y2Ba穿过阳极的是碳酸盐gydF4y2Ba17gydF4y2Ba.实验表明,COgydF4y2Ba2gydF4y2Ba在阳极处收集的氢氧根的化学计量特征与氢氧根的化学计量特征一致gydF4y2Ba-gydF4y2Ba产生和电子转移gydF4y2Ba17gydF4y2Ba(无花果。gydF4y2Ba3 fgydF4y2Ba),表示产地来源证gydF4y2Ba2gydF4y2Ba回收率接近100%(图;gydF4y2Ba3 ggydF4y2Ba).此外,阳极COgydF4y2Ba2gydF4y2Ba流量比O大3个数量级gydF4y2Ba2gydF4y2Ba(无花果。gydF4y2Ba3 fgydF4y2Ba),表示一氧化碳的纯度gydF4y2Ba2gydF4y2Ba从超过99%的阳极气流中回收(图;gydF4y2Ba3 ggydF4y2Ba).低水平的OgydF4y2Ba2gydF4y2Ba可以直接回收阴极中的阳极气流,而不需要分离和相关的能源成本。值得注意的是,氧气分数超过1.8%会使CO恶化gydF4y2Ba2gydF4y2BaRR选择性,如图所示的对照研究。gydF4y2BaS3gydF4y2Ba).具体来说,阴极气体产物FE分布(图;gydF4y2Ba3 dgydF4y2Ba)gydF4y2Ba2gydF4y2BaRR-ORR,和阳极COgydF4y2Ba2gydF4y2Ba流直接送入阴极,CO的绝对值接近5%以内gydF4y2Ba2gydF4y2Bar - oer电解槽(图;gydF4y2BaS3gydF4y2Ba).对照实验(图;gydF4y2Ba向gydF4y2Ba,gydF4y2BaS14系列gydF4y2Ba),gydF4y2Ba13gydF4y2BaC丰度分析gydF4y2BaS4gydF4y2Ba)表明>为99.8%的阳极COgydF4y2Ba2gydF4y2Ba不是来自葡萄糖的过度氧化。这些实验观测结果与图中所提供的物质平衡分析很好地吻合。gydF4y2Ba1 cgydF4y2Ba.gydF4y2Ba
避免阴极侧COgydF4y2Ba2gydF4y2BaRR液体产品交叉gydF4y2Ba
CO法生产乙烯gydF4y2Ba2gydF4y2BaRR伴随着液相产物,如乙醇、醋酸酯和丙醇,其中大部分穿过膜进入阳极流gydF4y2Ba4gydF4y2Ba.液体产品的阴极-阳极交叉是CO的一个挑战gydF4y2Ba2gydF4y2BaRR,因为这些产品在阳极液中有氧化和稀释的风险。阳极一侧的OOR存在额外的风险,即阴极产生的液体会污染液体阳极产品流和气体COgydF4y2Ba2gydF4y2Ba流gydF4y2Ba1gydF4y2Ba,gydF4y2Ba27gydF4y2Ba.当我们把温度从20提高到50gydF4y2BaogydF4y2BaC,我们发现fe元素倾向于CO的主要气体产物gydF4y2Ba2gydF4y2BaRR (CgydF4y2Ba2gydF4y2BaHgydF4y2Ba4gydF4y2Ba在恒流密度为100 mA cm时,CO)从48%增加到56%gydF4y2Ba−2gydF4y2Ba(无花果。S4,gydF4y2Ba3d和hgydF4y2Ba).这一观察结果与以往研究一致,归因于CO的正熵变gydF4y2Ba2gydF4y2BaRRgydF4y2Ba45gydF4y2Ba,gydF4y2Ba46gydF4y2Ba.FE向CO的液态产物转移gydF4y2Ba2gydF4y2BaRR从24%下降到9%,这一趋势与之前的报告一致gydF4y2Ba4gydF4y2Ba.较高的温度显著降低了乙醇和正丙醇的交叉(图。gydF4y2BaS8gydF4y2Ba)到阳极一侧,我们将这一发现归因于进入阴极气流的蒸发速率增加。因此,液态CO的重量比gydF4y2Ba2gydF4y2Ba在50时,阳极液中RR产物与GOR目标产物的比值<1%gydF4y2BaogydF4y2BaC(图。gydF4y2BaS9gydF4y2Ba),而35岁的比例为1.4%gydF4y2BaogydF4y2BaC(图。gydF4y2BaS9gydF4y2Ba).鉴于以下证据:(i)总产地来源证gydF4y2Ba2gydF4y2BaRR FE接近100%(图;gydF4y2Ba3 dgydF4y2Ba,由于阳极氧化造成的损失可以忽略不计)和(ii)在阳极液的CV曲线中没有乙醇氧化信号(图。gydF4y2BaS14系列gydF4y2Ba),得出CO的氧化gydF4y2Ba2gydF4y2BaRR液产物在阳极处不显著。因此,在适度升高的温度下工作有利于COgydF4y2Ba2gydF4y2Ba通过降低全电池电压,抑制液态CO的形成和交叉,实现了RR-GOR体系gydF4y2Ba2gydF4y2BaRR产品。gydF4y2Ba
有限公司gydF4y2Ba2gydF4y2BaRR-GOR系统性能gydF4y2Ba
在这些发现的鼓舞下,我们探讨了CO的碳效率上限gydF4y2Ba2gydF4y2BaRR-GOR系统。广泛使用的方法gydF4y2Ba14gydF4y2Ba,gydF4y2Ba21gydF4y2Ba确定碳效率上限就是限制COgydF4y2Ba2gydF4y2Ba阴极流的有效性和测量F3 (COgydF4y2Ba2gydF4y2Ba转化为产品)和F1 (CO .gydF4y2Ba2gydF4y2Ba喂养)。电流和FE分布决定F2和F3。通过调节F1来调节COgydF4y2Ba2gydF4y2Ba可用性。在CO中gydF4y2Ba2gydF4y2BaRR-GOR体系,F1 = F3 + F4,意味着需要通过降低F1来抑制F4以达到高碳效率。原则上,在给定的电解系统中,F1、F2、F3、F4的相对值与电解槽面积成正比。因此,我们在本研究中通过电解槽面积将所有流速归一化,以关注该系统的内在特性。gydF4y2Ba
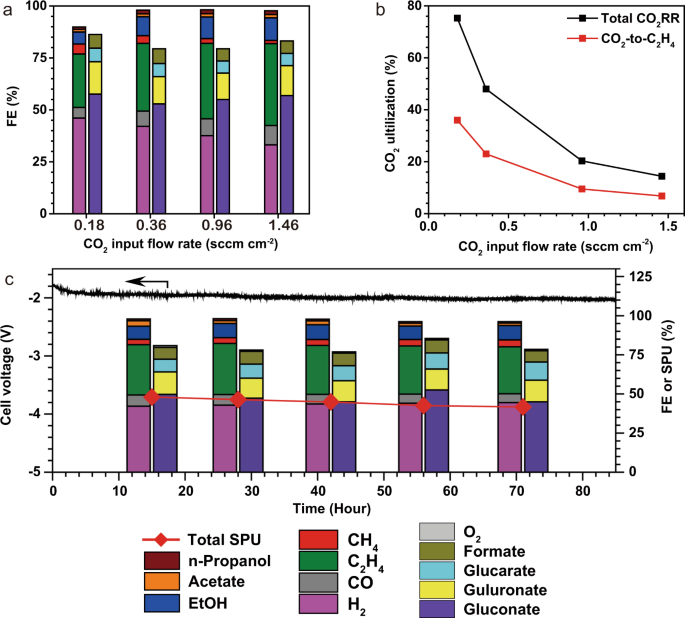
减少输入COgydF4y2Ba2gydF4y2Ba流量增加碳效率,这是典型的在这些系统(表gydF4y2BaS10gydF4y2Ba和无花果。gydF4y2Ba4 bgydF4y2Ba).在入口COgydF4y2Ba2gydF4y2Ba流量0.18立方厘米厘米gydF4y2Ba−2gydF4y2Ba(流速由电极面积归一化),系统总输送CgydF4y2Ba2 +gydF4y2Ba在100 mA cm的恒电流密度下,FE为~34%gydF4y2Ba−2gydF4y2Ba全电池电压为1.90 V,对应于对所有CO的碳效率为75%gydF4y2Ba2gydF4y2BaRR产物(总碳效率,图;gydF4y2Ba4a和bgydF4y2Ba),超过中性介质CO中碳效率上限gydF4y2Ba2gydF4y2BaRR电解槽gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba14gydF4y2Ba.在此条件下乙烯FE稳定在~26%,相当于COgydF4y2Ba2gydF4y2Ba-乙烯碳效率~36%(图;gydF4y2Ba4 bgydF4y2Ba).这一碳效率比CO的理论上限(25%)高出1.4倍gydF4y2Ba2gydF4y2Ba在传统的,中性介质,aem基电解槽中的乙烯转化gydF4y2Ba14gydF4y2Ba.限制流速会导致氢FE显著增加(图2)。gydF4y2Ba4gydF4y2Ba),我们和其他人gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba14gydF4y2Ba归因于CO的传质限制gydF4y2Ba2gydF4y2Ba.GOR在阳极保持一致的选择性和生产力,独立于COgydF4y2Ba2gydF4y2Ba阴极气流中的有效性(图;gydF4y2Ba4gydF4y2Ba和表gydF4y2BaS11gydF4y2Ba).gydF4y2Ba
一个gydF4y2Ba不同CO下FE的分布gydF4y2Ba2gydF4y2Ba输入流量。标签如下所示(gydF4y2BacgydF4y2Ba).gydF4y2BabgydF4y2Ba的有限公司gydF4y2Ba2gydF4y2Ba总CO的碳效率gydF4y2Ba2gydF4y2BaRR和COgydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2gydF4y2BaHgydF4y2Ba4gydF4y2Ba(输入CO的摩尔比gydF4y2Ba2gydF4y2Ba换算成CgydF4y2Ba2gydF4y2BaHgydF4y2Ba4gydF4y2Ba)在不同产地来源处gydF4y2Ba2gydF4y2Ba输入流量。gydF4y2BacgydF4y2BaCO的长期电解性能gydF4y2Ba2gydF4y2Ba输入流量0.36立方厘米厘米gydF4y2Ba−2gydF4y2Ba.实验在电流密度为100 mA cm的条件下进行gydF4y2Ba−2gydF4y2Ba.CO的流速gydF4y2Ba2gydF4y2Ba所提供的是由电极的几何面积归一化。gydF4y2Ba
碳效率和乙烯FE之间的平衡是CO的典型特征gydF4y2Ba2gydF4y2Ba乙烯电解gydF4y2Ba4gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba14gydF4y2Ba(无花果。gydF4y2Ba4a和bgydF4y2Ba).较高的碳效率降低了阴极分离的能量需求,但随之而来的乙烯FE的降低增加了电解槽的比能量需求。为了协调这些指标,我们评估了各种CO的总输入能量(每吨乙烯生产的电能、阴极分离和阳极分离)gydF4y2Ba2gydF4y2BaRR方法(参见“方法”)gydF4y2Ba6gydF4y2Ba.我们发现COgydF4y2Ba2gydF4y2BaRR-GOR系统的最低能耗为262 GJ /吨乙烯,并且是在输入CO的情况下实现的gydF4y2Ba2gydF4y2Ba流量0.36立方厘米厘米gydF4y2Ba−2gydF4y2Ba,对所有CO的总碳效率为48%gydF4y2Ba2gydF4y2BaRR产品。在此条件下,向C方向的FEgydF4y2Ba2 +gydF4y2Ba和乙烯分别为45%和32%(表gydF4y2Ba1gydF4y2Ba).gydF4y2Ba
与最先进的常规CO相比gydF4y2Ba2gydF4y2Ba乙烯体系(即基于AEM和中性电解质的mea), COgydF4y2Ba2gydF4y2BaRR-GOR系统消除了阳极分离能(>53 GJ /吨乙烯,补充注gydF4y2Ba1gydF4y2Ba).乙烯生产的整体能源强度比最节能的先前CO低46%gydF4y2Ba2gydF4y2Ba中性和酸性CO之间的RR体系gydF4y2Ba2gydF4y2Ba到乙烯电解槽(表gydF4y2Ba1gydF4y2Ba).gydF4y2Ba
稳定,碳效率高gydF4y2Ba
稳定性是CO工业化应用的前提gydF4y2Ba2gydF4y2BaRR。然而,长期操作COgydF4y2Ba2gydF4y2Ba具有高碳效率的RR(如COgydF4y2Ba2gydF4y2Ba碳效率>40%)迄今尚未实现。最好的COgydF4y2Ba2gydF4y2Ba运行100 h时,碳效率<4%gydF4y2Ba6gydF4y2Ba.gydF4y2Ba
我们进行了扩展COgydF4y2Ba2gydF4y2BaRR在操作条件下,使乙烯生产的能量强度最低。的有限公司gydF4y2Ba2gydF4y2BaRR-GOR体系实现了阴极C的稳定电合成gydF4y2Ba2 +gydF4y2Ba和阳极产品超过80小时,电流密度为100毫安厘米gydF4y2Ba−2gydF4y2Ba,与常规多边环境协定的稳定性相当gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba.该系统保持平均全电池电压为1.90±0.1 V,平均总电压为CgydF4y2Ba2 +gydF4y2BaFE为42%,对所有CO的平均碳效率为~45%gydF4y2Ba2gydF4y2BaRR乘积(图;gydF4y2Ba4摄氏度gydF4y2Ba、表gydF4y2BaS12gydF4y2Ba).同样,我们检测到整个过程中稳定的GOR生产力(图。gydF4y2Ba4摄氏度gydF4y2Ba、表gydF4y2Ba向gydF4y2Ba).值得注意的是,这个COgydF4y2Ba2gydF4y2Ba无论是小gydF4y2Ba2 +gydF4y2Ba电解槽在保持高碳效率的同时表现出高稳定性。gydF4y2Ba
讨论gydF4y2Ba
我们证明了配对COgydF4y2Ba2gydF4y2Ba在中性介质中采用全液体阳极反应,在可再生化学品和燃料的电合成中结合了高碳效率和低能量输入。实现这一策略的一个关键是配对阴极和阳极上的催化剂质量负载,以最大限度地提高COgydF4y2Ba2gydF4y2BaRR产物选择性和最小化阳极OER选择性同时。的有限公司gydF4y2Ba2gydF4y2Ba从阳极下游回收的交叉到阳极的高纯度>99%。退还产地来源证gydF4y2Ba2gydF4y2Ba对于阴极上游,该策略实现了高COgydF4y2Ba2gydF4y2Ba转化率高达75%。该组合系统在电流密度为100 mA cm时实现了1.90 V的低全电池电位gydF4y2Ba−2gydF4y2Ba稳定的电合成CgydF4y2Ba2 +gydF4y2Ba在保持高CO的情况下,产品可以保持80小时以上gydF4y2Ba2gydF4y2Ba转化率为45%。考虑到总电力和下游分离能源成本,该方法每吨乙烯的总能源强度为262 GJ,比以前的CO降低了46%gydF4y2Ba2gydF4y2BaRR电解槽。这为实现CO的高碳效率提供了一条途径gydF4y2Ba2gydF4y2BaRR电解。gydF4y2Ba
方法gydF4y2Ba
材料gydF4y2Ba
碳酸氢钾(KHCOgydF4y2Ba3 gydF4y2Ba, 99.7%), d -葡萄糖(99.5%),铜纳米颗粒(25 nm), NafiongydF4y2BaTMgydF4y2Ba1100 W (5 wt.)在低脂肪醇和水的混合物中%)和Pt/C (40 wt。% Pt在Vulcan XC72上)从Sigma Aldrich购买,并在收到时使用。aquvion D79-25BS离聚体从燃料电池商店购买。阴离子交换膜选用Piperion (40 μm),购自W7Energy公司,保存于0.5 M KOH中。本研究使用的水为18 MΩ milliq去离子水。gydF4y2Ba
电极gydF4y2Ba
产地来源证gydF4y2Ba2gydF4y2Ba采用1 mg mL的催化剂油墨喷涂沉积法制备了气体扩散电极gydF4y2Ba−1gydF4y2Ba含0.25 mg mL的铜纳米颗粒gydF4y2Ba−1gydF4y2Ba全氟磺酸树脂gydF4y2BaTMgydF4y2Ba1100w甲醇到PTFE衬底上,预溅射有200 nm厚的多晶Cu层。以1 Å s的溅射速率制备了Cu靶材gydF4y2Ba−1gydF4y2Ba磁控溅射系统中的聚四氟乙烯薄膜gydF4y2Ba5gydF4y2Ba.铜纳米颗粒在GDE上的质量负载在0.5 ~ 1.0 mg/cm之间gydF4y2Ba2gydF4y2Ba.实验前将gde在空气中干燥一夜。gydF4y2Ba
对于GOR阳极电极,首先将市售Pt/C与离聚体(Aquivion D79-25BS)在玻璃烧杯中物理混合,然后超声1小时。然后将得到的催化剂油墨喷涂在亲水碳布的两侧,直到Pt负载量为0.5-3.2 mg cmgydF4y2Ba−2gydF4y2Ba是实现。gydF4y2Ba
特征gydF4y2Ba
采用FEI Quanta FEG 250环境扫描电镜(SEM)对阴极和阳极进行扫描电镜(SEM)成像。过渡电子显微镜(TEM)图像和元素映射是由FEI Titan 80-300 kV TEM显微镜获得的。电极的x射线光电子能谱(XPS)由型号5600,PerkinElmer使用单色铝x射线源测定。gydF4y2Ba
CO的组装gydF4y2Ba2gydF4y2BaRR-GOR系统gydF4y2Ba
MEA组(5厘米gydF4y2Ba2gydF4y2Ba)是从Dioxide Materials购买的。将阴极切割成2.5 cm × 2.5 cm的片状,放置在具有2.23 cm × 2.23 cm流动窗口的MEA阴极板上。阴极的四个边缘用铜带密封,然后用卡普顿胶带密封,并确保胶带没有覆盖流动窗口。在阴极上小心地放置一个Piperion AEM (40 μm, 3 cm × 3 cm)。在阴极上放置一个2.23 cm × 2.23 cm窗口的垫片。将负载Pt/C的碳布阳极(2 cm × 2 cm)放置在AEM上。gydF4y2Ba
电化学测量gydF4y2Ba
本研究所有数据均以0.5 mg/cm采集gydF4y2Ba2gydF4y2Ba铜(阴极)和2毫克/厘米gydF4y2Ba2gydF4y2BaPt(阳极),除非另有说明。所有性能指标都是在特定条件下稳定至少1000秒后记录的。在这项工作中报告的全电池电压没有红外校正。所有的误差条以基于三次测量的标准偏差表示。电位截止值设置为10v,加在电池上的电流范围为0.2-1.0 A。gydF4y2Ba
评估CO的绩效gydF4y2Ba2gydF4y2Ba在不同条件下的RR-GOR系统中,在MEA的阴极侧加入COgydF4y2Ba2gydF4y2Ba流量(0.18-10 sccm cmgydF4y2Ba−2gydF4y2Ba电极面积,10立方厘米厘米gydF4y2Ba−2gydF4y2Ba(如未指明)来自两个产地来源证gydF4y2Ba2gydF4y2Ba给料和阳极气流,除非另有说明。阳极侧用含有1 M KHCO的溶液循环gydF4y2Ba3 gydF4y2Ba用蠕动泵以10 mL/min的速度注射不同浓度(0.1-2 M)的葡萄糖。阳极液储液器和气液分离器采用具有4个进出通道(进气口、出气口、进液口、出液口)的气密玻璃瓶。在典型CO中gydF4y2Ba2gydF4y2Barr - gregor性能评估表明,气体进口通道是密封的,气体出口通道连接到“Y”形油管连接器。gydF4y2Ba
由于阳极液储层/气液分离器是气密的,COgydF4y2Ba2gydF4y2Ba给料流和阳极流之间的压力最终将得到平衡,并从两侧促进稳定的流量。电化学测量使用恒电位器(Autolab PGSTAT204带10 a升压器)进行。gydF4y2Ba
加热CO的辅助系统gydF4y2Ba2gydF4y2BaRR-OOR电解槽示意图如图所示。gydF4y2BaS15gydF4y2Ba.gydF4y2Ba
评估CO的绩效gydF4y2Ba2gydF4y2BaRR-OER系统,和CO的设置一样gydF4y2Ba2gydF4y2Ba采用RR-GOR体系,只是阳极气流排出,阳极液中不含葡萄糖。gydF4y2Ba
为了评估HER-GOR系统的性能,将阴极替换为Pt/C催化剂喷涂在负载为1.0 mg cm的疏水性碳纸上gydF4y2Ba−2gydF4y2Ba.阴极馈电为8立方厘米厘米gydF4y2Ba−2gydF4y2BaNgydF4y2Ba2gydF4y2Ba执行;执行;gydF4y2Ba2gydF4y2Ba.gydF4y2Ba
产品分析gydF4y2Ba
的有限公司gydF4y2Ba2gydF4y2BaRR气体产物,氧气和COgydF4y2Ba2gydF4y2Ba通过将气体样品注入气相色谱仪(Perkin Elmer Clarus 590),并结合热导率检测器(TCD)和火焰电离检测器(FID)进行分析。气相色谱仪采用分子筛5a毛细管柱和以氩气为载气填料的Carboxen-1000柱。用气泡柱测量了进出电池的气体体积流速。气体产物的FE计算公式如下:gydF4y2Ba
在哪里gydF4y2BaxgydF4y2Ba我gydF4y2Ba气体积的体积分数是多少gydF4y2Ba我gydF4y2Ba,gydF4y2BaVgydF4y2BaMEA阴极出口气体流速为L sgydF4y2Ba−1gydF4y2Ba(由气泡流量计测量),gydF4y2BaPgydF4y2Ba为大气压101.325 kPa,gydF4y2BaRgydF4y2Ba理想气体的常数是8.314 J mol吗gydF4y2Ba−1gydF4y2BaKgydF4y2Ba−1gydF4y2Ba,gydF4y2BaTgydF4y2Ba为K单位的室温,gydF4y2BangydF4y2Ba我gydF4y2Ba生成一分子产物所需的电子数是多少gydF4y2BaFgydF4y2Ba法拉第常数是96485摩尔吗gydF4y2Ba−1gydF4y2Ba,gydF4y2BaJgydF4y2Ba为a中的总电流。为了分析阳极气流成分,将阳极液储层的气体出口通道与油管断开,以便循环到阴极。从阳极液储层的“气体入口”通道输入20 sccm的氩气流量作为载气,以促进CO的准确分析gydF4y2Ba2gydF4y2Ba和OgydF4y2Ba2gydF4y2Ba阳极气体中的组分。gydF4y2Ba
从SC-MEA的阴极侧的液体产品收集使用冷阱包含5 mL 0gydF4y2BaogydF4y2BaC水。采用质子核磁共振波谱法分别定量阴极侧和阳极液侧收集的液体(gydF4y2Ba1gydF4y2BaH NMR)在安捷伦DD2 500光谱仪DgydF4y2Ba2gydF4y2BaO采用水抑制方式和二甲基亚砜(DMSO)作为内标。典型的gydF4y2Ba1gydF4y2BaGOR的H NMR谱如图所示。gydF4y2BaS11gydF4y2Ba.每个液品定量图采用新鲜阳极液,采集时间为30~60分钟。液体产品的FE计算公式如下:gydF4y2Ba
在哪里gydF4y2Ba米gydF4y2Ba我gydF4y2Ba液体产品的数量是多少gydF4y2Ba我gydF4y2Ba在摩尔,gydF4y2BatgydF4y2Ba是产品收集的持续时间(1800~3600秒)。gydF4y2Ba
评价CO的稳定性gydF4y2Ba2gydF4y2BaRR-GOR系统,COgydF4y2Ba2gydF4y2Ba用上述方法对RR气体和阴极产物FE进行了评价。取50 μL(总容量为10升)阳极液,周期性(每15 ~ 20h)采样gydF4y2Ba1gydF4y2BaH核磁共振分析。CO的数量gydF4y2Ba2gydF4y2Ba由该时段开始到结束的浓度增量,推导出某一时段内过渡到阳极液的RR液体产物和GOR液体产物。gydF4y2Ba
还使用配备Aminex HPX-87H柱(Bio-Rad)和反射指数检测器的高效液相色谱法(UltiMate 3000 HPLC)测量GOR的副产物。洗脱液为0.05 M HgydF4y2Ba2gydF4y2Ba所以gydF4y2Ba4gydF4y2Ba,列数保持在60gydF4y2BaogydF4y2BaC。gydF4y2Ba
阳极COgydF4y2Ba2gydF4y2Ba、有限公司gydF4y2Ba2gydF4y2Ba从气缸,KHCOgydF4y2Ba3 gydF4y2Ba葡萄糖分析δgydF4y2Ba13gydF4y2BaC在多伦多大学地球生物学同位素实验室,使用斐尼根气体工作台和热斐尼根MAT 253气源同位素比监测质谱仪gydF4y2Ba47gydF4y2Ba.将Finnigan Gas Bench样品托盘加热至72°C,并装入CO小瓶gydF4y2Ba2gydF4y2Ba气体样品。样品瓶首先用氦气冲洗。有限公司gydF4y2Ba2gydF4y2Ba从阳极气流和钢瓶中提取的样品直接注入到小瓶中。的KHCOgydF4y2Ba3 gydF4y2Ba样品与磷酸反应释放COgydF4y2Ba2gydF4y2Ba.葡萄糖样品(60~300 μg)与1 mL氧化剂溶液(100 mL HgydF4y2Ba2gydF4y2BaO + 4.0 g KgydF4y2Ba2gydF4y2Ba年代gydF4y2Ba2gydF4y2BaOgydF4y2Ba8gydF4y2Ba+ 200 mL 85% HgydF4y2Ba3 gydF4y2Ba阿宝gydF4y2Ba4gydF4y2Ba)释放一氧化碳gydF4y2Ba2gydF4y2Ba48gydF4y2Ba.测量的碳同位素与参考物质CaCO进行了比较gydF4y2Ba3 gydF4y2BaMERCK(内部标准)、IAEA-CO-8、NBS-19和IAEA-CO-1(国际原子能机构环境与贸易参考产品)。碳同位素数据以相对于维也纳Pee Dee Belemnite (VPDB)的标准delta (δ)符号报告。gydF4y2Ba
能源评估gydF4y2Ba
我们评估了乙烯(世界上产量最大的原料)电解槽电、阴极分离和阳极分离的能耗。我们考虑最先进的COgydF4y2Ba2gydF4y2Ba文献中的RR系统,包括中性MEA电解槽,酸性流池和MEA。这种考虑是基于性能指标,包括选择性、生产率和全电池电压——它们的组合反映为生产多碳产品(即乙烯)的能量强度。这些性能指标的接近将有助于细化阳极和阴极分离对生产乙烯的能量需求的影响。我们总结了所有系统的输入参数到模型中。这些输入参数大部分列在表中gydF4y2Ba1gydF4y2Ba都来自文学gydF4y2Ba9gydF4y2Ba这个工作。阴极气体分离分为两个步骤:(i)变压吸附去除COgydF4y2Ba2gydF4y2Ba;(ii)低温蒸馏从氢和CO中分离乙烯。我们采用了最广泛使用的模型之一gydF4y2Ba20.gydF4y2Ba(即沼气升级)用于评估与阴极气体分离相关的能源成本。阳极CO的能量评估gydF4y2Ba2gydF4y2Ba/ OgydF4y2Ba2gydF4y2Ba分离评估详见附注gydF4y2Ba1gydF4y2BaSI。gydF4y2Ba
对于酸性流池和MEA电解槽,考虑到没有CO,我们假设与阳极分离相关的能量成本为零gydF4y2Ba2gydF4y2Ba阳极气体流的可用性gydF4y2Ba14gydF4y2Ba.阳极氧化戈尔产品的分离能不包括在本次评估中。之前的技术经济评估gydF4y2Ba40gydF4y2Ba对电化学气相交换工艺进行了分析,表明电化学气相交换工艺在经济上是可行的。因此,我们假设阳极氧化戈尔产品净化所消耗的能量可以通过销售增值氧化戈尔产品完全覆盖,不包括在不同CO的比较中gydF4y2Ba2gydF4y2BaRR设备。gydF4y2Ba
数据可用性gydF4y2Ba
本研究生成的数据在补充信息和源数据文件中提供。gydF4y2Ba源数据gydF4y2Ba提供了这篇论文。gydF4y2Ba
参考文献gydF4y2Ba
刘志刚,刘志刚,刘志刚。CO的共电解gydF4y2Ba2gydF4y2Ba由于低功耗,甘油作为碳化学品的技术经济改善的途径。gydF4y2BaNat。能源gydF4y2Ba4gydF4y2Ba, 466-474(2019)。gydF4y2Ba
García de Arquer, f.p.等。有限公司gydF4y2Ba2gydF4y2Ba电解多碳产物的活性大于1acmgydF4y2Ba−2gydF4y2Ba.gydF4y2Ba科学gydF4y2Ba367gydF4y2Ba, 661-666(2020)。gydF4y2Ba
Ma, W.等。CO的电催化还原gydF4y2Ba2gydF4y2Ba通过氟改性铜上的氢辅助碳-碳偶联,转化为乙烯和乙醇。gydF4y2BaCatal Nat。gydF4y2Ba3 gydF4y2Ba, 478-487(2020)。gydF4y2Ba
Gabardo, c.m.等人。连续二氧化碳电还原浓缩多碳产品使用膜电极组件。gydF4y2Ba焦耳gydF4y2Ba3 gydF4y2Ba, 2777-2791(2019)。gydF4y2Ba
Li, F.等。CO的分子调节gydF4y2Ba2gydF4y2Ba乙烯转换。gydF4y2Ba自然gydF4y2Ba577gydF4y2Ba, 509-513(2020)。gydF4y2Ba
Ozden, A.等人。采用催化剂/促进剂/传输层的高效乙烯电合成。gydF4y2BaACS Energy Lett。gydF4y2Ba5gydF4y2Ba, 2811-2818(2020)。gydF4y2Ba
Kibria, M. G.等。电化有限公司gydF4y2Ba2gydF4y2Ba化学原料还原:从机械电催化模型到系统设计。gydF4y2Ba放置板牙。gydF4y2Ba31gydF4y2Ba, 1-24(2019)。gydF4y2Ba
Ozden, A.等人。级联有限公司gydF4y2Ba2gydF4y2Ba电还原可以有效地生产无碳酸盐乙烯。gydF4y2Ba焦耳gydF4y2Ba1 - 14gydF4y2Bahttps://doi.org/10.1016/j.joule.2021.01.007gydF4y2Ba(2021)。gydF4y2Ba
希斯勒,J.,谢赫罗斯·卡,叶,a.h.,杰弗,M. W. S. S. a . &萨金特,E. H.乙烯电合成:碱性、膜电极组装和CO的技术经济比较分析gydF4y2Ba2gydF4y2Ba−−公司CgydF4y2Ba2gydF4y2BaHgydF4y2Ba4gydF4y2Ba三轮车。gydF4y2BaACS Energy Lett。gydF4y2Ba6gydF4y2Ba, 997-1002(2021)。gydF4y2Ba
李涛,曹勇,何俊杰,柏林盖特,中国电解有限公司gydF4y2Ba2gydF4y2Ba与氧化有机化学相结合的还原。gydF4y2BaACS分科学gydF4y2Ba3 gydF4y2Ba, 778(2017)。gydF4y2Ba
Bajada, m.a.等。一种无贵金属乙醇氧化耦合CO混合电解槽gydF4y2Ba2gydF4y2Ba合成气转化研究文章。gydF4y2BaAngew。化学。Int。艾德。gydF4y2Ba59gydF4y2Ba, 15633-15641(2020)。gydF4y2Ba
曹,C.等。不同的路径,相同的目标:通过金属有机框架衍生的二维电催化剂,实现具有成本效益和独家甲酸盐生产的配对电合成策略。gydF4y2Ba放置板牙gydF4y2Ba.gydF4y2Bahttps://doi.org/10.1002/adma.202008631gydF4y2Ba(2021)。gydF4y2Ba
梅德韦杰娃,梅德韦杰夫,J. J.,塔塔丘克,S. W., Choueiri, R. M. & Klinkova, A.可持续的两端:电化学CO .gydF4y2Ba2gydF4y2Ba氮废弃物利用与电化学处理相结合。gydF4y2Ba绿色的。化学。gydF4y2Ba22gydF4y2Ba, 4456-4462(2020)。gydF4y2Ba
黄,J. E.等。有限公司gydF4y2Ba2gydF4y2Ba在强酸中电解生成多碳产物。gydF4y2Ba科学gydF4y2Ba372gydF4y2Ba, 1074-1078(2021)。gydF4y2Ba
Rabinowitz, J. A. & Kanan, M. W.低温二氧化碳电解的未来取决于解决一个基本问题。gydF4y2BaCommun Nat。gydF4y2Ba11gydF4y2Ba, 10-12(2020)。gydF4y2Ba
马敏,金,肖肯多夫,I. & Seger, B.离子选择膜在CO碳平衡中的作用gydF4y2Ba2gydF4y2Ba电还原:通过气体扩散电极反应器设计。gydF4y2Ba化学。科学。gydF4y2Ba11gydF4y2Ba, 8854-8861(2020)。gydF4y2Ba
Ma, M., Clark, E. L., Chorkendorff, K. T. T. S. D. & Seger, B.利用气体扩散电极反应器设计对CO2电还原Cu的碳平衡进行了深入研究。gydF4y2Ba能源环境。科学。gydF4y2Ba13gydF4y2Ba, 977-985(2020)。gydF4y2Ba
徐毅,等。模拟烟气的环境科学。gydF4y2Ba能源环境。ScigydF4y2Ba.gydF4y2Ba13gydF4y2Ba, 554-561(2020)。gydF4y2Ba
沃勒尔,E,菲利普森,D,爱因斯坦,D,马丁,N。gydF4y2Ba美国化学工业的能源使用和能源强度gydF4y2Ba.(劳伦斯伯克利国家实验室,2000)。gydF4y2Ba
艾伯森,S. D. & Mogensen, M.低温二氧化碳电解的技术经济评估。gydF4y2BaNat。维持gydF4y2Ba.gydF4y2Bahttps://doi.org/10.1038/s41893-021-00739-xgydF4y2Ba(2021)。10.1002/9780470456309. ch25gydF4y2Ba
O 'Brien, c.p.等人。单道COgydF4y2Ba2gydF4y2Ba通过局部CO电合成多碳产品的转化率超过85%gydF4y2Ba2gydF4y2Ba再生。gydF4y2BaACS Energy Lett。gydF4y2Ba6gydF4y2Ba, 2952-2959(2021)。gydF4y2Ba
杨,K.等。阳离子驱动CO的增加gydF4y2Ba2gydF4y2Ba用于CO的双极膜电极组件gydF4y2Ba2gydF4y2Ba电解。gydF4y2BaACS Energy Lett。gydF4y2Ba6gydF4y2Ba, 4291-4298(2021)。gydF4y2Ba
Shi, X.等。了解水电化学氧化生成过氧化氢的活性趋势。gydF4y2BaCommun Nat。gydF4y2Ba8gydF4y2Ba, 1-12(2017)。gydF4y2Ba
夏,C.等。局部受限的氧气促进电化学水氧化成过氧化氢。gydF4y2BaCatal Nat。gydF4y2Ba3 gydF4y2Ba, 125-134(2020)。gydF4y2Ba
Quan, F.等。CO的高效电化学转化gydF4y2Ba2gydF4y2BaNaCl转化为CO和NaClO。gydF4y2Ba绿色的。化学。gydF4y2Ba21gydF4y2Ba, 3256-3262(2019)。gydF4y2Ba
Vass, endrzydi, B. & Janáky, C.耦合电化学二氧化碳转化与增值阳极过程:一个新兴的范式。gydF4y2Ba咕咕叫。当今。Electrochem。gydF4y2Ba25gydF4y2Ba, 1-9(2021)。gydF4y2Ba
不,j等人。有机氧化与二氧化碳还原电化学联产的一般技术经济分析。gydF4y2BaNat。CommungydF4y2Ba.gydF4y2Ba10gydF4y2Ba, 5193(2019)。gydF4y2Ba
崔,S.等。氧化镍纳米颗粒在CO中氧化生物质的机理研究gydF4y2Ba2gydF4y2Ba用于成对电解的饱和电解质。gydF4y2Ba期刊。化学。列托人。gydF4y2Ba11gydF4y2Ba, 2941-2948(2020)。gydF4y2Ba
王毅,等。CO电法同时合成合成气和醛gydF4y2Ba2gydF4y2Ba和一个醇通过分子电催化。gydF4y2BaACS达成。能源板牙。gydF4y2Ba2gydF4y2Ba, 97-101(2019)。gydF4y2Ba
特克,S.等人。CO的电还原gydF4y2Ba2gydF4y2Ba与CO配对的1,2-丙二醇氧化成乳酸。朝着经济上可行的系统。gydF4y2Ba印第安纳州,Eng。化学。Res。gydF4y2Ba58gydF4y2Ba, 6195-6202(2019)。gydF4y2Ba
贝维拉夸,M.,菲利皮,J.,拉瓦基,A. &马尔基奥尼,A. CO转换中的能源节约gydF4y2Ba2gydF4y2Ba用电解装置给燃料。gydF4y2Ba能源抛光工艺。gydF4y2Ba2gydF4y2Ba, 522-525(2014)。gydF4y2Ba
刘文杰等。葡萄糖电解高效电化学生产葡萄糖酸和H2。gydF4y2BaCommun Nat。gydF4y2Ba11gydF4y2Ba, 1-11(2020)。gydF4y2Ba
Tominaga, M., Shimazoe, T., Nagashima, M. & Taniguchi, I.碳电极负载的双金属金-银纳米颗粒在葡萄糖电催化氧化中的组成-活性关系。gydF4y2Baj . Electroanal。化学。gydF4y2Ba615gydF4y2Ba, 51-61(2008)。gydF4y2Ba
Tominaga, M., Shimazoe, T., Nagashima, M. & Taniguchi, I.葡萄糖在金纳米颗粒修饰的碳电极在碱性和中性溶液中的电催化氧化。gydF4y2BaElectrochem。Commun。gydF4y2Ba7gydF4y2Ba, 189-193(2005)。gydF4y2Ba
Mehtiö, T.等。碳水化合物衍生糖酸的生产和应用。gydF4y2Ba暴击。生物科技启》。gydF4y2Ba36gydF4y2Ba, 904-916(2016)。gydF4y2Ba
Ramachandran, S, Fontanille, P, Pandey, a . & Larroche, C.葡萄糖酸:综述。gydF4y2Ba食品工艺。Biotechnol。gydF4y2Ba44gydF4y2Ba, 185-195(2006)。gydF4y2Ba
伊格莱西亚斯等人。从生物质中生产羧酸的催化路线的进展:可持续聚合物向前迈进了一步。gydF4y2Ba化学。Soc。牧师。gydF4y2Ba49gydF4y2Ba, 5704-5771(2020)。gydF4y2Ba
辛格,O. V.和库马尔,R.葡萄糖酸的生物技术生产:未来的影响。gydF4y2Ba达成。Microbiol。Biotechnol。gydF4y2Ba75gydF4y2Ba, 713-722(2007)。gydF4y2Ba
葡萄糖酸市场规模。gydF4y2Bahttps://www.gminsights.com/industry-analysis/gluconic-acid-marketgydF4y2Ba(2018)。gydF4y2Ba
可汗,m.a.等。太阳能生物质电解途径联合生产氢和增值化学品的技术经济分析。gydF4y2Ba维持。能源燃料gydF4y2Ba4gydF4y2Ba, 5568-5577(2020)。gydF4y2Ba
臧,G.等。中性介质葡萄糖电氧化铜纳米线- mofs -氧化石墨烯杂化纳米复合材料的电化学学报。gydF4y2BaElectrochim。学报gydF4y2Ba277gydF4y2Ba, 176-184(2018)。gydF4y2Ba
A. Larew, L. & Johnson, D.碱性介质中金电极葡萄糖氧化机制的浓度依赖性。gydF4y2Baj . Electroanal。化学。gydF4y2Ba262gydF4y2Ba, 167-182(1989)。gydF4y2Ba
Mello, g.a.b, Cheuquepán, W., Briega-Martos, V. & Feliu, J. M.葡萄糖电氧化Pt(100)在磷酸盐缓冲溶液(pH值7):一个机制研究。gydF4y2BaElectrochim。学报gydF4y2Ba354gydF4y2Ba, 136765(2020)。gydF4y2Ba
丁,C. T.等。有限公司gydF4y2Ba2gydF4y2Ba氢氧化物介导的铜催化突发性界面电还原乙烯。gydF4y2Ba科学gydF4y2Ba360gydF4y2Ba, 783-787(2018)。gydF4y2Ba
Garg, S.等人。电化学CO研究进展与挑战gydF4y2Ba2gydF4y2Ba还原过程:超越新催化剂材料的工程和设计视角。gydF4y2Baj .板牙。化学。一个gydF4y2Ba8gydF4y2Ba, 1511-1544(2020)。gydF4y2Ba
张丽丽,赵志军,龚俊。非均相电催化CO的纳米结构材料gydF4y2Ba2gydF4y2Ba还原及其相关反应机理。gydF4y2BaAngew。化学。——Int。艾德。gydF4y2Ba56gydF4y2Ba, 11326-11353(2017)。gydF4y2Ba
侯,A.等。长寿珊瑚藻记录了拉布拉多海碳同位素的多年代际变化。gydF4y2Ba化学。青烟。gydF4y2Ba526gydF4y2Ba, 93-100(2019)。gydF4y2Ba
Lang, S. Q., Bernasconi, S. M. & Früh-Green, G. L.使用GasBench制备装置对小(μg C)样品和溶解有机质中有机碳的稳定同位素分析。gydF4y2Ba快速Commun。质量范围。gydF4y2Ba26gydF4y2Ba, 9-16(2012)。gydF4y2Ba
作者信息gydF4y2Ba
作者及隶属关系gydF4y2Ba
相应的作者gydF4y2Ba
道德声明gydF4y2Ba
相互竞争的利益gydF4y2Ba
K.X, a.o., D.S.和E.H.S.已经填写了一份临时专利申请:US 63/340,448关于COgydF4y2Ba2gydF4y2Ba这里描述的捕获和转换过程。gydF4y2Ba
同行评审gydF4y2Ba
同行评审信息gydF4y2Ba
自然通讯gydF4y2Ba感谢Sahil Garg和其他匿名审稿人对这项工作的同行评审所做的贡献。gydF4y2Ba
额外的信息gydF4y2Ba
出版商的注意gydF4y2Ba施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。gydF4y2Ba
补充信息gydF4y2Ba
源数据gydF4y2Ba
权利和权限gydF4y2Ba
开放获取gydF4y2Ba本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问gydF4y2Bahttp://creativecommons.org/licenses/by/4.0/gydF4y2Ba.gydF4y2Ba
关于本文gydF4y2Ba
引用本文gydF4y2Ba
谢凯,欧泽登,苗荣凯,苗荣凯gydF4y2Baet al。gydF4y2Ba无需在CO中进行阳极气体分离gydF4y2Ba2gydF4y2Ba通过液体到液体阳极升级的电还原系统。gydF4y2BaNat CommungydF4y2Ba13gydF4y2Ba, 3070(2022)。https://doi.org/10.1038/s41467-022-30677-xgydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/s41467-022-30677-xgydF4y2Ba
这篇文章被引用gydF4y2Ba
防止CO2还原反应电解中CO2交叉的膜电极总成设计gydF4y2Ba
化学通讯gydF4y2Ba(2023)gydF4y2Ba
评论gydF4y2Ba
通过提交评论,您同意遵守我们的gydF4y2Ba条款gydF4y2Ba而且gydF4y2Ba社区指导原则gydF4y2Ba.如果您发现一些滥用或不符合我们的条款或指导方针,请标记为不适当。gydF4y2Ba