摘要
模仿自然光合作用合成碳氢化合物燃料是太阳能到化学能转换的可行策略,其中利用低能光子,特别是近红外光子,是进一步提高转换效率的最终但具有挑战性的目标。等离子体金属已经证明了它们吸收低能光子的能力,然而,在有效地将这种能量耦合到反应物分子中仍然是一个障碍。在这里我们报道宽带等离子体诱导CO2与水发生还原反应,生成CH4产率0.55 mmol g−1h−1对400mw cm以下的碳氢化合物产品具有100%的选择性−2全光谱光照明和表观量子效率为0.38%在800 nm照明。我们发现增强的局域电场在高效多光子吸收和选择性能量转移中起着不可替代的作用,从而获得了如此优异的光驱动催化性能。这项工作为低能量光子利用技术铺平了道路。
简介
人工光合作用通过直接转化CO提供了一种有吸引力的储存间歇性太阳能的方法2H2O和阳光变成碳氢化合物1,2,3.,4.因此,大量的半导体和金属纳米催化剂已经被研究,证明了它们在光驱动CO中的可行性2还原反应(CO2RR)5,6,7.然而,太阳光谱的低利用效率,特别是低能光子,以及能量耦合到反应物分子的缓慢过程是限制其进一步向技术经济应用扩展的两个关键障碍。此外,高能值碳氢化合物的选择性生产涉及多个电子-质子转移步骤通过CO2RR是限制他们潜力的另一个巨大挑战8.
等离子体金属纳米颗粒以局域表面等离子体共振(LSPR)的形式与入射光表现出强烈的相互作用9,10.这种LSPR的吸收波长中心可以通过改变等离子体纳米材料的几何结构(包括对称性、尺寸等)轻松地从紫外(UV)范围调整到近红外(NIR)范围11,12这使得它们有广泛的可能性作为太阳能到化学能转换的光收集单元13,14,15,16,17,18,19.最近,研究证明了特定的等离子体纳米结构能够转化CO2在有机添加剂的帮助下,在激光照射下20.,21表明它们在CO方面的潜力2RR。此外,等离子体诱导的催化反应速率与入射光子数呈超线性幂律关系,量子效率与光子通量呈正相关22.在这种等离子体材料令人着迷的发展过程中,人们发现,快速LSPR弛豫(高达~100 ps)和缓慢的化学还原动力学(几毫秒或几秒)在时间尺度上的不匹配严重阻碍了太阳能的转换效率23,24,25.为了突破这一瓶颈,研究人员利用多功能共催化剂建立了一个有效的桥梁,将热载流子从等离子体材料转移到反应物分子中13,14,15,16,17,26.
在这方面,助催化剂的精确设计朝着高效的热载流子接受能力和独特的CO方向发展2化学吸附能力是非常需要的。本研究采用Au棒作为等离子体采光单元,铜钯合金壳作为辅助催化剂,在无额外牺牲剂的情况下,实现了高效的等离子体诱导人工光合作用,CH达到近100%4全光谱光照下的产品选择性。通过原位近环境压力x射线光电子能谱(NAP-XPS)和密度泛函理论(DFT)的计算,局域电场的出现导致了一个新的孤立态高于费米能量(Ef)和不同分子轨道内电子转移的分化,使得这种独特的太阳能到化学能的转换成为可能。通过优化反应体系,得到了令人印象深刻的CH4产率0.55 mmol g−1h−1通过气固两相系统实现,在800 nm近红外光照下,表观量子效率(AQE)达到了创纪录的0.38%。
结果
Plasmon-induced有限公司2用水还原
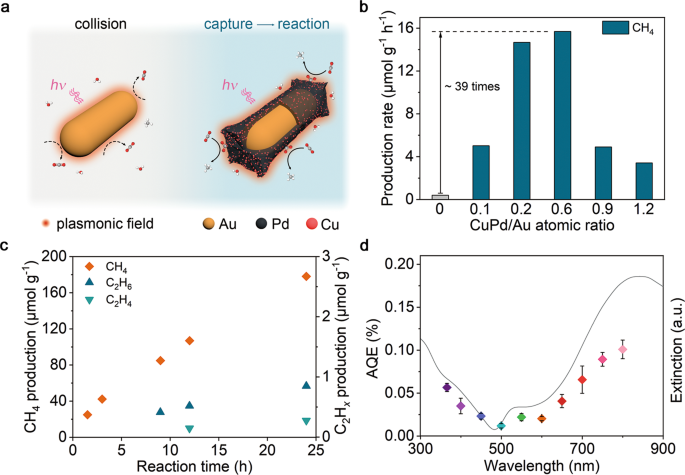
CuPd助催化剂可以捕获CO2并增强CO2这使得反应物能够定位在等离子体元诱导的局部场范围内,增加了它们进一步活化和转化的机会(见图。1).通常,我们通过湿法化学合成获得Au rod@CuPd核壳复合材料(图S1).通过改变金属前驱体的数量,可以很容易地控制Au rod@CuPd核壳复合材料的壳层厚度和Pd/Cu比(见表2)S1,S2和无花果。S2- - - - - -S5制备样品的清单)。带Au rod@CuPd2作为一个例子,透射电子显微镜(TEM)图像(图S3)表明CuPd壳层沉积到Au表面后,棒状结构得以保留。图S中所选区域的快速傅里叶变换模式和放大图像6 a、b,分别沿[110]和[100]方向观察,与纯面心立方晶体结构非常吻合。有序的点阵条纹(间距为2.35和2.05 Å)分别来自于Au晶格的(111)和(002)面,表明前驱体离子在Au棒表面外延还原形成CuPd单晶壳层。x射线衍射(XRD)分析也支持这一结果(图S7)和元素映射剖面(图S .8).此外,Pd和Cu k边x射线吸收近边结构(XANES,图S .9)和傅里叶变换扩展x射线吸收精细结构(EXAFS,图S10)的光谱分析表明,Pd和Cu的总配位数均小于12(见表1)S3),进一步证实了Pd和Cu元素位于样品的最外层。然后利用UV-vis消光光谱对所制备样品的捕光能力进行了评价。如图S所示11,在510 nm和740 nm附近的两个峰分别是Au纳米棒横向和纵向LSPR模式的典型特征27,28.研究发现,与Cu/Pd摩尔比相比,CuPd厚度对光学性能的影响更为突出,使得制备的样品在近红外区域的吸收范围显著拓宽。
一个CuPd助催化剂在捕获CO中的作用示意图2分子。等离子体催化通常发生在离催化剂表面非常近的地方(即在等离子体诱导的局部场范围内)。对于纯金纳米棒,纯金纳米棒和CO的概率2分子通过碰撞接触很低(左),导致CO低2转换效率。对于Au rod@CuPd, CuPd助催化剂可以捕获CO2并增强CO2催化剂表面的浓度,增加了它们进一步活化和转化的机会(右)。bCH的平均产量4在Au rod@CuPd2不同的壳厚度。c时间CH4生产超过Au rod@CuPd224小时后。d计算aques(色点)在Au rod@CuPd2,参照其UV-vis消光光谱(黑线)。误差条表示实验的标准差。的催化实验b,c)均在产地来源证内进行2-饱和水和CO2在400mw cm以下无任何牺牲剂的气氛- - - - - -2全光谱照明。
在全面了解Au rod@CuPd的结构信息和光学性质后,我们评估了它们对CO的有效性2由CO组成的常规反应器中的RR2-饱和水和悬浮催化剂(见图。S12).连续照明3小时后,只有CH4最大产率为15.6 μmol g−1h−1,约为Au棒的39倍,表明Au具有良好的催化性能rod@CuPd2(无花果。1 b).CH的产率4CuPd/Au比值呈现火山状关系,这可归因于CuPd增厚壳层中增加的表面活性位的竞争和加剧的电子-声子散射16.线性随时间变化的CH4产量如图所示。1 c证实了Au的卓越耐用性rod@CuPd2.此外,C2H6和C2H4长期测试后也能检测到,说明反应过程中存在多个质子耦合电子转移过程,这在常规光催化中并不常见。同时,在CH归一化之后4铜的产量(图S中的橙色点)13),不同Cu/Pd原子比样品的催化性能相似,说明Cu在CO中的作用不可分割2RR。波长相关的表观量子效率(aques),与Au的消光谱一致rod@CuPd2,在800 nm处达到0.1%(见图。1 d).这一结果明确地表明了Au rod@CuPd的独特特征2在没有牺牲剂的情况下有效利用低能量光子(参见图S14).在800 nm单色光光照下的循环试验中,CH的产率4保持良好10次(每次3小时,图S15),验证Au rod@CuPd的长期稳定性2.此外,羟基自由基(•OH)被电子自旋共振光谱检测为主要氧化产物(图S16).
产品来源的验证是另一个关键方面。各控制实验条件及结果如图S所示17(另见附表S4详情)。毫无疑问,催化剂,光,CO2和H2O是CO的键2RR over Au rod@CuPd2和CH4很难从碳质化合物的直接光解或热解(例如,用于催化剂合成的表面活性剂和还原剂)中生产。我们进一步利用同步辐射真空紫外光离质谱(SVUV-PIMS)对CH的来源进行了可靠的鉴定4产品。如图S所示18日,a, b, m/z = 16和17处的峰可以分配到12CH4而且13CH4当使用12有限公司2而且13有限公司2分别作为原料气,有力地表明CO2原料气确实是生产CH的碳源4.此外,我们利用离线和频发生振动光谱(SFG-VS)来监测光催化反应过程中形成的表面中间体。如图S所示19日,a, b,光照5分钟后,在2880、2945和2965 cm处出现三个SFG-VS信号−1,它可以被分配到对称拉伸(ν年代C-H),费米共振(ν费米C-H)和不对称拉伸(ν作为生成的甲基的C-H)模式29.这一观察结果有力地证明了CO的进化2和H2O在催化界面上变成甲基。
等离子体诱导催化过程的机理
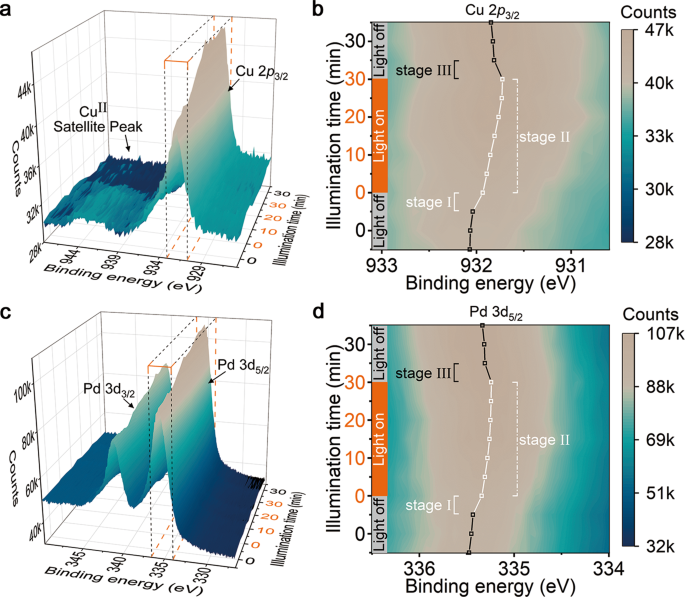
电荷直接转移机制为等离子体诱导催化过程的独特选择性提供了合理的解释30.,31,32.然而,在我们的工作中,一个关键的问题是,单个低能光子(800 nm光~1.55 eV)的能量不足以达到CO的能量势垒2RR不添加牺牲剂。为了深入了解CO的这种低能光子利用能力2RR,我们使用原位NAP-XPS研究了等离子体诱导的催化系统中的光-物质相互作用。所有的NAP-XPS光谱都已用Au 4校准f金箔的核心层,安装在样品旁边(见图S20.).在黑暗条件下,Cu的结合能没有明显的波动(图2)。2 a, b).一旦开灯,Cu峰的结合能瞬间降低(阶段I),随后在光照下逐渐降低(阶段II)。当关灯时,Cu的结合能立即增加(阶段III),但不能恢复到初始水平。根据这些观察,我们可以推断Cu的变化包括两个可以想象的过程,一个是快速可逆的(阶段I和III),另一个是缓慢不可逆的(阶段II)。在阶段I和III中,当入射光与催化剂相互作用发生变化时,电子能量出现波动。这种现象可以归因于热电子在费米能级(Ef),它们的寿命通常只有几百飞秒24,33.在第二阶段,它伴随着铜元素的逐渐消失2图中卫星峰。2,表明在光照下,由于LSPR弛豫产生的热电子,Cu元素逐渐被还原(见图)。S21而且S22).这种化学状态变化是相对缓慢的,可能是缓慢过程的原因。通过分析Pd 3的变化d图中的NAP-XPS谱图2 c, d,我们可以确认Pd与Cu 2表现出相似的三级行为p3/2.从催化作用的角度看,在此基础上存在缓慢的光还原和快速的热电子积累Ef两者是否都有利于提高催化剂的化学势34,35这对于打破其催化限制至关重要。同时,我们也监测c1年代通过原位表征的光谱。如图S所示23在284.4 eV和293.2 eV有两个峰,属于吸附态C (C广告物种)和气态CO2(公司2),可分别观测到。峰面积的相对增加(见图S21)和g-CO结合能的正移位2光照条件下的峰值代表CO的持续吸附2分子及其向碳氢化合物的转化过程36,37,38.
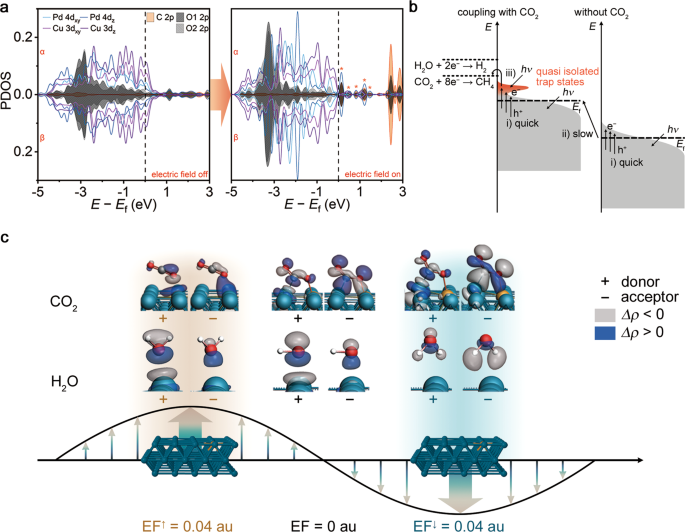
揭示CO2在光照射下被催化剂激活,我们进一步研究了未占据吸附质态的关键作用,通过分析态的投影密度(PDOS,图。3),由催化剂和CO组成的催化体系2分子。以CuPd为催化位点,CO2分子吸附后可与催化剂形成杂化态。在杂化态中引入电场后,计算结果表明杂化态的峰值为O1 2p和O2 2p向更低能量的方向转移,与局部化的Pd 4形成更大的重叠区域dz和cu3dz(平行于电场)状态,增强了关键吸附构型的稳定性39.更重要的是,一系列新的准孤立圈闭态出现Ef在电场存在的情况下,如图所示。3.与附近的连续状态相比Ef在PdCu金属中,这些准孤立阱态可以有效地延长热电子的寿命,并增加电子被另一个低能光子再激发的概率40,41,这使得利用低能光子成为可能。这种多光子吸收行为可以用CH与CH之间的超线性关系来证实4生产速率和光强(见图;S24- - - - - -S27)19,20.,22.综合NAP-XPS收集的信息和理论计算,可以提出CO中等离子体激元诱导电荷转移的机理2RR如图所示。3 b.一般来说,启动和增强等离子体诱导CO有三个关键过程2RR,包括(i)在费米能级以上积累热电子的快速激发(Ef), (ii)缓慢的光还原过程,提高催化位点的化学势,(iii)出现新的准孤立陷阱态,重新激发电子,获得足够的能量来触发CO2RR。在光驱动CO2RR,这三个不同的过程共同作用,实现了低能量近红外光的利用反应。
一个CO的预计态密度(PDOS)2吸附在CuPd(100)表面上,在没有(左)和存在(右)电场指向表面。主要的准孤立圈闭状态用橙色星号标记。bCO中等离子体诱导能量转移的示意图2RR,即y-轴为能量(E),灰色阴影表示填充电子状态。启动和增强等离子体诱导CO的三个关键过程2RR包括(i)费米能级以上的快速激发和电子积累(Ef), (ii)等离子体元诱导的Cu和Pd的缓慢光还原,(iii)耦合CO形成新的孤立陷阱态(原点阴影)2有金属轨道的分子和费米能级以上电子的再激发,最终导致CO2RR的过程。cNOCV轨道与CO中最重要的变形密度有关2和H2在CuPd(100)表面上,没有电场(中间一列),存在电场朝向(右一列)或远离(左一列)表面。左侧为供体NOCV,右侧为受体NOCV。Isovalue设置为0.015。
鉴于杂化态在反应机理中的关键作用,我们进一步研究了由催化位点和CO组成的杂化轨道2或H2O分子的DFT计算。不同场条件下CuPd(100)表面分子的优化几何形状和吸附能如图S所示28.虽然电子从CuPd(100)表面转移到H2O和CO2分子表现出类似的趋势(见图S29),即文书主任2和H2O显示不同的自然化学价轨道(nocv)(图。3 c).详细地说,当电场指向金属表面时,CO2从O单对轨道重新分布到反键π*轨道上,削弱了C-O键,增加了键长。当电场指向远离金属表面时,孤对电子转移到O和金属原子之间的σ轨道上。然而,吸附H2O分子只在H的成键轨道之间振荡2O和Pd原子的轨道。因此,电场对O-H键的裂解提供了很少的帮助。基于这些结果,确定了局域电场可以促进电子向CO的定向转移2分子,这有助于碳氢化合物的选择性生产。
基于催化机制的性能提升
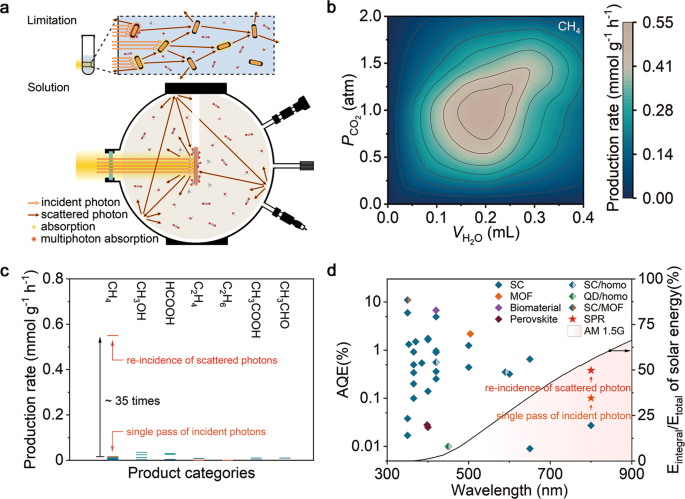
在演示了利用低能光子在等离子体诱导一氧化碳的机会2然而,是否有可能进一步提高光子利用率以增强多光子吸收,这仍然是一个悬而未决的问题。鉴于等离子体催化速率与光子通量(即光强)之间的超线性关系,图S26)时,入射光不可避免的散射损失成为传统反应体系的主要限制(如图2所示)。4).为了克服这一限制,我们设计了一个具有球形结构的气固反应体系来实现散射光子的再入射,该体系仅适用于等离子体催化体系,而不适用于传统的光催化。通过优化H的体积2O和CO的分压2, CH4生产速度的光驱动CO2在该体系中,RR达到0.55 mmol g−1h−1(7.5 mmol g铜−1h−1)低于400mw cm−2全光谱照明(图。4 b),比只允许入射光子通过一次的反应系统高约35倍。为了验证催化性质,计算了周转率(TON)(见补充的文本对细节)。在长期操作中没有观察到催化剂失活的情况下,光照3小时后,每个暴露的铜原子可获得9.6吨。同时,对照实验也在黑暗的高温下进行(图S .)30.和表S5),与催化剂纳米颗粒在光激发下表面的局部温度相匹配,证实了光照的不可缺少。利用等离子体催化机制设计的反应体系使这一转化率远远超过了目前的文献记录(图2)。4摄氏度和表S6).值得注意的是,800 nm气固反应的AQE提高到0.38%。在低能量的近红外光照射下,具有如此优异的光转换效率,甚至可以与CO中的代表性作品的效率相媲美2RR与高能光子,允许我们的Au rod@CuPd2催化剂导致二氧化碳含量创历史新高2近红外光照射下的RR aques(图。4 d和表S7).
讨论
这项工作强调了等离子体诱导局部场在太阳能到化学能量转移过程中不可替代的作用,为等离子体诱导催化实现宽带人工光合作用的潜力提供了引人注目的图景,特别是利用低能光子,为推动等离子体催化的未来发展提供了新的见解。这种低能量光子利用技术未来可能与现有的UV和可见光技术相结合。
方法
材料
四氯戊酸钾(K2PdCl4, 99.99%)取自北京华瑞化工股份有限公司。硼氢化钠(NaBH4, 98%)来自Sigma Aldrich。13有限公司2同位素是从Sigma Aldrich中获得的。二水氯化铜(II2h·22O)是从阿拉丁那里得到的。四水合氯化金(III4h·42O, 99.95%)、抗坏血酸(AA, 99.7%)、十六烷基三甲基溴化铵(CTAB, 99.0%)、十六烷基三甲基氯化铵(CTAC, 98.0%)购自国药控股化学试剂有限责任公司。所有实验使用的水都是去离子水。所有化学试剂均按原样使用,未作进一步纯化。
金棒的合成
通过改进的种子介导生长过程制备了由{100}和{110}面包围的高质量金棒42.在制备种液时,将CTAB (0.2 M, 2.25 mL)水溶液与2.25 mL 0.5 mM HAuCl混合4,并在20毫升的玻璃容器中不断搅拌。然后,将157.5 μL的冰水NaBH水溶液4(16.4 mM)很快增加。然后继续大力搅拌种子溶液,使其形成棕黄色溶液。搅拌1分钟后,在30°C保存30分钟后再使用。
在一个典型的金棒合成过程中,195 mL CTAB (0.1 M)在室温下磁搅拌保存在250 mL锥形瓶中。随后,5 mL HAuCl水溶液4(20 mM)和5 mL AgNO水溶液3.(4 mM)依次注入锥形瓶中。然后将0.1 M的AA水溶液加入上述溶液中,直至溶液的颜色由橙色变为无色。再加300 μL AA (0.1 M)后,用移液管迅速将制备好的种子液1 mL加入烧瓶中。反应1 h后,用去离子水在11000下离心3次rpm10分钟。将沉淀分散在去离子水中,并通过电感耦合等离子体质谱(ICP-MS)进行测量,以供进一步使用。
Au的合成rod@CuPd2
采用外延生长法在Au棒上共沉积了Cu和Pd原子。在典型的Au合成过程中rod@CuPd2样品,70.8 mL含有0.1 M十六烷基三甲基氯化铵(CTAC)的水溶液保存在100 mL圆底瓶中,磁搅拌50°C,然后加入含有4mg金棒的悬浮液。然后K的水溶液2PdCl4(1 mL, 10 mM)和CuCl2(1 mL, 10 mM)加入烧瓶中。随后,立即用移液管向烧瓶中加入2.4 mL 0.1 M的抗坏血酸水溶液。反应1 h后,用去离子水在9500下离心3次rpm10分钟后再分散到4ml去离子水中。
Au的合成rod@CuPdx-y
其他Au rod@CuPdx-y除了使用不同量的K外,采用类似的程序合成样品2PdCl4和CuCl2.K的使用2PdCl4和CuCl2(1) 1.2 mL K2PdCl4800 μL CuCl2Au rod@CuPd2.5, (2) 1.4 mL K2PdCl4600 μL CuCl2Au rod@CuPd3.6, (3) 1.6 mL K2PdCl4400 μL CuCl2Au rod@CuPd6.1, (4) 1.8 mL K2PdCl4200 μL CuCl2Au rod@CuPd8.8, (5) 1.9 mL K2PdCl4100 μL CuCl2Au rod@CuPd14.2(6) 200 μl k2PdCl4200 μL CuCl2Au rod@CuPd2-0.1, (7) 500 μl k2PdCl4500 μL CuCl2Au rod@CuPd2-0.2, (8) 1.5 mL K2PdCl41.5 mL CuCl2Au rod@CuPd2-0.9, (9) 2.0 mL K2PdCl4和2.0 mL CuCl2Au rod@CuPd2-1.2。
原位NAP-XPS表征
在国家同步辐射中心(NSRRC)的x射线光电子能谱和紫外光电子能谱终端站(BL24A1)进行了原位NAP-XPS。该装置由样品负载锁定室、制备室和分析室三个室组成。分析室配备了specphoibos 150能量分析仪。将催化剂滴到透明硅片上,在室温下干燥。样品装入负载锁定室,送入制备室进行10 min的氩离子溅射处理。高纯度有限公司2(99.9999%)进入分析室,分压保持在0.25 mbar。然后将样品送入分析室。以Xe灯源(PLS-SXE300D, Beijing Perfectlight)为光源,用1170 eV光子记录NAP-XPS。cu2p, Pd 3d及c1年代连续记录光谱1 h,中间30 min时在分析室内引入光照。入射光子能量以Au 4为基准进行校准f用安装在样品旁边的金箔测量核心水平。
和频产生振动光谱学表征
我们在Au rod@CuPd上进行了离线SFG-VS研究2使用自制的SFG-VS光谱仪。简单地说,一个1 kHz Ti:Sapphire激光放大系统(Spitfire Ace, spectrum - physics)被用于产生一个中心波长为800 nm的~80 fs脉冲,脉冲能量为6 mJ。大约3mj的输出被输入到一个光学参数放大器(TOPAS Prime, Light Conversion)中,以产生飞秒宽带红外(IR)脉冲,而另一部分800 nm基本光束(~1.2 mJ)被引导到一个4f脉冲整形器中,产生以800 nm为中心的窄带上转换脉冲,FWHM约为7 cm−1.宽带IR和窄带上转换脉冲在空间和时间上均在样品表面重叠,入射角分别固定在45°和63°。用高分辨率光谱仪(SR-500i-A, Andor Inc.)和CCD探测器(Du970P-BVF, Andor Inc.)在反射几何中获取和频产生信号。在SFG-VS测量之前,样品薄膜沉积在CaF的平坦一侧2半缸支撑,用水蒸气冲洗20分钟,完全去除碳氢化合物表面活性剂。将新制备的薄膜转入CO2-饱和超纯水环境封闭的聚四氟乙烯容器,随后暴露在宽频照射(Xe灯)20分钟。在离线SFG-VS实验中,Au rod@CuPd的IR和上转换脉冲的平均脉冲分别保持在3.0和9.0 μJ2在购买力平价(p-SFG, p-Vis, p-IR)和ssp(s-SFG, s-Vis和p-IR)极化,以避免任何表面损伤。所有SFG信号均为600k次。
描述
透射电镜(TEM)图像在日立H-7700型显微镜上拍摄,加速电压为100 kV。在JEOL ARM-200F型场发射透射电镜上,在200 kV加速电压下记录了高分辨率透射电镜图像和能谱图。粉末XRD图谱使用日本Rigaku DMax-γA旋转阳极x射线衍射仪,配备衍射束石墨单色仪(Cu Kα辐射(λ = 1.54178 Å))。用HCl和HNO的混合物溶解样品后,用Thermo Scientific PlasmaQuad 3电感耦合等离子体质谱仪(ICP-MS)测定样品中各元素的浓度3.(3:1,体积比)。用Agilent Technologies的Cary 60光谱仪记录了300 - 1000nm光谱区域的紫外-可见(UV-Vis)消光光谱。样品用去离子水稀释到相同浓度,然后在石英比色皿中测量。
光催化有限公司2还原反应测定
光驱动催化CO2RR是在自制石英管中进行的。通常情况下,将1 mg催化剂样品(基于电感耦合等离子体质谱,ICP-MS测量)分散在管中的去离子水(18.25 MΩ cm)中,使总悬浮液体积达到4 mL,然后将其抽真空并用高纯度CO饱和2(99.9999%)三次,充1atm高纯CO后用玻璃塞密封2(99.9999%)。随后大力搅拌悬浮液,并使用Xe光源(PLS-SXE300D, Beijing PerfectLight)在400 mW cm的光强下进行照明2(全光谱光线)。然后用配备火焰电离检测器(FID)的气相色谱法(GC, 7890 A, Agilent)分析所产生的反应气体。在黑暗环境中进行对照实验,除了用铝箔排除光线或用高纯度Ar(99.9999%)排除二氧化碳外,其余条件相同。
光催化有限公司2气固两相反应器的还原测量
光驱动催化CO2RR是在一个直径为10厘米的球形反应器中进行的,该反应器配有一个直径为1厘米的石英窗作为进光口。在球形反应器内部均匀涂覆泡沫聚四氟乙烯,其在400、600、800和1000 nm处的反射率分别为0.978、0.991、0.989和0.988。一般情况下,0.5 mg催化剂样品(基于ICP-MS测量)均匀分散在直径3 cm的石英棉片上,然后在惰性气氛中轻轻干燥,并安装在积分球反应器中心,面向光入口。随后,0-0.4 mL CO2将饱和水滴在石英羊毛片上。反应器用石英窗密封后,高纯度CO2(99.9999%)对反应器进行净化,并充装至0 - 2atm。然后是Xe灯源(PLS-SXE300D,北京完美之光,400毫瓦厘米2全光谱)作为光源,从光入口照射催化剂。然后用配备FID的气相色谱(GC, 7890 A, Agilent)分析所产生的反应气体。在相同的条件下,除用铝箔纸遮光或排除CO外,在黑暗环境中进行对照实验2含高纯度Ar(99.9999%)。
计算的细节
使用ADF-BAND 2019程序进行周期边界条件(PBC)的DFT计算。采用Perdew-Burke-Ernzerhof交换相关泛函与DFT-D3 (BJ)色散校正和TZP基集结合ZORA方法,在自旋不受限方案下考虑标量相对论效应。一个5×5块采用三层原子层来模拟掺杂Cu的Pd(100)表面。在几何优化过程中,只有顶部层被放松,底部两层被冻结在体块位置。一个3.×3.×1 k采用点网格对二维PBC下的第一布里渊区进行采样。一个\ \ varGamma \ ()只有k对化学价自然轨道扩展的扩展体系(pEDA)采用-网格法进行能量分解分析。由于光子与等离子体金属的强相互作用可产生交变电场,该电场在金属表面附近,遵循正弦定律(E=一个罪t,在那里E,一个而且t分别为电场强度、振幅和时间)。为了研究LSPR诱导的电场对吸附分子的影响,在特定电场条件下模拟了这些分子的吸附能和键长。考虑到正弦函数的单调性和周期性,研究了三个最具代表性的条件。具体地说,当t= 0或π,t= π/2和t= 3π/2,和一个= 0.04 au, theE取值分别为0、0.04和−0.04 au。综上所述,考虑表面等离子体激元极化子产生的场,在模拟中应用了指向/远离衬底方向的外部电场。
参考文献
曹哲,张春杰。人工光合作用的混合催化剂:分子、材料和生物催化的融合方法。Acc。化学。Res。53, 575-587(2020)。
金属配合物/半导体杂化光催化剂和光电极CO2可见光驱动的还原。放置板牙。31, e1808205(2019)。
张波,孙林。人工光合作用:分子催化剂的机遇与挑战。化学。Soc。牧师。48, 2216-2264(2019)。
陈松,齐勇,李春,杜门凯,张飞。人工光合作用颗粒光催化剂的表面策略。焦耳2, 2260-2288(2018)。
李霞,于俊,陈霞。CO选择性光还原的辅助催化剂2变成太阳能燃料。化学。牧师。119, 3962-4179(2019)。
Wan, L.等。铜2具有混合氧化态面的O纳米立方,用于二氧化碳的(光)催化加氢。Catal Nat。2, 889-898(2019)。
吴,等。M0.33WO3直接从空气中光催化CO2的高选择性转化:全光谱诱导反应机理研究j。化学。Soc。141, 5267-5274(2019)。
余淑娟,Wilson A. J., Kumari, G., Zhang X. & Jain P. K.太阳能驱动二氧化碳在等离子体催化剂燃料转化中的机遇和挑战。ACS Energy Lett。2, 2058-2070(2017)。
奥尔森,J.等。单等离子体纳米粒子的光学表征。化学。Soc。牧师。44, 40-57(2015)。
贵金属纳米结构动力学的光学研究。化学。牧师。111, 3858-3887(2011)。
李晓霞,夏阳。银纳米立方体和金纳米笼的合成。Protoc Nat。2, 2182-2190(2007)。
柯蒂,m.b. & McDonagh, m.a.杂化和合金等离子体纳米粒子的合成和光学性质。化学。牧师。111, 3713-3735(2011)。
胡,C.等。表面等离子体使氮固定在纯水通过解离机制在温和条件下。j。化学。Soc。141, 7807-7814(2019)。
郑铮,Tachikawa, T. & Majima, T.利用各向异性Pd-Au纳米棒在单颗粒水平上研究了等离子体元增强甲酸脱氢。j。化学。Soc。137, 948-957(2015)。
郑铮,田川,马岛,等。pt修饰金纳米棒在可见光到近红外区域等离子体增强产氢的单粒子研究。j。化学。Soc。136, 6870-6873(2014)。
黄,H.等。揭示核壳纳米结构表面等离子体衰变对宽带光驱动催化有机合成的影响。j。化学。Soc。138, 6822-6828(2016)。
郭,J.等。在异质上层结构中促进热电子的等离子体增强催化。j。化学。Soc。139, 17964-17972(2017)。
穆克吉,S.等。热电子做了不可能的事:等离子体诱导H2在非盟。Nano。13, 240-247(2013)。
张欣,等。等离子体光催化二氧化碳加氢反应的产物选择性。Commun Nat。8, 14542(2017)。
余淑娟,许俊杰,许建平,等。等离子体等离子体控制可见光驱动CO中多电子转移和碳碳耦合2金纳米粒子的教育。Nano。18, 2189-2194(2018)。
于淑娟,李志强,李志强,等1- c3.由离子液体辅助的二氧化碳中的碳氢化合物。Commun Nat。10, 2022(2019)。
李志刚,李志刚,李志刚。等离子体纳米结构光催化反应的奇异特性和独特的化学键激活机制。Nat。板牙。11, 1044-1050(2012)。
詹,C.等。从等离子体增强分子光谱到等离子体介导的化学反应。化学。2, 216-230(2018)。
张杨,等。表面等离子体驱动的热电子光化学。化学。牧师。118, 2927-2954(2018)。
波尔特,J.等。在毫秒时间分辨率下,通过原位小角度x射线散射研究了金纳米颗粒的成核和生长。ACS Nano4, 1076-1082(2010)。
Aslam, U, Chavez, S. & Linic, S.控制等离子体催化多金属纳米结构中的能量流。Nat。纳米技术。12, 1000-1005(2017)。
林克,S. & El-Sayed, M. A.金和银纳米点和纳米棒中表面等离子体电子振荡的光谱性质和弛豫动力学。期刊。化学。B103, 8410-8426(1999)。
杨丽娟,李丽娟,李丽娟。高纵横比圆柱形金纳米棒的湿化学合成。期刊。化学。B105, 4065-4067(2001)。
冯荣军,李晓霞,张志军,陆正哲,郭艳。DPPC单分子膜在空气/水界面振动和频生成中的光谱分配和方向分析。j .化学。理论物理。145, 244707(2016)。
Boerigter, C., Campana, R., Morabito, M. & Linic, S.直接电荷激发作为等离子体元介导的光催化的主导机制的证据和意义。Commun Nat。7, 10545(2016)。
Rao, V. G., Aslam, U. & Linic, S.从等离子体金属纳米颗粒中提取高能载流子以进行电子转移反应的化学要求。j。化学。Soc。141, 643-647(2019)。
Boerigter, C. Aslam, U. & Linic, S.电荷从等离子体纳米结构转移到化学附着材料的机制。ACS Nano10, 6108-6115(2016)。
Linic, S, Aslam, U, Boerigter, C. & Morabito, M.等离子体金属纳米颗粒的光化学转化。Nat。板牙。14, 567-576(2015)。
金,Y.,史密斯,J. G.和Jain, P. K.收集通过等离子体激发金纳米颗粒产生的多个电子空穴对。Nat,化学。10, 763-769(2018)。
金,Y. Dumett Torres, D. & Jain, P. K.等离子体催化剂的活化能。Nano。16, 3399-3407(2016)。
法瓦罗,等人。地下氧化物在CO中起着关键作用2被Cu(111)表面活化形成化学吸附CO2这是减少二氧化碳排放的第一步。国家科学院学报美国114, 6706-6711(2017)。
卡特尔,S.等。有限公司2氧化物载体PtCo催化剂上的加氢:氧化物载体在决定产物选择性中的作用。Angew。化学。Int。艾德。55, 7968-7973(2016)。
邓,等。CO存在下Cu的表面化学2和H2O。朗缪尔24, 9474-9478(2008)。
吴慧,张宁,王慧,洪山。CO的吸附2在铜2O(111)氧空位面:第一性原理研究。化学。理论物理。列托人。568 - 569, 84-89(2013)。
王晓霞,龙瑞。热驱动的双金属纳米颗粒动态形状变化延长了Pt/MoS的热电子寿命2催化剂。期刊。化学。列托人。12, 7173-7179(2021)。
梁,L.等。红外光驱动一氧化碳2室温下整体分裂。焦耳2中国农业科学,1004-1016(2018)。
nioobakht, B. & El-Sayed, M. A.利用种子介导生长方法制备金纳米棒(NRs)及其生长机制。化学。板牙。15, 1957-1962(2003)。
确认
国家重点研发计划项目(2020YFA0406103),国家自然科学基金(22122506,22075267,22109152,22232003,21725102,91961106,21950410514,22109148),中科院战略重点计划项目(XDPB14),中科院青年创新促进会(2019444),人因工程国家重点实验室开放基金项目(SYFD062010K),中国博士后科学基金(2021M693063)资助。在国家同步辐射中心(NSRRC)的x射线光电子能谱和紫外光电子能谱终端站(BL24A1)进行了原位NAP-XPS实验。XAFS测量在北京同步辐射设施(BSRF)的光束线1W1B和上海同步辐射设施(SSRF)的光束线BL14W1进行。感谢中国科技大学微纳米研究与制造中心的支持。
作者信息
作者及隶属关系
贡献
R.L.和Y.X.监督这个项目。C.H.和J.L.设计了实验。C.H.进行了实验并分析了结果。X.C.进行了DFT模拟。J.J.和He l帮助合成了催化剂。D.W.帮助评估催化剂的性能。y.w.y., s.c., h.j., c.h.w.和L.S.对近环境压力x射线光电子能谱(NAP-XPS)的原位表征做出了贡献。Hao L.和Z.L.对离线和频产生振动光谱(SFG-VS)的表征做出了贡献。c.h.、j.l.、r.l.和Y.X.撰写了这篇论文,并听取了其他作者的意见和意见。c.h.、X.C和J.L.对这项工作同样作出了贡献。
相应的作者
道德声明
相互竞争的利益
国家知识产权局授权专利申请(专利权人:中国科学技术大学;发明人姓名:Y.X., c.h., R.L.;专利申请号:202110378508.5;申请状态:收到;专利申请中涉及的手稿的具体方面:一种由红外光驱动的二氧化碳催化转化方法)。其余作者声明没有竞争利益。
同行评审
同行评审信息
自然通讯感谢Jennifer Strunk和其他匿名审稿人对这项工作的同行评审所做的贡献。可以获得同行评审报告。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
源数据
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
胡超,陈鑫,Low, J。et al。近红外宽带公司2表面等离子体与水还原成碳氢化合物。Nat Commun14, 221(2023)。https://doi.org/10.1038/s41467-023-35860-2
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41467-023-35860-2