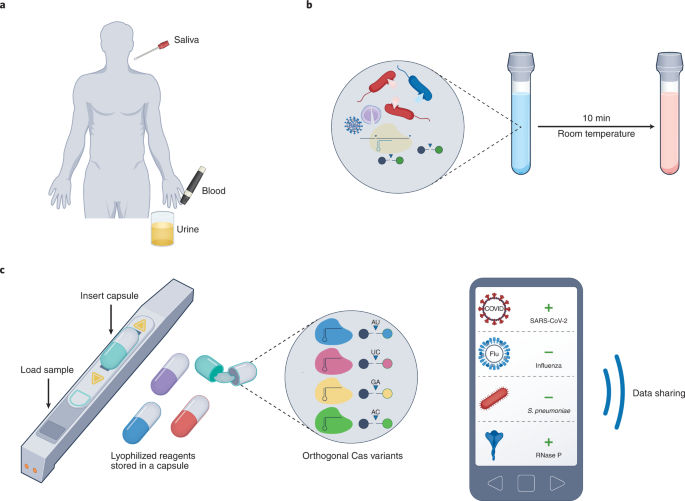
利用crispr相关酶Cas13和等温RNA扩增检测病毒RNA的方法正在简化,以便即时使用。
世界上近一半的人口无法获得适当的诊断1.这是一个多因素问题,在大流行期间,限制病毒传播和新关切变种(VOCs)的出现是至关重要的。基于逆转录定量PCR (RT-qPCR)的检测仍然是核酸检测的金标准,但它们需要中央设施、训练有素的人员和昂贵的试剂2.然而,常规监测和重复检测病原体需要廉价、敏感和特定的即时护理(POC)或在家诊断3..
基于CRISPR (clustered regularly interspaced short palindromic repeats的缩写)的诊断测试在敏感性、特异性和稳健性方面具有优势,其设计适用于POC或家庭使用。许多基于crispr的诊断(CRISPR-Dx)已经使用了crispr相关(Cas)酶Cas9(参考文献4,5);然而,Cas13(参考文献.6)和Cas12(参考文献7,8)可以更好地检测阳性信号,这是由于这些酶的旁切活性(也就是说,它们在酶激活时对核酸的不加区分的切割被利用来解淬核酸结合的荧光团)。然而,CRISPR-Dx还不符合世界卫生组织用于POC或家庭测试的ASSURED标准(即负担得起、敏感、特定、用户友好、快速、无需设备和交付)。主要挑战涉及样品处理、测定灵敏度、试剂的保质期以及开发可以大规模生产的廉价且易于使用的测定方法9.
两项研究发表于自然生物医学工程举例说明如何解决其中一些挑战。一方面,Cameron Myhrvold和他的同事报告了他们之前报道的简化样品处理和试剂存储解决方案10基于cas13的检测方法SHINE(流线型突出感染以导航流行病的缩写),并对其进行了修改,以检测新出现的VOCs11.另一方面,Patrick Hsu、David Savage、Jennifer Doudna及其合作者描述了一种便携式微流控设备,他们将其命名为DISCoVER(冠状病毒酶报告诊断的缩写),该设备半自动地执行环介导的等温扩增和RNA转录,cas13介导的检测和信号读出12.
Myhrvold及其合著者改进的SHINE检测方法(shinv .2)无需设备,并在环境温度下快速处理样品。作者发现,一种商用裂解试剂(“FastAmp病毒和细胞溶液”,与等温核酸扩增兼容,在环境温度下工作)与SHINE兼容,并通过添加RNase抑制剂有效灭活严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)病毒粒子和核酸酶。此外,他们优化了试剂冻干过程(通过添加辅料蔗糖作为稳定剂和甘露醇作为膨胀剂,并通过去除不稳定试剂聚乙二醇和氯化钾),以在缺乏冷链基础设施的情况下(在资源匮乏的情况下,经常需要将试剂长途运输到最终用户)保持测定的性能。SHINEv冻干试剂。2maintained their activity after five months at 4 °C, but only for one week when stored at room temperature. The authors also simplified the assay readout, performed in lateral-flow format via a paper strip, by optimizing the composition of a crowding polymer needed for nucleic acid amplification, to enhance flow and thus avoid the need for a dilution step. Moreover, the authors adapted SHINE to rapidly discriminate SARS-CoV-2 VOCs; however, the detection limit of the VOCs was lower than that for the original strain of the virus. Further improvements would be needed to ensure high confidence in the detection of VOCs from nasopharyngeal samples. Clinical validation against RT–qPCR and antigen-capture kits (Abbott’s BinaxNow and Access Bio’s CareStart) showed that SHINEv.2 was 50 times more sensitive than either antigen test, albeit with a slower turnaround time, and that the assay excelled at detecting samples with moderate viral loads (RT–qPCR cycle-thresholds of 25–30). Also, SHINEv.2 correctly identified all positive samples with titres above the analytical limit of detection of 200 copies of the virus per microlitre.
尽管克服了样品处理,保质期储存和读数的限制,SHINEv。2没有准备好POC使用。该方法包括两个液体处理步骤:冻干试剂的再水化,以及将10% (v/v)的裂解样品转移到检测混合物中。理想的POC诊断测试不需要液体处理,并且可以提供一步采样-输入-输出的解决方案。这可以通过开发将样品裂解、核酸扩增、cas13介导的检测和单步检测读出结合在一起的通用化学来实现,或者通过开发一种便携式封闭形式的设备来实现,该设备自动执行所有液体处理步骤,并且具有抗污染性(图2)。1).
事实上,这就是Hsu和DISCoVER实验的合著者所采用的方法。该设备由三个微流体室(承载导致核酸扩增和检测的温控反应,以及信号采集)、一个围绕扩增室的加热器(将其保持在65°C)、一个热电加热器和冷却器(将检测室保持在25°C)、空气排量泵、阀门和定制荧光探测器组成。将裂解的唾液样本装入第一个腔室,在那里进行扩增和转录反应30分钟。然后打开阀门,将4 μl的反应产物计量到cas13基检测混合物中(这大约需要5分钟)。然后,检测混合物进入荧光检测室,在那里获取信号。
DISCoVER检测使用两个简单的步骤进行无萃取样品处理:在75°C下热变性,然后使用耐架子稳定的还原剂TCEP(三(2-羧乙基)磷化氢)与离子螯合剂EDTA(乙二胺四乙酸)进行化学还原。TCEP-EDTA可以干扰cas13介导的扩增和反应,但低浓度的TCEP-EDTA可以保护RNA,不影响下游反应。
在优化反应化学反应后,Hsu和合著者使用一系列稀释病毒液和合成RNA样本测试了DISCoVER检测的敏感性和特异性。该检测方法的分析极限为每微升约40份RNA拷贝,并且当对添加了不同病毒的唾液样本进行测试时,其特异性为100%。使用20个每微升添加40-200个RNA拷贝的唾液样本和5个阴性样本,微流控设备在所有20个样本中检测到病毒RNA,平均样本-应答时间为78分钟。需要进行更大规模的验证研究,涉及具有广泛周期阈值范围的样本,以适当确定DISCoVER检测方法对POC使用的敏感性、特异性和适用性。
POC诊断试剂盒需要内部控制,以便可以验证试剂盒的正确性能。徐秀珍和合著者使用了SARS-CoV-2的引物N基因和RNaseP基因作为内控,并将扩增后的反应混合物分成两个检测室。这种多路检测可以通过利用Cas13和Cas12酶的不同侧枝切割活性来扩展13具有不同的解理基序,可产生不同的输出颜色,用于多种病毒的光学检测,并实现多种内控序列。
参考文献
弗莱明,k.a.等人。《柳叶刀》398, 1997-2050(2021)。
Esbin, M. N.等。核糖核酸26, 771-783(2020)。
Larremore, d.b.等人。科学。睡觉。https://doi.org/10.1126/sciadv.abd5393(2021)。
阿里,Z.等。ACS合成器。医学杂志。11, 406-419(2022)。
Marsic, T.等人。Nano。21, 3596-3603(2021)。
古登伯格,J. S.等。科学356, 438-442(2017)。
陈,J. S.等。科学360, 436-439(2018)。
阿曼,R.等人。前面。Bioeng。Biotechnol。9, 800104(2021)。
卡明斯基,M. M.,阿卜达耶,O. O.,古登堡,J. S.,张飞,柯林斯,J. J.。Nat,生物医学。Eng。5, 643-656(2021)。
Arizti-Sanz, J.等。Commun Nat。11, 5921(2020)。
Arizti-Sanz, J.等。Nat,生物医学。Eng。https://doi.org/10.1038/s41551-022-00889-z(2022)。
钱德拉塞卡兰,s.s.等人。Nat,生物医学。Eng。https://doi.org/10.1038/s41551-022-00917-y(2022)。
古登伯格,J. S.等。科学360, 439-444(2018)。
Hu, M.等。国家科学院学报美国119, e2202034119(2022)。
Mahas, A.等。国家科学院学报美国119, e2118260119(2022)。
作者信息
作者及隶属关系
相应的作者
道德声明
相互竞争的利益
M.M.已经申请了耐热Cas13用于CRISPR诊断应用的专利。A.G.声明没有竞争利益。
权利和权限
关于本文
引用本文
Ghouneimy, A., Mahfouz, M.通过Cas13简化SARS-CoV-2检测。Nat,生物医学。英格6, 925-927(2022)。https://doi.org/10.1038/s41551-022-00926-x
发表:
发行日期:
DOI:https://doi.org/10.1038/s41551-022-00926-x