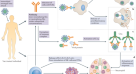
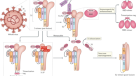
此前对严重急性呼吸综合征冠状病毒(SARS-CoV)疫苗的研究发现,细胞免疫病理和抗体依赖性增强是潜在的安全问题。我们讨论了这些发现对COVID-19疫苗开发的影响,以及我们优化安全性和有效性的方法。
在未来几周和几个月里,我们可能预计至少有十几种新的COVID-19疫苗将进入临床测试和开发阶段。这些实验性疫苗包括一系列创新和传统技术,从包装的核酸和病毒载体到与佐剂结合的重组蛋白1.这些疫苗的设计基于自2003年以来收集的人类免疫学数据,当时严重急性呼吸综合征冠状病毒(SARS-CoV)首次在中国南方出现,以及在实验动物和体外模型上进行的近20年的研究。
人类相关人群研究包括评估康复患者抗SARS-CoV的持续抗体,特别是针对SARS-CoV刺突(S)蛋白及其受体结合结构域(RBD)的人抗体,RBD是病毒与其唯一已知的宿主细胞进入受体血管紧张素转换酶2 (ACE2)结合所需的成分。2.由于从SARS-CoV康复患者身上转移的血浆可能会降低死亡率,许多研究人员现在将S蛋白或RBD作为疫苗靶点。事实上,在一系列实验动物(包括表达人类ACE2的转基因小鼠、雪貂和非人灵长类动物)中进行的研究证实,这类疫苗对SARS-CoV挑战感染具有保护性免疫。

虽然由SARS-CoV-2引起的COVID-19最近才出现,但已经有研究正在研究S蛋白或其RBD是否具有类似的疫苗靶标。早期临床试验将需要迅速加速新型SARS-CoV-2疫苗的研制1或者在某些情况下,重新利用已经开发出的“现成”疫苗来对抗sars冠状病毒3.基于对SARS-CoV的中和抗体可以交叉结合并中和SARS-CoV-2的发现(参考文献)。4).
虽然必须及时推进COVID-19疫苗,以应对当前的大流行,但我们也必须认识到,存在潜在的安全问题,可能会减缓临床开发和测试的进程。尽管之前对SARS疫苗进行的两项I期临床试验没有发现早期的安全性问题,但基于体外观察或在动物接种SARS冠状病毒疫苗的实验中进行的观察,人们存在担忧。具体来说,这些研究确定了病毒攻击后免疫动物的两个潜在安全信号:细胞免疫病理;抗体依赖性增强(ADE)。在这里,我们简要地总结了这种免疫增强的双重或双面性,并就如何指导COVID-19疫苗设计提出了我们的观点。
细胞免疫病理
在第一批实验性SARS-CoV疫苗的早期测试期间,在免疫和病毒挑战感染之后,一些实验动物出现了肺或肝脏组织病理学,其特征是淋巴细胞、单核细胞和嗜酸性粒细胞的大量组织浸润5.与组织免疫病理相关的嗜酸性粒细胞的优势引起了人们对辅助性T细胞2 (TH2)类型的免疫反应可能是负责的,有时直接指向病毒诱导的SARS核衣壳(N)蛋白的表达。然而,我们深入的文献分析表明TH反应可以指导这些细胞反应6在使用灭活病毒和以病毒载体提供的疫苗进行免疫之后,以及其他关键要素。在某种程度上,这些证据包括TH细胞发育和IL-6,一种细胞因子在经历细胞因子风暴的COVID-19患者中强烈上调(连同IL-8诱导)。进一步的支持来自IL-17在促进嗜酸性粒细胞活化、从骨髓募集和外渗到靶器官(如肺)中的作用7研究发现,明矾是一种促进TH2型免疫,实际上减少了免疫病理5.这些观察结果强调了选择疫苗传递平台和佐剂的潜在重要性,使宿主反应远离TH17型免疫偏倚。
锁定增强
ADE是第二个问题,通常发生在非中和抗体与新感染的病毒结合,通过Fcγ受体(Fcγ rs)促进增强的病毒摄取进入宿主细胞时。8.也许最著名的ADE例子发生在感染多种登革热病毒血清型之后,由Halstead和O 'Rourke在20世纪70年代首次报道,现在正在影响新的登革热疫苗的设计。然而,ADE也可能影响几种重要的人类呼吸道病毒感染的临床病程。例如,一项观察性研究发现,2008-2009年的三价季节性流感灭活疫苗可能在H1N1流感大流行期间导致了加重的疾病,尽管另一项研究实际上发现了相反的结果。由20世纪60年代福尔马林灭活呼吸道合胞病毒(RSV)疫苗引起的免疫增强疾病也可能部分来自ADE,可能来自对由福尔马林改变的病毒抗原的非中和抗体,尽管也有可能TH上面强调的17种回答也可能是相关的。
关于ADE在严重冠状病毒感染中的作用,有相互矛盾的数据。针对S蛋白的抗体可以在体外增强细胞对病毒的摄取,尽管这些发现的临床相关性是相互矛盾的。例如,有临床研究发现SARS- cov特异性抗体对SARS患者无害,尽管已经注意到非中和性冠状病毒抗体可能导致猫传染性腹膜炎的ADE。这些努力促使研究人员去除位于RBD之外的潜在的促进ade的S蛋白表位,并将重点放在RBD作为主要疫苗候选9,10.
我们的小组正在开发一种使用基于蛋白质的SARS-CoV RBD的疫苗,以提供对同源病毒攻击的保护性免疫,同时最大限度地减少或防止免疫增强9,10.基于假病毒、恢复期血清和多克隆抗体和单克隆抗体的交叉结合和交叉中和研究,它也被作为一种潜在的针对SARS-CoV-2的异体疫苗而推进。外源疫苗是否会增加ADE的风险尚不清楚。例如,在用异源灭活病毒接种的实验动物中注意到ADE,可能是由于非中和抗体。然而,从使用MERS-CoV疫苗的研究中,也有人提出,中和抗体可能会诱发ADE。
总结评论
上述讨论如何指导疫苗的设计、开发和试验?其中最值得考虑的主要发现是,第一,在实验动物病毒攻毒模型的临床前测试发现,病毒载体中的实验性疫苗可由于单个核细胞和嗜酸性粒细胞浸润肺而引起免疫病理。第二,反过来,明矾减少细胞浸润,而ADE在体外与S蛋白RBD外的非中和抗体以及中和抗体有关。虽然我们没有强有力的证据表明这种体外研究或动物挑战模型可以预测临床安全性,但它们指出了包括RBD和明矾佐剂在内的亚单位疫苗的前景。我们现在正在努力将这种方法推进到临床进行I期研究。
参考文献
Thanh Le, T.等。COVID-19疫苗研发情况。Nat. Rev.药物发现https://doi.org/10.1038/d41573-020-00073-5(2020)。
曹哲,等。在康复患者中,针对SARS-CoV刺突蛋白受体结合结构域的有效和持久的抗体反应。性研究。J。7, 299(2010)。
Hotez, P. J. & Bottazzi, M. E.为全球健康开发低成本和可获得的COVID-19疫苗。预印本2020, 2020030464(2020)。
Tai, W.等。2019新型冠状病毒受体结合结构域(RBD)的表征:RBD蛋白作为病毒附着抑制剂和疫苗的开发意义细胞。摩尔。Immunol。https://doi.org/10.1038/s41423-020-0400-4(2020)。
曾,C.-T。et al。SARS冠状病毒疫苗免疫在SARS病毒的挑战下导致肺部免疫病理。《公共科学图书馆•综合》7, e35421(2012)。
霍特兹,P. J., Bottazzi, M. E. & Corry, D. bH冠状病毒免疫病理和疫苗诱导免疫增强中的免疫反应。微生物感染。https://doi.org/10.1016/j.micinf.2020.04.005(2020)。
Keely, S. & Foster, p.s.停止按:嗜酸性粒细胞被征召加入Th17队。免疫力43, 7-9(2015)。
Smatti, M. K. Al Thani, A. A. & Yassine, H. M.病毒诱发的强化疾病。前面。Microbiol。9, 2991(2018)。
Du, L.等。SARS-CoV刺突蛋白的受体结合域在动物模型中诱导长期保护性免疫。疫苗25, 2832-2838(2007)。
陈,w.h.等。SARS候选疫苗酵母表达的SARS- cov重组受体结合域(RBD219-N1)的生产工艺优化和表征j .制药。科学。106, 1961-1970(2017)。
确认
由于篇幅和其他限制,作者希望感谢许多为这一努力贡献了主要研究论文的作者,这里没有引用。
作者信息
作者及隶属关系
贡献
作者对文章的各个方面都作了同样的贡献。
相应的作者
道德声明
相互竞争的利益
pj.h.和M.E.B.是研究人员,领导了针对SARS-CoV、MERS-CoV和SARS-CoV-2的冠状病毒疫苗的开发。D.B.C.是Atropos Therapeutics, LLC的科学顾问和知识产权持有者。
权利和权限
关于本文
引用本文
Hotez, p.j., Corry, D.B.和Bottazzi, M.E. COVID-19疫苗设计:免疫增强的双面人。Nat Rev Immunol20., 347-348(2020)。https://doi.org/10.1038/s41577-020-0323-4
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41577-020-0323-4
这篇文章被引用
高病毒载量:是什么导致疫苗接种者出现COVID-19致命病例?——尸检研究
现代病理学(2022)
一种针对令人担忧的SARS-CoV-2变种的有效、广泛保护的疫苗
npj疫苗(2022)
COVID-19疫苗开发:里程碑、教训和展望
信号转导与靶向治疗(2022)
从SARS-CoV2的刺突蛋白制备多表位疫苗
国际多肽研究与治疗杂志(2022)
COVID-19发病机制、诊断、预防和治疗的免疫学视角
分子生物医学(2021)