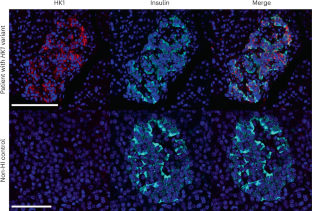
基因组测序和公共表观基因组数据的分析能够在己糖激酶1的非编码调控区域识别致病变异(HK1)在患有先天性高胰岛素血症的个体中。这些变异导致了不恰当的HK1胰腺β细胞的表达,导致胰岛素分泌增加和低血糖。
这是订阅内容的预览,通过你所在的机构访问
访问选项
订阅《自然》+
立即在线访问《自然》和其他55种《自然》杂志
29.99美元
每月
订阅期刊
获得1年的完整期刊访问权限
79.00美元
每期只要6.58美元
所有价格均为净价格。
增值税稍后将在结帐时添加。
税务计算将在结账时完成。
买条
在ReadCube上获得时间限制或全文访问。
32.00美元
所有价格均为净价格。
参考文献
先天性高胰岛素症的遗传学和诊断观点。j .中国。性。金属底座。101, 815-826(2016)。一篇综述性文章描述了CHI的遗传学和临床诊断。
Spielmann, M. & Mundlos, S.超越基因:非编码变异在人类疾病中的作用。嗡嗡声。摩尔,麝猫。25, r157-r165(2016)。回顾非编码基因组变异的发现及其对人类遗传学的影响。
普伦,t.j.等。鉴定胰岛中选择性禁用的基因。小岛2, 89-95(2010)。一篇论文报道了一组普遍表达的基因的鉴定,这些基因在胰岛和极有可能的β细胞中被特异性抑制。
Pasquali, L.等人。胰岛增强子簇富集于2型糖尿病风险相关变异。Nat,麝猫。46, 136-143(2014)。本研究绘制了关键胰岛转录因子图谱;我们用这些数据来确定HK1变体存在于胰岛调控区域,由β细胞中表达的转录因子结合。
Chiou, J.等。单细胞染色质可及性识别胰岛细胞类型和状态特异性的糖尿病风险调节程序。Nat,麝猫。53, 455-466(2021)。本研究报告了胰岛的单细胞染色质可及性数据;我们使用这些数据来确定的可达性HK1胰岛细胞类型的调节区域。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
这是一个总结:弗拉纳根,s.e.等。非编码变异破坏了组织特异性的调控元件HK1引起先天性高胰岛素症。Nat麝猫。.https://doi.org/10.1038/s41588-022-01204-x(2022)。
权利和权限
关于本文
引用本文
中断的β细胞特异性基因沉默导致先天性高胰岛素症。Nat麝猫54, 1597-1598(2022)。https://doi.org/10.1038/s41588-022-01206-9
发表:
发行日期:
DOI:https://doi.org/10.1038/s41588-022-01206-9
