摘要
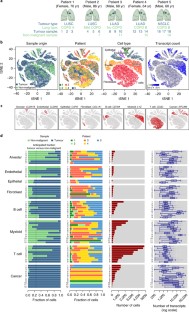
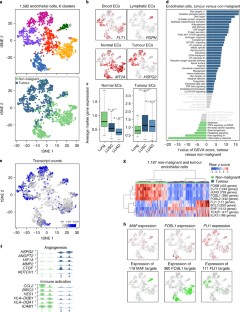
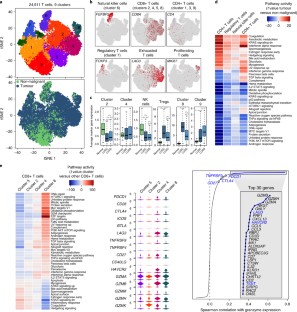
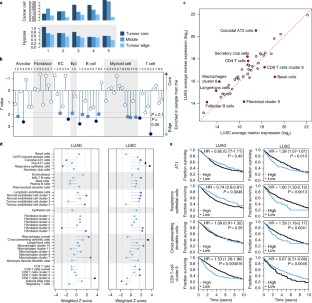
癌细胞嵌入肿瘤微环境(TME)中,这是一个复杂的基质细胞生态系统。在这里,我们在单细胞分辨率下展示了人类肺肿瘤中52,698个细胞的TME转录组目录,并在独立样本中进行了验证,其中40,250个细胞进行了测序。通过与匹配的非恶性肺样本进行比较,我们揭示了一个高度复杂的TME,它深刻地塑造了基质细胞。我们鉴定了52种基质细胞亚型,包括迄今为止被认为是同质的细胞类型中的新亚群,以及其异质性背后的转录因子。例如,我们发现成纤维细胞表达不同的胶原集合,内皮细胞下调免疫细胞归巢和基因与已建立的免疫检查点转录本共调控,并与t细胞活性相关。通过在1572例患者的大量rna测序数据中评估这些细胞亚型的标记基因,我们说明了这些细胞亚型如何与生存相关,而选择的标记物的免疫组织化学验证了它们在独立的一系列肺肿瘤中是独立的细胞实体。因此,通过提供基质细胞类型的综合目录,并通过表征其表型和共选行为,该资源提供了对肺癌生物学的更深入了解,这将有助于推进肺癌的诊断和治疗。
这是订阅内容的预览,通过你的机构访问
相关的文章
引用这篇文章的开放获取文章。
代谢组学及其他:研究癌症代谢的技术组合
信号转导和靶向治疗开放获取2023年3月22日
衰老微环境和抗肿瘤免疫对老年肿瘤的影响:前景和未来意义
血液学与肿瘤杂志开放获取2023年3月21日
单细胞差异表达的标杆整合
自然通讯开放获取2023年3月21日
访问选项
访问Nature和其他54种Nature组合期刊
获取自然+,我们最具价值的在线订阅
每月29.99美元
随时取消
订阅本刊
接收12个印刷问题和在线访问
每年189美元
每期只要15.75美元
租用或购买这篇文章
只要你需要,就可以得到这篇文章
39.95美元
价格可能会在结账时计算当地税收


参考文献
帕特尔等人。单细胞RNA-seq强调原发性胶质母细胞瘤的肿瘤内异质性。科学344科学通报,1396-1401(2014)。
肿瘤微环境作为化学预防的靶标。奈特,癌症牧师7, 139(2007)。
Vaupel, P., Kallinowski, F. & Okunieff, P.人类肿瘤血流量、氧和营养供应与代谢微环境的研究进展。癌症Res。49, 6449-6465(1989)。
埃伯哈德,A.等。人类肿瘤血管生成和血管成熟的异质性:对抗血管生成肿瘤治疗的意义。癌症Res。60, 1388-1393(2000)。
Gordon, S. & Taylor, P. R.单核细胞和巨噬细胞异质性。Nat, Rev. immuno1。5, 953(2005)。
Sugimoto, H., Mundel, T. M., Kieran, M. W.和Kalluri, R.肿瘤微环境中成纤维细胞异质性的鉴定。癌症医学杂志。其他。5, 1640-1646(2006)。
Lavin, Y.等。通过配对单细胞分析早期肺腺癌的先天免疫景观。细胞169, 750 - 765。e717(2017)。
Rittmeyer, A.等。Atezolizumab与多西他赛在先前治疗过的非小细胞肺癌(OAK)患者中的疗效:一项开放标签、多中心随机对照试验。《柳叶刀》389, 255-265(2017)。
雷克等人。Pembrolizumab与化疗治疗pd - l1阳性非小细胞肺癌。心血管病。j .地中海。2016, 1823-1833(2016)。
雷克等人。多西他赛加尼达尼布与多西他赛加安慰剂对先前治疗过的非小细胞肺癌患者(LUME-Lung 1):一项3期、双盲、随机对照试验。柳叶刀杂志。15, 143-155(2014)。
Macosko, e.z.等。使用纳升液滴对单个细胞进行高度平行的全基因组表达谱分析。细胞161[j] .农业科学学报,2015。
Tirosh, i。利用单细胞RNA-seq分析转移性黑色素瘤的多细胞生态系统。科学352, 189-196(2016)。
van den Brink, S. C.等。单细胞测序揭示了组织亚群中解离诱导的基因表达。Nat方法。14, 935-936(2017)。
用单细胞基因组学定义细胞类型和状态。基因组Res。25, 1491-1498(2015)。
马佐尼等人。PHD2杂合子缺乏恢复肿瘤氧合并通过内皮正常化抑制转移。细胞136; 839-851(2009)。
Subramanian, A.等。基因集富集分析:解释全基因组表达谱的一种基于知识的方法。Proc。国家的。学会科学。美国102, 15545-15550(2005)。
林春英等。c-Myc升高的肿瘤细胞的转录扩增。细胞151, 56-67(2012)。
Baudino, T. A.等人。c-Myc在肿瘤发育和进展过程中对血管生成和血管生成至关重要。Dev的基因。16, 2530-2543(2002)。
Cantelmo, a.r.等。抑制内皮中糖酵解激活因子PFKFB3可诱导肿瘤血管正常化,损害转移,并改善化疗。癌症细胞30., 968-985(2016)。
Arany, Z.等人。转录辅激活因子pgc -1 α对VEGF和血管生成的不依赖于hif的调控。自然451, 1008-1012(2008)。
De Bock, K.等。pfkfb3驱动糖酵解在血管发芽中的作用。细胞154, 651-663(2013)。
非典型MHC ii类表达抗原呈递细胞:有什么能取代树突状细胞吗?Nat, Rev. immuno1。14, 719-730(2014)。
田璐,等。肿瘤血管正常化与免疫刺激重编程的相互调节。自然544, 250-254(2017)。
Aibar, S.等。风景:单细胞调节网络推理和聚类。Nat方法。14, 1083(2017)。
王宁等。腺病毒介导的c-Jun和c-Fos过表达可诱导人内皮细胞细胞间粘附分子-1和单核细胞趋化蛋白-1。Arterioscler。Thromb。Vasc。医学杂志。19, 2078-2084(1999)。
成纤维细胞在癌症中的生物学和功能。奈特,癌症牧师16, 582-598(2016)。
Gelse, K., Poschl, E. & Aigner, T.胶原蛋白的结构、功能和生物合成。药物输送牧师。55, 1531-1546(2003)。
Lin, Q., Schwarz, J., Bucana, C.和Olson, E. N.通过转录因子MEF2C控制小鼠心脏形态发生和肌肉发生。科学276, 1404-1407(1997)。
Lu, J, Webb, R., Richardson, J. A. & Olson, E. N. MyoR:一种肌肉限制性基本螺旋-环-螺旋转录因子拮抗MyoD的作用。Proc。国家的。学会科学。美国96, 552-557(1999)。
薛杰,等。基于转录组的网络分析揭示了人类巨噬细胞激活的频谱模型。免疫力40, 274-288(2014)。
比斯瓦斯,s.k.等。一个由肿瘤相关巨噬细胞表达的独特的转录程序(NF-kappaB缺陷和IRF-3/STAT1激活增强)。血107; 2112-2122(2006)。
干扰素调节因子决定巨噬细胞表型极化。Mediat。Inflamm。2013, 731023(2013)。
炎症反应的转录控制。Nat, Rev. immuno1。9, 692(2009)。
癌症免疫治疗中免疫检查点的阻断。奈特,癌症牧师12, 252(2012)。
张勇,等。在具有代谢挑战性的肿瘤微环境中增强CD8+ T细胞脂肪酸分解代谢可提高黑色素瘤免疫治疗的疗效。癌症细胞32, 377 - 391。e39(2017)。
Treutlein, B.等。利用单细胞RNA-seq重建远端肺上皮的谱系等级。自然509, 371-375(2014)。
Shaykhiev, R.等。吸烟诱导的CXCL14在人气道上皮中的表达与慢性阻塞性肺疾病和肺癌有关点。j .和。细胞。摩尔。杂志。49, 418-425(2013)。
Buffa, F. M, Harris, a . L, West, C. M. & Miller, C. J.对多种癌症的大型荟萃分析揭示了一种常见的、紧凑的、高度预后的缺氧元生现象。Br。j .癌症102, 428-435(2010)。
Ishibashi, M.等。cd200阳性癌症相关成纤维细胞增强表皮生长因子受体突变阳性肺腺癌对EGFR酪氨酸激酶抑制剂的敏感性。科学。代表。7, 46662(2017)。
Djureinovic等人。非小细胞肺癌的癌睾丸抗原分析。江森自控的洞察力1, e86837(2016)。
肺腺癌分子分类主任挑战联盟。et al。基于基因表达的肺腺癌生存预测:一项多位点、盲法验证研究。Nat,地中海。14, 822-827(2008)。
克莱弗斯,H.等。在成熟生物体的背景下,你对“细胞类型”的概念性定义是什么?细胞系统。4, 255-259(2017)。
饥饿和窒息:CD8+ T细胞在肿瘤微环境中如何阻止肿瘤进展。前面。Immunol。7, 32(2016)。
霍恩,J. L. A .因子分析中因子数量的基本原理与检验。心理测量学30., 179-185(1965)。
《随机森林》。马赫。学习。45, 5-32(2001)。
Thienpont, B.等人。肿瘤缺氧通过降低TET活性导致DNA超甲基化。自然537, 63-68(2016)。
结合独立检验的概率:加权Z -方法优于Fisher的方法。j .另一个星球。医学杂志。18, 1368-1373(2005)。
肿瘤组织特异性和会聚性代谢转化与转移潜力和患者生存相关。Commun Nat。7, 13041(2016)。
Hänzelmann, S., Castelo, R. & Guinney, J. GSVA:基因集变异分析的微阵列和RNA-seq数据。BMC Bioinform。14, 7(2013)。
基塞列夫,V. Y.等。SC3:单细胞RNA-seq数据的一致聚类。Nat方法。14, 483(2017)。
Lin, P., Troup, M. & Ho, J. W. CIDR:通过插入的单细胞RNA-seq数据的超快速准确聚类。基因组医学杂志。18, 59(2017)。
李,H.等。单细胞转录组的参考成分分析阐明了人类结直肠肿瘤的细胞异质性。Nat,麝猫。49, 708(2017)。
沃特斯,E.等。非小细胞肺癌的DNA甲基化分析揭示了copd驱动的免疫相关特征。胸腔70科学通报,1113-1122(2015)。
克里斯托弗,D.等。衰老果蝇大脑的单细胞转录组图谱。细胞https://doi.org/10.1016/j.cell.2018.05.057(2018).
致谢
我们感谢De Waegeneer先生、T. Van Brussel先生、G. Peuteman先生、E. Vanderheyden先生和B. Tembuyser先生提供的技术援助。本工作由VIB TechWatch资助D.L.和B.T.,抗癌基金会资助S.Aerts(2016-070)和e.w., ERC Consolidator资助s.a aerts(724226_顺- control)和D.L.(变色龙),研究基金-弗兰德斯资助H.D. (1701018N)和D.L. (G065615N),奥地利科学基金(FWF)资助A.P. (J3730-B26)和KU Leuven资助D.L.和s.a aerts (PFV/10/016 SymBioSys)和B.T. (BOFZAP)支持。
作者信息
作者及单位
贡献
D.L.和B.T.设计并监督了这项研究,并撰写了手稿。E.W.监督样本收集和临床注释,h.d.、a.p.、k.v.d.e.、b.w.、e.v.、P.D.L.和j.v.b.t.进行数据分析,b.b.、s.a.i.也做出了重要贡献。, S.Ae。a.b.d.n.和B.T.进行免疫组织荧光分析。助理,助理,助理和助理。提供关键数据解释。所有作者都阅读了稿件或对稿件进行了评论。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益冲突。
额外的信息
出版商的注意:b施普林格《自然》杂志对已出版的地图和机构的管辖权要求保持中立。
权利和权限
关于本文
引用本文
兰布雷希茨,D.,沃特斯,E.,伯克斯,B.。et al。肺肿瘤微环境中基质细胞的表型塑造。Nat地中海24, 1277-1289(2018)。https://doi.org/10.1038/s41591-018-0096-5
收到了:
接受:
发表:
发行日期:
DOI:https://doi.org/10.1038/s41591-018-0096-5
这篇文章是由
多组学特征的评分系统量化缺氧模式头颈部鳞状细胞癌患者
转化医学杂志(2023)
基因、DNA甲基化和免疫谱在早期单一原发性肺癌和同步多发性原发性肺癌之间的差异
临床实验胚胎学(2023)
衰老微环境和抗肿瘤免疫对老年肿瘤的影响:前景和未来意义
血液学与肿瘤杂志(2023)
局部来源:部位特异性免疫屏障转移
Nature Reviews免疫学(2023)
单细胞分析揭示预后成纤维细胞亚群与分子和免疫亚型肺癌相关
自然通讯(2023)
