摘要gydF4y2Ba
COVID-19的病原体SARS-CoV-2的迅速出现及其在全球的传播给公共卫生造成了前所未有的压力。目前正在紧急开发针对SARS-CoV-2的动物模型,以帮助合理设计疫苗和治疗方法。免疫组织化学和原位杂交技术有助于在福尔马林固定石蜡包埋(FFPE)标本中可靠和可重复地检测SARS-CoV和SARS-CoV-2病毒产物,这将是非常有用的。选择针对SARS-CoV刺突蛋白和核蛋白、双链RNA和刺突基因RNA探针产生的商业抗体,评估检测FFPE感染细胞的能力。我们还测试了热介导和酶介导的病毒抗原回收方法,以确定最佳的病毒抗原回收方法,并确定替代的回收方法,以实现免疫组化方法的灵活性。除了使用原生病毒感染细胞作为阳性对照材料外,还评估了表达冠状病毒(SARS, MERS)刺峰的未感染细胞作为生物安全替代活病毒检测的方法。优化方案成功应用于实验动物源性组织。本研究展示的多种病毒检测和控制材料生成技术可应用于冠状病毒发病机制的研究和动物模型的治疗研究。gydF4y2Ba
介绍gydF4y2Ba
2019年底,一种新型冠状病毒SARS-CoV-2在中国中部出现,主要导致一种名为COVID-19的呼吸道疾病gydF4y2Ba1gydF4y2Ba。这种病毒在全球迅速传播,并于2020年3月11日被世卫组织宣布为大流行。截至2020年10月,全球已造成4000万例感染,其中100万人死亡gydF4y2Ba2gydF4y2Ba。gydF4y2Ba
SARS-CoV-2是gydF4y2BaBetacoronavirusgydF4y2Ba按命令分类gydF4y2BaNidoviralesgydF4y2Ba和家人gydF4y2BaCoronaviridaegydF4y2Ba其RNA基因组与sars冠状病毒密切相关gydF4y2Ba3.gydF4y2Ba。SARS-CoV-2和SARS-CoV进入细胞依赖于受体血管紧张素转换酶2 (ACE2)。在细胞启动蛋白酶TMPRSS2和组织蛋白酶激活刺突蛋白后,病毒包膜和细胞膜发生融合,使病毒基因组进入宿主细胞gydF4y2Ba4gydF4y2Ba。刺突蛋白由S1和S2亚基组成,是抗体介导的中和作用的主要靶标,其中免疫原性表位位于S1结构域gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba。在冠状病毒复制过程中,核蛋白是表达最丰富的蛋白质,其次是刺突gydF4y2Ba7gydF4y2Ba。此外,在病毒复制周期中,双链RNA (dsRNA)作为中间产物产生gydF4y2Ba8gydF4y2Ba。gydF4y2Ba
SARS-CoV-2的致病性和传播动力学与SARS-CoV不同gydF4y2Ba9gydF4y2Ba迫切需要利用人类疾病和易感动物物种的动物模型来解决病毒学和病理学问题。虽然不是一个详尽的清单,但实验研究已经在动物模型中进行了,包括雪貂gydF4y2Ba10gydF4y2Ba,食蟹猴gydF4y2Ba11gydF4y2Ba,恒河猴gydF4y2Ba12gydF4y2Ba、非洲绿猴gydF4y2Ba13gydF4y2Ba埃及果蝠gydF4y2Ba14gydF4y2Ba金色的叙利亚仓鼠gydF4y2Ba15gydF4y2Ba,转基因hACE2小鼠gydF4y2Ba16gydF4y2Ba、猫gydF4y2Ba17gydF4y2Ba,gydF4y2Ba18gydF4y2Ba和狗gydF4y2Ba18gydF4y2Ba。目前,利用免疫组织化学(IHC)和原位杂交(ISH)靶向病毒抗原和基因,在体内实验后确定病毒-宿主相互作用的报道有限gydF4y2Ba11gydF4y2Ba,gydF4y2Ba14gydF4y2Ba由于缺乏用于测试开发的合适试剂和组织。gydF4y2Ba
本文报道了抗体和RNA探针分别用于检测福尔马林固定石蜡包埋(FFPE)标本中存在的SARS冠状病毒的适用性。此外,还描述了用于测试开发和质量保证的控制材料的选择。随后,这些优化的测定方法在感染动物的组织和病毒成分的细胞分布上的比较效用被证明。gydF4y2Ba
结果gydF4y2Ba
SARS-CoV和SARS-CoV-2抗原的检测gydF4y2Ba
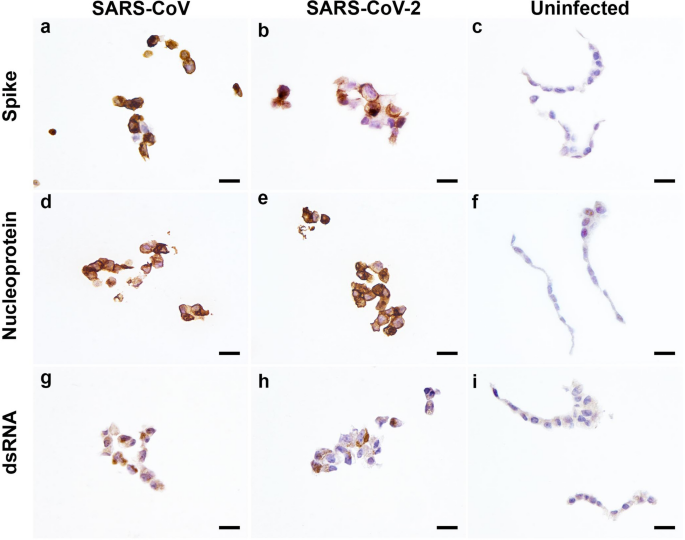
使用热(ph6或9)和酶介导的表位揭露技术评估几种市售的SARS-CoV抗体,以检测FFPE原生病毒感染细胞颗粒中病毒抗原的存在(表1)gydF4y2Ba1gydF4y2Ba).兔单克隆(mAb;经鉴定,中国生物公司40150-R007刺突抗体和兔多克隆核蛋白抗体(中国生物公司,40143-T62)适合在FFPE细胞颗粒上进行免疫组化,其中在SARS-CoV和SARS-CoV-2感染的细胞中观察到特异性的细胞质色素颗粒,而在未感染的细胞上则没有(图2)。gydF4y2Ba1gydF4y2Baf)。兔单克隆(mAb;中国生物公司40150-R007)刺突抗体与pH9或pH6的检索方法兼容,而兔多克隆核蛋白抗体(中国生物公司,40143 - t62)可以应用于用加热的pH6缓冲液或蛋白酶检索的病毒抗原(表)gydF4y2Ba1gydF4y2Ba).在不同的机构(EMC)使用相同的抗体和抗原检索方法检测核蛋白也证明了可重复的免疫标记(补充图gydF4y2Ba1gydF4y2Baa、b)。gydF4y2Ba
除了开发检测SARS-CoV特异性抗原的免疫组化技术外,还评估了免疫组化检测dsrna -病毒复制中间体的效果。在评估的三种抗体中,小鼠和家兔培养的J2重组克隆都能够检测到带有细胞质色素沉积的感染细胞颗粒中的dsRNA(图2)。gydF4y2Ba1gydF4y2Bag h;增刊。gydF4y2Ba1gydF4y2Bac, d)。然而,与SARS特异性抗原检测方法相比,免疫标记的数量并不丰富。另一个克隆,9D5,在IHC中没有产生色素沉积。用抗猫传染性腹膜炎病毒(FIPV)的冠状病毒抗体评估细胞颗粒的非特异性结合。使用FIPV抗体在未感染和SARS-CoV感染的细胞中未检测到染色体(未显示)。gydF4y2Ba
SARS-CoV和SARS-CoV-2刺突蛋白编码RNA的检测gydF4y2Ba
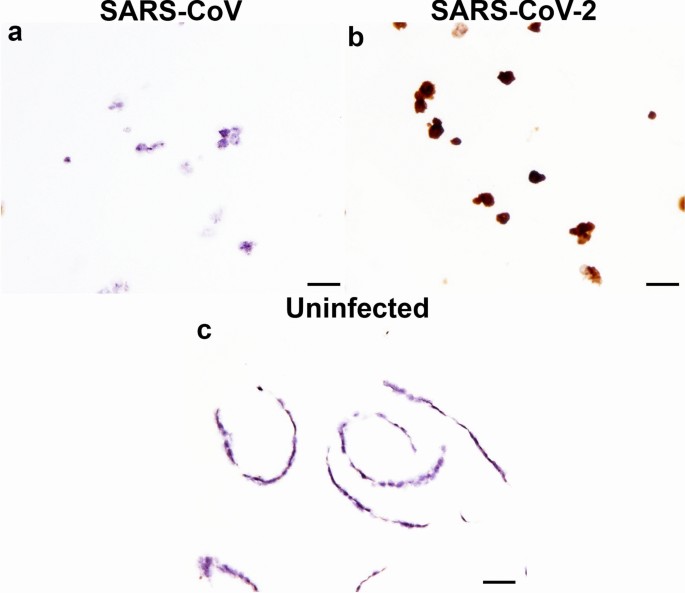
评估了一种RNAScope®探针在FFPE细胞颗粒中检测SARS冠状病毒RNA的能力。V-nCoV2019-5探针未对SARS-CoV产生标记(图2)。gydF4y2Ba2gydF4y2Baa)但成功地标记了SARS-CoV-2感染的细胞颗粒(图2)。gydF4y2Ba2gydF4y2Bab).未感染的细胞微球未见标记(图2)。gydF4y2Ba2gydF4y2Bac)。gydF4y2Ba
SARS-CoV和SARS-CoV-2伪病毒在生产细胞中的检测gydF4y2Ba
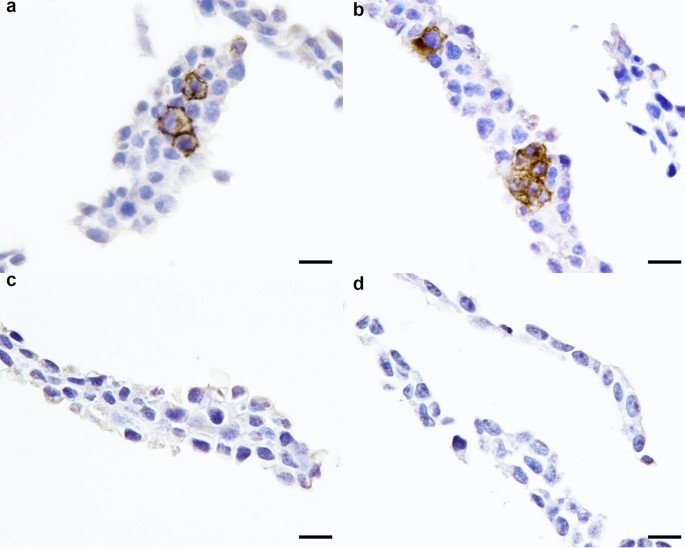
为了确定FFPE体外生成的表达重组刺突蛋白的伪病毒是否适合用于免疫反应检测,使用上述鉴定的刺突单抗对表达SARS-CoV、SARS-CoV-2或MERS刺突蛋白的慢病毒伪病毒的生产细胞进行了免疫反应检测。在该试验中,刺钉单抗能够检测SARS-CoV和SARS-CoV-2,显示特异性的细胞质和膜色素沉积(图2)。gydF4y2Ba3.gydF4y2Baa、b)。表达MERS尖峰的细胞未检测到免疫标记(图2)。gydF4y2Ba3.gydF4y2Bac)或未转染的细胞(图2)。gydF4y2Ba3.gydF4y2Bad)。gydF4y2Ba
IHC和ISH在动物组织中的应用gydF4y2Ba
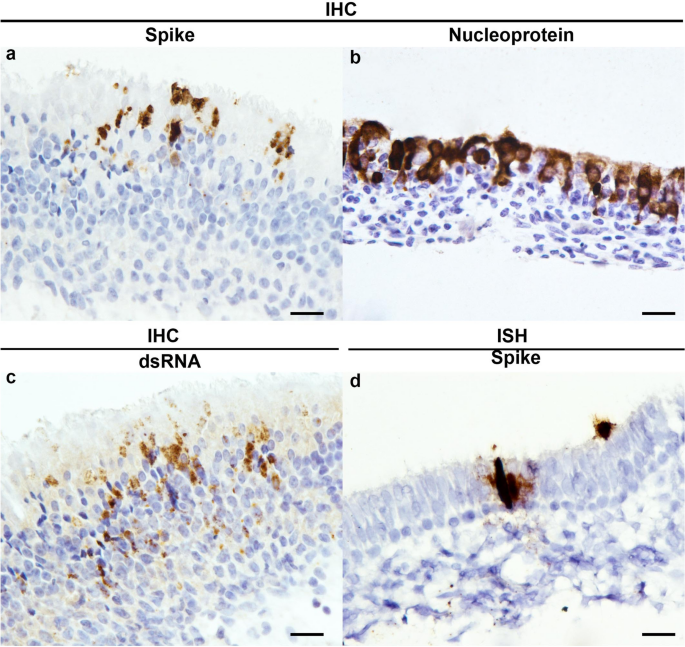
在实验获得的SARS-CoV-2感染雪貂的鼻甲骨上,对建立并优化的FFPE细胞微球的IHC和ISH方法进行了测试。使用刺突抗体,观察到免疫标记特异性地标记嗅觉上皮粘膜的腔细胞(图2)。gydF4y2Ba4gydF4y2Baa).核蛋白标记(图2)gydF4y2Ba4gydF4y2Ba与穗标记相比,B)在细胞质中更为普遍。dsRNA免疫标记仅限于核周区域的细胞质(图2)。gydF4y2Ba4gydF4y2BaC),对应于冠状病毒的复制位点gydF4y2Ba19gydF4y2Ba。对于抗穗基因ISH,染色原在感染的上皮细胞细胞质内弥散沉积(图2)。gydF4y2Ba4gydF4y2Bad)用核蛋白、spike或dsRNA抗体进行免疫标记的序列切片(图2)。gydF4y2Ba4gydF4y2Baa、c)或刺突ISH在受感染细胞群中显示一致的标记,证实了在动物组织中检测SARS-CoV-2的特异性。gydF4y2Ba
讨论gydF4y2Ba
在本报告中,我们对FFPE标本中存在的SARS-CoV和SARS-CoV-2的抗原和RNA检测方法进行了优化。利用针对SARS-CoV刺突和核蛋白的抗体,我们能够检测到感染细胞中存在的SARS-CoV和SARS-CoV-2抗原,并对其进行组织学处理。此外,RNAScopegydF4y2Ba®gydF4y2Ba专为SARS-CoV-2设计的探针,专门标记同源病毒株。病毒复制产物dsRNA的检测在免疫组化上也很明显。此外,我们利用FFPE伪病毒产生细胞进行SARS- cov刺突免疫嵌合,并证明了对两种SARS病毒株的免疫标记特异性。gydF4y2Ba
在免疫组化或ISH应用中,需要为病理调查开发和验证阳性对照材料,以确保所产生结果的质量。感染了原生病毒的易感细胞系可以在不需要动物组织的情况下产生。然而,对于缺乏进行体外工作所需的高密封设施的实验室来说,这可能是有问题的。作为替代方案,具有相关基因工程专业知识的机构可以通过转染和伪型系统在细胞培养中产生表达的蛋白质gydF4y2Ba20.gydF4y2Ba,可作为活病毒工作的替代方案,以证明福尔马林固定和石蜡包埋后表达的病毒蛋白的检测。gydF4y2Ba
虽然福尔马林可以可靠地灭活感染因子,但固定可导致表位交联并阻碍抗体结合。酶或热介导(pH 6或9缓冲液)抗原回收可用于重新暴露表位,尽管这些方法的生化影响尚未得到评估gydF4y2Ba21gydF4y2Ba。通常,只有一种抗原回收方法,通常是热介导的回收,用于检测SARS-CoV-2病毒抗原gydF4y2Ba22gydF4y2Ba,gydF4y2Ba23gydF4y2Ba。在我们目前的研究中使用的刺突抗体之前被报道不适合FFPE切片的IHCgydF4y2Ba24gydF4y2Ba。在这里,pH 9的检索被证明比pH 6在试图揭示刺突表位时更有效。至于核蛋白检测,pH 6抗原检索在两个独立的机构设置中是可重复的。此外,在我们的研究中证明了蛋白酶抗原检索检测核蛋白的适用性。核蛋白抗原的热或酶介导的抗原检索的多功能性可以为研究者提供更大的灵活性,以针对其他感兴趣的抗原进行多标记。gydF4y2Ba
由于比较SARS-CoV和SARS-CoV-2的发病机制的科学兴趣越来越大,我们评估了抗体对两种病毒株交叉反应的能力。刺突S1受体结合域(RBD)特异性抗体能够检测SARS-CoV原生病毒的刺突抗原和表达的刺突蛋白。尽管SARS-CoV和SARS-CoV-2的rbd只有76%的氨基酸相同gydF4y2Ba25gydF4y2Ba,用单一抗体制备的检测表明,所评估的两株菌株之间存在表位保守性。相反,SARS-CoV刺突S1抗体未与MERS刺突蛋白发生交叉反应和结合,可能是由于SARS-CoV-2与MERS- cov之间的氨基酸同源性较低(33%)gydF4y2Ba26gydF4y2Ba。gydF4y2Ba
相反,SARS冠状病毒核蛋白氨基酸在SARS- cov和SARS- cov -2之间高度保守,氨基酸同源性为90%gydF4y2Ba27gydF4y2Ba。我们发现核蛋白抗体与两种病毒发生交叉反应,证实了这一事实。除了检测病毒特异性蛋白外,病毒复制中间体dsRNA还可用于检测包括冠状病毒在内的RNA病毒gydF4y2Ba28gydF4y2Ba。除了如前所述的检测sars冠状病毒的能力之外gydF4y2Ba28gydF4y2Ba在美国,SARS-CoV-2也可以通过免疫组化检测,使用dsRNA抗体。然而,这需要被感染的细胞作为阳性对照,因为dsRNA只在病毒复制期间合成。gydF4y2Ba
在检测实验感染的SARS-CoV-2动物组织中的病毒产物时,也证明了这些检测方法的实用性。在鼻鼻甲上皮细胞中,dsRNA存在于核周细胞质中。早期病毒复制涉及负链基因组模板和dsRNA复制中间体的合成,其中dsRNA先前使用免疫金染色技术在位于核周区域的修饰ER膜的双膜囊泡中观察到gydF4y2Ba19gydF4y2Ba。我们的研究证实在呼吸上皮细胞的顶端可以检测到尖峰糖蛋白。该定位与最近报告的SARS-CoV-2感染肠道类器官相似gydF4y2Ba29gydF4y2Ba。gydF4y2Ba
总之,我们已经证明了琼脂糖包埋的表达靶蛋白的感染或转染细胞颗粒,固定并常规处理用于组织病理学,在开发用于动物模型研究的原位检测方法方面的适用性。组织切片病毒检测的初步评估证明了免疫组化和ISH在FFPE组织上的适用性,重要的是通过常规光学显微镜提供了病毒成分的空间细胞分布的知识。在细胞颗粒平台中检测SARS冠状病毒抗原和核酸也允许快速开发病理工具,可用于未来评估SARS- cov -2发病机制和干预研究。gydF4y2Ba
材料与方法gydF4y2Ba
细胞和病毒gydF4y2Ba
Vero E6细胞在添加10%胎牛血清(FCS)、HEPES、碳酸氢钠、青霉素(100 IU/mL)和链霉素(100 IU/mL)的Dulbecco改良Eagle’s培养基(DMEM, Gibco)中维持。人胚胎肾(HEK) 293T-17细胞在添加FCS、青霉素(100 IU/mL)和链霉素(100 IU/mL)的DMEM中生长。细胞在37°C的潮湿CO中生长gydF4y2Ba2gydF4y2Ba孵化器。sars冠状病毒(分离株HKU-39849)gydF4y2Ba29gydF4y2Ba和SARS-CoV-2分离株BetaCoV/Munich/BavPat1/2020;欧洲病毒档案全球#026V-03883)gydF4y2Ba29gydF4y2Ba用于体外实验,而SARS-CoV-2 (nCoV/Victoria/1/2020)用于体内实验gydF4y2Ba30.gydF4y2Ba。SARS-CoV和SARS-CoV-2均在VeroE6 (ATCC)上传播gydF4y2Ba®gydF4y2BaCRL 1586TM)细胞在Opti-MEM I (1X) + GlutaMAX (Thermofisher)中,在37°C加湿CO中补充青霉素(100 IU/mL)和链霉素(100 IU/mL)gydF4y2Ba2gydF4y2Ba孵化器。以感染倍数(MOI)为0.01的条件感染VeroE6细胞,培养72 h (h)。培养上清经离心清除,在- 80°C等分液中保存。使用传染性病毒的调查是在荷兰伊拉斯谟医疗中心生物安全3级实验室内进行的。gydF4y2Ba
病毒感染细胞的生成gydF4y2Ba
用SARS-CoV和SARS-CoV-2分别接种Vero E6细胞,MOI为0.3。感染24小时后,用10%中性缓冲福尔马林(NBF)固定细胞,同时用另一个未感染细胞的烧瓶固定细胞。gydF4y2Ba
病毒假颗粒在产生细胞中的产生gydF4y2Ba
如前所述,将重组刺突蛋白假型化为慢病毒核心gydF4y2Ba31gydF4y2Ba,gydF4y2Ba32gydF4y2Ba。这是在APHA的BSL2实验室进行的。简单地说,用p8.91 (gag-pol)、pCAGGS-s(全长SARS-CoV、SARS-CoV-2或MERS spike)和pCSFLW转染HEK 293T-17细胞。转染后5天,用10%的NBF固定细胞。gydF4y2Ba
准备用于组织学处理的细胞gydF4y2Ba
将体外感染或转染的固定单层细胞从烧瓶上刮下,1500℃离心gydF4y2BaggydF4y2Ba。去除上清后,将细胞颗粒重新悬浮在2%琼脂糖(Sigma)中,并使其凝固。琼脂糖包埋细胞微球用常规组织学方法在组织学处理机上处理gydF4y2Ba33gydF4y2Ba。gydF4y2Ba
动物实验感染gydF4y2Ba
根据1986年动物(科学程序)法案,在英国APHA危险病原体咨询委员会3级(ACDP3)认证的动物复合体内进行体内实验。动物实验经APHA动物福利与伦理审查机构(AWERB;HOL-PP3405816/1/001)。用1 ml 2 × 10的SARS-CoV-2经鼻接种雪貂gydF4y2Ba6gydF4y2Ba组织培养感染剂量50gydF4y2Ba50gydF4y2Ba).在预先确定的时间点对动物进行人道安乐死,并将组织收集到10%的NBF中。gydF4y2Ba
免疫组织化学(包含IHC)gydF4y2Ba
4个微米厚的切片分别用二甲苯和梯度醇脱蜡和再水化,用3%过氧化氢在甲醇(VWR International)中淬灭内源性过氧化物酶,室温(RT)下淬灭15分钟,然后用pH6 (10 mM柠檬酸缓冲液,用1 M氢氧化钠调至pH6)揭开表位;, pH9目标检索缓冲液(Envision FLEX,高pH;Dako)在97°C下保存10分钟,或蛋白酶XXIV (Sigma-Aldrich)在RT下保存15分钟。载玻片用正常山羊血清在RT中阻断30分钟(1/66稀释;病媒实验室)并组装成盖板,以便使用山东Sequenza系统(山东)进行免疫组化。然后用一抗在4°C下过夜或在室温下孵育1小时,然后用小鼠或兔特异性Envision™聚合物(Dako)在室温下孵育30分钟,用3,3-二氨基苯丙胺(DAB) (Sigma Aldrich)在室温下孵育10分钟。Tris缓冲盐水中加入Tween (145 mM NaCl, 5 mM Tris(羟甲基)甲胺,0.1% w/v Tween®20,用1 M HCl调节到pH7.6;费舍尔科学;VWR International)用于在孵育之间冲洗切片。随后,切片用Mayer’s haematoxylin (Surgipath)反染,用乙醇和二甲苯脱水,用邻苯二甲酸二丁酯二甲苯固定玻璃盖。gydF4y2Ba
原位杂交(ISH)gydF4y2Ba
针对SARS-CoV-2 (V-nCoV2019-5)刺突基因的20对双Z专有RNA探针。848569)由Advanced Cell Diagnostics (ACD, USA)合成。使用RNAScope进行ISHgydF4y2Ba®gydF4y2Ba2.5高清棕色检测试剂盒(ACD),按照制造商的说明。组织分别通过二甲苯和酒精脱蜡和水化,RNAscope处理gydF4y2Ba®gydF4y2Ba过氧化氢(ACD)在室温下加热10分钟,用目标提取液(ACD)在97°C下加热18分钟,蛋白酶加液(ACD)在40°C下加热10分钟。然后将RNA探针添加到切片中,在40°C下杂交2小时,然后在40°C下使用Hybridise Amp (ACD)进行6轮扩增,在HybEZ™烘箱(ACD)中交替培养30至15分钟。在孵育之间用1倍洗涤缓冲液(ACD)在RT下洗涤2分钟。用DAB检测信号。切片用Mayer氏血红素(Surgipath)反染,用乙醇和二甲苯脱水,玻璃盖上Cytoseal (ACD)。gydF4y2Ba
数据可用性gydF4y2Ba
本研究中产生或分析的所有数据都包含在这篇发表的文章(及其补充信息文件)中。gydF4y2Ba
参考文献gydF4y2Ba
朱,N。gydF4y2Baet al。gydF4y2Ba2019年中国肺炎患者的新型冠状病毒。gydF4y2Ba心血管病。j .地中海。gydF4y2Ba382gydF4y2Ba, 727 - 733。gydF4y2Bahttps://doi.org/10.1056/NEJMoa2001017gydF4y2Ba(2020)。gydF4y2Ba
JHU。gydF4y2BaCOVID-10仪表板gydF4y2Ba,gydF4y2Bahttps://coronavirus.jhu.edu/map.htmlgydF4y2Ba(2020)。gydF4y2Ba
《严重急性呼吸综合征相关冠状病毒:分类2019-nCoV并命名为SARS-CoV-2》gydF4y2BaMicrobiol Nat。gydF4y2Ba5gydF4y2Ba, 536 - 544,gydF4y2Bahttps://doi.org/10.1038/s41564-020-0695-zgydF4y2Ba(2020)。gydF4y2Ba
霍夫曼,M。gydF4y2Baet al。gydF4y2BaSARS-CoV-2细胞的进入依赖于ACE2和TMPRSS2,并被临床证实的蛋白酶抑制剂阻断。gydF4y2Ba细胞gydF4y2Ba181gydF4y2Ba, 271-280 e278;gydF4y2Bahttps://doi.org/10.1016/j.cell.2020.02.052gydF4y2Ba(2020)。gydF4y2Ba
何玉娟,李军,贺玉娟,李建军,姜建军,李建军,李建军,卢斯提格曼。重组杆状病毒表达的严重急性呼吸综合征冠状病毒刺突蛋白的抗原和免疫原性研究。gydF4y2Baj .性研究。gydF4y2Ba80gydF4y2Ba, 5757 - 5767。gydF4y2Bahttps://doi.org/10.1128/JVI.00083-06gydF4y2Ba(2006)。gydF4y2Ba
局域网,J。gydF4y2Baet al。gydF4y2Ba与ACE2受体结合的SARS-CoV-2刺突受体结合域的结构。gydF4y2Ba自然gydF4y2Ba581gydF4y2Ba, 215 - 220。gydF4y2Bahttps://doi.org/10.1038/s41586-020-2180-5gydF4y2Ba(2020)。gydF4y2Ba
Irigoyen, N。gydF4y2Baet al。gydF4y2Ba利用RNA测序和核糖体谱分析冠状病毒基因表达的高分辨率分析。gydF4y2Ba公共科学图书馆Pathog。gydF4y2Ba12gydF4y2Ba, e1005473。gydF4y2Bahttps://doi.org/10.1371/journal.ppat.1005473gydF4y2Ba(2016)。gydF4y2Ba
伊万诺夫,k.a。gydF4y2Baet al。gydF4y2Ba与严重急性呼吸综合征冠状病毒解旋酶相关的多种酶活性gydF4y2Baj .性研究。gydF4y2Ba78gydF4y2Ba, 5619 - 5632。gydF4y2Bahttps://doi.org/10.1128/JVI.78.11.5619-5632.2004gydF4y2Ba(2004)。gydF4y2Ba
裴伟士,袁国英,陈家祥,陈家祥,陈家祥。gydF4y2Ba心血管病。j .地中海。gydF4y2Ba349gydF4y2Ba, 2431 - 2441。gydF4y2Bahttps://doi.org/10.1056/NEJMra032498gydF4y2Ba(2003)。gydF4y2Ba
Kim, Y. I。gydF4y2Baet al。gydF4y2BaSARS-CoV-2在雪貂中的感染与快速传播gydF4y2Ba细胞宿主微生物gydF4y2Ba27gydF4y2Ba, 704-709 e702gydF4y2Bahttps://doi.org/10.1016/j.chom.2020.03.023gydF4y2Ba(2020)。gydF4y2Ba
Rockx B。gydF4y2Baet al。gydF4y2BaCOVID-19、中东呼吸综合征和SARS在非人灵长类动物模型中的比较发病机制gydF4y2Ba科学gydF4y2Ba368gydF4y2Ba, 1012 - 1015。gydF4y2Bahttps://doi.org/10.1126/science.abb7314gydF4y2Ba(2020)。gydF4y2Ba
明斯特,v·J。gydF4y2Baet al。gydF4y2Ba接种了SARS-CoV-2的恒河猴的呼吸道疾病。gydF4y2Ba自然gydF4y2Bahttps://doi.org/10.1038/s41586-020-2324-7gydF4y2Ba(2020)。gydF4y2Ba
Woolsey C。gydF4y2Baet al。gydF4y2Ba新冠肺炎非洲绿猴模型的建立。bioRxivgydF4y2Bahttps://doi.org/10.1101/2020.05.17.100289gydF4y2Ba(2020)。gydF4y2Ba
Schlottau, K。gydF4y2Baet al。gydF4y2Ba果蝠、雪貂、猪和鸡中的SARS-CoV-2:一项实验性传播研究gydF4y2Ba柳叶刀的微生物gydF4y2Ba1gydF4y2Ba, e218-e225。gydF4y2Bahttps://doi.org/10.1016/s2666 - 5247 (20) 30089 - 6gydF4y2Ba(2020)。gydF4y2Ba
陈家富。gydF4y2Baet al。gydF4y2Ba2019冠状病毒病(COVID-19)临床病理表现在金色叙利亚仓鼠模型中的模拟:对疾病发病机制和传播性的影响gydF4y2Ba中国。感染。说gydF4y2Ba。gydF4y2Bahttps://doi.org/10.1093/cid/ciaa325gydF4y2Ba(2020)。gydF4y2Ba
包,L。gydF4y2Baet al。gydF4y2BaSARS-CoV-2在hACE2转基因小鼠中的致病性gydF4y2Ba自然gydF4y2Bahttps://doi.org/10.1038/s41586-020-2312-ygydF4y2Ba(2020)。gydF4y2Ba
施,J。gydF4y2Baet al。gydF4y2Ba雪貂、猫、狗和其他家养动物对sars冠状病毒的易感性gydF4y2Ba科学gydF4y2Ba(2020)。gydF4y2Ba
博斯科-劳斯,m.a。gydF4y2Baet al。gydF4y2Ba家养狗和猫感染SARS-CoV-2的实验:猫的发病机制、传播和再暴露反应gydF4y2BaProc。国家的。学会科学。gydF4y2Ba117gydF4y2Ba, 26382 - 26388。gydF4y2Bahttps://doi.org/10.1073/pnas.2013102117gydF4y2Ba(2020)。gydF4y2Ba
努,K。gydF4y2Baet al。gydF4y2Basars冠状病毒的复制是由修饰的内质网网状泡状网络支持的。gydF4y2Ba公共科学图书馆杂志。gydF4y2Ba6gydF4y2Ba, e226。gydF4y2Bahttps://doi.org/10.1371/journal.pbio.0060226gydF4y2Ba(2008)。gydF4y2Ba
J. M.尼科尔斯。gydF4y2Baet al。gydF4y2BaSARS死亡病例肺中SARS冠状病毒核蛋白和RNA的时间过程和细胞定位。gydF4y2Ba科学硕士。gydF4y2Ba3.gydF4y2Ba, e27。gydF4y2Bahttps://doi.org/10.1371/journal.pmed.0030027gydF4y2Ba(2006)。gydF4y2Ba
Ramos-Vara, J. A.和Miller, M. A.当组织抗原和抗体相处:重新审视免疫组织化学的技术方面——红、棕、蓝技术。gydF4y2Ba兽医。病理学研究。gydF4y2Ba51gydF4y2Ba42 - 87。gydF4y2Bahttps://doi.org/10.1177/0300985813505879gydF4y2Ba(2014)。gydF4y2Ba
Best Rocha, A。gydF4y2Baet al。gydF4y2Ba使用市售试剂检测福尔马林固定石蜡包埋组织切片中的SARS-CoV-2。gydF4y2Ba实验室。投资。gydF4y2Bahttps://doi.org/10.1038/s41374-020-0464-xgydF4y2Ba(2020)。gydF4y2Ba
Carossino, M。gydF4y2Baet al。gydF4y2Ba应用RNAscope®原位杂交和免疫组织化学技术检测SARS-CoV-2。gydF4y2Ba放置性研究。gydF4y2Ba165gydF4y2Ba, 2373 - 2377。gydF4y2Bahttps://doi.org/10.1007/s00705-020-04737-wgydF4y2Ba(2020)。gydF4y2Ba
刘,J。gydF4y2Baet al。gydF4y2Ba福尔马林固定石蜡包埋标本中SARS-CoV-2的分子检测。gydF4y2Ba江森自控的洞察力gydF4y2Ba5gydF4y2Ba,gydF4y2Bahttps://doi.org/10.1172/jci.insight.139042gydF4y2Ba(2020)。gydF4y2Ba
Wan, Y., Shang, J., Graham, R., Baric, R. S.和Li, F.武汉新型冠状病毒的受体识别:基于SARS冠状病毒长达十年的结构研究的分析。gydF4y2Baj .性研究。gydF4y2Ba94gydF4y2Ba,gydF4y2Bahttps://doi.org/10.1128/JVI.00127-20gydF4y2Ba(2020)。gydF4y2Ba
好吧,n.m.a.。gydF4y2Baet al。gydF4y2Ba冠状病毒病患者的冠状病毒2特异性抗体反应gydF4y2Ba紧急情况。感染。说。gydF4y2Ba26gydF4y2Ba, 1478 - 1488。gydF4y2Bahttps://doi.org/10.3201/eid2607.200841gydF4y2Ba(2020)。gydF4y2Ba
周,P。gydF4y2Baet al。gydF4y2Ba与一种可能来源于蝙蝠的新型冠状病毒有关的肺炎暴发。gydF4y2Ba自然gydF4y2Ba579gydF4y2Ba, 270 - 273。gydF4y2Bahttps://doi.org/10.1038/s41586-020-2012-7gydF4y2Ba(2020)。gydF4y2Ba
理查森,s.j。gydF4y2Baet al。gydF4y2Ba使用针对dsRNA的抗血清检测福尔马林固定石蜡包埋组织中的病毒感染。gydF4y2Baj .中国。性研究。gydF4y2Ba(2010)。gydF4y2Ba
Lamers, M。gydF4y2Baet al。gydF4y2BaSARS-CoV-2可有效感染人类肠道细胞。gydF4y2Ba科学gydF4y2Ba369gydF4y2Ba, 50 - 54。gydF4y2Bahttps://doi.org/10.1126/science.abc1669gydF4y2Ba(2020)。gydF4y2Ba
佳力,L。gydF4y2Baet al。gydF4y2Ba从澳大利亚首位被诊断为COVID-19的患者身上分离并快速分享2019年新型冠状病毒(SARS-CoV-2)。gydF4y2Ba奥斯特gydF4y2Ba。gydF4y2Bahttps://doi.org/10.5694/mja2.50569gydF4y2Ba(2020)。gydF4y2Ba
Grehan, K., Ferrara, F. & Temperton, N.一种优化的方法,用于生产表达病毒伪型的MERS-CoV刺突。gydF4y2BaMethodsXgydF4y2Ba2gydF4y2Ba, 379 - 384。gydF4y2Bahttps://doi.org/10.1016/j.mex.2015.09.003gydF4y2Ba(2015)。gydF4y2Ba
汤普森,C。gydF4y2Baet al。gydF4y2Ba苏格兰献血者对SARS冠状病毒2的中和抗体——血清学测定人群暴露价值的初步研究medRxiv: 2020.2004.2013.20060467,gydF4y2Bahttps://doi.org/10.1101/2020.04.13.20060467gydF4y2Ba(2020)。gydF4y2Ba
Puranik,。gydF4y2Baet al。gydF4y2Ba受感染的水禽和陆生家禽之间的传播动力学:鸭、鸡和火鸡之间H5N8高致病性禽流感病毒(进化枝2.3.4.4a)的传播和趋向性差异gydF4y2Ba病毒学gydF4y2Ba541gydF4y2Ba, 113-123(2020)。gydF4y2Ba
加纳,先生。gydF4y2Baet al。gydF4y2Ba家貂一种类似猫传染性腹膜炎的全身性冠状病毒相关疾病的临床病理特征(gydF4y2BaMustela putoriusgydF4y2Ba).gydF4y2Ba兽医。病理学研究。gydF4y2Ba45gydF4y2Ba, 236 - 246。gydF4y2Bahttps://doi.org/10.1354/vp.45-2-236gydF4y2Ba(2008)。gydF4y2Ba
致谢gydF4y2Ba
SARS-CoV HKU-39849和SARS-CoV-2 BetaCoV/Munich/BavPat1/2020病毒分离株分别由香港大学Malik Peiris教授和charit
作者信息gydF4y2Ba
作者及单位gydF4y2Ba
贡献gydF4y2Ba
F.Z.X.L, M.M.L, R.S.和S.P.S.进行了实验。F.Z.X.L, M.M.L.和A.N.进行了形式分析。F.Z.X.L, M.M.L, d.s., N.T.和K.R.B.提供了研究方法。i.b., s.m.b., m.w.c., b.l.h., A.C.B.和A.N.提供资源。F.Z.X.L.和M.M.L.写了最初的草稿。所有作者(F.Z.X.L M.M.L,名号,R.S,个终身制,齿数,B.L.H, A.C.B, K.R.B, M.W.C, S.M.B, I.B.和A.N.)审查和编辑的手稿。gydF4y2Ba
相应的作者gydF4y2Ba
道德声明gydF4y2Ba
相互竞争的利益gydF4y2Ba
作者声明没有利益冲突。gydF4y2Ba
额外的信息gydF4y2Ba
出版商的注意gydF4y2Ba
b施普林格《自然》杂志对已出版的地图和机构的管辖权要求保持中立。gydF4y2Ba
补充信息gydF4y2Ba
权利和权限gydF4y2Ba
开放获取gydF4y2Ba本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览gydF4y2Bahttp://creativecommons.org/licenses/by/4.0/gydF4y2Ba。gydF4y2Ba
关于本文gydF4y2Ba
引用本文gydF4y2Ba
利恩,F.Z.X,拉默斯,m.m.,史密斯,S.P.gydF4y2Baet al。gydF4y2Ba福尔马林固定石蜡包埋标本中SARS-CoV和SARS-CoV-2免疫组化和原位杂交检测方法的建立。gydF4y2BaSci代表gydF4y2Ba10gydF4y2Ba, 21894(2020)。https://doi.org/10.1038/s41598-020-78949-0gydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/s41598-020-78949-0gydF4y2Ba
这篇文章是由gydF4y2Ba
COVID-19的脂肪组织:脂肪细胞中SARS-CoV-2的检测和干扰素- α反应的激活gydF4y2Ba
内分泌学研究杂志gydF4y2Ba(2022)gydF4y2Ba
评论gydF4y2Ba
通过提交评论,您同意遵守我们的gydF4y2Ba条款gydF4y2Ba和gydF4y2Ba社区指导原则gydF4y2Ba。如果你发现一些滥用或不符合我们的条款或指导方针,请标记为不适当。gydF4y2Ba