摘要
为缓解SARS-CoV2全球大流行,需要提高诊断能力。然而,目前还存在样本采集拭子和运输介质短缺的挑战。唾液被推荐为一种简单、低成本、非侵入性的选择。然而,来自不同人群和环境的数据是有限的。在这里,我们表明唾液可能是诊断COVID-19患者的一个很好的替代样本。从152例有症状的患者中采集了对nps -唾液样本;并对确诊患者的阳性率、病毒载量、病毒脱落时间进行比较。152例NPS患者中,SARSA-CoV2阳性80例(52.63%),阴性72例(47.37%)。入院当日唾液检测阳性129例(92.14%),阴性11例(7.86%)。唾液RT-PCR结果与NPS的总体符合率为70%(196/280)。 A comparison of viral load from 72 NPS-saliva pair samples on day of admission shows saliva contains significantly higher viral load (P< 0.001)。综上所述,唾液对SARS-CoV2的检测率较高,COVID-19患者唾液中病毒载量较高,病毒脱落时间较长。因此,我们推荐唾液作为NPS更好的替代样本来诊断COVID-19患者。
简介
2020年3月11日,世界卫生组织(WHO)宣布COVID-19疫情为全球大流行1.截至2021年3月15日,全球有119,956,955例COVID-19确诊病例,2,655,280人死亡。在埃塞俄比亚,175,467人被诊断感染了SARS-CoV2,其中2550人死于该病2.近年来,出现了几种与新型呼吸道感染相关的病毒,如2009年甲型流感病毒(H1N1)、甲型禽流感病毒(H7N9)和甲型禽流感病毒(H5N6)以及中东呼吸综合征(MERS)冠状病毒3..最新的大流行是新型冠状病毒SARS-CoV2,于2019年12月在中国武汉出现4.目前,为了确认SARS-CoV-2感染,世界依赖于基于PCR的检测各种体液中的病毒RNA。报告显示,不同体液中SARS-CoV2 RNA的检出率存在高度的变异性。例如——王文玲等。5采用支气管肺泡灌洗液,93%(14/15)标本检测出SARS-CoV2 RNA, 72%(72/104)标本在痰中检测出SARS-CoV2 RNA;鼻拭子63%(5/ 8),纤维支气管镜刷活检46%(6/13),咽拭子32% (126/398);粪便中29%(44/153),血液中1%(3/307),72份尿液样本中无一发现。另一项类似的研究在88份咽拭子样本中的16份(18.2%)、63份痰拭子样本中的38份(61.3%)、175份鼻咽拭子样本中的89份(50.9%)和17%(28/165)粪便样本中检测到SARS-CoV2 RNA6.世卫组织建议同时使用急性期感染上呼吸道和下呼吸道样本6,7,8.具体来说,建议使用鼻咽拭子(NPSs)、鼻咽吸液(NPA)和鼻或喉咙拭子/冲洗来诊断检测病毒RNA7,9.在常见的临床实践和许多监测研究中,鼻咽标本通常被认为是呼吸道感染性病毒诊断测试的最佳标本类型10.然而,在使用多种样本类型的报告中,在一些被证实患有呼吸道病毒感染的患者中,鼻咽样本被检测为阴性11,12.另一方面,一些患者的痰液或其他下呼吸道样本中病毒载量较高,有利于病毒的识别。然而,许多呼吸道病毒感染的患者不产痰或不能咳出优质的痰。此外,气管或支气管标本的采集涉及侵入性操作,会给患者带来严重不适和风险,并对医护人员构成风险3..此外,获得NPS样本不像获得其他类型的样本(如唾液)那么容易,因为它对患者非常刺激,有助于收集次优样本,特别是当样本由经验不足的人员获得时。更重要的是,获取NPS样本的过程会导致大多数患者咳嗽,这可能会导致空气中产生含有传染性病毒的颗粒,并增加传染给医护人员的风险3.,13,14.
唾液很少用于呼吸道病毒的检测,因为与其他呼吸道样本相比,唾液的敏感性较低。然而,唾液可以很容易地从患者身上获得,而无需任何侵入性手术3..一项研究报告,唾液中呼吸道病毒的检出率与nps的检出率相当。nps中呼吸道病毒检出率为77.5%(183/236),唾液检出率为76.3%(180/236)。11.
为了缓解SARS-CoV2的全球大流行,需要扩大诊断。然而,还存在一些挑战,包括样本采集拭子和运输介质的短缺。与金标准鼻咽拭子相比,唾液被推荐为一种简单、低成本、无创的选择。然而,来自不同人群和环境的数据是有限的。因此,本研究旨在研究唾液样本与NPS相比对SARS-COV-2感染的诊断价值。
结果
COVID-19阳性率:鼻咽拭子与唾液
在第0天从152名患者中共收集了152个NPS和140个唾液样本。所有样本均取自入院前5至7天通过RT-PCR检测出SARS-CoV2 RNA阳性的患者。在这项研究中,我们从患者身上收集了140对唾液- nps样本。入院当天,129份(92.14%)唾液样本SARSA-CoV2 RNA检测阳性,11份(7.86%)唾液样本检测阴性(表2)1及补充表S1a). NPS样品中阳性80份(52.63%),阴性72份(47.37%)。在67名NPS样本检测为阴性和提供唾液样本的患者中,57名SARSA-CoV2 RNA检测呈阳性。然而,只有1例患者唾液检测呈阴性,但NPS样本检测呈阳性(补充表)S1一个)。
第0天,唾液RT-PCR检测结果与NPS的总体符合率为70%(196/280)。检测结果唾液与NPS的阳性符合率(PPA)为92.14%(129/140),阴性符合率(NPA)为47.86%(67/140)。唾液和NPS样本检测SARS-CoV2的McNemar检验比较显示,唾液的阳性率高于NPS,具有统计学意义(P< 0.01),优势比为6.64,优势比的95% CI在3.5 ~ 12.5之间(表1).
第2周,第8天采集第二轮样本。这一次,我们从共69名参与研究的患者中获得并测试了62份唾液和69份NPS样本。在唾液中,48例(77.42%)患者被鉴定出SARS-CoV2,其余14例(22.58%)病毒呈阴性。在NPS中,只有16例(20.28%)患者检测呈阳性(补充表)S1b)。
第8天,唾液RT-PCR检测的PPA和NPA与NPS的总符合率分别为75.83%(91/120)、76.67%(46/60)和75% (45/60)2).
在第三轮随访中(第15天),我们收集了14个NPS和10个唾液样本。RT-PCR结果显示,50% (7/14)NPS患者唾液中SARS-CoV2阳性,100%(10/10)患者唾液中SARS-CoV2阳性(补充表)S1c)。
鼻咽拭子和唾液样本病毒载量
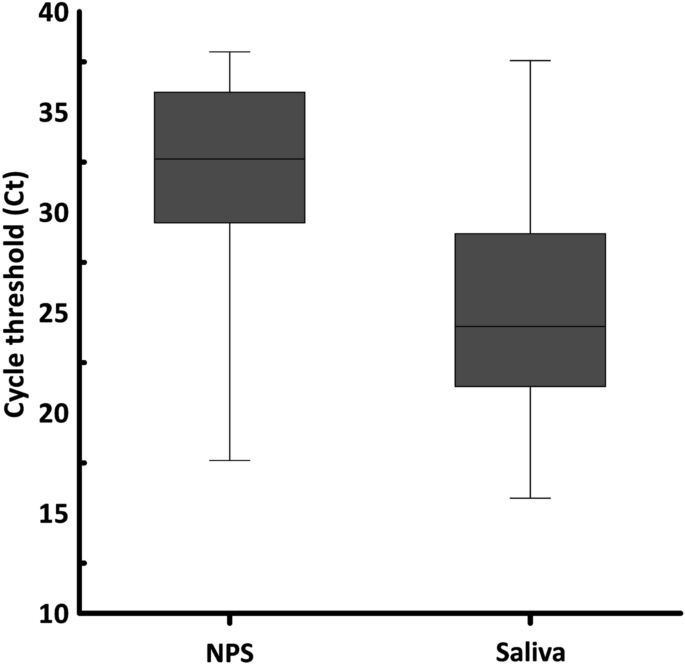
样本类型检测病毒RNA的适用性取决于其病毒载量。在本研究中,我们使用循环阈值(Ct)作为病毒载量的代理测量,其中病毒载量与Ct值呈负相关。第0天72对NPS与唾液样本病毒载量比较,唾液病毒载量明显高于NPS (P< 0.001)(补充表S1d). 86%的患者(62/72)唾液中的病毒载量高于NPS。如图所示。1NPS的Ct中位数为32.66,唾液的Ct中位数为24.31P值< 0.001。
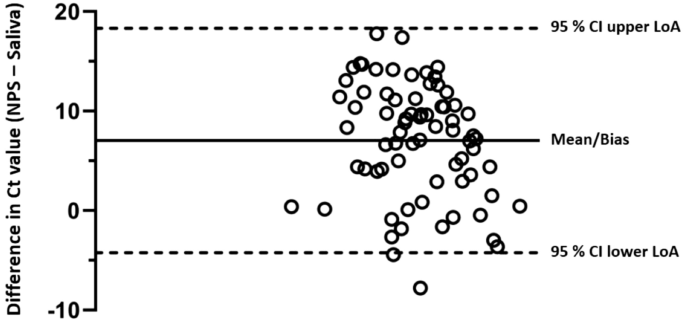
另一方面,从Bland-Altman图(图。2),两种测试的病毒载量差值(NPS减去唾液)与两种测量值的平均差值的比值显示两种测试是一致的。即95%以上的数据点位于一致性下限和上限(LoA)的95%置信区间(CI)内。
为了评估鼻咽拭子和唾液样本中SARS-CoV2 RNA脱落的动态,我们比较了在第0天(入院当天)、入院后一周(第8天)和第15天呈阳性的55对唾液和38对NPS样本的状态。对于唾液,在第0天检测出阳性的55个唾液样本中,只有11个在第8天病毒RNA呈阴性。对于那些在第0天和第8天都检测出病毒阳性的患者,在第三轮随访中,我们只获得了9名患者的唾液样本,有趣的是,所有患者的唾液样本都呈阳性。
在38个NPS阳性样本中,超过一半(38个中的26个)变成阴性。在第15天,在第8天NPS呈阳性的12名患者中,有5名仍呈阳性。
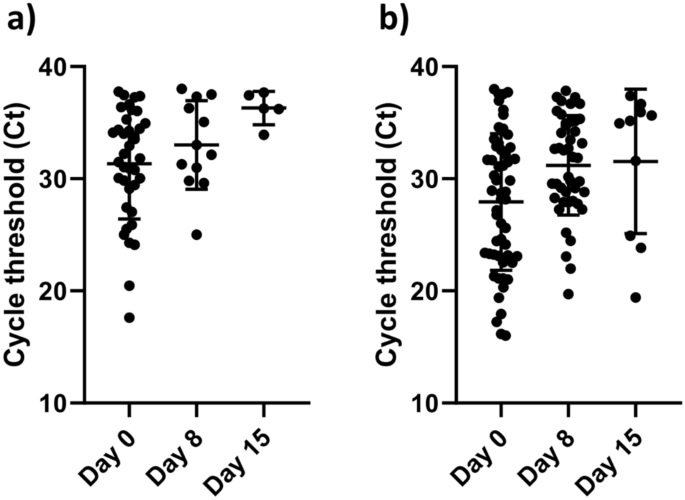
另一方面,在第8天,44名唾液患者和12名NPS患者仍然呈阳性;与第8天相比,他们的病毒载量在第8天显著下降P< 0.05。然而,唾液和NPS中的病毒载量随时间的变化几乎显示出相似的模式(图2)。3.).
讨论
COVID-19诊断的金标准检测方法是实时RT-PCR检测SARS-CoV2 RNA8,15建议使用鼻咽拭子取样9,15,16,17.但是,我们的结果表明,唾液在检测SARS-CoV2时具有较高的阳性率,即;COVID-19患者的唾液含量比NPS高1.7倍。这意味着唾液比NPS样本更适合用于诊断COVID-198.这与美国食品和药物管理局最近批准使用唾液样本检测SARS-CoV2 RNA的决定一致18.唾液不仅因为其SARS-CoV2 RNA检测阳性率高而优于NPS,而且唾液允许自我管理样本收集,这减少了医护人员接触医院感染的风险。患者可在家收集唾液;这进一步减少了对卫生保健工作者的需求和样本收集的等待时间,确保了临床环境中的少量患者,从而有助于减少病毒的进一步传播。此外,与NPS引起大多数患者咳嗽不同,唾液样本收集过程是非侵入性的,这使得收集简单、快速和廉价,并允许广泛的公众筛查11,19,20..
我们观察到COVID-19患者唾液中病毒载量较高,即;86%的患者唾液中的病毒载量高于NPS。这是另一个表明唾液是可靠的21与NPS相比,更适合用于诊断COVID-19患者。Xu等人的研究。22发现SARS-CoV2受体血管紧张素转换酶2 (ACE2)在口腔黏膜上皮细胞和舌头中高度表达,这表明COVID-19患者唾液中病毒载量高的原因。此外,在COVID-19患者唾液中发现高病毒载量与世界卫生组织的声明一致,即导致COVID-19的病毒传播的主要途径是通过感染者咳嗽或打喷嚏时的唾液飞沫或鼻子分泌物(https://www.who.int/health-topics/coronavirus#tab=tab_1).
有报道显示,唾液中的SARS-CoV2 RNA长期脱落23,24.在这里,我们的研究表明,与NPS相比,COVID-19患者在第7天的唾液中被诊断为阳性,这意味着与NPS相比,唾液中的SARS-CoV2 RNA脱落持续时间更长。
这项研究并非没有局限性。例如,缺乏疾病早期发病和无症状个体的样本。
总之,我们的数据表明,唾液对SARS-CoV2感染的诊断率高于NPS。此外,COVID-19患者唾液中病毒载量较高,SARS-CoV-2 RNA脱落时间延长。考虑到这些因素,我们建议在诊断COVID-19患者时使用唾液作为NPS样本的良好替代。
材料与方法
临床样本
收集症状确诊患者的鼻咽拭子和漱口前的晨唾液。通过逆转录酶聚合酶链式反应(RT-PCR)使用NPS样本确认SARS-CoV2 RNA阳性5至7天后,患者被送入圣保罗医院。NPS样本采用病毒转运介质(VTM)收集,唾液样本采用收集杯收集。第一批唾液和NPS样本是在患者入院当天采集的,也就是说,5至7天后,他们的NPS样本检测呈阳性(这里是第0天之后),然后在第8天和第15天以一周的间隔收集了两份唾液和NPS样本。NPS和唾液样本均在4 - 8°C的适当冷链下从圣保罗医院运输,并在Armauer Hansen研究所冷藏4°C,并在收集后8-12小时内进行处理。所有唾液样品按1:1的比例用生理盐水稀释。
RNA提取
对于NPS和唾液这两种类型的样本,根据制造商(中国中山大学大安基因有限公司)推荐的NA提取纯化试剂,从200 μL中提取病毒核酸(NA)。简单地说,将50 μL蛋白酶K和200 μL裂解缓冲液与200 μL NPS和/或唾液样品混合。然后,将裂解样品在72℃的干热块上热灭活10 min,然后加入抑制剂去除剂并进行洗涤。最后用72℃预热的50 μL分子级水洗脱NA。
RT-PCR检测病毒RNA
为了检测SARS-CoV2 RNA,我们使用了华大基因生物技术(武汉)有限公司的检测试剂盒[实时荧光RT-PCR检测新型冠状病毒试剂盒]。该试剂盒的检测靶点和荧光报告组合为:ORF1ab区域的特定靶点,由FAM报告,内部控制(IC)由VIC或HEX报告25.RT-PCR分析的循环阈值(Ct)被用作病毒载量的代理测量。阳性检测的截止值≤38;大于38的为阴性检验。最后,根据制造商提供的协议,在Agilent Technologies Stratagene, Max3005P RT-PCR系统上运行两个实验的扩增反应混合物。
统计分析
计算四分位间距(IQR)中位数和比例(%)等描述性统计。适当时采用Bland-Altman分析,t检验:对两个样本进行均值配对,采用McNemar检验进行比较。使用Free trail Grapher软件制作箱线图。所有的概率都是二尾的P值< 0.05为有统计学意义。
道德声明
该研究得到了Armauer Hansen研究所/ALERT伦理审查委员会的批准。所有方法均按照埃塞俄比亚国家COVID-19综合管理手册中规定的指导方针和规定执行。此外,所有研究参与者都获得了知情同意。
数据可用性
在本研究过程中产生或分析的所有数据均包含在本文中(补充表)S1模拟)。
参考文献
Cucinotta, D. & Vanelli, M.世卫组织宣布COVID-19大流行。《生物医学。91, 157-160(2020)。
约翰·哈普金斯大学。约翰霍普金斯大学系统科学与工程中心(CSSE)的COVID-19仪表盘。https://coronavirus.jhu.edu/map.html.2020年11月25日访问。
To, K。et al。唾液样本的额外分子检测提高了呼吸道病毒的检测。紧急情况。微生物感染。6, 1-7(2017)。
Ashour, H. M., Elkhatib, W. F., Rahman, M. M. & Elshabrawy, H. A.根据过去人类冠状病毒爆发对最近2019年新型冠状病毒(SARS-CoV-2)的洞察。Pathog。(瑞士巴塞尔)9, 1-15(2020)。
陈,L。et al。COVID-19患者唾液中SARS-CoV-2检测及口腔症状表征细胞Prolif。https://doi.org/10.1111/cpr.12923(2020)。
太阳,J。et al。SARS-CoV-2 RNA在体液中持续时间延长。紧急情况。感染。说。26, 1834-1838(2020)。
谁。2009年甲型H1N1流感大流行人类感染的临床管理:修订指南.http://www.who.int/csr/resources/publications/swineflu/clinical_management_h1n1.pdf?ua=1%0Ahttp: / / scholar.google.com/scholar ? hl = en&btnG = Search&q =取名:临床+管理+ +和+ +人+感染流行+ H1N1(+ +) + 2009 +: # 0 +修正+指导.2020年11月17日访问。(2009)。
粉丝,J。et al。以聚合酶链反应(pcr)为基础的SARS-CoV-2诊断样本:诊断效度研究中国。詹。学报511, 177-180(2020)。
巴伦,e.j.。et al。微生物实验室用于传染病诊断指南:美国传染病学会(IDSA)和美国微生物学会(ASM) 2013年建议。中国。感染。说。57, e22-e121(2013)。
Ruuskanen, O., Lahti, E., Jennings, L. C. & Murdoch, D. R.病毒性肺炎。《柳叶刀》377, 1264-1275(2011)。
Kim Y. G.et al。唾液与鼻咽拭子标本多重反转录pcr检测呼吸道病毒的比较。j .中国。Microbiol。55, 226-233(2017)。
郑俊宏。et al。痰和鼻咽拭子检测呼吸道病毒的比较。J.医学病毒。86, 2122-2127(2014)。
陈,Y。et al。从生鲜市场家禽中人类感染新出现的A型H7N9禽流感病毒:临床分析和病毒基因组特征《柳叶刀》381, 1916-1925(2013)。
郑维昌、杜建伟、谢宏、洪元芳年、袁桂云、A/2009/H1N1流感大流行两年后:我们学到了什么?中国。Microbiol。牧师。25, 223-263(2012)。
威利,a.l.。et al。唾液对新冠病毒的检测比鼻咽拭子更敏感。(2020)。https://doi.org/10.1101/2020.04.16.20067835
Ceron, J。et al。唾液用于SARS-CoV-2的诊断和监测:一般观点。j .中国。地中海。9, 1491(2020)。
王,D。et al。武汉市138例新型冠状病毒感染的肺炎住院患者临床特征分析JAMA J. Am地中海,协会。https://doi.org/10.1001/jama.2020.1585(2020)。
FDA批准用于紧急使用的首个COVID-19唾液测试|《科学家杂志》https://www.the-scientist.com/news-opinion/first-saliva-test-for-covid-19-approved-for-emergency-use-by-fda-67416(2020年12月28日访问)。1 - 2(2020)。
库尔希德,Z,阿西里,F. Y. I.和Al Wadaani, H.人类唾液:用于检测新型冠状病毒(2019-nCoV)的无创液体。Int。j .包围。公共卫生决议案17, 17-20(2020)。
Vinayachandran, D. & Balasubramanian, S. COVID-19的唾液诊断:未来的研究意义。j .凹痕。科学。15, 364-366(2020)。
Azzi, L。et al。唾液是检测新冠病毒的可靠工具。j .感染。81, e45-e50(2020)。
徐,H。et al。新型冠状病毒ACE2受体在口腔黏膜上皮细胞高表达。Int。口腔科学。12, 1-5(2020)。
李,问。et al。COVID-19患者严重急性呼吸综合征冠状病毒2的长时间脱落。紧急情况。微生物感染。https://doi.org/10.1080/22221751.2020.1852058(2020)。
朱娟,郭娟,徐勇,陈霞。SARS-CoV-2在患者唾液中的病毒动态。j .感染。81, e48-e50(2020)。
华大基因基因有限公司SARS-2019-CoV2实时荧光RT-PCR检测试剂盒.可以在https://www.bgi.com/us/wp-content/uploads/sites/2/2020/04/BGI-Amended-EUA-SARS-CoV-2-Detection-Kit.pdf(2020)。
作者信息
作者及隶属关系
贡献
g.t.b.:概念化,形式分析,方法论,写作-评论和编辑。文科:形式分析,方法论,写作评论和编辑。e.s.k.:调查,方法论,回顾和编辑。D.H.A:调查,方法论,审查和编辑。d.a.t.:调查,方法论,回顾和编辑。t.s.:调查,方法论,回顾和编辑。g.a.:调查,方法论,回顾和编辑。a.t.:调查,方法论,回顾和编辑。a.h.:调查,方法论,回顾和编辑。g.b.:调查,方法论,监督,审查和编辑。 B.T.: Investigation, methodology, review & editing. M.Y.: Investigation, methodology, review & editing. L.W.: Investigation, methodology, supervision, review & editing. A.M.: Investigation, methodology, review & editing. A.A.: Investigation, methodology, supervision, writing—review & editing. A.M.: Conceptualization, formal analysis, methodology, writing—review & editing.
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
贝耶恩,g.t.,阿勒木,F.,凯贝德,E.S.et al。在检测COVID-19患者的SARS-CoV2时,唾液优于鼻咽拭子。Sci代表11, 22640(2021)。https://doi.org/10.1038/s41598-021-02097-2
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-021-02097-2
这篇文章被引用
直接从唾液中检测SARS-CoV-2的无创一步多重RT-qPCR方法性能评价
科学报告(2022)