摘要
据报道,新冠肺炎疫情在中国已得到控制。为了了解COVID-19在中国的爆发并为世界其他地区提供潜在的经验教训,在本研究中,我们应用具有多数据集的数学模型来估计SARS-CoV-2病毒的传播性和与感染相关的疾病的严重程度,以及前所未有的控制措施如何影响两者。我们的分析表明,在2020年1月19日之前,检测到3.5% (95% CI 1.7-8.3%)的感染者;此后这一比例增加到36.6% (95% CI 26.1-55.4%)。基本复制编号(R02020年2月8日之前为2.33 (95% CI 1.96-3.69);有效繁殖数降至0.04(95% CI 0.01 ~ 0.10)。这一估计还表明,自2020年1月23日以来采取的控制措施在实施约两周后影响了传播力。2020年2月15日之前,确诊病例病死率估计为9.6%(95%可信区间8.1-11.4%),随后降至0.7%(95%可信区间0.4-1.0%)。这表明SARS-CoV-2病毒具有高度传染性,但可能不如SARS-CoV-1和MERS-CoV严重。我们发现,在早期阶段,大多数R0来自未被发现的感染者。这意味着中国通过降低普通人群的接触率和提高传染病病例的检出率和隔离率实现了成功的控制。
介绍
2019年12月,中国报告了一场严重肺炎(一种现在被命名为COVID-19的传染病)的爆发。病原SARS-CoV-2是一种新型冠状病毒,中国当局于2020年1月7日分离出该病原体,世卫组织于2020年1月9日报告了该病原体。中国首例COVID-19病例报告于2019年12月1日在湖北省武汉市出现症状1之后,病毒迅速传播到中国其他地区2,3.中国境外首例病例于2020年1月13日报告(见表1)1)。由于疾病传播迅速,世卫组织于2020年1月30日宣布COVID-19疫情为“国际关注的突发公共卫生事件”,并于2020年3月11日将COVID-19评估为大流行4.截至2020年3月25日,全球共报告新冠肺炎确诊病例405742例,死亡病例18791例,其中中国大陆确诊病例81218例,死亡病例3281例。到2020年4月10日(25天后),虽然中国的相应数字保持相对不变(81953例病例和3339例死亡),但全球数字急剧增加至1,521,252例病例和92,798例死亡。中国大陆的病例和死亡人数增幅相对较小,这可归因于自2020年1月下旬以来实施的严厉和迅速的控制措施,从2020年1月23日封锁震中武汉市开始,然后扩展到整个中国大陆3..这些措施包括全面关闭和隔离整个城市,取消中国新年庆祝活动,禁止上学和上班,频繁播放重要信息(例如,提倡洗手、戴口罩和就医),大规模动员卫生和公共卫生人员以及军事医疗单位,快速建设重症患者医院,为无症状或轻度症状患者重建庇护所。控制措施包括旅行禁令和限制、减少接触者和保持社交距离、筛查和接触者追踪、早期病例识别和隔离2,5遏制疫情。
作为一种新型冠状病毒,了解其传播性和严重性,并判断中国的控制措施如何有效地阻止了SARS-CoV-2病毒的传播,这可能有助于控制全球COVID-19疫情以及未来可能再次出现的疫情,这一点非常重要。在之前对中国传播动力学的分析中,Kucharski等人。6将随机传播动态模型拟合到武汉的四个病例数据集,并仅考虑截至2020年2月11日的时间。他们估计平均每天的繁殖数量(Rt)从2020年1月23日实施旅行限制前一周的2.35 (95% CI 1.15-4.77)下降到一周后的1.05 (95% CI 0.41-2.39)。其他模型研究2,3.,7,8并利用大流行早期的确诊病例数据,对中国COVID-19疫情的传播、动态和控制进行了建模和估计。中国大陆新增确诊病例数在2月17日之后才达到峰值,而且病死率和出院率等相关数据也在不断增加,需要进一步研究,包括更多数据流,以显示全国实施的综合防控措施的总体效果。
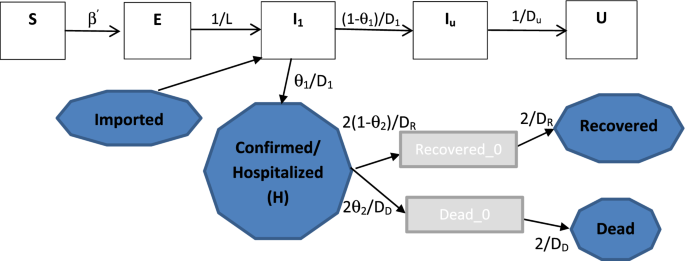
基于已发表的与确诊病例、死亡和康复相关的数据,在本研究中,我们使用了一个综合模型(图3)。1),内容包括SARS-CoV-2病毒的传播动态和COVID-19的疾病报告过程,以估计SARS-CoV-2在中国的传播性和COVID-19的严重程度,以及中国政府自2020年1月下旬以来采取的控制措施对COVID-19传播的影响。
结果
模型参数的估计值见表2.2020年1月19日之前,中国大陆地区新冠肺炎病例的检测和报告比例约为3.5%(95%置信区间(CI): 1.7-8.3%),之后上升至36.6% (95% CI: 26.1-55.4%)。在2020年2月8日之前的早期阶段,COVID-19的传播率很高R0= 2.33 (95% ci 1.96-3.69);然而,从2020年2月8日(2020年2月7日至9日)开始,它急剧下降到0.04 (95% CI 0.01-0.10)。通过确定从出现症状到死亡和恢复的持续时间分别为17.8天和22.6天9,出现症状并确诊后被隔离者的平均感染期为2.28天(95% CI 2.01 ~ 3.12天),未发现感染者的平均感染期为4.44天(95% CI 3.91 ~ 11.71天)。
在我们的模型中,基本繁殖数由两部分组成:确诊病例和未检测到的感染。本研究假定确诊病例和未发现感染具有同等传染性;再加上估计只有约3.5%的感染在早期阶段得到确认和报告,这表明,在早期阶段,约有98%的人感染艾滋病毒R0(表2)是由于未被发现的感染。如果未发现感染的传染性仅为确诊病例的一半或三分之一7,R0在没有干预的情况下几乎保持不变,大约96%的R0是由于未被发现的感染(补充表S21)。这表明,仅隔离确诊病例及其接触者不足以阻止传播,阻止中国大陆新冠肺炎疫情爆发的主要因素是普通人群接触率的大幅下降。7)。
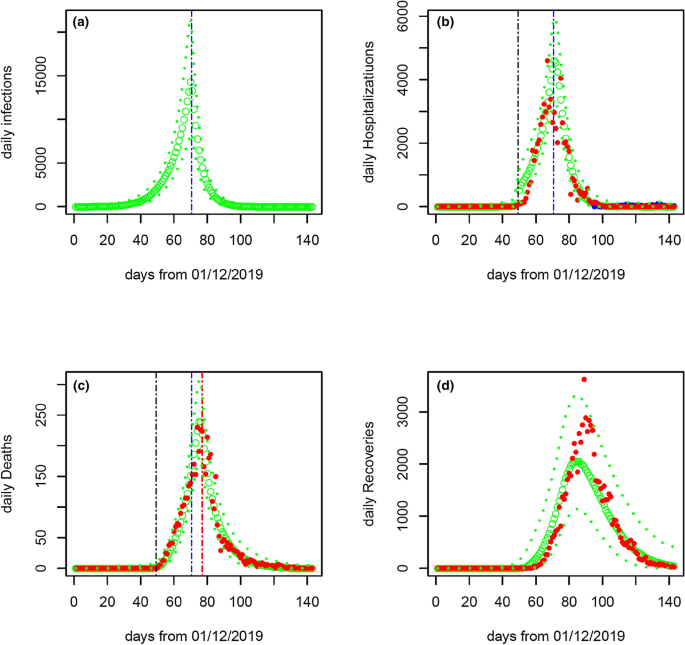
每日住院人数(确诊病例)、每日死亡人数和每日康复人数的拟合模型如图所示。2.我们的模型分析表明,死亡率可能在2020年2月15日左右发生变化(95%置信区间为2020年2月14日至16日)。在此日期之前,确诊病例死亡率(cCFR)为9.6% (95% CI 8.1-11.4%),在此日期之后降至0.7% (95% CI 0.4-1.0%)。根据对病例确诊率和病死率的估计,2020年1月19日之前感染病死率(IFR)为0.33% (95% CI 0.17-0.85%),并在2020年1月20日至2月15日期间上升至3.51%(2.60-5.12%);之后下降到0.24% (95% CI 0.15-0.41%)。我们的模型推断表明,在2019年12月1日,有41人(95% CI 13-207)感染了SARS-CoV-2病毒。这些估计数是根据2020年4月17日增加的1290例死亡是在2020年2月20日之前分配的假设得出的。如果我们假设1290例死亡是在2020年4月17日之前分布的,那么除了与死亡相关的数量外,大多数模型参数的估计值几乎保持不变(表2)2)。例如,在2020年2月15日之后,cCFR从0.67变为1.28%,IFR从0.24变为0.50%。
2019年12月1日至2020年4月21日的流行曲线。感染的模型预测(图)一个)和每日确诊病例数的模型拟合(图1)b),死亡(小组c)和恢复病例(小组)d)所示。模型预测是根据2020年4月17日之前报告的每日死亡人数,将2020年4月17日官方数据中新增的1290例死亡重新分配到2020年2月20日之前的期间后得出的。绿色虚线表示模型预测(大的绿色圆圈表示中位数,细的绿色虚线表示95%置信区间的上下水平)。红点是观测到的数据。黑色、蓝色和红色竖线分别表示估计病例确定率、传播率和确诊病死率发生变化的时间。内嵌板(b),蓝点表示几乎看不见的每日输入病例数。请注意,2020年2月12日(第74天)每日确诊病例数(15152例)超出了图表(b)。
如果公众更早地了解COVID-19并更早地采取控制措施,疫情的规模可能会小得多。这可以通过假设相同的流行病学特征,但移动报告、传播和死亡率发生变化的开始时间来进行定量分析。结果列于表中3..它表明,如果早1周、2周或3周开始采取控制措施,本可避免约57%(57%)、81%(82%)和93%(93%)的确诊病例(和死亡)。但是,如果在1周、2周或3周后开始采取控制措施,中国大陆的确诊病例(和死亡人数)将分别增加2.3倍(2.3)、5.3倍(5.4)和12.4倍(12.5)。
为了研究中心内的疫情与全国的疫情有何不同,我们还获得了湖北省和武汉市的模型参数估计值(补充表)S31)。结果表明,在震中范围内,传播率和病例确诊率差异不大。然而,在估计的确诊病例死亡率方面存在很大差异。在时间点之前τF当估计确诊病死率发生变化时(2020年2月15日),全国的cCFR估计为9.6% (95% CI 8.1-11.4%),湖北省为11.5% (95% CI 10.4-13.5%),武汉市为15.1% (95% CI 13.3-17.6%)。然而,在所有三种情况下,cCFR的估计似乎几乎相同τF.这些估计表明,在2020年2月15日之前,疫情中心的死亡率明显高于全国平均水平,许多COVID-19患者的死亡是由于疫情中心治疗不足造成的。
讨论
了解新型冠状病毒(SARS-CoV-2)的传播性和严重性至关重要;了解其在中国大陆的快速传播是如何得到控制的,对其他正在面临COVID-19持续爆发的国家具有实际意义。在这项研究中,我们利用数学模型重建了2019年12月1日至2020年4月21日中国大陆的COVID-19疫情,研究了SARS-CoV-2在中国的传播和控制。我们的分析表明,在没有干预措施的情况下,SARS-CoV-2的基本繁殖数为2.33 (95% CI 1.96-3.69),因此具有高度传染性。在2020年2月15日之前,有症状和确诊患者的死亡率约为9.6%,随后降至0.7%。中国政府从2020年1月23日起采取的严厉控制措施,使SARS-CoV-2在中国大陆的传播得到了控制。然而,控制措施的效果在两周多后才显现出来。
我们的研究表明,早期报告率(3.5%)非常低,这表明在2020年1月19日之前,约有96.5%的感染未被发现。7,10,11)。这可能主要是由于对这种新型疾病的认识有限和定义不明确所致12.晚期报告率为36.6%,反映出人们对该病毒的认识有所提高,因此因呼吸道症状寻求医疗帮助的比例有所上升;然而,这一比率似乎相对较低,表明许多感染与轻微症状或无症状有关。中国疾控中心分析13根据截至2020年2月11日的数据,估计81%的感染者的COVID-19病情轻微。2020年2月在“钻石公主”号游轮上发生的一次调查充分的疫情进一步证实了轻度症状或无症状感染的高比例:在696例确诊病例中,410例(58.9%;出口的。14)无症状15.
中国政府采取的措施似乎已经阻止了新冠病毒在中国大陆的传播。这是在非常严格的控制措施下实现的,有效繁殖数为0.04,为其初始值的1.8%R0= 2.33 (c.f.)3.)。这个估计R0在早期阶段与大多数以前的估计一致3.,6,7,8,10,11,16,17,18,19,20.,21,22.我们发现确诊病例在隔离前的感染期约为2.3天,与估计值相当23,24,25,26;尽管它似乎比Tian等人得到的要短.3.: 5.19天(95% CI 4.51-5.86天)。我们对未检测和未隔离感染的感染期的估计(4.4天,范围从3.2天到11.7天)与先前研究确定的范围一致27,281-14天。
虽然提高对有症状病例的检出率和隔离率有助于减少传染源的数量。2),传播的主要力量来自未被发现的病例,这些病例在中国大陆暴发的早期阶段促成了SARS-CoV-2的大部分传播。7)。因此,限制一般人群的流动可能是阻止新冠病毒在中国大陆传播的最大贡献。这可能进一步解释了为什么中国自2020年1月23日以来实施的严厉控制措施需要大约16天(即从2020年1月23日延迟到2月8日)才能影响社区内的传播。
中国政府采取的行动的影响也反映在COVID-19相关死亡率的变化上。在2020年2月15日之前,cCFR估计为9.6%,然后降至7%左右(即0.67%)。cCFR的大幅下降可能是由于中国医疗条件的显著改善和医疗资源的可用性,特别是在震中湖北省。
将我们对平均病死率的估计值与其他研究的估计值进行比较是有趣的,在对2月15日之前和之后的估计值进行平均之后,其他研究的估计值为5.14%。这比Deng等人的结果略低.29: 5.65% (95% ci 5.50-5.81%)。包括截至2020年4月17日的死亡数据,Deng等.29使用病例的个人层面数据获得的估计值接近于相应的原油或naïve确诊病死率风险:4632/82,758 = 5.60%,以及截至2020年4月21日的死亡/(死亡+康复)= 4632/(4632 + 78,112)= 5.60%的近似值。根据截至2020年2月11日的数据,Verity等人.9提示中国暴发的总CFR为1.38% (95% CI 1.23-1.53%)。Wu等人使用截至2020年2月29日的数据.30.发现有症状病例的总病死率(出现症状后死亡的概率)为1.4% (95% CI 0.9-2.1%)。Russell等人.31使用几个简化的假设得到中国CFR的估计为1.2% (95% CI 0.3-2.7)。我们对CFR的估计高于这些,这在很大程度上是因为这三项研究没有包括中国国家卫生健康委员会在2020年4月17日官方数据中增加的1290例死亡32.
通过对中国大陆观测数据的模型拟合,我们发现该模型预测的病例数是疫情爆发初期报告病例数的28倍;即使在2020年1月19日以来的后期阶段,估计感染人数也是报告人数的两倍多。根据从COVID-19暴发数据获得的流行病学特征,我们的分析表明,即使提前一周开始采取控制措施,也可以避免57%的确诊病例和57%的死亡病例。如果早3周开始,那么93%的确诊病例和93%的死亡病例本可以避免。这种对控制措施开始时间影响的估计小于Lai等人的估计,但与Lai等人的估计相当.2Yang等人.5尽管这两项研究都只估计了感染的数量。这些发现强调了早期应对对控制人群传播的重要性。
就像Kucharski等人所说的.6,我们假设潜伏期等于潜伏期。鉴于有证据表明存在症状前传播28,33,34有趣的是,这是否会改变我们模型的结果。为此,我们对模型系统进行了修改(图2)。1)通过划分曝光阶段E分成两个相等的子类E1和E2并假设人们在E2可以传播与病例具有相同传染性的病毒(SI第4节)。我们得到了类似的结果(补充表S41):例如,采取控制措施前的基本繁殖数为2.22 (95% CI 1.95-2.92),其中98%是由于未发现的病例,2020年2月15日之前的cCFR为9.5% (95% CI 8.0-11.2%),然后降至0.7% (95% CI 0.4%, 1.1%)。这表明我们的结论相对不受有关症状前传播的假设的影响。
在中国大陆引入的非药物干预措施似乎已经阻止了病毒的传播,但再次爆发疫情的风险仍然存在。根据我们的分析估计,在疫情爆发期间,截至2020年4月21日,最多有223,111人受到感染(表2)3.),不到中国人口的0.02%。即使所有从感染中恢复的人都已完全免疫35中国人群的这一免疫水平远低于控制传播所需的群体免疫阈值55%36,37.这只是意味着,一旦中国大陆目前实施的严格隔离措施放松,SARS-CoV-2在中国的传播很可能会反弹,特别是考虑到世界其他地区正在传播的程度(例如美国)。38)。尽管如此,非药物干预措施似乎已经阻止了SARS-CoV-2病毒在中国大陆的传播,并为疫苗和药物的开发和使用争取了时间。
将新型冠状病毒SARS-CoV-2与引起人群大规模暴发的其他两种冠状病毒SARS-CoV-1和MERS-CoV进行比较是有意义的。SARS-CoV-1有R0从2到539中国大陆疑似病例病死率为9.6%40.据估计,2015年在韩国爆发的中东呼吸综合征冠状病毒有一个R0从2到741实验室确诊病例病死率为34.5%42.这表明,SARS-CoV-2几乎与SARS-CoV-1和MERS-CoV一样具有传染性,但它可能不那么严重,特别是在有足够治疗方法的情况下。此外,与2003年sars冠状病毒和2015年mers冠状病毒在韩国爆发不同,没有证据表明在中国任何为COVID-19患者提供服务的医疗机构发生了超级传播者事件。由于先进的现代交通工具,人们可以在世界各地方便快捷地移动,这使得新冠病毒迅速传播到其他国家。这与SARS-CoV-1和中东呼吸综合征- cov形成鲜明对比,后者已在世界上相对有限的地区得到控制和限制。这种显著差异可能归因于冠状病毒的另一个方面:很大一部分SARS-CoV-2感染与轻微症状或无症状有关13,14,15而SARS-CoV-1和mers - cov都是高度症状21,33.在缺乏高效疫苗的高覆盖率的情况下,SARS-CoV-2病毒的这一特征将使人类难以控制和管理它。
与以往的研究相比2,3.,5,6,21,22我们的分析有两个关键优势:我们的调查基于三个数据集(确诊病例、死亡病例和康复病例),我们对长期(143天)的疫情进行了建模,这应避免由于短期观察而产生的任何偏差和混淆。这项研究也有一些局限性。为了模拟传播动力学和疾病报告,我们的综合模型进行了一些简化。为了反映COVID-19的确诊率、传播率和病死率的时间变化,每种假设两个不同的值。在疫情期间,这些数量可能会逐渐改变,公众意识和干预措施也是如此3..例如,Tsang等人.12发现,在1月15日至3月3日期间,随着COVID-19病例定义从最初的狭窄到逐渐变宽,确诊率发生了变化。从症状出现到死亡的时间间隔也可能随着流行病的发展而改变9,24,26随着更可靠的医疗资源的出现,从症状出现到住院的时间可能会缩短22,24.此外,在本研究中,我们忽略了地理和年龄的异质性3.,7,13.为了为控制措施提供更具体和实际有用的信息,它需要研究区域之间的差异3.,7在不同的年龄组13.进一步的限制是,我们对综合干预措施的总体有效性进行了建模,而不是对不同类型的控制措施进行建模,因此无法深入了解它们在阻止感染传播方面的相对影响。2,3.,16)。
综上所述,我们发现SARS-CoV-2在中国大陆爆发初期传播的主要驱动因素来自未被发现的感染,这为决策者设计最佳干预策略提供了有益的信息。在没有疫苗接种和有效药物的情况下,早期发现和隔离对于遏制和控制SARS-CoV-2的传播至关重要,但降低普通人群中的接触率可能会产生最大的影响。
方法
数据
我们从中国国家卫生健康委员会网站上的3个数据集中提取了2019年12月1日至2020年4月21日中国大陆COVID-19的相关数据:每天确诊/住院病例数、每天死亡人数和每天康复患者人数。这里的数据是根据2019年12月1日至2020年1月1日期间的症状出现日期给出的1由于难以通过中国国家卫生健康委员会网站收集这些病例的发病日期,因此需要在中国国家卫生健康委员会网站上报告这些病例的发病日期。假定报告日期与病例被诊断的日期相同。在2020年2月12日之前,确诊病例被定义为PCR检测为SARS-CoV-2阳性的患者;从2020年2月12日起,确诊病例被定义为(疫情中心湖北省)临床诊断或PCR检测为SARS-CoV-2阳性的病例12以及中国其他地区SARS-CoV-2 PCR阳性的人。这一病例定义导致确诊病例数在2020年2月11日至12日期间从2015年增加到15,151例。
根据中国政府对死亡人数的变化,对每日报告的死亡人数进行了调整,具体如下:具体而言,2020年4月17日,中国国家卫生健康委将疫情爆发以来武汉市新冠肺炎相关死亡总人数估计数从2579人修订为3869人32.报告指出,新增的1290例死亡病例可能发生在2020年2月20日之前,因为在2月20日之后,可治疗新冠肺炎患者的医院从2家增加到48家,此后新建的后深、雷深医院和方仓避难所也提供了更多床位,以满足不同症状的新冠肺炎患者的需求。此外,数据收集系统得到迅速改进,在疫情期间遗漏病例/死亡人数大大减少。由于无法获得这1290例死亡的详细信息,为了模型拟合,将这1290例死亡按首次死亡之日(2020年1月10日)至2020年2月20日每天报告的死亡人数按比例进行分配。例如,2020年1月18日报告的死亡人数为26人,现在该数字修正为26 + 26 × 1290/2236 = 26 + 15 = 41。其中2236是截至2020年2月20日报告的累计死亡人数,此前政府于4月修订了其估计数字。在敏感性分析中,我们还探讨了假设2020年4月17日新增的1290例死亡与2020年1月10日至4月17日整个期间报告的每日死亡人数成比例分布的影响。除死亡率估计数外,结果见表2(并在“结果在分配2020年4月17日官方统计数据中增加的1290例死亡人数的两种方式上非常相似。
模型
在本研究中,我们使用了一个综合模型43(无花果。1),将SARS-CoV-2病毒的隐性传播动态与COVID-19报告系统相结合,调查COVID-19的传播性和严重程度以及遏制和控制SARS-CoV-2的努力。我们假设SARS-CoV-2病毒的传播动力学由SEIR区室模型描述,并进行了一些修改,如图所示。1.也就是说,易受影响的人(年代)可以从有传染性的人身上感染SARS-CoV-2病毒,然后进入潜伏类(E);平均潜伏期后(l),受感染的人会发展为具有传染性(我1)。分数(θ1的人(有严重症状)会被发现并入院(H),然后进行治疗并与社区隔离,分数为(1−θ2)在平均周期后恢复DR另一部分人在平均时间后死亡DD.另一个分数(1−θ1受感染的人,通常有轻微或无症状的感染(我u)不会被发现,因此在一段平均时间内仍将作为传染源存在于社区Du之前恢复。为简单起见,我们假设平均潜伏期等于潜伏期,潜伏期固定在l= 5.2天,由18,26,44.SARS-CoV-2病毒可以通过三种可能的方式传播:呼吸道传播(通过有症状的人打喷嚏或咳嗽时的呼吸道飞沫)、气溶胶传播(通过雾化的细病毒颗粒)和接触传播(通过接触污染表面)。为了简单和一致性,这些简单和快速的传播方式,我们假设人们随机混合。虽然中国是一个拥有140万人口的大国,居住在9,596,960公里的广阔土地上2在中国,最近的城市化和快速交通系统的发展使人们在全国各地出行变得方便快捷。这使得将SARS-CoV-2在全国范围内的传播建模为一个混合良好的人群是合理的。为了进行比较,我们还模拟了COVID-19在湖北省和爆发疫情的武汉市的传播(SI章节3)。
综合模型由式(1)描述。1)。9个隔间的定义见表4模型参数定义见表2.
在这里N= 1,400,050,000是中国大陆的总人口规模,假设在疫情期间保持不变。该模型还包括输入病例(即:进口(t)的方程式我1中国国家卫生健康委员会自2020年3月24日以来报告的来自中国境外的新冠肺炎病例,这可能有助于提高我们对疫情后期传播力估计的可靠性和干预措施的有效性。在模型中纳入输入病例的数量意味着我们隐含地包括在潜伏阶段进入中国的人员。例如,由于疫情后期检测和追踪服务的加强和改进,他们在进入中国后将被隔离两周,并在此期间被发现为病例。
与我们的假设一致,人们随机混合,传染力(每单位时间内易感人群被感染的比率)被认为与当时感染人数成正比t,易感个体数量变化率(即d年代(t) / dt):
这个短语包括三个术语:我1(t)θ1-每次感染人数t有严重症状的人将被发现并住院治疗,我1(t)(1−θ1)——有轻微症状或没有症状、不会被发现、因此会转移到隔室的感染者人数我u,我u(t)——未被发现并将继续被发现的有传染性的人数。的参数ξ与确诊病例相比,未发现感染者的相对传染性。
为了模拟由于中国政府采取的综合和戏剧性的控制措施而导致的传播率(单位时间内两个特定人员有效接触的速度)的潜在变化,我们简单地假设传播系数,β,引入前后的差异如式(2)
(出口的。3.,41)。在这里τβ是传播率因干预措施而发生变化的时间点,将在我们的分析中进行估计。
此外,在疫情爆发的早期阶段,对COVID-19的知识有限,定义不明确,这意味着发现和报告的病例比例可能很低,并随着对COVID-19知识的提高和检测SARS-CoV-2的先进技术的可用性的增加而增加12.特别是自2020年1月20日以来,病例发现、诊断和报告速度加快。中国各地政府鼓励并支持对来自湖北省的旅客进行常规筛查和隔离,以便尽早发现COVID-19感染病例2.为了反映这些变化,我们假设被检测和报告的人数比例(θ1)(或病例确定率)随时间变化如下
这里τθ为病例确定率发生变化的时间点。
随着医疗资源的增加和治疗的改善,病死率也可能随着时间的推移而变化。为简单起见,我们引入一个时间点τF在那之前,确诊病例的死亡率是θ2,在这个时间点之后,它变成θ2, b,详情如下:
θ2,和θ2, b和τF将在我们的分析中估计。
虽然可能有一些散发的COVID-19病例可能没有机会住院,因此会在家中死亡,特别是在疫情爆发的早期阶段,但我们假设的COVID-19确诊患者的流量应该与中国大陆疫情爆发期间的实际流程相当接近45.在这项研究中,我们确定了从出现症状到死亡和出院的平均持续时间为(D1+DD=) 17.8天及(D1+DR=) 22.6天,与估计一致9从中国的疫情数据中允许从住院到死亡和从住院到康复的持续时间遵循伽马分布,而不是通常的指数分布46,我们介绍中间隔间死_0,恢复_0。由于我们使用(大部分)报告日期的数据,时间-事件长度(持续时间)应该被认为包括这种报告延迟,这在本研究中没有明确处理6.
基本复制数R0,定义为由一个感染者引入一个完全易感人群而产生的继发感染者的平均人数,是表征传染因子传播能力的一个重要数量36.我们可以得到的表达式R0考虑无输入情况,得到方程系统(1)的稳态解,其S*(在平衡状态下易受感染的人口数量)由
\ (^ {*} = N \压裂{{1 / D_ {1}}} {{\ beta_{{\文本{一}}}[\ theta_{{1,{\文本{一}}}}+ \ xi \离开({1 - \ theta_{{1,{\文本{一}}}}}\右)+ \ xi \离开({1 - \ theta_{1,{\文本{一}}}}\右)D_{{\文本{你}}}/ D_ {1}]}} \).
在稳态时,R0×(年代*/N) = 136,37,由上式可得前期的基本繁殖数如下
同样,在定义为max()的时间点之后的后期τβ,τθ),干预下的有效繁殖数为
从Eq. (5),未被发现的感染对早期传播的贡献为
在这里D1+Du是未被发现的感染者的平均感染期。的参数ξ为衡量未检出感染对确诊病例的相对传染性,取值为1.0(即未检出感染与确诊感染具有相同传染性)。以上基本繁殖数的方程也可以用Diekmann等人描述的Next Generation Matrix方法得到。47(见第六章第五节)。
为了了解相对传染性如何影响我们的研究结果,估计R0和其他模型参数ξ= 1/2, 1/3在补充表中给出S21。。
最初播种
在本研究中,我们对2019年12月1日起的传播过程进行了建模,初始感染为我1(0) =我0这需要从模型拟合到数据(见下文)中进行估计。其他变量的初始值由我0假设2019年12月1日左右的疫情处于早期指数增长阶段(如SI第1节所述),总人口规模。相反,Wu等人.21假设2019年12月1日至31日期间的疫情是由持续的人畜共患病感染力量播种的,在2020年1月1日市场关闭之前,每天造成86例病例(是43例人畜共患病确诊病例的两倍)。Kucharski等人.6假设疫情始于2019年11月22日的1例或10例感染病例。
推理方法
我们将要推断的模型参数集表示为Θ = {我0,β一个,βb,τβ,θ1,一个,θ1, b,τθ,θ2,,θ2, b,τF,D1,Du},如表所示2.对于每组参数值,采用龙格-库塔四阶方法求解模型方程,得到模型预测的感染、确诊病例、死亡病例和康复病例时间序列。在模型参数的推断中,使用直接观测的确诊/住院/报告病例数据集(以下简称HOS)、死亡和康复数据集,如下图所示。为了捕捉这些观测的日数量的大离散性,假设负二项似然函数。数字的可能性xC(t)的日间观察资料t为
在哪里
在这里\ \(η^ {C} \)是色散参数,它是估计的和μC(t)是对住院人数、死亡人数或新康复人数(视情况而定)的预测t从综合模型(1)C代表三个不同的数据集:居屋计划、死亡及康复。
特别值得注意的是,由于湖北省病例定义的变化,2020年2月12日(2019年12月1日起第74天)每日病例数特别高(15,152例)12,48.原则上,这些病例中的大多数可能是在2020年2月12日之前的几天内积累的。为了处理这种复杂性,在模型推理中只使用2月12日的累计病例数和此后的每日病例数。以每日报告居屋数目为x(1),x(2)、…x(T),T即从2019年12月1日至2020年4月21日的天数。2月12日累计病例数的可能性X = \ \(和\ nolimits_ {t = 1} ^ {74} X左(t \) \ \)被认为是
在这里文本\ ({\ {M}} = \ \ nolimits_总和{t = 1} ^{74}{\μ^{{{文本\ {HOS}}}}} \左(t \) \)表示模型预测的累计确诊病例数。假设观察到的每日死亡人数:y(1),y(2)、…y(T)及每日康复人数:z(1),z(2)、…z(T)是条件独立的,则给定模型参数Θ的总似然为
参数推理:我们假设无信息先验分布f(Θ),这些参数是统一的(表1)2)。采用贝叶斯框架通过组合先验分布f(Θ)和可能性l(Θ,η累积量,η死亡,η复苏;X y z),后验分布可以通过马尔可夫链蒙特卡罗模拟(MCMC)得到。49.从这些样本中,我们得到了模型参数的中位数和95%置信区间。模型参数的后验将提供SARS-CoV-2在中国大陆的传播力和严重程度的估计,以及中国政府实施的控制措施对传播力的影响。在对震中湖北省和武汉市的疫情进行建模时,也将使用相同的推断方法。
为了探讨控制措施实施时间的影响,我们计算了如果控制措施比实施时间早1、2或3周实施,或者比实施时间晚1、2或3周实施,可能发生的感染、病例和死亡人数。为此,我们只需改变报告、传播和死亡率发生变化的开始时间,而传播参数、确定率和死亡率保持不变。
参考文献
黄,C。et al。武汉市新型冠状病毒感染患者临床特征分析《柳叶刀》395, 497 - 506。https://doi.org/10.1016/s0140 - 6736 (20) 30183 - 5(2020).
赖,S。et al。非药物干预措施对中国遏制新冠肺炎疫情的影响自然585, 410 - 413。https://doi.org/10.1038/s41586-020-2293-x(2020).
田,H。et al。中国新冠肺炎疫情前50天传播控制措施调查科学368(638 - 642), 2020。https://doi.org/10.1126/science.abb6105(2020).
世界卫生组织。存档:世卫组织时间表- covid -19。2020.https://www.who.int/news-room/detail/27-04-2020-who-timeline-covid-19.
杨,Z。et al。公共卫生干预下中国新冠肺炎流行趋势的改进SEIR和AI预测j . Thorac。说。12(3), 165 - 174。https://doi.org/10.21037/jtd.2020.02.64(2020).
库查斯基,a.j.。et al。COVID-19传播和控制的早期动态:数学模型研究柳叶刀感染。说. .20.(5), 553 - 558。https://doi.org/10.1016/s1473 - 3099 (20) 30144 - 4(2020).
李,R。et al。大量未记录的感染促进了新型冠状病毒(SARS-CoV2)的快速传播。科学368, 489 - 493。https://doi.org/10.1126/science.abb3221(2020).
杨,Y。et al。2019年中国新型冠状病毒感染的流行病学和临床特征medrxivhttps://doi.org/10.1101/2020.02.10.20021675(2020).
真实性,R。et al。2019年冠状病毒病严重程度的估计:基于模型的分析柳叶刀感染。说。20., 669 - 677。https://doi.org/10.1016/s1473 - 3099 (20) 30243 - 7(2020).
李建军,李建军,李建军,李建军,李建军。新型冠状病毒2019-nCoV:流行病学参数的早期估计和流行预测。medRxivhttps://doi.org/10.1101/2020.01.23.20018549.thisversionpostedJanuary28,2020(2020).
赵,S。et al。2019- 2020年中国新型冠状病毒(2019- ncov)基本繁殖数初步估计:疫情早期数据驱动分析Int。j .感染。说。92, 214 - 217。https://doi.org/10.1016/j.ijid.2020.01.050(2020).
曾荫权。et al。新冠肺炎病例定义变化对中国大陆疫情曲线和传播参数的影响:模型研究《柳叶刀公共卫生》5(5) e289-e296。https://doi.org/10.1016/s2468 - 2667 (20) 30089 - x(2020).
新型冠状病毒肺炎应急流行病学小组。中国- 2019年新型冠状病毒病(COVID-19)暴发的流行病学特征中国疾病预防控制周刊。https://doi.org/10.46234/ccdcw2020.032(2020).
水本,K, Kagaya, K, Zarebski, A.和Chowell, G.估算钻石公主号邮轮上2019冠状病毒病(COVID-19)无症状病例比例,日本横滨欧元Surveill。2510。https://doi.org/10.2807/1560-7917.ES.2020.25.10.2000180(2020).
https://en.wikipedia.org/wiki/2020_coronavirus_pandemic_on_cruise_ships.2020年4月1日访问。
Chinazzi, M。et al。旅行限制对2019年新型冠状病毒(2019- ncov)疫情传播的影响科学368, 395 - 400。https://doi.org/10.1126/science.aba9757(2020).
Imai表示N。等.报告3(帝国):2019-nCoV的传播性。https://www.imperial.ac.uk/media/imperial-college/medicine/sph/ide/gida-fellowships/Imperial-College-COVID19-transmissibility-25-01-2020.pdf(2020).
李,问。et al。武汉新型冠状病毒感染的肺炎早期传播动态分析心血管病。j .地中海。382, 1199 - 1207。https://doi.org/10.1056/NEJMoa2001316(2020).
刘,T。等.2019新型冠状病毒(2019- ncov)传播动力学。bioRxiv。(1月26日在线发表)(预印本)。doi:https://doi.org/10.2139/ssrn.3526307(2020)
Riou, J. & Althaus, C. L. 2019年12月至2020年1月武汉2019新型冠状病毒(2019- ncov)早期人际传播模式。欧元Surveill。254。https://doi.org/10.2807/1560-7917.ES.2020.25.4.2000058(2020).
吴建涛,梁凯,梁国明。中国武汉新型冠状病毒爆发的临近预测和潜在的国内和国际传播:一项模型研究。《柳叶刀》395, 689 - 697。https://doi.org/10.1016/s0140 - 6736 (20) 30260 - 9(2020).
太阳,G.-Q。et al。COVID-19在中国武汉的传播动态:封锁和医疗资源的影响非线性动力学。https://doi.org/10.1007/s11071-020-05770-9(2020).
新墨西哥州林顿市。et al。2019新型冠状病毒右截断感染的潜伏期及其他流行病学特征:对公开病例数据的统计分析j .中国。地中海。17(9), 2。https://doi.org/10.3390/jcm9020538(2020).
Sanche, S。et al。严重急性呼吸综合征冠状病毒的高传染性和快速传播性紧急情况。感染。说。26, 1470 - 1477。https://doi.org/10.3201/eid2607.200282(2020).
徐晓伟。et al。中国武汉以外地区感染2019年新型冠状病毒(SARS-Cov-2)患者的临床发现:回顾性病例系列BMJ368, m606。https://doi.org/10.1136/bmj.m606(2020).
张,J。et al。中国湖北省以外地区2019冠状病毒病流行病学和传播动力学的演变:一项描述性和建模研究柳叶刀感染。说。20.(7), 793 - 802。https://doi.org/10.1016/s1473 - 3099 (20) 30230 - 9(2020).
京,Q.-L。et al。中国广州家庭COVID-19继发发病率及相关决定因素:一项回顾性队列研究柳叶刀感染。说。20., 1141 - 1150。https://doi.org/10.1016/s1473 - 3099 (20) 30471 - 0(2020).
Siordia, J. A. Jr.。COVID-19的流行病学和临床特征:当前文献综述。j .中国。性研究。127(2020), 104357。https://doi.org/10.1016/j.jcv.2020.104357(2020).
邓,X。et al。新型冠状病毒病2019 (COVID-19)在中国第一波大流行的病例死亡风险。感染。说。https://doi.org/10.1093/cid/ciaa578(2020).
吴家泰。et al。从武汉传播动态估计COVID-19临床严重程度Nat,地中海。26(4), 506 - 510。https://doi.org/10.1038/s41591-020-0822-7(2020).
罗素,t.w.。et al。利用2020年2月钻石公主号游轮上爆发的年龄调整数据估计冠状病毒病(COVID-19)的感染率和病死率。欧元Surveill。25(12), 2000256。https://doi.org/10.2807/1560-7917.ES.2020.25.12.2000256(2020).
中华人民共和国国家卫生健康委员会。关于修改武汉市新型冠状病毒肺炎确诊病例数和死亡人数的通知。http://www.nhc.gov.cn/xcs/yqtb/202004/6f8eb06d959f4ab7b56fe03236920be1.shtml(2020).2020年3月17日(中文).
他,X。et al。COVID-19病毒脱落和传播的时间动态。Nat,地中海。26(5), 672 - 675。https://doi.org/10.1038/s41591-020-0869-5(2020).
Savvides, C.和Siegel, R. SARS-CoV-2的无症状和症状前传播:一项系统综述。medRxivhttps://doi.org/10.1101/2020.06.11.20129072(2020).
徐,X。et al。中国SARS-CoV-2免疫球蛋白M和G抗体的血清阳性率Nat,地中海。26(8), 1193 - 1195。https://doi.org/10.1038/s41591-020-0949-6(2020).
安德森,r.m.和梅,r.m.。人类传染病:动力学与控制(牛津大学出版社,牛津,1991)
温尼奇,E. &怀特,R. G.。传染病模型导论(牛津大学出版社,牛津,2010)
新墨西哥州弗格森等.非药物干预措施对降低covid - 19死亡率和医疗保健需求的影响。帝国理工学院建模报告。https://doi.org/10.25561/77482(2020)
Wallinga, J. & Teunis, P.不同的严重急性呼吸综合征流行曲线显示控制措施的影响相似。点。j .论文。160, 509 - 516。https://doi.org/10.1093/aje/kwh255(2004)。
贾,N。et al。中国大陆SARS病死率及相关危险因素。太。地中海,Int。健康14(增刊1),21-27。https://doi.org/10.1111/j.1365-3156.2008.02147.x(2009)。
张,X.-S。et al。2015年韩国疫情期间中东呼吸综合征冠状病毒传播能力的估计和建模流感和呼吸。病毒11(5), 434 - 444。https://doi.org/10.1111/irv.12467(2017)。
噢,博士。et al。中东呼吸综合征:我们从2015年韩国疫情中学到的教训。韩文:J. Int地中海。232(2), 233 - 246。https://doi.org/10.3904/kjim.2018.031(2018)。
博雷尔,P。et al。使用多种动态传播模型预测2017/2018年英国季节性流感流行:案例研究BMC公共卫生20., 486年。https://doi.org/10.1186/s12889-020-8455-9(2020).
劳尔,美国。et al。从公开报告的确诊病例看2019冠状病毒病(COVID-19)的潜伏期:估计与应用安。实习生。地中海。172, 577 - 582。https://doi.org/10.7326/M20-0504(2020).
李艳。新冠肺炎患者的识别与治疗策略。新的地中海。51(3), 161 - 167。https://doi.org/10.3969/j.issn.0253-9802.2020.03.001(2020).
韦林,H. J, Rohani, P. & Keeling, M. J.传染病管理的适当模型。科学硕士。2(7) e174。https://doi.org/10.1371/journal.pmed.0020174(2005)。
中国国家卫生健康委员会发布第七版病例定义。http://www.nhc.gov.cn/yzygj/s7653p/202003/46c9294a7dfe4cef80dc7f5912eb1989.shtml.2020年3月12日(中文).
Diekmann, O., Heesterbeek, J. A. P. & Roberts, M. G.构建分区流行病模型的新一代矩阵。J. R接口7, 873-885(2010)。
博雷尔,P。et al。贝叶斯模型揭示和预测伦敦甲型h1n1流感动态。Proc。国家的。学会科学。美国108, 18238 - 18243。https://doi.org/10.1073/pnas.1103002108(2011)。
致谢
本研究由英国公共卫生部和云南省创新研究团队(2019(6))联合资助。综合模型的代码和本研究中使用的数据可向相应作者索取。谨以此文纪念于2019年9月2日逝世的云南大学杨子田教授,感谢他的教诲和鼓励。
作者信息
作者及单位
贡献
构思和设计数学模型和分析:x.s z, E.V, a.c., D.D.A.和w.l.;整理资料:z.c;进行研究:x - s.z.和W.L.;论文写道:x - s.z.和E.V.
相应的作者
道德声明
相互竞争的利益
作者声明没有利益冲突。
额外的信息
出版商的注意
b施普林格《自然》杂志对已出版的地图和机构的管辖权要求保持中立。
补充信息
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
张,x。,Vynnycky, E., Charlett, A.et al。中国新冠肺炎疫情传播动态及控制措施:模型研究Sci代表11, 2652(2021)。https://doi.org/10.1038/s41598-021-81985-z
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-021-81985-z
这篇文章是由
印度及其各邦COVID-19最优控制的数学模型
模拟地球系统和环境(2022)
在COVID-19大流行期间新死亡、治愈、康复和确诊病例之间的小组关联
流行病学与全球健康杂志(2022)
估算COVID-19中每日死亡感染(补救)的回顾性方法:西班牙案例研究
科学报告(2021)