摘要
威胁生命的COVID-19与强烈的炎症有关,其中il -6驱动的细胞因子风暴似乎是增强病理的基石。然而,这种途径的特异性抑制显示出不同的结果。这可能是由于使用托珠单抗的剂量、给药阶段或疾病表现的严重程度的变化。因此,我们对140例中重度COVID-19患者进行了回顾性多中心研究,其中79例患者在病毒期(症状发作后1-7天)、早期炎症期(8-15天)或晚期炎症期(16或以上)接受了不同标准剂量的托珠单抗治疗(< 400mg、400 - 800mg或> 800 mg),并与标准治疗患者进行了比较。测量死亡率、降低的呼吸支持需求和病理标志物。托珠单抗显著降低了所有患者的呼吸支持需求(OR 2.71, CI 1.37-4.85, 95%)和炎症标志物(OR 4.82, CI 1.4-15.8),但死亡率仅降低(4.1% vs 25.7%,p= 0.03),当药物在早期炎症阶段给药,剂量范围为400 - 800mg,在重症患者中。尽管Tocilizumab明显无法防止COVID-19进展为危重症,但在早期炎症期和中等剂量使用Tocilizumab可能有益于重症患者。
简介
冠状病毒病-19 (COVID-19)是由SARS-CoV-2病毒感染呼吸道引起的,SARS-CoV-2病毒是一种细胞病变剂,通过诱导焦上导致肺组织损伤1,2这是一种细胞溶解性的,因此是一种高度炎症性的程序性细胞死亡,通常发生在细胞内感染之后3.因此,COVID-19不仅是一种依赖病毒增殖的疾病,而且是一种炎症驱动的疾病。
开创性的研究4重症患者炎症标志物水平高于轻、中度疾病患者,死亡患者淋巴细胞减少、中性粒细胞增多、c反应蛋白(CRP)、乳酸脱氢酶(LDH)、d-二聚体和IL-6产生程度较高5;所有这些标记都对应于强t辅助1型(Th1)免疫反应。
因此,提出了COVID-19的典型自然史,其中症状出现后的前≈7天以病毒脱落为主,炎症情况较低6,因此被认为是病毒阶段(VS)。在日≈8时,开始进入一个阶段,病毒脱落大部分减少,而炎症变得更加主要,患者往往发展成严重的疾病形式,因此被认为是早期炎症期(EIS)。如果炎症进展超过16天,达到炎症晚期(LIS),最可能发生急性呼吸窘迫综合征、急性心脏损伤、多器官衰竭和死亡的危重疾病7,8.
重要的是,这一思路导致了一种假设,即该疾病的VS可能是用抗病毒药物进行最佳治疗,而不需要强效多效抗炎药物6;而炎症期最好的控制方法是使用抗炎药物9,10,同时服用抗病毒药物几乎没有益处11.
因为IL-6在COVID-19的严重到危重症状中高度表达5在美国,许多研究团队已经使用了Tocilizumab (Tcz),这是一种人源化单克隆抗体,靶向IL-6受体(IL-6R)的膜结合和可溶性形式12以降低炎症,从而避免呼吸和多器官功能障碍。这些研究显示了不同的结果,从缺乏对死亡率的影响,到临床改善的时间,实验室参数和/或预防进展到更严重的疾病13,14,15,16对这些参数的部分或全部进行适度的调制,才能成功17,严重18,19,20.,21,22,及/或危重病人23,24,25.
尽管这些变化看起来很有希望,但它们指出了一个事实,即目前还没有建立Tcz的标准化剂量或不同疾病阶段的给药时间,而且我们对可能从使用这种药物中获益最多的患者类型缺乏了解。另一种解释可能是其他因素,如不同的菌株和患者的特征,可能在疾病的病理生理学中发挥重要作用26甚至认为IL-6在整个现象中的重要性可能被高估了27因为它的水平不像其他病理中il - 6r中和表现出一致的益处那样高。然而,剂量和给药时间的标准化可能仍然是思考IL-6信号在疾病病理生理学中的作用的有价值的一步,从而在tocilizumab治疗COVID-19的疗效中发挥作用。
根据这一思路,我们对中重度COVID-19患者使用Tcz进行了回顾性、观察性、病例对照研究,研究了三种不同的标准剂量区间(< 400 mg、400 - 800 mg和> 800 mg)及其对三个不同疾病阶段(VS、EIS和LIS)的给药。
材料与方法
确认了Español de Pachuca医院、Sociedad Española de Beneficencia (Pachuca)医院和Español de Veracruz医院2020年5月1日至2021年7月1日期间260名COVID-19阳性患者的临床档案。根据以下纳入标准筛选记录:(i) SARS-CoV-2检测结果呈阳性的患者,(ii)中重度COVID-19后住院的患者,(iii)在至少80%的住院天数中有实验室评估的文件,(iv)接受任何类型呼吸支持的患者,以及(v)签署了知情同意书的患者。然后使用排除标准排除档案:(i)自愿出院的患者,(ii)入院后48小时死亡的患者(因为治疗可能没有发挥其效果的最佳时间),(iii)在Tcz给药当天死亡的患者(因为治疗需要3天才能达到最大浓度),以及(iv)临床档案缺乏关键信息的患者。
相关数据收集在谷歌Docs文件中,确定了两个主要治疗组:标准治疗组(ST)(依诺肝素+ 6mg地塞米松,每天一次)和Tcz治疗组(ST +不同Tcz标准剂量)。收集到的数据由一位盲人研究人员反复检查,以确保准确性。
每位患者的病情严重程度由入院时使用在线计算器的CALL评分来评估28.将患者分为三类:(i)需要无创呼吸支持但CALL评分累计达到7分的中度患者,(ii)需要无创呼吸支持但CALL评分达到8分及以上的重度患者,(iii)需要机械通气的危重患者。在这两类患者中,都有接受Tcz或ST治疗的患者。
Tcz平均在入院后3.5天给予,但由于患者在不同的疾病阶段寻求医疗护理,治疗在不同的时间点进行。当症状出现后第1-7天给予Tcz时,患者被视为VS组的一部分;但当药物在症状出现后8-15天或16天或更长时间使用时,患者分别被认为是EIS组或LIS组的一部分。此外,患者根据三种剂量间隔进行分类:< 400mg、400 - 800mg和> 800 mg。当患者在48小时内CRP水平没有降低时,使用第二剂量,但考虑到给药Tcz的总量,将患者分为两组。
通过计算两组的死亡率(死亡率% =(死亡人数× 100)/n)来评估Tcz对生存的影响。这些数据的差异通过Fisher精确检验进行评估,当p值≤0.05。住院时间采用学生t检验进行量化、平均和比较。使用GraphPad Prism 9软件将所有数据绘制成条形图。p值≤0.05为显著。
使用在线计算器VassarStats对Tcz治疗后5天内呼吸支持需求(RSR)降低、机械通气(MV)进展的预防、白细胞、淋巴细胞、中性粒细胞、LDH、CRP、d-二聚体和铁蛋白恢复正常水平的比值比(OR)进行量化29.选择这个时间框架是因为该药物在3天内达到最大浓度,在给药后第5天达到最大临床可观察效果30..
本研究的方案由Sociedad Española de Beneficencia (Pachuca, Hidalgo)的研究伦理机构委员会进行了评估,并于2020年4月23日获得批准。我们的赞助商在研究设计中没有任何作用。所有方法都是按照有关准则和条例,包括《赫尔辛基宣言》进行的。
结果
临床记录和患者特点的选择
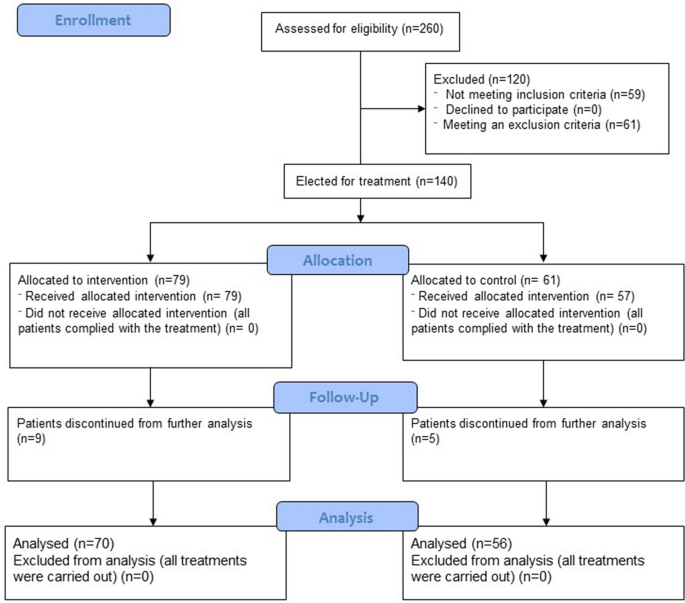
在筛选上述医院的数据库以寻找合格的临床档案后,我们确定了260个记录。201例符合我们的纳入标准,但在剔除符合任何或所有排除标准的患者后,其中只有140例可纳入研究(图2)。1).这些档案被分为两类:st型患者(n = 61)和tcz型患者(n = 79)。ST组危重5例,重36例,中重20例;Tcz组重症9例,重症39例,中轻31例。中度、重度和危重症患者分别采用ST或Tcz方案,以不同剂量和疾病阶段进行治疗。
详见补充表S1在线Tcz治疗平均在入院后3.5天进行,危重、重度和中度患者的平均标准剂量分别为790 mg、790 mg和550 mg。虽然大多数(55.5%)危重患者接受了800mg的剂量,但更大比例的重症患者(25.6%)和中度患者(58%)接受了400至800mg的剂量。此外,76%的患者只接受了一次抗炎治疗,而在危重、重症和中危患者中,有22%、26%和24%的患者在48小时内CRP水平没有下降的情况下接受了额外的抗炎治疗。Tcz患者中有26.6±7%的患者和ST患者中有18±3.4%的患者因既往病情接受了额外的抗炎治疗。
临床参数调节
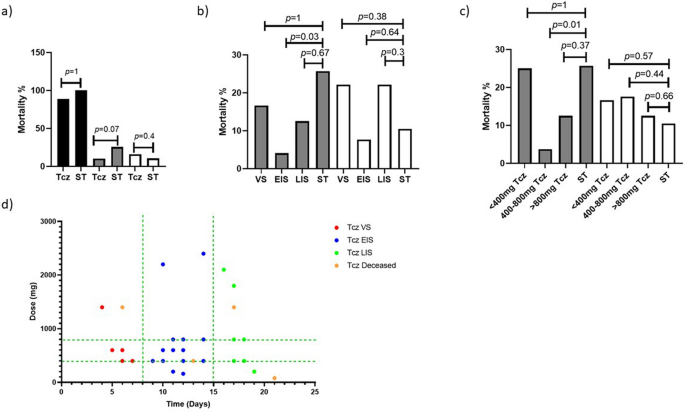
在危重、重度或中度患者中,与危重程度相似但接受ST治疗的患者相比,ST组和Tcz组的死亡率均无显著差异(图2)。2a).尽管如此,当Tcz组根据给药的COVID-19阶段进一步分层为三类(VS、EIS和LIS)时,我们观察到EIS时重症患者的死亡率显著降低(4.1% VS 25.7%;p= 0.03;n= 24)。此外,当Tcz患者根据接受的剂量进行分层时,死亡率显著降低(3.7% vs 25.7%;p= 0.01;n = 27),与疾病严重程度相当的ST组患者相比,接受400-800 mg的患者中n = 27。2b, c)。然而,在VS治疗的重症患者中未观察到这种现象(n= 6)或LIS (n= 9);也不能含有< 400毫克或> 800毫克的Tcz。
此外,中度患者(n= 31)在VS (n= 9), eis (n= 13)或LIS (n= 9),任何剂量,也被发现对这种治疗是不耐的(图。2b, c)。我们缺乏足够的数据来对危重患者进行同样的分析,因为只有14例纳入研究,因此被排除在进一步的分析之外。
此外,多变量分析表明,上述Tcz的标准剂量范围和给药周期之间的收敛代表了一种具有更高生存概率的治疗策略(图2)。2d)。
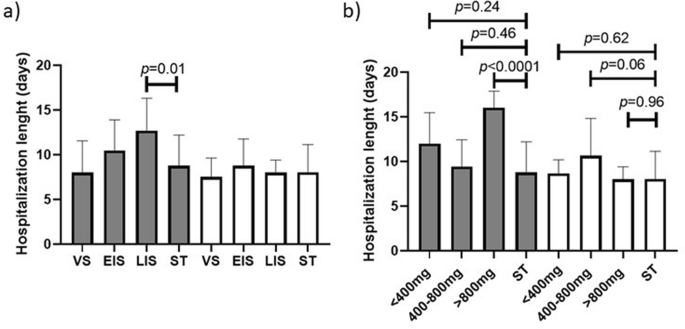
此外,Tcz可显著降低重症患者(OR 2.71, CI 1.37 ~ 4.85, 95%)和中重度患者(OR 2.82, CI 1.47 ~ 4.91, 95%)给药后5天的RSR。Tcz组有9例患者病情恶化,ST组有5例患者病情恶化,需要MV, Tcz无法阻止病情恶化(OR 2.02, CI 0.51-8.0 at 95%)(表2)1).另一方面,该药也不能缩短住院时间,重症患者在LIS治疗(图。3.a)或与> 800 mg Tcz(图。3.B)似乎住院时间很长。
血液和生化参数的调节
测量Tcz给药后5天CRP、LDH、铁蛋白和d-二聚体达到正常值的几率,发现该药物有效降低了第一个标志物的值(OR 4.82, CI 1.4-15.8),但在重症患者中,后三个标志物的值没有显著降低(表2)2).在中度患者中未观察到这些标志物的显著影响。
此外,对总白细胞、淋巴细胞和总中性粒细胞的值进行相同的处理,以确定Tcz是否具有改变这些参数的能力。我们发现该药仅能显著降低重症患者的中性粒细胞水平(OR 2.88, CI 1.23-8.69)2),其他参数均无变化。此外,这些标志物在中度疾病患者中没有改变。
讨论
总的来说,我们观察到Tcz用于治疗重症COVID-19时对疾病具有有效的调节作用,因为重症患者的CRP、中性粒细胞值和RSR均有显著的调节作用,但在中度患者中未观察到这种作用(除RSR降低外)。然而,该药物不能显著降低死亡率,除非在EIS中给重症患者,和/或标准剂量为400-800 mg,这表明其疗效可能与剂量和时间有关。
Tcz对CRP和中性粒细胞水平的影响是可以预料的,因为这种药物阻断了IL-6-CRP轴,这是急性和慢性炎症的一个核心部分,影响急性期蛋白的表达、造血、对微生物损伤的反应和组织损伤的碎片清除31.这种炎症的减轻可能与所观察到的呼吸功能的改善相一致32,33因此,我们发现tcz治疗患者的死亡率降低了。
Tcz在调节COVID-19方面的疗效好坏参半,从完全无效到完全无效13,14,15,16对疾病有显著的调节作用18,19,20.,21,22这种差异可能是由于所有这些研究在参与者的疾病严重程度、使用的总剂量和给药时间方面都有所不同34.事实上,围绕Tcz治疗COVID-19的疗效存在很多争议,因为缺乏关于其使用的许多细节,甚至有人提出了个性化的使用方法35,36.因此,我们研究了这种药物在一系列疾病的表现、剂量和阶段中的作用,旨在获得关于这种药物在COVID-19中的最佳用途的明确数据。
我们认为重症患者的效果最好,因为与中轻患者相比,重症患者的炎症状态增强,EIS是Tcz给药的最佳阶段,因为此时免疫病理开始发展。另一方面,我们认为Tcz在早期阶段对COVID-19的调节能力有限,可能源于炎症在VS的整个病理中很少参与;其后期活动受限可能是因为炎性损伤已经在LIS发生37.
此外,正如其他研究人员发现的那样,中等剂量(400-800毫克)在调节covid -19衍生的死亡率方面表现出的增强效应,可能是因为虽然较小剂量可能缺乏稳健性,但增强剂量可能会缓解继发感染38.
我们没有观察到在任何情况下住院时间的缩短,也没有观察到这种药物降低患者进展到机械通气的可能性。但Tcz对危重症患者的疗效尚不能正确评估,因为我们发现此类患者的临床文献很少。然而,在LIS给药和/或> 800 mg剂量的Tcz似乎延长了住院时间,这可能与描述Tcz治疗患者发生上述医院重叠感染倾向增强的数据一致23,从而表现出在重症监护病房的长时间住院25.我们缺乏来自患者的细菌培养数据作为证实这一假设的手段,但它似乎是合理的,我们认为进一步调查预防性使用抗生素以避免tcz治疗的COVID-19患者长时间住院将有助于澄清这一点。
虽然所有收集到的数据都经过了另一位盲人研究者的验证,以确保准确性,但我们认为我们的研究存在一定的局限性。例如,根据疾病严重程度、阶段和使用剂量对患者进行分层需要增强的力量,因为这种策略形成的亚组往往规模较小。这一事实在危重患者中尤其明显,这一组患者的死亡率很高n= 14。因此,我们无法完成Tcz在监管重症COVID-19中的潜力分析。另一方面,另一个潜在的限制是我们的研究是回顾性的,因为在这样的研究设计中不能对几个变量施加加强的控制。另外,另一个问题可能是其他因素,如不同的菌株和患者的特征,可能在疾病的病理生理学中发挥重要作用,因此与治疗的疗效有关26在这种情况下,细胞因子风暴可能不是唯一的,甚至不是主要的因素27,计算疾病结局。在这种情况下,可能需要进行进一步的多变量研究,以确保本主题更加清晰。
综上所述,这些观察结果表明,COVID-19可能具有广泛的临床谱系,而这一点尚未得到很好的理解,Tcz的疗效可能因不同的临床表现,特别是COVID-19的不同阶段而有所不同。为了对不同的临床表现进行适当的药物治疗,需要进一步的研究来充分了解这一现象。
结论
Tcz在EIS使用时,对降低重症患者的死亡率和RSR以及CRP和中性粒细胞水平有相当大的疗效,剂量范围为400至800 mg。
数据可用性
资料可向通讯作者索取。
参考文献
Tay, M. Z, Poh, C. M., Renia, L., MacAry, P. A. & Ng, L. F. COVID-19的三位一体:免疫、炎症和干预。Nat. Rev. Immunol。20., 363 - 374。https://doi.org/10.1038/s41577-020-0311-8(2020)。
汉明,我。et al。SARS冠状病毒功能受体ACE2蛋白的组织分布。了解SARS发病机制的第一步。j .分册。203, 631 - 637。https://doi.org/10.1002/path.1570(2004)。
芬克,S. L. & Cookson, B. T.凋亡,焦亡和坏死:死亡和垂死真核细胞的机制描述。感染。Immun。73, 1907 - 1916。https://doi.org/10.1128/iai.73.4.1907-1916.2005(2005)。
黄,C。et al。武汉地区新型冠状病毒感染患者临床特征分析《柳叶刀》395, 497 - 506。https://doi.org/10.1016/s0140 - 6736 (20) 30183 - 5(2020)。
张,B。et al。82例COVID-19死亡病例临床特征分析《公共科学图书馆•综合》15, e0235458。https://doi.org/10.1371/journal.pone.0235458(2020)。
潘艳,张东,杨萍,潘丽丽梅,王强。SARS-CoV-2临床样本病毒载量的研究。《柳叶刀》。感染。说20., 411 - 412。https://doi.org/10.1016/s1473 - 3099 (20) 30113 - 4(2020)。
胡斌,郭宏,周平,石志林。新型冠状病毒感染与新型冠状病毒感染的特征。Nat. Rev.微生物。19, 141 - 154。https://doi.org/10.1038/s41579-020-00459-7(2021)。
博恩,M. K。et al。COVID-19的病理生理学:疾病严重程度和进展的潜在机制。生理学35, 288 - 301。https://doi.org/10.1152/physiol.00019.2020(2020)。
Gautret, P。et al。COVID-19的自然史和治疗方案。克林牧师专家。Immunol。16, 1159 - 1184。https://doi.org/10.1080/1744666X.2021.1847640(2020)。
组钢筋混凝土et al。地塞米松在Covid-19住院患者中的应用。心血管病。j .地中海。384, 693 - 704。https://doi.org/10.1056/NEJMoa2021436(2021)。
沃尔什,k。et al。SARS-CoV-2检测、病毒载量和感染过程中的传染性。j .感染。81, 357 - 371。https://doi.org/10.1016/j.jinf.2020.06.067(2020)。
田中,T, Narazaki, M. & Kishimoto, T. IL-6阻断对细胞因子风暴的免疫治疗意义。免疫疗法8, 959 - 970。https://doi.org/10.2217/imt-2016-0020(2016)。
Campochiaro C。et al。托珠单抗治疗重症COVID-19患者的疗效和安全性:一项单中心回顾性队列研究欧元。j .实习生。地中海。76, 43-49。https://doi.org/10.1016/j.ejim.2020.05.021(2020)。
Rojas-Marte G。et al。托珠单抗治疗严重COVID-19疾病患者的结果:一项病例对照研究QJM113, 546 - 550。https://doi.org/10.1093/qjmed/hcaa206(2020)。
Colaneri, M。et al。Tocilizumab治疗严重COVID-19患者:来自smmatteo COvid19 REgistry (SMACORE)的初步结果。微生物https://doi.org/10.3390/microorganisms8050695(2020)。
罗萨斯,i.o.。et al。Tocilizumab在COVID-19肺炎住院患者中的应用medRxivhttps://doi.org/10.1101/2020.08.27.20183442(2020)。
Potere, N。et al。低剂量皮下托珠单抗用于预防中度COVID-19肺炎和过度炎症患者的疾病进展。Int。j .感染。说。One hundred., 421 - 424。https://doi.org/10.1016/j.ijid.2020.07.078(2020)。
Gokhale, Y., Mehta, R., Karnik, N., Kulkarni, U. & Gokhale, S. Tocilizumab可提高重症COVID-19肺炎持续缺氧患者的生存率。EClinicalMedicine24, 100467年。https://doi.org/10.1016/j.eclinm.2020.100467(2020)。
R·卡普拉。et al。低剂量托珠单抗对COVID-19相关肺炎患者死亡率的影响欧元。j .实习生。地中海。76, 31-35。https://doi.org/10.1016/j.ejim.2020.05.009(2020)。
Sciascia, S。et al。针对重度COVID-19患者超说明书使用托珠单抗的前瞻性开放单臂多中心试点研究中国。Exp Rheumatol。38, 529-532(2020)。
, T。et al。Tocilizumab治疗降低了COVID-19患者的重症监护病房入院率和/或死亡率。医学疾病感染。50, 397 - 400。https://doi.org/10.1016/j.medmal.2020.05.001(2020)。
普赖斯,c.c。et al。托珠单抗治疗2019年冠状病毒疾病住院患者的细胞因子释放综合征:生存和临床结果胸部158, 1397 - 1408。https://doi.org/10.1016/j.chest.2020.06.006(2020)。
萨默斯,e.c.。et al。托珠单抗用于治疗COVID-19机械通气患者。中国。感染。说。https://doi.org/10.1093/cid/ciaa954(2020)。
古普塔,S。et al。托珠单抗早期治疗与COVID-19危重患者死亡率的相关性JAMA实习生。地中海。181, 41-51。https://doi.org/10.1001/jamainternmed.2020.6252(2021)。
Rajendram, P。et al。托珠单抗在2019冠状病毒疾病相关危重疾病中的应用:倾向匹配分析。暴击。保健空洞。3., e0327。https://doi.org/10.1097/CCE.0000000000000327(2021)。
德默勒,K,安格斯,D. C.和西摩,C. W.针对COVID-19的精准医疗:表型混乱还是承诺实现?《美国医学会杂志》325, 2041 - 2042。https://doi.org/10.1001/jama.2021.5248%JJAMA(2021)。
雷斯曼,d。E。et al。重症和危重型COVID-19的细胞因子升高:快速系统回顾、荟萃分析和与其他炎症综合征的比较和出版的《柳叶刀》杂志上。地中海。8, 1233 - 1244。https://doi.org/10.1016/s2213 - 2600 (20) 30404 - 5(2020)。
咨询,r。C。C。打电话给分数.https://www.rccc.eu/COVID/CALL.html(2020)。
VassarStats。带有比值比的2x2列联表:VassarStats.http://vassarstats.net/odds2x2.html(2001)。
Zhang, X., Georgy, a . & Rowell, L. tocilizumab是一种人源化抗白介素-6受体单克隆抗体,经皮下和静脉单剂量给药后对健康受试者的药代动力学和药效学。Int。j .中国。杂志。其他。51, 443 - 455。https://doi.org/10.5414/CP201819(2013)。
田中,T, Narazaki, M. & Kishimoto, T. IL-6在炎症、免疫和疾病中的作用。冷泉港。教谕。医学杂志。6, a016295。https://doi.org/10.1101/cshperspect.a016295(2014)。
汤姆逊,B. T.钱伯斯,R. C. &刘k.d .急性呼吸窘迫综合征。心血管病。j .地中海。377, 1904 - 1905。https://doi.org/10.1056/NEJMc1711824(2017)。
Fajgenbaum, d.c. & June, c.h.细胞因子风暴。心血管病。j .地中海。383, 2255 - 2273。https://doi.org/10.1056/NEJMra2026131(2020)。
Atzeni F。et al。治疗COVID-19的风湿病药物:使用哪种药物,何时使用?j .中国。地中海。10, 783年。https://doi.org/10.3390/jcm10040783(2021)。
组,T. W. R. E. A. f. c . t。W. IL-6拮抗剂的应用与COVID-19住院患者死亡率之间的关系:一项荟萃分析。《美国医学会杂志》326, 499 - 518。https://doi.org/10.1001/jama.2021.11330%JJAMA(2021)。
雪,t.a.c。et al。Tocilizumab在COVID-19中的应用:随机对照试验的meta分析、试验序列分析和meta回归重症监护室。47, 641 - 652。https://doi.org/10.1007/s00134-021-06416-z(2021)。
Dos Santos, W. G. COVID-19的自然史和目前关于治疗方案的知识。生物医学。Pharmacother。129, 110493年。https://doi.org/10.1016/j.biopha.2020.110493(2020)。
帕瓦尔,。et al。类风湿性关节炎患者托珠单抗与其他生物药物的严重感染风险:一项多数据库队列研究安。感冒。说。78, 456 - 464。https://doi.org/10.1136/annrheumdis-2018-214367(2019)。
确认
所有作者都希望感谢Sociedad Española de Beneficencia, Pachuca, Hidalgo,为本研究的实现和出版提供财政和技术支持。作者也希望感谢奖学金和教育,他们从这样的机构接受。
资金
本研究全部由Sociedad Española de Beneficencia, Pachuca, Hgo资助。
作者信息
作者及隶属关系
贡献
A.D.M A.D.A.A。,E.V.G E.N.O, D.P.O, C.J.P, A.R.H.R, A.N.P. A.C.J.V.分析数据;K.Y.H.S G.M.B。,O.J.R.R F.R.L, D.M.S, P.O.R, J.R.F.H, J.D.M.C, D.M.O, K.C.F.L, M.T.C, A.V.H, F.S.C, S.O.R, M.A.S.G, A.R.M, L.M.P.M, M.C.B.和E.L.L研究收集的数据;A.D.M.和A.N.P.设计了这项研究,并撰写了这篇文章。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
Durán-Méndez, A,阿奎拉-阿罗约,ad, Vivanco-Gómez, E。et al。Tocilizumab以剂量和时间依赖的方式降低COVID-19死亡率和病理:一项多中心研究Sci代表11, 19728(2021)。https://doi.org/10.1038/s41598-021-99291-z
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-021-99291-z
这篇文章被引用
对抗SARS-CoV-2的被动免疫治疗:从基于血浆的治疗到单一强效抗体,在竞争中保持领先
BioDrugs(2022)