文摘gydF4y2Ba
单克隆抗体与高亲和力是有价值的目标SARS-CoV-2广泛的生物医学应用程序涉及新型冠状病毒病(COVID-19)诊断、治疗和预防干预。这些抗体的快速和可靠的隔离策略,尤其是有效的中和抗体,是至关重要的对改善COVID-19响应和通知未来应对突发传染病。在这项研究中,单一的B细胞筛选抗体用来审问能免疫小鼠和抗原IgG1隔离gydF4y2Ba+gydF4y2Ba记忆B细胞。使用这些方法,高亲和性,确定了有效的中和抗体这一目标SARS-CoV-2的受体结合域。确定分子的进一步工程价导致增强的中和活动增加。机械的调查显示,这些抗体与ACE2争夺绑定SARS-CoV-2的受体结合域。这些抗体可能保证紧急COVID-19应用程序的进一步发展。总的来说,这些结果强调单一的B细胞的潜在筛查的高亲和性的快速和可靠的识别,为传染病应用有效的中和抗体。gydF4y2Ba
介绍gydF4y2Ba
新型冠状病毒病(COVID-19)大流行,造成的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2),已严重影响人类健康,导致超过一百万人死亡gydF4y2Ba1gydF4y2Ba。减轻的负担COVID-19,广泛获得有效的治疗,诊断和疫苗是非常必要的。令人鼓舞的是,几个候选疫苗已成为及时的预防性干预措施的初步迹象非常有前途。然而,大规模的生产,分配和管理仍然主要障碍,许多人尚未接种疫苗由于缺乏访问。此外,COVID-19仍然是一个严重的全球威胁人类健康gydF4y2Ba2gydF4y2Ba。gydF4y2Ba
高亲和力抗体绑定SARS-CoV-2在打击COVID-19发挥着重要的作用,疫苗预防干预的补充。事实上,抗体已经成功地用于COVID-19诊断,治疗,预防和疫苗开发gydF4y2Ba3gydF4y2Ba,gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba。特别的注意,一些单克隆抗体及其组合收到紧急使用授权治疗COVID-19轻度到中度患者的症状和降低疾病进展和住院治疗的目标gydF4y2Ba3gydF4y2Ba,gydF4y2Ba4gydF4y2Ba。这些包括bamlanivimab etesevimab从礼来和casirivimab imdevimab Regeneron。令人鼓舞的是,标准抗体的发现和开发时间表,包括从目标识别到临床典型的发展从年到几十年来大大加快,导致快速发现、开发和制造抗体紧急COVID-19应用程序。gydF4y2Ba
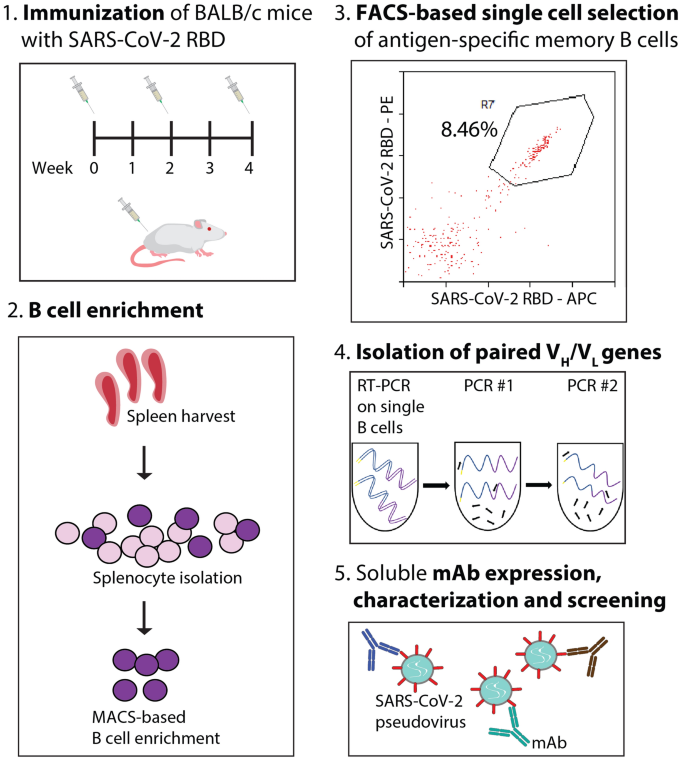
在这种加速发展的早期阶段,高亲和性的快速和可靠的发现策略,有效的中和抗体是至关重要的对提供及时响应COVID-19等传染病。越来越多的证据表明,广泛实用的单身B细胞的高亲和性抗体筛查的隔离的周内所需的靶抗原gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba。这个过程包括隔离可行的细胞(通常来自免疫动物或恢复期的病人),高通量单细胞排序所需的抗原特异的亚种,复苏的配对VgydF4y2BaHgydF4y2Ba/ VgydF4y2BalgydF4y2Ba抗体基因通过rt - PCR和PCR的步骤,和表达和评价抗体的候选人。图中说明了这种方法的一个例子。gydF4y2Ba1gydF4y2Ba。单一的B细胞克隆导致的高亲和性抗体的识别各种抗原使用各种物种的样本(包括小鼠、兔、和人类)和组织(包括脾脏、骨髓和血液)gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba。总的来说,单一的B细胞筛选是有吸引力的,鉴于其自然抗体的使用体验,保留原生VgydF4y2BaHgydF4y2Ba/ VgydF4y2BalgydF4y2Ba搭配,适合高通量发现和评估,相对于替代方法和简单性。gydF4y2Ba
概述的方法发现和描述的SARS-CoV-2中和抗体分离出单一的B细胞。(gydF4y2Ba1gydF4y2Ba)免疫BALB / c小鼠SARS-CoV-2 RBD三次间隔2周。(gydF4y2Ba2gydF4y2Ba)脾细胞收获六周后的初始接种B细胞通过mac和孤立的细胞分类的标签。(gydF4y2Ba3gydF4y2Ba)细胞阳性绑定SARS-CoV-2 RBD贴上两个独特的荧光团(门R7)被分类为单个细胞成96 -孔板。(gydF4y2Ba4gydF4y2BaV)多重PCR步骤被孤立gydF4y2BaHgydF4y2Ba和VgydF4y2BalgydF4y2Ba抗体基因。(gydF4y2Ba5gydF4y2Ba)抗体表达、纯化和评估抗原绑定,中和活动和生物物理属性。gydF4y2Ba
本研究的目的是评估单的效用B细胞筛查SARS-CoV-2强有力的中和抗体的隔离。值得注意的是,先前的报道表明,高亲和力抗体中和活动和目标抗原决定基是关键因素gydF4y2Ba14gydF4y2Ba,gydF4y2Ba15gydF4y2Ba为了有效地破坏的高亲和力(低海里)交互SARS-CoV-2受体结合域与人类ACE2 (RBD)gydF4y2Ba14gydF4y2Ba,gydF4y2Ba15gydF4y2Ba,gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba,gydF4y2Ba18gydF4y2Ba。为了实现这个目标,我们试图确定的高亲和性IgG1抗体gydF4y2Ba+gydF4y2Ba记忆B细胞来源于免疫小鼠的脾脏。对免疫,一个关键的要求是引起足够的IgG1gydF4y2Ba+gydF4y2Ba等单一细胞筛选,记忆B细胞反应,中和抗体代表这个响应的一个子集。我们推断SARS-CoV-2 RBD结合标准辅助明矾就代表一个合乎逻辑的和低风险的疫苗,鉴于RBD是涉及病毒传染性gydF4y2Ba16gydF4y2Ba明矾是强大的体液反应有关gydF4y2Ba19gydF4y2Ba。通过使用这种疫苗接种的方法与单一的B细胞筛选,我们报告的一代,工程和描述小说的高亲和性和强有力的中和抗体,具有对SARS-CoV-2活动。gydF4y2Ba
结果gydF4y2Ba
小鼠免疫与SARS-CoV-2受体结合域展示重要的抗原免疫球蛋白和IgG1反应gydF4y2Ba
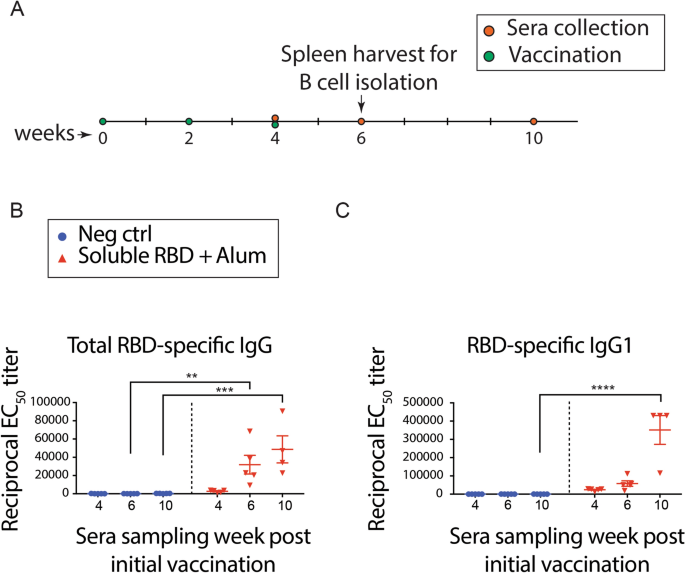
引出一个IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞响应对RBD、BALB / c小鼠接种三次,为期两周的时间间隔通过皮下注射剂量尾巴基地(无花果。gydF4y2Ba1gydF4y2Ba)。每剂包含0.5µg SARS-CoV-2 RBD和500µg明矾。血清样本收集的活老鼠在星期4,6和10。描述RBD-specific免疫反应,血清样本评估RDB-specific总免疫球蛋白和IgG1抗体反应使用RBD-specific ELISA(无花果。gydF4y2Ba2gydF4y2BaA、B)。相对于消极的控制(未接种疫苗)小鼠,RBD-immunized小鼠血清显示重要总RBD-specific IgG抗体效价在6周(p < 0.01),在10周(p < 0.001,通过双向方差分析其次是行比较),如无花果所示。gydF4y2Ba2gydF4y2Baa .进一步RBD-immunized小鼠血清表现出显著RBD-specific IgG1抗体反应在10周(p < 0.0001),如无花果所示。gydF4y2Ba2gydF4y2Bab在一起,这些数据表明这种疫苗接种策略导致重大anti-RBD抗体反应,这是第一次明显6周接种后(RBD-IgG效价),和更重要的是证实了周10 (RBD-IgG和IgG1效价)。此外,这些数据支持的可行性筛查单一anti-RBD IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞在6 - 10周的时间点。gydF4y2Ba
总RBD-specific RBD-immunized老鼠证明重要的免疫球蛋白和IgG1响应。(gydF4y2Ba一个gydF4y2Ba)BALB / c小鼠接种三次间隔2周。在周4、6和10,血清样本收集总免疫球蛋白(gydF4y2BaBgydF4y2Ba)和IgG1 (gydF4y2BaCgydF4y2Ba)使用RBD-specific ELISA效价测量。一个子集的老鼠被用来收割脾脏B细胞隔离在星期6。提出了数据相互EC的意思gydF4y2Ba50gydF4y2Ba±SEM。* * * * * p < 0.01, p < 0.001, * * * * p < 0.0001的双向方差分析后跟行比较。gydF4y2Ba
单细胞排序可以有效的隔离anti-RBD IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞gydF4y2Ba
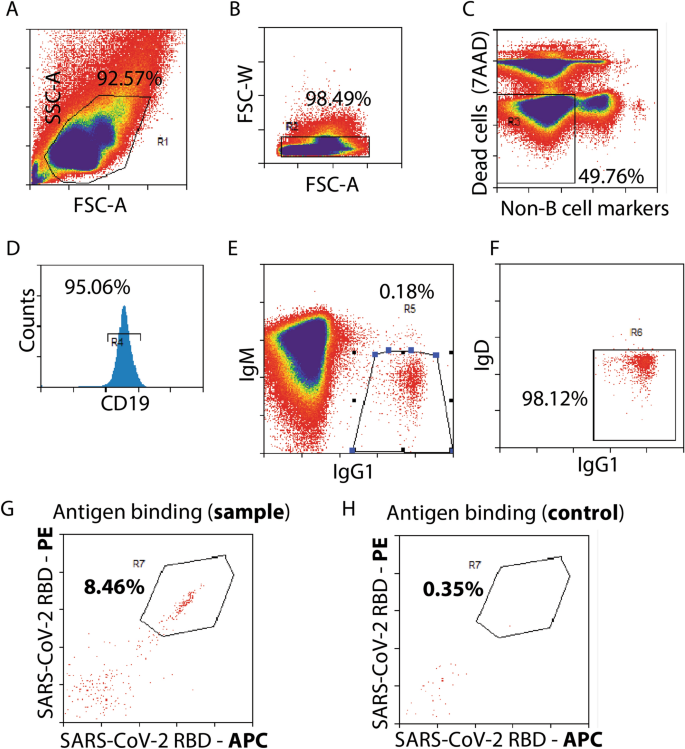
鉴于我们关注的发现SARS-CoV-2中和抗体,免疫小鼠的一个子集,一个接种疫苗和一个控制,牺牲在第6周对单个B细胞排序(图。gydF4y2Ba2gydF4y2BaA)。从免疫和控制小鼠脾脏被切除,立即处理单个细胞悬浮液的淋巴细胞,并进一步加工为B细胞通过丰富magnetic-activated细胞为CD19排序(mac)gydF4y2Ba+gydF4y2Ba细胞。细胞悬浊液随后被标以检测抗体(表的面板gydF4y2BaS1gydF4y2Ba),以及两个RBD-fluorophore共轭,即allophycocyanin (APC)和R-phycoerythrin (PE)。细胞的一个子集是单一颜色补偿标签。单细胞分选,一系列的盖茨是用于隔离anti-RBD IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞(图。gydF4y2Ba3gydF4y2Bag)。分析细胞悬液显示大量的CD19的标签gydF4y2Ba+gydF4y2BaB细胞(图。gydF4y2Ba3gydF4y2BaD,门R4 > 95%),表明MACS-based B细胞预富集策略的有效性。细胞拥有IgG1的表型gydF4y2Ba+gydF4y2Ba和IgMgydF4y2Ba- - - - - -gydF4y2Ba细胞的一种罕见的子集(图表示。gydF4y2Ba3gydF4y2BaE,门R5 < 0.5%)与大多数细胞事件展示一个IgMgydF4y2Ba+gydF4y2Ba天真的B细胞的表型特征(图gydF4y2Ba3gydF4y2BaE)。令人鼓舞的是,双阳性(RBD-APCgydF4y2Ba+gydF4y2Ba和RBD-PEgydF4y2Ba+gydF4y2Ba)IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞代表8.46%的事件每cytogram RBD-immunized示例(图。gydF4y2Ba3gydF4y2BaG),而相当于人口未接种疫苗控制样本每cytogram代表只有0.35%的事件(无花果。gydF4y2Ba3gydF4y2BaH),这对应于一个signal-to-background比率> 24日建议低风险的识别假阳性细胞,即那些anti-RBD IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞表型(如评估我们的控制策略),否则缺乏anti-RBD抗体表达。成套流cytograms控制鼠标样品详细的补充图。gydF4y2Ba1gydF4y2Ba。基于这些结果,单个细胞分为个别井在96孔板,和加工V的复苏gydF4y2BaHgydF4y2Ba/ VgydF4y2BalgydF4y2Ba基因。gydF4y2Ba
控制策略的隔离RBD-specific记忆B细胞通过单细胞排序。流cytograms细胞样本(gydF4y2Ba一个gydF4y2Ba- - - - - -gydF4y2BaGgydF4y2Ba)免疫BALB / c小鼠和(gydF4y2BaHgydF4y2Ba天真的老鼠所示)控制。以下(gydF4y2Ba一个gydF4y2Ba- - - - - -gydF4y2BaGgydF4y2BaR7)控制策略应用于系列和门被分类为单个细胞在96 -孔板:(gydF4y2Ba一个gydF4y2Ba)选择基于大小的淋巴细胞(向前散射区域)和粒度(侧散射区域),(gydF4y2BaBgydF4y2Ba)双重歧视向前向前散射宽度和散射面积,(gydF4y2BaCgydF4y2Ba)和缺乏可行性non-B细胞标记(T细胞标记CD4, CD8 T细胞标记,中性粒细胞GR-1标志,巨噬细胞标记F480), (gydF4y2BaDgydF4y2Ba)B细胞标记CD19, (gydF4y2BaEgydF4y2Ba)为IgM阴性(天真的B细胞标记)和积极IgG1, (gydF4y2BaFgydF4y2Ba)为阴性IgD(天真的B细胞标记)和(gydF4y2BaGgydF4y2Ba)绑定到SARS-CoV-2 RBD用PE和APC荧光蛋白标记。流cytograms控制天真的老鼠在补充图。gydF4y2Ba1gydF4y2Ba。绑定cytogram SARS-CoV-2 RBD抗原(gydF4y2BaHgydF4y2Ba比较的)天真的老鼠了。gydF4y2Ba
单细胞分析提供有效的复苏配对VgydF4y2BaHgydF4y2Ba/ VgydF4y2BalgydF4y2Ba基因gydF4y2Ba
评估配对V的效率gydF4y2BaHgydF4y2Ba/ VgydF4y2BalgydF4y2Ba基因恢复,一个96孔板包含anti-RBD IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞(每个)一个V的探索gydF4y2BaHgydF4y2Ba和VgydF4y2BalgydF4y2Ba使用一系列的基因PCR步骤之前报道gydF4y2Ba20.gydF4y2Ba。rt - PCR的过程一轮转换细胞RNA cDNA,最初一轮PCR扩增VgydF4y2BaHgydF4y2Ba和VgydF4y2BalgydF4y2Ba使用一套引物特定(κ)基因共同IgG1小鼠抗体框架区域,和第二轮PCR扩增全长VgydF4y2BaHgydF4y2Ba和VgydF4y2BalgydF4y2Ba基因。通过Sanger测序PCR产品随后被测序。96口井的评估,18导致复苏配对VgydF4y2BaHgydF4y2Ba/ VgydF4y2BalgydF4y2Ba基因,48 V导致复苏gydF4y2BaHgydF4y2Ba基因,3 V导致复苏gydF4y2BalgydF4y2Ba基因。在检查结果配对VgydF4y2BaHgydF4y2Ba/ VgydF4y2BalgydF4y2Ba复制的基因序列,共14个独特的抗体对被识别。结果14对被克隆到重型和轻型链哺乳动物表达质粒含有人类IgG1常数区域和kappa轻链区域嵌合抗体的表达。抗体表达在HEK 293 - 6 e通过瞬时转染细胞,随后使用蛋白质纯化珠子,导致五导致抗体的隔离(12 h2, 13 i1, 1 a1, 4 a7, 6 c5)与净化的产量~ 10-40 mg / L。导致抗体序列和系统发育分析分别提出了补充无花果。gydF4y2Ba2gydF4y2Ba和gydF4y2Ba3gydF4y2Ba。sds - page分析导致克隆表示分子量与理论值一致(补充图。gydF4y2Ba4gydF4y2Ba)。令人鼓舞的是,分析凝胶排阻色谱(SEC)进一步验证预测抗体大小和高纯度non-denaturing条件。超过95%的单体内容观察所有抗体检测(补充图。gydF4y2Ba5gydF4y2Ba)。gydF4y2Ba
孤立SARS-CoV-2 RBD展示高度的亲和力的抗体gydF4y2Ba
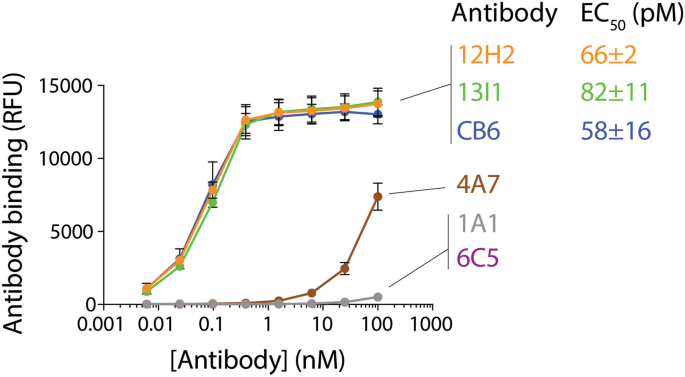
评价铅的亲和力抗体SARS-CoV-2 RBD,二价抗体与生物素化的co-incubated SARS-CoV-2 RBD固定在磁珠和绑定通过流式细胞术进行评估。这个关联分析显示,两个铅克隆h2(12和13 i1)拥有低点ECgydF4y2Ba50gydF4y2Ba值对RBD(无花果。gydF4y2Ba4gydF4y2Ba)。拟合剂量依赖性绑定响应曲线表明,铅克隆12 h2和13 i1拥有电子商务gydF4y2Ba50gydF4y2Ba值66±2和82±11点,分别(无花果。gydF4y2Ba4gydF4y2Ba)。相比较而言,人类SARS-CoV-2抗体CB6之前报道,据报道,高亲和力RBD和强有力的中和活性gydF4y2Ba21gydF4y2Ba表达和纯化内部,包括积极控制。令人鼓舞的是,我们的分析显示,我们的领导具有亲和力的抗体接近CB6积极的控制(ECgydF4y2Ba50gydF4y2Ba58±16点)。其他三个铅克隆(4 a7、1 a1和6 c5)显示更低的亲和力。总的来说,这些数据证明的一个子集确定绑定SARS-CoV-2 RBD高亲和力的抗体。gydF4y2Ba
证明有效的中和抗体活动SARS-CoV-2 pseudovirus化验gydF4y2Ba
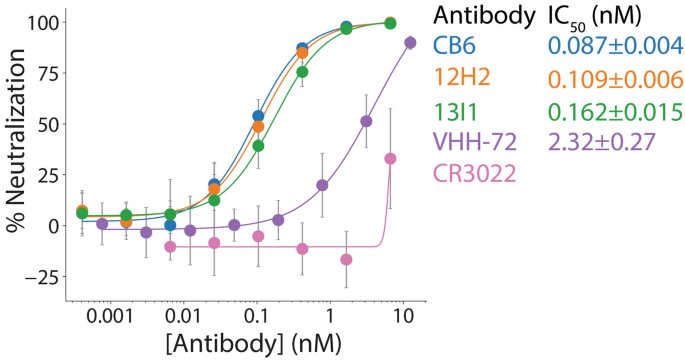
评估导致抗体的中和活性,以慢病毒为基础的pseudovirus分析是基于以前的工作gydF4y2Ba22gydF4y2Ba。在这个试验,pseudovirus粒子,显示SARS-CoV-2飙升表面蛋白和包含的RNA编码荧光素酶的表达与抗体或co-incubated控件,然后连续稀释这些混合物被应用于工程HEK293T细胞稳定表达人类ACE2在细胞表面。Pseudovirus传染性是量化的相对荧光素酶表达感染后48 h。抗体12 h2和13 i1评估相对于控制中和抗体CB6,以及两个额外的控制,被发现对SARS-CoV-2对冠状大。这些包括vhh - 72, SARS-CoV-2中和nanobodygydF4y2Ba23gydF4y2Ba,CR3022 anti-SARS-CoV-2高亲和力的单克隆抗体中和有限的活动gydF4y2Ba24gydF4y2Ba,gydF4y2Ba25gydF4y2Ba。如无花果所示。gydF4y2Ba5gydF4y2Ba,高亲和性抗体12 h2和13 i1拥有强力的中和活性。的集成电路gydF4y2Ba50gydF4y2Ba值分别为0.109±0.006,0.162±0.015 nM 12 h2和13 i1,分别。同样,积极控制中和抗体CB6 ICgydF4y2Ba50gydF4y2Ba0.087±0.004海里。12 h2和13 i1显著提高集成电路gydF4y2Ba50gydF4y2Ba值相对于vhh - 72 (ICgydF4y2Ba50gydF4y2Ba2.32±0.27海里)和CR3022 (ICgydF4y2Ba50gydF4y2Ba> 6.7海里)。总的来说,这些数据表明,小说RBD-specific抗体拥有强有力的sub-nM中和活动。鉴于高序列相似的抗体12 h2和13 i1 (VgydF4y2BaHgydF4y2Ba= 99.2%相似,VgydF4y2BalgydF4y2Ba= 99.1%相似,补充图。gydF4y2Ba2gydF4y2Ba),随后的调查是只有13 i1进行的。gydF4y2Ba
有效的中和抗体竞争与ACE2 SARS-CoV-2 RBD绑定gydF4y2Ba
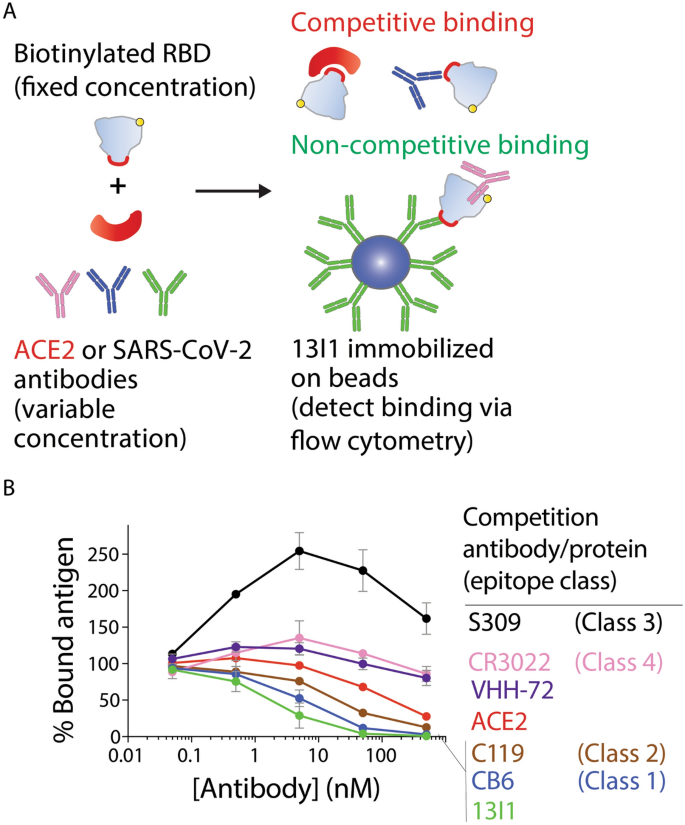
评价中和抗体绑定表位和机制,竞争结合分析使用的抗体(13 i1, CB6、CR3022 vhh - 72, C119, S309)或人工ACE2与生物素化的pre-incubated SARS-CoV-2 RBD (5 nM)在一系列抗体或ACE2的浓度,然后用13 co-incubated i1固定化蛋白质磁珠(无花果。gydF4y2Ba6gydF4y2Ba)。RBD的百分比绑定到13 i1-coated珠子,流式细胞术评估,报告相对于RBD绑定的数量没有竞争对手。正如所料,孵化的RDB 13 i1导致附近完全抑制RBD绑定到13 i1-coated珠子。值得注意的是,RBD pre-incubation ACE2导致部分抑制13 i1与RBD的接触。从力学上看,这表明13 i1的中和活动至少部分归因于抑制人类ACE2 RBD参与。gydF4y2Ba
中和抗体13 i1竞争与ACE2绑定到SARS-CoV-2受体结合域。(gydF4y2Ba一个gydF4y2Ba)之间的竞争分析示意图13 i1, ACE2和其他抗体(CR3022, CB6 vhh - 72、C119 S309)。竞争结合分析采用13 i1,参考抗体或ACE2与生物素化的pre-incubated RBD (5 nM)在一系列浓度的抗体或ACE2,然后用固定化co-incubated 13 i1蛋白质磁珠。(gydF4y2BaBgydF4y2Ba)的百分比SARS-CoV-2 RBD绑定报告相对于一定数量与抗体或pre-blocking ACE2的缺失。结果从两个独立的实验,平均误差标准差。gydF4y2Ba
重要的是,竞争进行了分析与之前报道SARS-CoV-2抗体gydF4y2Ba26gydF4y2Ba进行独特的抗原表位SARS-CoV-2突起蛋白:CB6(1级),C119(二班),S309(3班),CR3022(第4类)。有趣的是,CB6抗体,显示类似的高亲和力和中和活动相对于12 h2和13 i1,观察与13 i1强烈竞争RBD绑定。同样,C119抗体也观察到竞争与13 i1 RBD绑定,这表明13 i1承认部分重叠或近端抗原决定基的RBD相对于CB6(1级)和C119(二班)。相反,S309没有与13 i1 RBD绑定。有趣的是,13 i1绑定RBD S309的存在明显增强,表明接触RBD的抗原决定基特征类的3抗体可能稳定13 i1绑定到一个非竞争性RBD抗原决定基。此外,CR3022抗体和vhh - 72 nanobody也没有竞争力,13 i1 RBD约束力,建议13 i1承认一个独特的抗原决定基相对于这些控件。gydF4y2Ba
价提高13 i1中和活动增加gydF4y2Ba
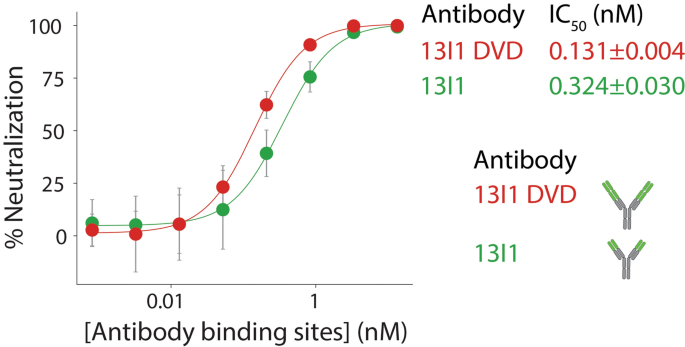
接下来,我们试图探讨抗体中和活动价的影响。为了实现这个目标,我们设计了一个四价的二元变量域(DVD)版本的13 i1抗体和直接评估中和活动相对于二价13 i1免疫球蛋白通过SARS-CoV-2 pseudovirus化验(无花果。gydF4y2Ba7gydF4y2Ba)。抗体进行比较的基础上,结合位点浓度占价的差异。令人鼓舞的是,13 i1 DVD显示增强的中和活动(ICgydF4y2Ba50gydF4y2Ba0.131±0.004海里)相对于二价13 i1马伯(ICgydF4y2Ba50gydF4y2Ba即使占0.324±0.030海里)价的差异。这些数据表明,增加化合价协同提高13 i1抗体的中和活性。gydF4y2Ba
价提高13 i1中和活动增加。中和活动四价13 i1 DVD-formatted抗体显示相对于13 i1二价抗体。以慢病毒为基础的SARS-CoV-2 pseudovirus化验工作,和相对荧光素酶信号测量48 h后感染。计算half-maximal抑制剂量(ICgydF4y2Ba50gydF4y2Ba提出了)。13 i1 DVD中和活动并行评估13 i1收集的数据图。gydF4y2Ba5gydF4y2Ba这里显示清晰。这些数据是三个独立的重复的平均值,而误差标准差。gydF4y2Ba
中和抗体具有较高的特异性和稳定性gydF4y2Ba
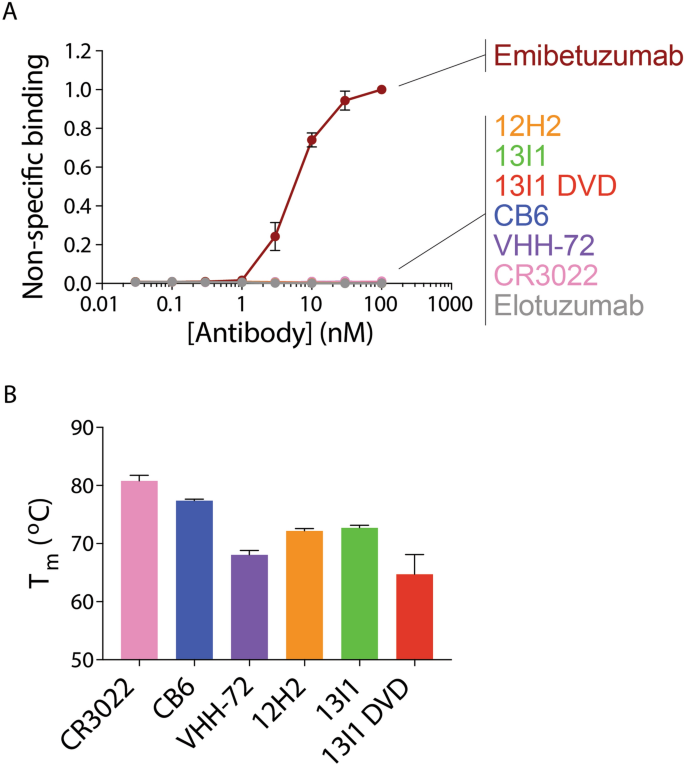
我们下一个试图描述最中和抗体的生物物理特性(图中确定这项工作。gydF4y2Ba8gydF4y2Ba)。为了实现这个目标,我们进行了非特异性结合分析通过孵化的抗体polyspecificity试剂,由生物素化的可溶膜蛋白来源于CHO细胞gydF4y2Ba27gydF4y2Ba,gydF4y2Ba28gydF4y2Ba。生物素化的可溶膜蛋白质的相对绑定每个蛋白质抗体固定在一个磁珠是评估使用流式细胞仪(无花果。gydF4y2Ba8gydF4y2Ba)。控制临床分期抗体(emibetuzumab)和低(elotuzumab)高水平的非特异性结合同时进行比较。令人鼓舞的是,这项工作中产生的抗体(12 h2, 13 i1, 13 i1 DVD)显示极低水平的非特异性结合,可比elotuzumab。我们进一步评估抗体稳定的熔化温度(gydF4y2BaTgydF4y2Ba米gydF4y2Ba通过差示扫描荧光测定法)。控制抗体显示gydF4y2BaTgydF4y2Ba米gydF4y2Ba值为80.8±0.8°C (CR3022), 77.4±0.2°C (CB6)和68.1±0.6°C (vhh - 72;无花果。gydF4y2Ba8gydF4y2BaB),免疫球蛋白中发现这项工作被观察到gydF4y2BaTgydF4y2Ba米gydF4y2Ba值为72.2±0.3°C (12 h2), 72.7±0.4°C (13 i1)和64.7±3.0°C (13 i1 DVD)。13 i1 DVD抗体展出一个展开概要文件包含两个局部极大值,表明多个发生转换,而其他抗体显示出一个正在转变。总的来说,这些数据强调了良好的特异性和稳定性产生的抗体在这工作。gydF4y2Ba
讨论gydF4y2Ba
之前的报告显示单一的B细胞筛选的高亲和性抗体可以用来隔离一周内尽快(从单一的B细胞隔离导致分子评价),这是极具吸引力的应用程序对传染病gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba。整个过程的病原反应步骤是引起抗体反应所需的时间。在这里,我们表明,强有力的中和抗体可以隔绝BALB / c小鼠6周后接种疫苗。我们的RBD-specific ELISA结果(图gydF4y2Ba2gydF4y2Ba)显示为单一的B细胞筛选重要机会十周后接种疫苗,虽然这并不是评估。我们进一步证明小鼠抗体基因可以直接克隆到哺乳动物表达质粒的表达和纯化嵌合抗体(鼠标变量和人类IgG1常数区域),具有强有力的中和活性。以前的工作展示了另一种方法,称为transcriptionally-active PCR (TAP),也可以用于提高吞吐量和加速时间gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba。这种开发方法允许表达式的铅抗体不需要subcloning表达式磁带,和可能对大规模的吸引力,单一的B细胞发现活动。gydF4y2Ba
值得注意的是,我们预计,所述抗体可能立即实用价值,包括诊断应用程序和工具研究转基因小鼠模型SARS-CoV-2(人类ACE2表达)gydF4y2Ba29日gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba,gydF4y2Ba31日gydF4y2Ba,gydF4y2Ba32gydF4y2Ba,gydF4y2Ba33gydF4y2Ba,gydF4y2Ba34gydF4y2Ba,gydF4y2Ba35gydF4y2Ba。而BALB / c小鼠的使用作为一个主机物种带来发展的固有局限性therapeutically-relevant抗体没有人性化,这里描述的方法很容易服从来自人体的抗体的筛查使用从人类获得的样本或人性化的小鼠。需要修改协议,包括替代检测抗体和PCR引物集,并详细的其他地方gydF4y2Ba10gydF4y2Ba,gydF4y2Ba12gydF4y2Ba。gydF4y2Ba
我们的工作与其他先前的研究gydF4y2Ba14gydF4y2Ba,gydF4y2Ba36gydF4y2Ba,gydF4y2Ba37gydF4y2Ba,gydF4y2Ba38gydF4y2Ba激励的继续探索隔离SARS-CoV-2抗体疫苗接种后,特别是从治疗人类样本应用程序。这项工作中产生抗体具有高亲和力(低点ECgydF4y2Ba50gydF4y2Ba二价格式)中的值,表明体内亲和力成熟后六个星期从最初一轮接种疫苗。相对于采购抗体从SARS-CoV-2感染对象,证据表明疫苗接种可能导致更好的免疫反应对抗体亲和力成熟通过体细胞hypermutation和长期记忆B细胞反应gydF4y2Ba36gydF4y2Ba,gydF4y2Ba39gydF4y2Ba,gydF4y2Ba40gydF4y2Ba,gydF4y2Ba41gydF4y2Ba。例如,脾脏和淋巴结组织分离gydF4y2Ba事后剖析gydF4y2Ba从被感染的人类缺乏生发中心,指示不完整的亲和力成熟和内存不足的反应gydF4y2Ba36gydF4y2Ba。这些和其他的研究gydF4y2Ba36gydF4y2Ba,gydF4y2Ba37gydF4y2Ba,gydF4y2Ba38gydF4y2Ba,gydF4y2Ba39gydF4y2Ba,gydF4y2Ba40gydF4y2Ba,gydF4y2Ba41gydF4y2Ba建议接种对象可能是一个孤立的丰富来源与高亲和力抗体和强有力的中和活动,和B细胞疫苗接种后取样的时间应该仔细考虑优化抗体分离过程。gydF4y2Ba
我们的调查可以从逻辑上延长了有力回应COVID-19和其他新兴传染病。单一B细胞排序策略使用是专门设计来降低假阳性导致识别的风险,从而调查关注细胞最有可能拥有的高亲和性抗体。这是通过使用一个double-positive选择策略,利用抗原分别贴上两个独特的荧光团(无花果。gydF4y2Ba3gydF4y2BaG),这种策略是依据以前的报告中发现肿瘤坏死因子受体抗体2点较低的亲和力gydF4y2Ba9gydF4y2Ba。在这以前的工作,流cytograms暗示某种程度的非特异性结合,说明清楚理由精制抗原选择策略gydF4y2Ba9gydF4y2Ba。有趣的是,在我们的工作中,非特异性抗原结合很低,这是说明了流cytograms免疫和控制小鼠脾脏样本(图。gydF4y2Ba3gydF4y2BaG H)和阳性细胞的罕见(RBD-PEgydF4y2Ba+gydF4y2Ba或RBD-APCgydF4y2Ba+gydF4y2Ba细胞)。总的来说,这一发现表明,非特异性抗原结合的程度可能取决于采用的特异性抗原。gydF4y2Ba
提供非特异性抗原绑定是最少关注的(至少在这项研究),单一的B细胞筛选可以使细胞的有效选择同时进行多个不同的抗原。例如,扩展我们的一般方法可能使快速生成有效的中和抗体具有广泛的中和活性。确切地说,该控制策略可以被修改以屏幕double-positive细胞结合rbd SARS-CoV-2和冠状。这项工作描述的抗体显示高度的亲和力SARS-CoV-2冠但缺乏亲和力(补充图。gydF4y2Ba6gydF4y2Ba),这表明12个h2和13 i1的抗原决定基SARS-CoV-2冠不是守恒的。而权衡之间的亲和力和中和活动可能使隔离广泛中和抗体,单一的B细胞排序可能负担得起简单的方法实现这一目标。在另一个相似的提议延长这项工作,单一的B细胞克隆也可能使筛查B细胞拥有double-positive绑定表型与野生型和高传染性SARS-CoV-2变体。这个建议是出于多个报告显示SARS-CoV-2突变体变体的出现可能逃离订婚SARS-CoV-2抗体gydF4y2Ba42gydF4y2Ba,gydF4y2Ba43gydF4y2Ba,gydF4y2Ba44gydF4y2Ba。令人鼓舞的是,13 i1观察保留绑定SARS-CoV-2 S1蛋白(B.1.1.7)英国的变体。然而,绑定活动很大程度上是废除对南非的S1蛋白变体(B.1.351),如补充图所示。gydF4y2Ba7gydF4y2Ba。这一发现与其他抗体和nanobodies报道是一致的gydF4y2Ba45gydF4y2Ba,gydF4y2Ba46gydF4y2Ba与类1和2类抗体RBD绑定,并可能提供有价值的见解告知未来一代的广泛中和性的抗体。gydF4y2Ba
精致的无法控制的抗原表示和浓度在FACS-based细胞筛选,单一的B细胞克隆也是很有吸引力的控制提供疫苗接种的阶段。未来的调查可能的单一B细胞筛选与优化小鼠接种疫苗抗原浓度和替代疫苗配方和优化。例如,RBD的相对较低的数量每注射(0.5µg /剂量)可能是导致低滴度在星期4。然而,我们观察到的健壮的sero-conversion在星期6。相比之下,其他SARS-CoV-2疫苗研究RBD的使用显著大量的蛋白质gydF4y2Ba47gydF4y2Ba,gydF4y2Ba48gydF4y2Ba,gydF4y2Ba49gydF4y2Ba。进一步通知疫苗设计的逻辑扩展这项工作可能是评价SARS-CoV-2抗原的影响(gydF4y2Ba例如,gydF4y2BaRBD, S1, S1三聚物)以及辅助制定产生的抗体反应。针对单一B细胞识别最有前途的候选人排序、血清样本可以分析通过抗原ELISA抗体反应和中和活动通过SARS-CoV-2 pseudovirus化验。此外,抗体同形像和子类也在未来的工作考虑的重要因素。抗体孤立在这个工作是IgG1s鉴于anti-mouse IgG1检测抗体被用于积极的选择在我们的控制策略。大多数的选择策略在以前的报告也关注IgG1抗体gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba。然而,进一步的研究可能对单一的B细胞筛选的方式向IgG1抗体不偏见的选择,尤其是在设置其他子类的调节或主导。gydF4y2Ba
未来的研究应该考虑并解决一些潜在缺陷关联着我们的学业。首先,纯系小鼠的使用(如在本研究)可能是次优的B细胞成熟相对于远系小鼠,小鼠近交与MHC II级减少多样性远系繁殖相比,老鼠gydF4y2Ba50gydF4y2Ba,gydF4y2Ba51gydF4y2Ba。然而,许多疫苗研究,包括SARS-CoV-2研究gydF4y2Ba52gydF4y2Ba,gydF4y2Ba53gydF4y2Ba,gydF4y2Ba54gydF4y2Ba,gydF4y2Ba55gydF4y2Ba使用纯系小鼠(例如,BALB / c小鼠)临床前概念验证数据翻译。第二,最后一个静脉注射抗原注射前3 - 4 d脾切除术(不用于本研究)同样应该考虑。当目标是产生杂种细胞,通常使用一个升压注入后达到合适的浓度gydF4y2Ba56gydF4y2Ba,gydF4y2Ba57gydF4y2Ba,涉及脾循环B细胞的迁移。然而,其他单一的B细胞抗体发现活动报告类似的给药方案,我们使用gydF4y2Ba9gydF4y2Ba。未来调查的进一步描述抗体的亲和力发现此处(例如,通过SPR)和评估这些抗体的中和活动现场SARS-CoV-2 CDC变异的病毒和pseudovirus担忧。未来努力优化免疫和B细胞筛选过程预计将继续推进与高亲和力和特异性抗体的生成,这是解决当前和未来的大流行的尤其重要。gydF4y2Ba
结论gydF4y2Ba
我们演示了使用单一的B细胞筛查发现的高亲和性的中和抗体SARS-CoV-2。这项工作突出的简单方法的快速发现抗体解决COVID-19等传染病。我们希望这里适用的方法可以方便地扩展到其他高度传染性SARS-CoV-2变异和新兴传染病。gydF4y2Ba
材料和方法gydF4y2Ba
生产重组RBDgydF4y2Ba
SARS-CoV-2 RBD产自HEK293T细胞克隆请提供的Florian克雷默教授(伊坎在西奈山医学院)和纯化报道gydF4y2Ba58gydF4y2Ba有轻微修改净化RBD的单体的形式用于这项研究。蛋白质进一步纯化Superdex 75列(Cytiva)与磷酸缓冲盐预平衡。gydF4y2Ba
体内接种疫苗的研究gydF4y2Ba
动物照顾后,联邦、州和地方的指导方针。密歇根大学安娜堡是一个AAALAC国际认证机构,和所有工作依法进行动物和批准的机构动物保健和使用委员会(IACUC)。所有动物实验进行了按照到达(体内实验动物研究:报告)的指导方针。雌性BALB / c小鼠每组(n = 5) 5 - 6周的年龄从杰克逊实验室购买。老鼠没有进一步使用随机化。老鼠每组(n = 5)给出了一个星期的适应和接种3次间隔2周。每剂含有0.5µg RBD和500µg明矾(Alhydrogel Invivogen)皮下注射尾巴基地。免疫血清收集在周4、6和10和分析RBD-specific免疫球蛋白和IgG1 ELISA抗体滴度。短暂,RBD蛋白质涂层在96 - ELISA板(0.1µg /),和连续稀释血清样本补充道。经过一个小时的孵化和多次水洗,辣根过氧化物酶(合)添加了标记二次抗体和孵化1 h在室温下。 Secondary antibodies used were rabbit anti-mouse IgG H&L-HRP (Abcam) and goat anti-mouse IgG1-HRP (Southern Biotech). TMB substrate solution was added, and the reaction was stopped by the addition of NaF. The absorbance was measured at a 620 nm wavelength using a plate reader (Synergy Neo, BioTek). To measure antibody titers, titration curves were evaluated based on the absorbance and the dilution factor, from which half maximal effective concentration (EC50gydF4y2Ba)值计算使用软件Gen5 (BioTek)。老鼠的子集用于脾收获在6周。gydF4y2Ba
B细胞隔离和染色gydF4y2Ba
隔离B细胞,刚切除小鼠脾脏与冰冷的流式细胞仪清洗缓冲(哈佛商学院没有钙或镁与1毫米EDTA, 25毫米消息灵通的,1%的边后卫)和处理通过70µm细胞过滤器。细胞被洗一次冰冷的流式细胞仪缓冲区,然后处理AKC裂解缓冲2分钟溶解红细胞。细胞与流式细胞仪又洗缓冲区,经过40µm细胞过滤器。Magnetic-activated细胞排序(mac)然后进行丰富基于CD45R表达式的B细胞。短暂,脾细胞培养用鼠标货代阻塞试剂(Miltenyi研究,130-092-575)后,制造商的协议。脾细胞被孵化用鼠标CD45R (B220)微(Miltenyi研究,130-049-501)和mac制造商的协议后执行使用LS列(Miltenyi研究,130-042-401)和Midi mac分离器(Miltenyi研究,130-042-302)。gydF4y2Ba
丰富细胞数和准备fluorescence-activated细胞排序(流式细胞仪)通过添加荧光标记抗体和抗原的混合物。标签抗体被添加在1:1000稀释1毫升/ 10的体积gydF4y2Ba7gydF4y2Ba在室温下细胞为30分钟。以下标签计划,列在“分子目标(荧光团)”的格式:CD19 (AF700) IgG1 (BV421), CD4 (FITC) CD8 (FITC) GR-1 (FITC) F4/80 (FITC), IgM (PE Cy7)。SARS-CoV-2 RBD-PE和RBD-APC每个添加1µg / 10gydF4y2Ba8gydF4y2Ba细胞。试验前,SARS-CoV-2 RBD(在生物系统,SPD-C52H3)标签使用闪电链接PE和APC标签工具(罗福斯生物制剂,705 - 0030和703 - 0030年)后,制造商的协议。细胞(5×10gydF4y2Ba5gydF4y2Ba)是留给每一个颜色补偿控制,和标记抗体和抗原RBD同样应用于1:1000稀释30分钟在室温下。标签抗体/抗原孵化后一步,细胞被洗两次冷流式细胞仪缓冲区。死细胞标记7-Aminoactinomycin D (7-AAD)(表达载体,A1310)添加细胞排序前10分钟。gydF4y2Ba
以下标签抗体被用于流式细胞仪准备:老鼠anti-mouse免疫球蛋白艳紫421(克隆A85-1;BD生物科学,562580),鼠anti-mouse IgM PE-Cy7 (PE / Cy7 anti-mouse IgM抗体克隆RMM1;生物的传说,406513),鼠anti-mouse IgD APC-Cy7 (APC / Cy7 anti-mouse IgD抗体克隆11-26c;BioLegend, 405715),鼠anti-mouse CD19 AF700 (Alexa萤石®700鼠anti-mouse CD19,克隆1 d3;BD生物科学,557958),鼠抗小鼠CD4 FITC (FITC老鼠Anti-Mouse CD4,克隆GK1.5;BD生物科学,557307),鼠抗小鼠CD8 FITC (FITC鼠标Anti-Rat CD8a,克隆OX-8;BD生物科学,561965),鼠抗小鼠GR1一起FITC (FITC鼠Anti-Mouse Ly-6G LY-6C,克隆RB6-8C5;BD生物科学,553126),鼠抗小鼠F4/80 FITC (FITC F4/80单克隆抗体BM8, eBioscience;热费舍尔,11-4801-82)。gydF4y2Ba
以下标签抗体被用于单一颜色补偿控制:鼠抗小鼠CD45-Brilliant紫421(克隆30-F11;BD生物科学,563890),鼠抗小鼠CD45-PE Cy7(克隆30-F11;BD生物科学,561868),鼠抗小鼠CD45-APC Cy7(克隆30-F11;BD生物科学,561037),鼠抗小鼠CD45-AF700(克隆30-F11;BD生物科学,560510),鼠抗小鼠CD45-FITC(克隆30-F11;BD生物科学,553080),鼠抗小鼠CD45-PE(克隆30-F11;BD生物科学,553081),鼠抗小鼠CD45-APC(克隆30-F11;BD生物科学,553092)。gydF4y2Ba
鼠标一B细胞排序gydF4y2Ba
抗原IgG1gydF4y2Ba+gydF4y2Ba记忆B细胞排序每到有缘的单细胞包含4µl 96 -孔板细胞溶菌作用的解决方案gydF4y2Ba20.gydF4y2Ba使用BD Moflo Astrios细胞分选仪。以下控制策略应用于系列:选择基于大小的淋巴细胞(向前散射区域)和粒度(侧散射区域),双重歧视向前向前散射宽度和散射面积,生存能力和缺乏non-B细胞标记(T细胞标记CD4, CD8 T细胞标记,中性粒细胞GR-1标志,巨噬细胞标记F4/80), B细胞标记CD19,为IgM阴性(天真的B细胞标记)和IgG1阳性,阴性IgD(天真的B细胞标记)和绑定SARS-CoV-2 RBD贴上PE和APC荧光蛋白质。gydF4y2Ba
互补脱氧核糖核酸的生成和pcrgydF4y2Ba
排序后单B细胞到一个96孔板包含4μL裂解缓冲在每个好,反转录是由添加7μL RT混合的我(表gydF4y2BaS2gydF4y2Ba)每个和孵化预热thermocycler (65°C) 5分钟gydF4y2Ba20.gydF4y2Ba。板被放置在冰5分钟和7μL RT混合的二世(表gydF4y2BaS2gydF4y2Ba)被添加到每个。盘子被孵化thermocycler和下运行下面的程序来产生互补脱氧核糖核酸(表gydF4y2BaS3gydF4y2Ba)。稀释cDNA、10μL nuclease-free水被添加到每个。首先,PCR扩增进行变量重型和轻型链在单独的PCR反应通过混合38μL PCR结合我(表gydF4y2BaS4gydF4y2Ba)与4μL互补。放大后thermocycler进行第一次PCR程序(表gydF4y2BaS4gydF4y2Ba)。第二个PCR扩增步骤是由混合38μL seq-PCR混合(表gydF4y2BaS5gydF4y2Ba)与4μL PCR产品从第一放大后thermocycler seq-PCR程序(表gydF4y2BaS5gydF4y2Ba)。Seq-PCR产品从每个被加载到一个琼脂糖凝胶2% (w / v)和运行在120 v 30分钟。预期的乐队(450 - 500个基点)纯化,对桑格和PCR产物测序使用适当的反向引物重型和轻型链。gydF4y2Ba
克隆和重组抗体的表达gydF4y2Ba
V抗体gydF4y2BaHgydF4y2Ba基因与EcoRI-HF消化(新英格兰生物学实验室,R3101L)和NheI-HF(新英格兰生物学实验室,R3131L),而VgydF4y2BalgydF4y2Ba基因消化和EcoRI-HF BsiWI-HF(新英格兰生物学实验室,R3553L)和纯化试剂盒,28104)。表达质粒(VgydF4y2BaHgydF4y2Ba或VgydF4y2BalgydF4y2Ba)和适当的限制酶消化后,制造商的协议,随后接受小牛肠碱性磷酸酶(新英格兰生物学实验室,M0525L)。分析了消化向量使用1%琼脂糖凝胶电泳。适当大小的DNA切除和净化。与T4酶消化插入和向量的结扎(新英格兰生物学实验室,M0202L)和通过热休克变成DH5α化学主管细胞。细胞被孵化的磅媒体(抗生素免费)1 h在37°C(摇晃在200 rpm),然后镀磅盘子补充与氨苄青霉素(100µg /毫升)一夜之间在37°C。单一的殖民地了,生长在磅媒体与氨苄青霉素一夜之间,miniprepped(试剂盒,27106),并通过Sanger测序测序。的质粒双变量域四价抗体类似克隆,表达和纯化。gydF4y2Ba
本研究中使用的抗体表达HEK293-6E细胞从加拿大国家研究委员会。抗体重型和轻型链质粒(7.5μg)与裴(45μg)在室温下混合F17媒体(没有补充)10 - 15分钟和增加细胞密度为1.5每毫升-200万个细胞。细胞媒体增强20% w / v yeastolate (BD科学,292804)24 - 48 h后转染。细胞生长为一个额外的5天在37°C F17媒体包含补充:谷氨酰胺(表达载体,25030081),Kolliphor(热费希尔科学、NC0917244)和G418(热费希尔科学,10131035)。细胞悬浊液离心3500×gydF4y2BaggydF4y2Ba40分钟。细胞上清液转移到新管,和0.5 1毫升干燥体积的蛋白质一个珠子(每个文化热费希尔科学,20333)补充说,紧随其后的是隔夜温和的摇摆在4°C。蛋白质一个珠子分开媒体使用真空过滤机列(热费希尔科学,89898)。珠子被用75 - 150毫升的PBS。抗体是从蛋白质筛选了珠子用甘氨酸缓冲(pH值3.0)0.1米和1米力图中和后最后的pH值为7.4。抗体然后使用0.2µm过滤器过滤,整除和存储在−80°C。在280纳米抗体吸光度测量和抗体大小评估了sds - page(热费希尔科学、WG1203BOX)。sds - page凝胶图像获得使用lightbox (Kaiser Slimlite普莱诺5000 K 8×11”)和相机(iPhone 11)。gydF4y2Ba
关联分析gydF4y2Ba
生物素化的RBD的关联性分析,0.3µg固定化在3×10gydF4y2Ba7gydF4y2Ba链霉亲和素Dynabeads PBSB (PBS 1 g / L BSA)在最后一卷1.2毫升。蛋白质和珠子是孵化在室温下2 - 3天,然后储存在4°C。绑定的研究中,珠被洗两次PBSB阻塞和10%的牛奶PBSB由立式圆筒形在室温下搅拌1小时之后,另一个与PBSB洗。10gydF4y2Ba5gydF4y2Ba珠子/孵化与不同浓度的抗体在1%牛奶PBSB在室温下2 - 3 h。孵化,珠被离心洗一次,其次是孵化与山羊反人类免疫球蛋白AF647(杰克逊ImmunoResearch, 109-605-098)在冰上4分钟。标签之后,珠子是洗一次冰冷的PBSB通过流式细胞术和评估。gydF4y2Ba
SARS-CoV-2 pseudovirus中和试验gydF4y2Ba
pseudovirus准备和SARS-CoV-2中和试验修改从先前的协议gydF4y2Ba22gydF4y2Ba。准备病毒颗粒,Lenti-X 293 t细胞(豆类,632180)被播种在6×10gydF4y2Ba5gydF4y2Ba每在6-well盘子RPMI媒体补充含10%胎牛血清(青霉素、链霉素的边后卫)和1% (P / S)。细胞培养在37°C公司为5%gydF4y2Ba2gydF4y2Ba直到达成目标confluency 50 - 70%。细胞然后使用lipofectamine 2000和第三代慢病毒转染质粒:HDM-Hgpm2质粒(贝nr - 52517)编码HIV gag pol CMV启动子(0.22µg)下,HDM-tat1b质粒(贝,nr - 52518)编码艾滋病毒乙CMV启动子(0.22µg)下,pRC-CMV-Rev1b质粒(贝nr - 52519)编码艾滋病毒(0.22µg)牧师,pHAGE-CMV-Luc2-IRES-ZsGreen-W(贝nr - 52516)慢病毒转移荧光素酶质粒编码co-expression和ZsGreen(1.00µg), pCMV3 SARS-CoV2年代未加标签的三角洲19 aa c项质粒编码SARS-CoV-2峰值(S)蛋白在糖基19-amino酸删除(0.34µg)。手机媒体交换与10%的边后卫和1%新鲜RPMI P / S在24 h post-transfection。然后,隔离并集中SARS-CoV-2 pseudovirus(没有ultracentriguation),收集细胞上清液,然后通过一个0.45在72 h post-transfectionµm过滤器。Lenti-X集中器(豆类,631232)添加到上层的体积比为1:3,一夜之间在4°C的环境。集中pseudovirus,混合物在1500×离心机gydF4y2BaggydF4y2Ba45分钟。上层清液了,病毒颗粒在一卷50µL resuspended Opti-MEM每口井的病毒的收获。gydF4y2Ba
确定数量的组织培养病毒,传染性单位(每毫升TCIU) 293 t-ace2细胞(贝,nr - 52511)被播种在每口井的10000个细胞在DMEM 96孔板与10%的边后卫和1% P / S,在37°C和5%的股份有限公司gydF4y2Ba2gydF4y2Ba。播种后24小时,细胞被感染各种病毒的稀释,稀释DMEM媒体的聚凝胺5µg /毫升、10%的边后卫,1% P / S。代表每口井的细胞数量也决定在24 h后播种。然后,ZsGreen-expressing细胞的百分比确定通过流式细胞术使用Bio-Rad ZE5细胞分析仪和进一步验证使用荧光显微镜在感染后48 h。gydF4y2Ba
pseudovirus中和化验,293 t-ace2细胞被播种在10000细胞/在白色底96 -孔板(康宁,3917)在DMEM(10%的边后卫和1% P / S)和培养在37°C和5%的公司gydF4y2Ba2gydF4y2Ba。在293年24 h种子期后,t-ace2细胞治疗最后5µg /毫升聚凝胺的浓度,和混合物包含350 TCIU SARS-CoV-2 pseudovirus每口井和抗体治疗(连续稀释四倍)。抗体的混合物和SARS-CoV-2 pseudovirus一起孵化1 h在37°C之前,除了293 t-ace2细胞。接下来,中和活动决心通过生物荧光检测使用一个微型板块读者在感染后48 h。这个过程,荧光素酶底物(Promega ONE-Glo, E6110)使用后,制造商的协议。具体来说,96 -孔板平衡至室温10分钟和媒体在每个减少到100µL体积。荧光素酶底物制备并添加(100µL /)。盘子被孵化在室温下10分钟,和生物荧光测量(500集成/小姐)使用分子设备SpectraMax微型板块读者。gydF4y2Ba
特异性分析gydF4y2Ba
评估抗体的亲和力,他贴上RBD的冠和SARS-CoV-2病毒分别固定在微(热费希尔,10103 d)。96孔板包含RBD-coated珠子与13 i1抗体或孵化vhh - 72 nanobodies /一系列浓度(3点到12.5海里)在室温下在PBSB 2 h。初级孵化后,珠子都用冰冷的PBSB孵化和山羊反Fc房颤488(杰克逊ImmunoResearch 109-545-008) 4分钟在冰上。二次孵化后,珠与冰冷的PBSB洗两次,流式细胞术分析。同样,13 i1涂布珠子评估绑定WT SARS-CoV-2 S1蛋白以及S1蛋白变体的担忧(B.1.1.7和B.1.351)使用商业化抗原(开头生物系统;SPD-C52H3、SPD-C52Hn SPD-C52Hp)。简要13 i1-coated微被封锁在PBSB 10%牛奶1 h,用PBSB洗净,孵化SARS-CoV-2 S1蛋白在96孔板格式3 h 25°C和225 rpm。盘子洗了PBSB,孵化与他抗体(表达载体,pa - 9531)对冰,30分钟洗PBSB,孵化与检测抗体(杰克逊ImmunoResearch 703-606-155) 4分钟在冰上,用PBSB洗净,通过流式细胞术分析。gydF4y2Ba
竞争结合分析gydF4y2Ba
评估13 i1的抗原决定基竞争结合分析ACE2受体和其他出版SARS-CoV-2抗体。生物素化的RBD (5 nM)第一次被孵化与可溶性抗体或ACE2在一系列浓度(0.05,0.5,5、50和500海里)在室温下2 h。接下来,antibody-RBD复合物与13 i1-coated孵化微PBSB 1%牛奶在室温下对3 h。孵化后,珠子是用冷洗净PBSB其次是孵化与链霉亲和素AF647(1:1000) 4分钟在冰上。二次孵化后,珠与冷PBSB洗两次,流式细胞术分析。gydF4y2Ba
熔化温度分析gydF4y2Ba
使用差示扫描荧光抗体融化的温度测量。短暂,抗体是准备在0.12毫克/毫升PBS和结合蛋白染料热转移(应用生物系统公司,4461146)的体积比7:1抗体:染料。背景样本由1×PBS染料混合在同一比例。平均2 - 3 PBS-dye混合物被用来计算背景信号。antibody-dye和PBS-dye混合物添加到清晰的384孔板。盘子被提交给密歇根大学先进的基因组学核心进行分析。384孔板在1000 - 2000转离心1分钟和7900插入ABI棱镜ht序列检测系统(应用生物系统公司)。热循环条件下分析了增加温度25到98°C / 45分钟。背景信号中减去从样本信号分析。熔化温度的测定温度的最大信号观察(一阶导数等于零)。DVD的构造,第一个局部极大值用于确定观察两种转换时的熔化温度。gydF4y2Ba
分析凝胶排阻层析法gydF4y2Ba
抗体纯度在蛋白质纯化与岛津制作所使用凝胶排阻层析法分析了突出高效液相色谱系统配备一个LC-20AT泵,SIL-20AC autosampler和FRC-10A馏分收集器。抗体在20毫米醋酸(pH值5)缓冲交换到PBS (pH值7.4)。分析秒100µL样本(稀释到0.1毫克/毫升)加载到列(Superdex增加200 10/300 GL列;通用电气、28990944)和评估0.75毫升/分钟的流量使用PBS运行缓冲与200毫米补充精氨酸(pH值7.4)。吸光度在280 nm信号监测和用于分析。蛋白质单体的比例是评估通过分析峰下的面积之间的排斥体积和溶剂洗脱*(8 - 22分钟)。gydF4y2Ba
Polyspecificity分析gydF4y2Ba
Polyspecificity试剂(PSR)准备如前所报道gydF4y2Ba27gydF4y2Ba。简单地说,CHO细胞(10gydF4y2Ba9gydF4y2Ba、Gibco A29133)颗粒状,与PBSB洗,洗再次与缓冲B(50毫米消息灵通的,0.15 M氯化钠,CaCl 2毫米gydF4y2Ba2gydF4y2Ba5毫米氯化钾5毫米MgClgydF4y2Ba2gydF4y2Ba,10%的甘油,pH值7.2),然后用子弹射击。细胞颗粒在5毫升resuspended B的缓冲区补充蛋白酶抑制剂(西格玛奥德里奇,4693159001)。90年代的细胞均质(三个30年代周期),然后用90年代(三个30年代周期)。当时细胞悬液离心40000×gydF4y2BaggydF4y2Ba1 h。当时上层的删除和丢弃。gydF4y2Ba
丸(浓缩细胞膜分数)是悬浮在缓冲B Dounce均质器30中风。蛋白质浓度测定用洗涤剂兼容的蛋白质分析工具包(BioRad, 5000116)。浓缩膜分数是1毫克/毫升的浓度稀释溶解缓冲区(pH值7.2)包含50 mM玫瑰,CaCl 0.15 M氯化钠,2毫米gydF4y2Ba2gydF4y2Ba5毫米氯化钾5毫米MgClgydF4y2Ba2gydF4y2Ba,1% n-dodecyl-b -gydF4y2BadgydF4y2Ba-maltopyranoside(西格玛奥德里奇,D4641)和蛋白酶抑制剂(西格玛奥德里奇,11873580001)。然后,解决方案是混合在一夜之间通过立式圆筒形混合在4°C。溶解膜蛋白分数然后离心机在40000 xg 1 h和上层的收集。最后的上层清液的浓度测定,稀释到1.0毫克/毫升。gydF4y2Ba
Sulfo-NHS-LC-biotin(热费希尔科学、PI21335)溶解在蒸馏水~ 11.5毫克/毫升。股票解Sulfo-NHS-LC-biotin(150毫升)和PSR试剂在1.0毫克/毫升(4.5毫升)在室温下混合立式圆筒形45分钟。淬火反应,10毫升1.5羟胺在pH值7.2是补充道。生物素化的PSR整除,然后储存在−80°C。gydF4y2Ba
蛋白涂层磁珠(表达载体,88846)与PBSB洗了三次,然后孵化与抗体或nanobodies在不同浓度从0.03×10×饱和珠与免疫球蛋白的结合能力在96 -孔板(VWR, 650261)在一夜之间在4°C。抗体和nanobody浓度是由相同物质的量浓度保持Fc规范化整个样品浓度。IgG-coated珠子与PBSB洗两次,centriguation 2500×gydF4y2BaggydF4y2Ba4分钟之间的清洗步骤。接下来,珠子暂停10×稀释溶液的生物素化的PSR和孵化20分钟在冰上。这个孵化后,珠与PBSB洗一次,然后孵化1000×稀释的链霉亲和素af - 647(表达载体,S32357)和1000×稀释的山羊反Fc (F (ab)gydF4y2Ba2gydF4y2Ba]af - 488(表达载体,H10120) 4分钟在冰上。珠子是洗一次,resuspended PBSB,通过流式细胞术和评估。高和低非特异性抗体绑定控制本试验中使用的变量地区emibetuzumab和elotuzumab移植到一个共同的IgG1框架,分别。控制抗体两步纯化,蛋白A和秒。结果从所有复制标准化在0和1之间基于控制抗体。gydF4y2Ba
数据可用性gydF4y2Ba
所有生成的数据或分析在本研究中包括发表的这篇文章(及其补充信息文件)。gydF4y2Ba
引用gydF4y2Ba
埃尼迪斯,j . p . a . COVID-19流行病学的一个完整的大流行的全球视角。gydF4y2Ba欧元。j .中国。投资。gydF4y2Ba50gydF4y2Ba,1 - 10 (2020)。gydF4y2Ba
王,J。,Peng, Y., Xu, H., Cui, Z. & Williams, R. O. The COVID-19 vaccine race: Challenges and opportunities in vaccine formulation.aap PharmSciTechgydF4y2Ba21gydF4y2Ba225 (2020)。gydF4y2Ba
Mahase大肠Covid-19: FDA授权中和抗体bamlanivimab non-admitted患者。gydF4y2BaBMJgydF4y2Ba371年gydF4y2Ba4362 (2020)。gydF4y2Ba
当然喽,n . & Weissman d开发疫苗和抗病毒药物防治病毒性传染病。gydF4y2BaNat,生物医学。Eng。gydF4y2Ba4gydF4y2Ba,1128 - 1133 (2020)。gydF4y2Ba
Marovich, M。,Mascola, J. R. & Cohen, M. S. Monoclonal antibodies for prevention and treatment of COVID-19.《美国医学会杂志》gydF4y2Ba324年gydF4y2Ba131 (2020)。gydF4y2Ba
DeFrancesco, l . COVID-19抗体受审。gydF4y2Ba生物科技Nat。》。gydF4y2Ba38gydF4y2Ba,1242 - 1252 (2020)。gydF4y2Ba
TsikalaVafea, M。gydF4y2Baet al。gydF4y2Ba新兴技术在这项研究中,使用COVID-19患者的诊断和治疗。gydF4y2Ba细胞。摩尔。Bioeng。gydF4y2Ba13gydF4y2Ba,249 - 257 (2020)。gydF4y2Ba
Clargo, a . M。gydF4y2Baet al。gydF4y2Ba的快速生成重组从个人功能性单克隆抗体,抗原来源于浆细胞的骨孤立的使用一种新型的荧光技术方法。gydF4y2Ba米gydF4y2Ba腹肌gydF4y2Ba6gydF4y2Ba,143 - 159 (2014)。gydF4y2Ba
斯塔基,d . O。,Compson, J. E., Rapecki, S. & Lightwood, D. J. Generation of recombinant monoclonal antibodies from immunised mice and rabbits via flow cytometry and sorting of antigen-specific IgG+ memory B cells.《公共科学图书馆•综合》gydF4y2Ba11gydF4y2Bae0152282 (2016)。gydF4y2Ba
何,即Y。gydF4y2Baet al。gydF4y2Ba完善协议生成从单一的人类和小鼠B细胞单克隆抗体。gydF4y2Baj . Immunol。方法gydF4y2Ba438年gydF4y2Ba,67 - 70 (2016)。gydF4y2Ba
舵柄,T。,Busse, C. E. & Wardemann, H. Cloning and expression of murine Ig genes from single B cells.j . Immunol。方法gydF4y2Ba350年gydF4y2Ba,183 - 193 (2009)。gydF4y2Ba
舵柄,T。gydF4y2Baet al。gydF4y2Ba高效代单克隆抗体从单一的人类B细胞单细胞rt - pcr克隆和表达载体。gydF4y2Baj . Immunol。方法gydF4y2Ba329年gydF4y2Ba,112 - 124 (2008)。gydF4y2Ba
Ojima-Kato, T。gydF4y2Baet al。gydF4y2Ba从单一的B细胞单克隆抗体的快速生成ecobody技术。gydF4y2Ba抗体gydF4y2Ba7gydF4y2Ba38岁(2018)。gydF4y2Ba
鲍尔,G的潜在意义高活动性免疫球蛋白G(免疫球蛋白)对SARS-CoV-2保护性免疫。gydF4y2BaInt。j .感染。说。gydF4y2Ba106年gydF4y2Ba,61 - 64 (2021)。gydF4y2Ba
Khatri,我。,Staal, F. J. T. & van Dongen, J. J. M. Blocking of the high-affinity interaction-synapse between SARS-CoV-2 spike and human ACE2 proteins likely requires multiple high-affinity antibodies: An immune perspective.前面。Immunol。gydF4y2Ba11gydF4y2Ba2258 (2020)。gydF4y2Ba
局域网,J。gydF4y2Baet al。gydF4y2Ba结构的受体结合域绑定到ACE2受体SARS-CoV-2飙升。gydF4y2Ba自然gydF4y2Ba581年gydF4y2Ba,215 - 220 (2020)。gydF4y2Ba
黄、z和柴,j . COVID-19细胞的门开了,主要治疗方法。gydF4y2Ba钙信号。目标。其他。gydF4y2Ba5gydF4y2Ba104 (2020)。gydF4y2Ba
Wrapp D。gydF4y2Baet al。gydF4y2Ba低温电子显微镜的结构2019 - ncov激增十二构象。gydF4y2Ba科学gydF4y2Ba367年gydF4y2Ba,1260 - 1263 (2020)。gydF4y2Ba
Sanmamed, m F。gydF4y2Baet al。gydF4y2Ba受体激动剂的co-stimulation癌症免疫疗法针对CD137 OX40、GITR, CD27, CD28、国际安全和发展理事会。gydF4y2BaSemin。肿瘤防治杂志。gydF4y2Ba42gydF4y2Ba,640 - 655 (2015)。gydF4y2Ba
冯》,L。gydF4y2Baet al。gydF4y2Ba测序和克隆老鼠记忆B细胞的抗原抗体。gydF4y2BaProtoc Nat。gydF4y2Ba11gydF4y2Ba,1908 - 1923 (2016)。gydF4y2Ba
施,R。gydF4y2Baet al。gydF4y2Ba人类的中和抗体SARS-CoV-2的目标受体结合部位。gydF4y2Ba自然gydF4y2Ba584年gydF4y2Ba,120 - 124 (2020)。gydF4y2Ba
克劳福德,k . h . D。gydF4y2Baet al。gydF4y2Ba协议和试剂与SARS-CoV-2 pseudotyping慢病毒颗粒突起蛋白中和化验。gydF4y2Ba病毒gydF4y2Ba12gydF4y2Ba13 - 15 (2020)。gydF4y2Ba
Wrapp D。gydF4y2Baet al。gydF4y2Ba由单极结构基础的有力中和betacoronaviruses骆驼科抗体。gydF4y2Ba细胞gydF4y2Ba181年gydF4y2Ba,1004 - 1015。e15 (2020)。gydF4y2Ba
元,M。gydF4y2Baet al。gydF4y2Ba一个高度保守的神秘的抗原决定基的受体结合域SARS-CoV-2和冠状。gydF4y2Ba科学gydF4y2Ba368年gydF4y2Ba,630 - 633 (2020)。gydF4y2Ba
田,X。gydF4y2Baet al。gydF4y2Ba强有力的绑定2019小说由SARS冠状病毒突起蛋白coronavirus-specific人类单克隆抗体。gydF4y2Ba紧急情况。微生物感染。gydF4y2Ba9gydF4y2Ba,382 - 385 (2020)。gydF4y2Ba
巴恩斯,c . O。gydF4y2Baet al。gydF4y2BaSARS-CoV-2中和抗体结构通知治疗策略。gydF4y2Ba自然gydF4y2Ba588年gydF4y2Ba,682 - 687 (2020)。gydF4y2Ba
徐,Y。gydF4y2Baet al。gydF4y2Ba解决polyspecificity抗体选择从一个体外酵母表达系统:FACS-based,高通量筛选和分析工具。gydF4y2Ba蛋白质中。Des,选取。gydF4y2Ba26gydF4y2Ba,663 - 670 (2013)。gydF4y2Ba
Jain, T。gydF4y2Baet al。gydF4y2Ba生物物理属性的临床分期抗体景观。gydF4y2BaProc。国家的。学会科学。美国gydF4y2Ba114年gydF4y2Ba,944 - 949 (2017)。gydF4y2Ba
汉族,K。gydF4y2Baet al。gydF4y2Ba肺表达人类血管紧张素转换酶2的糖分会让鼠标SARS-CoV-2感染。gydF4y2Ba点。j .和。细胞摩尔。生物。gydF4y2Ba64年gydF4y2Ba,79 - 88 (2021)。gydF4y2Ba
太阳,工程学系。gydF4y2Baet al。gydF4y2Ba一只老鼠SARS-CoV-2感染和发病机理的模型。gydF4y2Ba细胞宿主细菌gydF4y2Ba28gydF4y2Ba,124 - 133。e4 (2020)。gydF4y2Ba
温克勒,大肠。gydF4y2Baet al。gydF4y2BaSARS-CoV-2人类ACE2-transgenic老鼠引起严重肺感染发炎和受损的功能。gydF4y2BaImmunol Nat。gydF4y2Ba21gydF4y2Ba,1327 - 1335 (2020)。gydF4y2Ba
Rattanapisit, K。gydF4y2Baet al。gydF4y2Ba快速的生产SARS-CoV-2受体结合域(RBD)和峰值特定单克隆抗体在烟草CR3022 benthamiana。gydF4y2Ba科学。代表。gydF4y2Ba10gydF4y2Ba17698 (2020)。gydF4y2Ba
Shanmugaraj B。,Malla, A. & Phoolcharoen, W. Emergence of novel coronavirus 2019-nCoV: need for rapid vaccine and biologics development.病原体gydF4y2Ba9gydF4y2Ba,1 - 10 (2020)。gydF4y2Ba
西迪基,m z单克隆抗体诊断;一个评估。gydF4y2Ba印度j .制药。科学。gydF4y2Ba72年gydF4y2Ba12 - 17 (2010)。gydF4y2Ba
Irmen k·e·凯莱赫& j·j·使用单克隆抗体在社区医院呼吸道病毒的快速诊断。gydF4y2Ba中国。成岩作用。实验室。Immunol。gydF4y2Ba7gydF4y2Ba,396 - 403 (2000)。gydF4y2Ba
金子,N。gydF4y2Baet al。gydF4y2Ba失去Bcl-6-expressing T卵泡COVID-19辅助细胞和生发中心。gydF4y2Ba细胞gydF4y2Ba183年gydF4y2Ba,143 - 157。e13 (2020)。gydF4y2Ba
王,Z。gydF4y2Baet al。gydF4y2Ba信使核糖核酸疫苗诱导抗体SARS-CoV-2和循环变体。gydF4y2Ba自然gydF4y2Ba592年gydF4y2Ba,616 - 622 (2021)。gydF4y2Ba
Muik,。gydF4y2Baet al。gydF4y2Ba中和的SARS-CoV-2血统B.1.1.7 pseudovirus由BNT162b2疫苗诱导人类血清。gydF4y2Ba科学gydF4y2Ba371年gydF4y2Ba,1152 - 1153 (2021)。gydF4y2Ba
莱德尔,K。gydF4y2Baet al。gydF4y2BaSARS-CoV-2 mRNA疫苗培养强大的抗原生发中心反应与中和抗体生成有关。gydF4y2Ba免疫力gydF4y2Ba53gydF4y2Ba,1281 - 1295。e5 (2020)。gydF4y2Ba
伯顿,d . r . & Topol e . j .向超人SARS-CoV-2免疫力?。gydF4y2BaNat,地中海。gydF4y2Ba27gydF4y2Ba5 - 6 (2021)。gydF4y2Ba
金,d S。,Rowland-Jones, S. & Gea-Mallorquí, E. Will SARS-CoV-2 infection elicit long-lasting protective or sterilising immunity? implications for vaccine strategies (2020).前面。Immunol。gydF4y2Ba11gydF4y2Ba571481 (2020)。gydF4y2Ba
德梅伦,J。gydF4y2Baet al。gydF4y2Ba人类对SARS冠状病毒单克隆抗体组合:协同和逃避突变体的报道。gydF4y2Ba科学硕士。gydF4y2Ba3gydF4y2Bae237 (2006)。gydF4y2Ba
Weisblum Y。gydF4y2Baet al。gydF4y2Ba逃离SARS-CoV-2突起蛋白变体的中和抗体。gydF4y2Ba埃尔gydF4y2Ba机上娱乐系统gydF4y2Ba9gydF4y2Ba61312 (2020)。gydF4y2Ba
Baum,。gydF4y2Baet al。gydF4y2Ba抗体鸡尾酒防止SARS-CoV-2突起蛋白快速突变逃避与单个抗体。gydF4y2Ba科学gydF4y2Ba369年gydF4y2Ba,1014 - 1018 (2020)。gydF4y2Ba
Zupancic, j . M。gydF4y2Baet al。gydF4y2Ba设计多价nanobodies强有力地和广泛中和SARS-CoV-2变体。gydF4y2Ba放置其他。gydF4y2Ba4gydF4y2Ba,2100099 (2021)。gydF4y2Ba
Zupancic, j . M。gydF4y2Baet al。gydF4y2Ba定向演化的有效中和nanobodies SARS-CoV-2使用CDR-swapping诱变。gydF4y2Ba细胞化学。医学杂志。gydF4y2Ba28gydF4y2Ba,1379 - 1388 (2021)。gydF4y2Ba
刘,Z。gydF4y2Baet al。gydF4y2BaRBD-Fc-based COVID-19候选疫苗引发高度有力SARS-CoV-2中和抗体反应。gydF4y2Ba钙信号。目标。其他。gydF4y2Ba5gydF4y2Ba282 (2020)。gydF4y2Ba
棕褐色,H.-X。gydF4y2Baet al。gydF4y2Ba启动—提高免疫原性的蛋白质亚单位疫苗策略对SARS-CoV-2老鼠和猕猴。gydF4y2BaCommun Nat。gydF4y2Ba12gydF4y2Ba1403 (2021)。gydF4y2Ba
杨,J。gydF4y2Baet al。gydF4y2BaS蛋白的疫苗针对RBD SARS-CoV-2诱发保护性免疫。gydF4y2Ba自然gydF4y2Ba586年gydF4y2Ba,572 - 577 (2020)。gydF4y2Ba
查尔斯Janeway, J。特拉弗斯,P。,Walport, M. & Shlomchik, M. J. The major histocompatibility complex and its functions. (2001).
埃里森,一个。gydF4y2Baet al。gydF4y2Ba维护功能主要组织相容性复合体多样性在近亲繁殖:自交的脊椎动物。gydF4y2BaProc。r . Soc。B杂志。科学。gydF4y2Ba279年gydF4y2Ba,5004 - 5013 (2012)。gydF4y2Ba
van Doremalen, N。gydF4y2Baet al。gydF4y2BaChAdOx1 nCoV-19疫苗防止SARS-CoV-2肺炎在恒河猴。gydF4y2Ba自然gydF4y2Ba586年gydF4y2Ba,578 - 582 (2020)。gydF4y2Ba
张,n。gydF4y2Baet al。gydF4y2Ba耐热性的mRNA COVID-19疫苗。gydF4y2Ba细胞gydF4y2Ba182年gydF4y2Ba,1271 - 1283。e16天(2020)。gydF4y2Ba
高,Q。gydF4y2Baet al。gydF4y2Ba灭活疫苗SARS-CoV-2候选人的发展。gydF4y2Ba科学gydF4y2Ba369年gydF4y2Ba,77 - 81 (2020)。gydF4y2Ba
Bos, R。gydF4y2Baet al。gydF4y2BaAd26基于矢量COVID-19疫苗编码prefusion-stabilized SARS-CoV-2飙升免疫原诱导的体液和细胞免疫反应。gydF4y2BaNPJ疫苗gydF4y2Ba5gydF4y2Ba91 (2020)。gydF4y2Ba
Spanier, j . A。gydF4y2Baet al。gydF4y2Ba有效的代单克隆抗体肽MHCII的上下文中使用磁富集。gydF4y2BaCommun Nat。gydF4y2Ba7gydF4y2Ba11804 (2016)。gydF4y2Ba
单克隆抗体:r . C . C(美国)gydF4y2Ba。m·p·代杂种细胞:永久细胞系分泌单克隆抗体gydF4y2Ba。(1999)。gydF4y2Ba
Stadlbauer D。gydF4y2Baet al。gydF4y2BaSARS-CoV-2人类血清转化:详细协议血清学试验,抗原的生产和测试设置。gydF4y2Ba咕咕叫。Protoc。Microbiol。gydF4y2Ba57gydF4y2Ba,1 - 10 (2020)。gydF4y2Ba
确认gydF4y2Ba
我们感谢亚当·罗兰提供试剂和建议有关pseudovirus中和试验。我们要感谢密歇根大学结构生物学中心与梅兰妮Ohi合作的实验室提供免疫接种的试剂。我们感谢迈克尔•Pihalja马克Savary,密歇根大学的流式细胞仪的核心成员提供建议和技术支持。我们感谢Tessier实验室成员的有益建议。这项工作是由美国国立卫生研究院(RF1AG059723 R35GM136300 P.M.T.,F32 GM137513 J.S.S.,和R01 AI 51588 01 to M.C.), National Science Foundation [CBET 1159943, 1605266 and 1813963 to P.M.T., Graduate Research Fellowship to M.D.S.], Biointerfaces Institute (to P.M.T.), the Albert M. Mattocks Chair (to P.M.T), MICHR Education PTSP 2020 (U069943 to M.G.M.B), COVID-19: CVC Impact Research Ignitor Grant Award (to M.C.), University of Michigan MICHR Accelerating Synergy Award (to M.C.), and University of Michigan Institutional Funds (to T.M.L). The protocol for producing recombinant SARS-CoV-2 spike RBD was developed in the University of Michigan Center for Structural Biology with support from the Open Philanthropy Project Fund.
作者信息gydF4y2Ba
作者和联系gydF4y2Ba
贡献gydF4y2Ba
J.S.S.,他的,一个。一个。D。,K.S.P.,J.J.M.,和P.M.T. designed the research. K.S.P. and J.M.M. designed and conducted immunizations. J.S.S designed and conducted cell sorting. G.P. designed and conducted antibody gene isolation. J.S.S., G.P., A.A.D., E.M.K., J.M.Z., and H.C. produced and/or performed the characterization of antibodies. T.M.L, M.C., and M.G.M.B. planned and constructed reagents for the pseudovirus assay. J.S.S., G.P., M.D.S., and P.M.T. analyzed the data. J.S.S, G.P., and P.M.T. wrote the paper with input from the co-authors.
相应的作者gydF4y2Ba
道德声明gydF4y2Ba
相互竞争的利益gydF4y2Ba
作者宣称没有利益冲突。gydF4y2Ba
额外的信息gydF4y2Ba
出版商的注意gydF4y2Ba
施普林格自然保持中立在发表关于司法主权地图和所属机构。gydF4y2Ba
补充信息gydF4y2Ba
权利和权限gydF4y2Ba
开放获取gydF4y2Ba本文是基于知识共享署名4.0国际许可,允许使用、共享、适应、分布和繁殖在任何媒介或格式,只要你给予适当的信贷原始作者(年代)和来源,提供一个链接到创作共用许可证,并指出如果变化。本文中的图片或其他第三方材料都包含在本文的创作共用许可证,除非另有说明在一个信用额度的材料。如果材料不包括在本文的创作共用许可证和用途是不允许按法定规定或超过允许的使用,您将需要获得直接从版权所有者的许可。查看本许可证的副本,访问gydF4y2Bahttp://creativecommons.org/licenses/by/4.0/gydF4y2Ba。gydF4y2Ba
关于这篇文章gydF4y2Ba
引用这篇文章gydF4y2Ba
专家赞成,j.s,Pornnoppadol, G., Desai, A.A.et al。gydF4y2Ba发现和描述的高亲和性,强有力的SARS-CoV-2中和抗体通过单一的B细胞筛选。gydF4y2BaSci代表gydF4y2Ba11gydF4y2Ba20738 (2021)。https://doi.org/10.1038/s41598 - 021 - 99401 - xgydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/s41598 - 021 - 99401 - xgydF4y2Ba
本文引用的gydF4y2Ba
格林-巴利综合征Ad26.COV2后和重型脑脊髓炎。疫苗接种:双重危险gydF4y2Ba
神经系统研究与实践gydF4y2Ba(2022)gydF4y2Ba
发展功能相关效力化验单价和多价疫苗由发展技术gydF4y2Ba
npj疫苗gydF4y2Ba(2022)gydF4y2Ba
评论gydF4y2Ba
通过提交评论你同意遵守我们的gydF4y2Ba条款gydF4y2Ba和gydF4y2Ba社区指导原则gydF4y2Ba。如果你发现一些滥用或不符合我们的条件或准则请国旗是不合适的。gydF4y2Ba