摘要
SARS-CoV-2(严重急性呼吸综合征冠状病毒2)是引起呼吸道大流行COVID-19(冠状病毒病2019)的冠状病毒毒株。为了了解SARS-CoV-2在人类中的病理生物学,有必要揭示感染发生后个体产生的代谢变化。这项工作的目的是提供关于SARS-CoV-2感染导致不同临床情况下患者生物分子谱改变以及生物途径改变的新信息。这是通过代谢组学方法完成的,使用HPLC-QTOF-MS分析来自145名成年患者的covid诊断血浆样本,根据其随后的临床结果分为不同的临床阶段(25名阴性对照(非covid);无症状且无需住院治疗的阳性患者28例;总住院时间小于10天的轻症阳性患者27例;36例阳性的重症患者,住院总时间超过20天和/或在ICU住院;阳性患者29例(死亡或死亡)。对预后较轻的住院患者出院后2 ~ 3个月进行随访。这项工作的最终目标是提供生物标志物,以帮助更好地了解COVID-19疾病的演变过程,并根据感染早期获得的血浆代谢物谱预测患者的进展情况。 In the present work, several metabolites were found as potential biomarkers to distinguish between the end-stage and the early-stage (or non-COVID) disease groups. These metabolites are mainly involved in the metabolism of carnitines, ketone bodies, fatty acids, lysophosphatidylcholines/phosphatidylcholines, tryptophan, bile acids and purines, but also omeprazole. In addition, the levels of several of these metabolites decreased to “normal” values at hospital discharge, suggesting some of them as early prognosis biomarkers in COVID-19 at diagnose.
介绍
SARS-COV-2(严重急性呼吸综合征冠状病毒2)具有极强的传染性,已引发全球大流行。这种冠状病毒感染肺部和人类呼吸道会导致发烧、肌痛和咳嗽,一些患者还会出现急性呼吸窘迫综合征(ARDS)。虽然大多数患者会出现非常轻至中度的症状,但约五分之一的患者会出现肺炎并伴有严重呼吸窘迫。这些患者需要在医院重症监护病房(ICU)接受治疗,那里的感染可导致多器官功能障碍、衰竭,有时甚至死亡。COVID-19(2019冠状病毒病)大流行导致对该疾病、其病原体及其与人类宿主的相互作用进行了紧急和密集的调查。然而,由于冠状病毒感染反映了广泛的患者症状,因此在疾病过程中多种病理生理途径受到干扰,因此准确的SARS-CoV-2患者风险分类仍然存在许多困难,这是COVID-19复杂性的结果。鉴于循环代谢组提供了生物体生理状态的快照,这种复杂性促使许多小组利用代谢组学来研究这个令人兴奋的话题1,2。
尽管核磁共振(NMR)已经在一些代谢组学研究中得到应用3.基于质谱(MS)的代谢组学已成为寻找COVID-19疾病潜在诊断生物标志物候选物的首选技术。虽然这些工作中有许多是使用质谱耦合液相色谱(LC)完成的,但使用气相色谱耦合质谱也显示出关于疾病演变的有趣结果4。利用代谢组学研究了关于COVID-19疾病的许多主题,例如,代谢组学显示了COVID-19非重症患者在康复过程中的性别特异性代谢变化,表明男性的主要血浆代谢变化是脂肪酸,女性的主要血浆代谢变化是甘油磷胆碱和碳水化合物5。代谢组学还表明,有可能区分肺功能异常的COVID-19幸存者与健康供体或肺功能正常的受试者的血浆代谢物谱。这些改变主要涉及氨基酸和甘油磷脂代谢途径,甘油三酯(TG)、磷脂酰胆碱(PC)、前列腺素E2、精氨酸水平升高,甜菜素和腺苷水平降低6。由于许多关于免疫反应的问题,包括先天和适应性,仍然不清楚,它们受到正在进行的多组学研究的影响1以及对COVID-19全球代谢组学数据集的综合荟萃分析2。代谢组学还显示,COVID-19患者血清中甘油磷脂、鞘脂和脂肪酸(FA)等100多种脂质下调,可能是由于肝脏受损,这也反映在胆红素和胆汁酸的异常上7。在嘌呤、谷氨酰胺、白三烯D4 (LTD4)和谷胱甘肽代谢方面,COVID-19患者与健康对照组之间也存在显著差异。R - S乳谷胱甘肽和谷氨酰胺水平降低,次黄嘌呤、肌苷和LTD4水平升高8)。
如上所述,通过使用在COVID-19疾病开始时确定的临床严重程度的潜在代谢标志物对SARS-COV-2患者进行充分分类仍然存在许多困难,这就是为什么许多不同的工作都解决了这一具有挑战性的主题。因此,使用高通量组学,研究了非/严重到严重疾病队列代谢组(和蛋白质组)谱的动态变化,并可用于预测疾病发展:例如,在健康到轻度到致命组中苹果酸和甘油3-磷酸水平同时下降9。另一方面,在轻至重度患者中,单磷酸鸟苷水平与氨基甲酸甲酯一起被调节,提示免疫功能障碍和核苷酸代谢在非/重度COVID-19向重症进展中的作用9。
Danlos等人还报道了血浆代谢组的改变,反映了COVID-19患者的临床表现,包括轻度(门诊)疾病、中度疾病(放射学证实的肺炎、住院和氧气治疗)和危重疾病(重症监护室)。10;色氨酸代谢进入犬尿氨酸途径的改变与COVID-19危重患者的炎症和免疫有关,而与轻度疾病患者相比10。犬尿氨酸水平升高,精氨酸、肌氨酸和LPC水平降低,也是从健康对照中识别COVID-19阳性患者的最佳代谢物11。色氨酸-烟酰胺通路(与炎症信号和微生物群有关)的作用以及胞嘧啶的参与也被描述为区分和预测疾病演变的可能标记12。
Xiao等人描述了与健康对照组相比,COVID-19患者的整体代谢途径和细胞因子/趋化因子水平失调。他们发现,从轻度到重度患者,循环代谢物和细胞因子/趋化因子之间的相关性不断增强,并揭示了与重度COVID-19高炎症相关的紊乱代谢途径,证明精氨酸、色氨酸或嘌呤代谢调节炎症细胞因子的释放13。
可以从上面和其他作品中推断出来14,16,16在美国,与SARS-CoV-2感染有关的生物学机制仅部分被了解。因此,在当前的工作中,我们通过反相液相色谱耦合四极杆飞行时间质谱(RP/HPLC-qTOF MS/MS)分析,探讨了非COVID对照和145例COVID诊断患者的血浆代谢组学。此外,根据无症状(不需要住院)、轻度疾病(住院总时间低于10天)、严重疾病(住院总时间超过20天和/或入住ICU)和致命结局或死亡患者的临床进展对患者进行分层。此外,对预后较轻的住院患者出院后2 ~ 3个月的随访样本,研究疾病在代谢组中的后遗症以及康复如何反映在改变的生物学途径上。目前工作的最终目标是找到生物标志物,这些生物标志物将增加我们对COVID-19疾病如何演变的理解,并将改进我们对患者如何根据感染早期获得的血浆代谢物谱进行进展的预测。
结果
代谢物鉴定
为了更广泛地了解COVID-19患者疾病过程中的代谢组学变化,使用两种不同的电离模式(ESI(+)和ESI(−)),采用基于RP/HPLC-qTOF MS/MS分析的非靶向代谢组学分析,以增加鉴定代谢物的覆盖率。从每个ESI电离模式获得的数据被独立处理,以避免强度偏差。数据后处理后,RP/HPLC-qTOF MS/MS分析得到203个代谢物注释:ESI(+) 117个,ESI(−)70个,两种电离模式均有16个。每种电离模式下鉴定代谢物的完整列表以及不同分析(ANOVA, U检验和PLS-DA)的统计值显示在补充表中S1和S2。
入院时样本分析
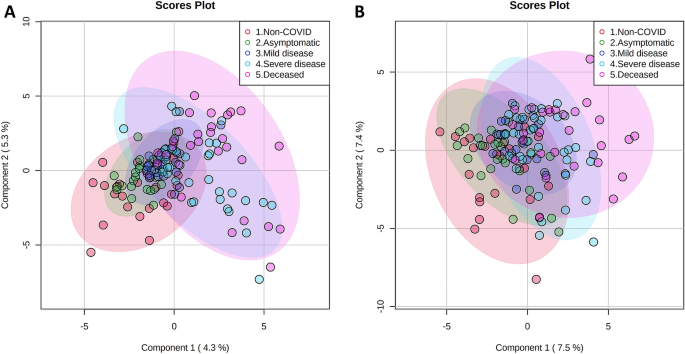
入院时采集样本的ESI(+)和ESI(−)电离模式的PCA分析显示,非COVID-19对照组和/或不同COVID-19阳性组之间没有差异(补充图2)。S1A、B)。另一方面,尽管“留一”交叉验证方法表明,模型的变异解释百分比和预测能力相当低(R2Y = 0.591, Q2ESI = 0.327 (+);R2Y = 0.540, Q2ESI = 0.325(−),PLS-DA分析提示无症状和轻度疾病组更接近非covid对照组;病情严重的患者更接近死亡组(图2)。1A、B)。该分析还显示,在ESI(+)和ESI(−)模式下,VIP评分分别为> - 1.5的代谢物分别为17和11种(补充表)S1和S2)。值得注意的是,大多数这些化合物的丰度随着COVID-19严重程度阶段的增加而增加。S2)。
ESI(+)数据的Kruskal-Wallis方差分析显示,35种代谢物丰度显著改变,而30种代谢物在ESI(−)模式下发生了改变(补充表)S1和S2)。这些改变的代谢物的热图表示显示了与PLS-DA分析相似的结果:无症状和轻度疾病的COVID-19患者更接近非covid对照组;重症患者更接近死亡组(补充图2)。S3A、B)。ANOVA分析后,大部分显著改变的代谢物在PLS-DA分析中已呈现VIP评分> 1.5,并获得少数代谢物。
相关分析显示,不同组的代谢物丰度相似。在ESI(+)中,几种酰基肉碱(3-羟基丁基肉碱、己醇基肉碱)l肉碱,decanoyl -l肉碱、辛酰-l肉碱,arachidonoyl -l-肉碱,亚油基肉碱,乙酰基l-肉碱,月桂肉碱,油酰l-肉碱和棕榈酰l-肉毒碱)、PC/LPC化合物(2-溶血磷脂酰胆碱、PC (p-16:0/0:0)、LPC (o-16:0)、LPC(20:2)、PC(18:1/16:0)、LPC(16:0)、LPC (p-18:0)、LPC(17:0)、PC (18:2e)、PC (18:11 e)和PC (20:4e))和氨基酸(色氨酸、l -缬氨酸、l -异亮氨酸、l -蛋氨酸和l -酪氨酸)归为一类;而在ESI(−)中,最相关的集合是由LPC、FA衍生物或胆汁酸(糖去氧胆酸、牛磺酸去氧胆酸、糖胆酸、糖醛酸和牛磺胆酸)组成的。Pearson相关(r)值和相应的p值在补充表中给出S3和S4ESI(+)和补充表S5和S6为ESI(−)。
新冠肺炎不同阳性组与非新冠肺炎对照组间的Mann-Whitney U检验显示,无症状组有8项代谢物发生改变(其中5项代谢物升高,3项代谢物降低)。轻度疾病组显著改变的代谢物数量增加到26个,14个和12个分别增加和减少。其中一些在无症状组已经观察到改变,如s -甲基-3-硫代对乙酰氨基酚和烟酰胺核苷正离子,其值在轻度疾病组增加更多;n -甲基-2-吡咯烷酮、甲氧苄啶和l-蛋氨酸,这些数值在轻度疾病组继续下降。在严重疾病组中,显著改变的代谢物数量增加到45个(32个值增加,13个值减少);死亡组的代谢产物变化总数为35个(23个升高,12个降低)。在之前的PLS-DA和ANOVA分析中,已经观察到许多这些代谢物具有显著性。
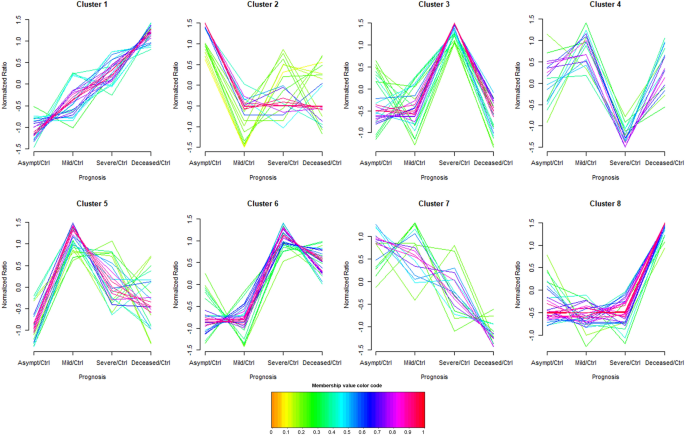
对先前比较中获得的褶皱变化比模式进行进一步分析表明,形成了8个主要集群(图2)。2, MFuzz隶属度值和聚类组成见补充表S7和S8)。
该分析提供了不同样本组(非covid对照组归一化后)之间具有相似变化模式的代谢物组的总体概述,并允许将ESI(+)和ESI(-)数据组合在一起,因为使用非covid对照组的归一化消除了使用不同ESI电离模式产生的偏差。需要注意的是,该分析并未考虑COVID-19阳性样本与对照组之间进行非参数Mann-Whitney U检验后的统计差异,因为它只是根据其倍变化率相似性对代谢物进行聚类。在鉴定的聚类中,聚类1代表从无症状组到死亡组丰度持续增加的代谢物,包括3-羟基丁基肉碱、糖胆酸、LPE(22:6)、神经酸和棕榈酸等。聚类7代表从无症状组到死亡组丰度持续下降的代谢物,由3种PC (PC(16:0/20:4)、PC (20:4e)和PC (20:5e))和色氨酸组成。根据先前的PLS-DA和方差分析结果,第6类代谢物特别有趣,因为它们的丰度在严重疾病组和死亡组中最高。该簇包括2-溶血磷脂酰胆碱、α -亚麻酸、亚油酸或l -异亮氨酸、甲酯。最后,聚类8最拥挤(24种代谢物),由丰度主要在死亡组增加的代谢物组成。其中一些代谢物是己脂酰l-肉碱,糖去氧胆酸和牛磺酸去氧胆酸。
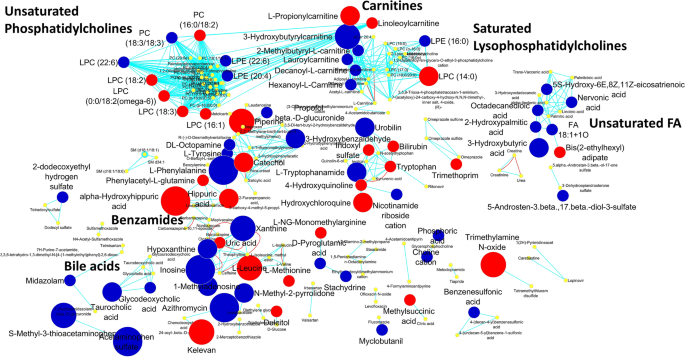
为了提供在不同组比较中显著改变的化学类别,使用ChemRICH进行了化学富集分析。无症状组与非新冠对照组比较,化学类无显著变化;但在轻度疾病组,化学类“肉碱”增加,“不饱和溶血磷脂酰胆碱”改变(有些种类增加,有些减少)。在严重疾病组,“雄烯醇”显著降低(考虑3种代谢物);黄嘌呤含量变化显著,有的物种增加,有的物种减少;2-吡啶基甲基亚砜基苯并咪唑、吡啶类和不饱和脂肪酸显著增加。根据神经酸、亚油酸、α -亚麻酸、反式vaccenic酸和棕榈油酸的丰富程度,最后一类化学物质在死者组中也有所增加。化学类的全部列表和每次比较得到的各自的p值列在补充表中S9- - - - - -S11,所有带注释的代谢物在生化网络中的表示,使用MetaMapp的化学和生化相似性构建,如补充图所示。S4- - - - - -S7。
最后,使用MBROLE 2.0对每个比较中显著改变的代谢物进行代谢物集富集分析(表1)1)。需要指出的是,在无症状组、轻症组、重症组和死亡组中,分别只有5、17、28和16种改变的代谢物可以用有效的KEGG id进行映射(许多肉毒碱和奥美拉唑衍生物无法进行映射)。
分析表明苯丙氨酸代谢和不饱和脂肪酸的生物合成在严重疾病组和死亡组中富集。在…的情况下苯丙氨酸代谢,在两种比较中,3-羟基苯基乙酸的水平升高,而马尿酸的水平降低。在…的情况下不饱和脂肪酸的生物合成α -亚麻酸、神经酸和亚油酸均升高。在轻度和重度疾病组中另一个富集的途径是嘌呤代谢。发现与这一途径相匹配的三种代谢物(尿素、肌苷和黄嘌呤)发生了变化,在两个COVID-19阳性组中,它们的值都有所增加。最后,咖啡因代谢根据黄嘌呤和咖啡因(增加值)以及茶碱(减少值)的丰度,严重疾病组Pathway富集。
轻症患者出院时随访研究
第二种统计方法是比较轻度疾病组患者入院时和出院后2-3个月的血浆代谢物。PCA和PLS-DA分析可以区分两组样本(补充图2)。S8和S9),但PLS-DA分析提供了更多信息(补充表S12和向)。在ESI(+)数据中,13个化合物的VIP评分为bb0 1.5,其中6个化合物的VIP评分升高(kelan、LPC(14:0)、phenylacetyl-)l-谷氨酰胺、胆红素、l -蛋氨酸和LPC(16:1))和7个值降低的(次黄嘌呤、肌苷、LPC (p-18:0)、硫酸对乙酰氨基酚、myclobutanil、1-甲基腺苷和l -色氨酸)。在ESI(−)的情况下,11个化合物的VIP评分为bb0 1.5,其中2个值较高(甲基琥珀酸和LPC为18:2),9个值较低(次黄嘌呤、黄嘌呤、3-羟基丁酸、3-羟基苯甲醛、s -甲基-3-硫代对乙酰氨基酚、硫酸对乙酰氨基酚、十八烯二酸、神经酸和LPE为20:4)。这些代谢物的图形表示以及对照样本的值表明,其中一些代谢物的强度在出院时恢复到“正常”值(补充图2)。S10)。然而,必须注意的是,这些患者可能具有独特的代谢特征,这可能与生活质量的好坏有关。在这方面,病史表明,在出院后采集样本时,患者均无任何生活质量差的症状,此后也未报告该疾病的后遗症。
配对非参数U检验显示,ESI(+)中43种代谢物丰度显著改变(其中19种丰度升高,24种丰度降低);在ESI(−)中,出院时有35种代谢物发生改变(13种代谢物较多,22种代谢物较少),证实PLS-DA分析后VIP评分为> 1.5的代谢物在两组间均有统计学意义。
化学类分析和代谢组学变化的生化过度表征表明,芳香氨基酸、肉碱、饱和月桂酸盐和吡啶显著减少,而苯酰胺显著增加(图2)。3.及补充表S14系列)。其他化学类别,如不饱和LPC(7种代谢物),有增加的也有减少的。
对显著改变的代谢物进行代谢物集富集分析,再次表明苯丙氨酸代谢和嘌呤代谢与入院时的水平相比,轻度疾病组出院时的含量丰富(补充表)S15)。有趣的是,所有被认为的代谢物(苯丙氨酸、马尿酸、苯乙酸)l-谷氨酰胺苯丙氨酸代谢;次黄嘌呤,肌苷,尿酸和黄嘌呤嘌呤代谢)与入院时轻度疾病组与非新冠肺炎对照组的方向相反。
讨论
自2019年COVID-19大流行发生以来,已经发表了几项研究,旨在调查COVID-19阳性患者血清代谢组学变化1,2。在大多数这些文献中,代谢组学和/或脂质组学方法已应用于不同的患者队列,但只有少数文献根据住院总时间(无症状、少于10天、超过20天和死亡)纳入了四种不同的COVID-19阳性组,并结合对出院时COVID-19轻病患者的随访研究。
在本研究中,经过不同的统计分析,几种代谢物可以区分终末期和早期(或非covid)疾病组。这些代谢物主要参与肉碱、酮体、脂肪酸、LPC/PC、色氨酸、胆汁酸、嘌呤和奥美拉唑的代谢。此外,其中几种代谢物的水平在出院时降至“正常”值,表明其中一些代谢物在诊断时是COVID-19的早期预后生物标志物。其中一些代谢物的改变在以往的研究中已经被观察到,但它们之间仍然存在一些差异。
在不同的分析样品中观察到一组具有良好Pearson相关性的代谢物是酰基肉碱。酰基肉碱参与FAs进入线粒体进行β氧化和能量产生。这些代谢物通过线粒体内膜转运,肉毒碱棕榈酰转移酶2从酰基肉毒碱中去除肉毒碱,再生酰基辅酶a。在肝脏中,酰基辅酶a参与β-氧化,最终生成乙酰辅酶a,肉毒碱返回细胞质进行另一个循环17。我们的研究结果表明,其中一些代谢物在COVID-19阳性患者中显著增加(如轻病组中具有长链脂肪酰基的肉毒碱,以及死亡组中具有中链酰基肉毒碱)。这些结果与之前的结果一致,即酰基肉碱水平增加18但它们也与其他研究相矛盾,其中COVID-19患者的酰基肉碱减少19。另一项研究报告说,呼吸道病毒,如流感病毒,促进酰基肉碱的积累20.这可能是SARS-CoV-2的情况,因为我们观察到大多数酰基肉碱的水平在出院时降至“正常”值。此外,在β-氧化过程中,还会产生3-羟基丁酸等酮体。酮体在禁食、运动后或怀孕期间提供替代燃料,但它们也扮演炎症、免疫细胞功能和氧化应激调节剂的角色21。我们观察到这种代谢物在轻度疾病组(p-val = 0.021)和死亡组(p-val = 0.001)中显著增加,在严重疾病组中几乎显著增加(p-val = 0.057)。据报道,COVID-19感染导致酮症,住院天数和死亡率增加22新冠肺炎患者体内乙酰乙酸、3-羟基丁酸和丙酮含量异常23。另一方面,3-羟基丁酸与烟酸一起,通过降低促炎蛋白(iNOS, COX-2)或分泌的细胞因子(IL-6和IL-1β)的水平,显示出对TNF-α的抗炎作用。24这可能解释了在不同的COVID-19阳性组中观察到的3-羟基丁酸水平持续升高的原因。
我们的研究结果还表明,几种ufa(神经酸、亚油酸、α -亚麻酸、反式痘酸和棕榈油酸)的水平与COVID-19预后较差相关;这些代谢物的水平在轻度疾病患者出院时下降。在这些脂肪酸中,亚油酸参与了包膜病毒(如流感)的灭活;外源性补充已被证明可以抑制中东呼吸综合征冠状病毒(MERS-CoV)的复制25。此外,其他针对HCoV-229E冠状病毒的研究也表明,宿主脂质代谢重塑,特别是亚油酸,与冠状病毒的传播有关26。特别是在SARS-CoV-2中,亚油酸可以减少病毒刺突蛋白与ACE2受体的相互作用27。事实上,它可能会将刺突蛋白稳定在一个封闭的构象中,阻止其与ACE2的相互作用28。其他多不饱和脂肪酸(PUFAs)也可以改变宿主膜的流动性,并通过破坏病毒的包膜来灭活病毒29。膜流动性的变化可能会影响宿主和病毒蛋白的构象,并对SARS-CoV-2起决定作用27。PUFAs如何抑制病毒进入的机制可能通过抑制宿主的内体蛋白酶来解释。FAs采用扁平构象或球形脂质体界面,可中断宿主膜与抑制SARS-CoV-2附着的病毒包膜之间的接触27。因此,在我们的研究结果中,冠状病毒感染期间不饱和脂肪酸水平较高可能是由于PUFAs对病毒结合的抑制作用。
在分析样品之间具有良好Pearson相关性的另一组代谢物是LPC/PC化合物。其中,LPC(14:0和0:0/16:2(omega-6))的VIP评分为bbbb1.5,其丰度随感染预后最差而降低;轻症组LPC(16:1)明显降低;轻症组和死亡组LPC(18:2)降低;重症组LPC(22:6)降低。另一方面,我们观察到不同LPEs(16:0和22:6)的水平在终末期疾病组中升高。先前的研究报道,SARS-CoV-2疾病与健康患者分离的标志是溶血磷脂(LPs)和甘油磷脂的变化30.在COVID-19阳性患者中发现了多个LPC(16:0, 18:0, 18:1和18:2)的减少31。这些分子的减少与严重患者的ARDS和败血症有关。然而,其他研究表明LPC和LPE水平有所增加18。宿主细胞脂质稳态的改变被认为是病毒创造良好复制环境的一种策略。从这个意义上说,PLA2(一组水解磷脂以产生FA和LPs的酶)被认为参与了冠状病毒的复制,以产生溶血磷脂,而溶血磷脂是形成病毒RNA合成所需的膜结构所必需的32。
先前的研究还表明,COVID-19患者的色氨酸代谢发生了改变10,15,33。色氨酸代谢的一个重要代谢物是犬尿酸。这种代谢物在感染末期的患者中显著增加,而色氨酸在同一组患者中显著减少。Danlos等人(2021)的研究结果显示,在COVID-19严重阶段,色氨酸水平下降,而其免疫抑制代谢物犬尿氨酸在危重患者中升高10。与对照组相比,危重患者的色氨酸减少表明消耗了色氨酸2,3-双加氧酶和吲哚胺2,3-双加氧酶,它们产生犬尿氨酸前体犬尿氨酸。其他研究表明,犬尿氨酸的增加与SARS-CoV-2的炎症和器官损伤有关33,34。此外,犬尿氨酸和色氨酸比值升高与促炎因子和COVID-19感染的不良预后呈正相关11,34,35,36。
在我们的研究中发现的另一组代谢产物与胆汁酸代谢有关(牛磺胆酸、牛磺去氧胆酸、糖去氧胆酸、糖胆酸和糖脲去氧胆酸)。这些代谢物的水平主要随着疾病的严重程度而增加,在轻度疾病组中,一些代谢物在出院时恢复到“正常”值。在先前的研究中发现胆汁酸水平升高7,15。胆汁酸的主要功能是消除胆固醇和促进脂溶性营养物质的吸收,但它们也可以作为信号分子促进或抑制病毒复制37。已经证明胆汁酸可以限制单纯疱疹病毒的体外复制38或甲型流感病毒39或者它们可以促进乙型和丙型肝炎病毒的体外复制40。我们的研究结果表明,最后一种选择可能是SARS-CoV-2的情况,但目前尚不清楚其具体作用和分子机制。
其他可能参与SARS-CoV-2复制的代谢物与嘌呤代谢有关,有研究表明,SARS-CoV-2重塑宿主叶酸和单碳代谢,以支持从头合成嘌呤41。然而,嘌呤代谢物也与SARS-CoV-2诱导的炎症过程有关13,15。在最后一项研究中,黄嘌呤水平与重症患者的促炎细胞因子(如IL-6)相关,证实了COVID-19代谢途径紊乱与高度炎症之间的联系。我们的研究结果表明,参与嘌呤代谢的不同代谢物(尿素和黄嘌呤)随着严重阶段的增加而增加,但其他代谢物(肌苷)没有明显的趋势。无论如何,大多数人在出院时都恢复了“正常”值。
除了内源性代谢物外,在不同的样本组之间,还观察到几种外源性代谢物和外源性衍生物的变化,但由于在选择样本队列时没有考虑患者的临床病史,因此大多数被丢弃。然而,有趣的是,奥美拉唑及其衍生物的水平在严重感染患者中较高,但在无症状感染的COVID-19患者中也较高,这表明这种外源药物可能是SARS-CoV-2感染的标志物。这一点很有趣,因为尽管质子泵抑制剂不会使患者更容易感染SARS-CoV-2,但最近的观察性研究表明,服用它们的患者患严重COVID-19的风险可能会增加42我们在这里已经证实了这一点。
结论
综上所述,COVID-19阳性患者在肉碱、酮体、脂肪酸、LPC/PC、色氨酸、胆胆酸、嘌呤和奥美拉唑等代谢方面发生改变,提示3-羟基丁酸盐、亚油酸、LPC(14:0和18:2)、LPE(22:6)、犬尿酸和色氨酸等代谢产物可能是临床严重程度的潜在生物标志物。这项工作还表明,代谢组学是一个非常有价值的资源,可以更好地了解与COVID-19相关的宿主代谢反应,扩大我们对不同症状条件下患者发病机制的了解,并有助于识别疾病生物标志物,开发诊断检测方法,以及可能的治疗策略9。用于对抗大流行的代谢组学战略可以为未来疫情的长期计划奠定基础。此外,通过这种组学(和多组学)方法取得的新突破不仅有助于防治这一流行病,而且还将推动科学界和政府机构更广泛地采用这些技术。然而,关于COVID-19的许多问题仍有待解答。
方法
患者招募和样本注意
在2020年3月至4月COVID-19爆发期间,共有145名18岁以上的成年患者在“Clínico巴利亚多利德大学医院”(西班牙巴利亚多利德)的A&E部门就诊,经当地伦理委员会(investigación con medicamento - ceem - de Valladolid este;pi20 - 1716)。所有研究均按照相关指南/法规进行。获得了所有参与者的知情同意。所有患者的样本都是在入院时采集的(没有任何标准护理),根据病史,没有患者使用任何药物治疗covid -19相关症状。
患者包括25例因非covid相关问题就诊的阴性对照(非covid)(男性52%,平均年龄66.4±9.6岁)和120例经鼻咽标本聚合酶链反应证实为严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)感染阳性的COVID-19患者。其中28例无症状,无需住院(50%为男性,65.2±15.2岁);27例为轻症,总住院时间小于10天(44%为男性,65.3±11.5岁);36例病情严重,以住院总时间超过25天和/或在ICU住院定义(66.7%为男性,65.3±11.5岁);死亡或死亡29例(男性45%,71.6±8.4岁)。最后,对预后较轻的住院患者进行出院后2 ~ 3个月的随访。这些患者的详细人口统计、合并症和治疗可在补充表中找到S16。
化学品和试剂
lc - ms级乙腈(ACN)和甲醇由VWR Chemicals (Barcelona, Spain)获得,而超纯水由Millipore系统(Billerica, MA, USA)获得。甲酸购自Fisher Scientific (Waltham, MA, USA)。
在所有病例中,当患者到达急症室时,立即获得血液样本(在肝素真空管中)。血液保存在4°C,并在24小时内通过密度梯度离心在ficoll上处理。收集血浆,引用并保存在- 80°C直到使用。
代谢物提取
所有患者的血浆标本在冰上解冻并涡流30 s。然后,每个样品取100µL,在-20℃下加入400µL甲醇,将混合物涡旋1 min,在冰上培养10 min。然后在4℃下以148000 rpm离心20 min,收集300µL上清,使用SpeedVac (Savant SPD1030, Thermo Scientific, USA)蒸发。干燥后的样品在100µL 80%的甲醇中重组,混合1分钟,在4°C下再次以148000 rpm离心5分钟。收集新上清80µL,保存于- 80°C,待HPLC-MS /MS分析。
反相液相色谱-四极杆飞行时间质谱(RP/HPLC-qTOF MS/MS)分析
采用安捷伦公司(Agilent Technologies)的四极杆Q-TOF系列6540和高效液相色谱(型号1290)组成的液相色谱-质谱/质谱系统,配以Agilent Jet Stream (AJS)热正交ESI源,将等量2 μL (ESI(+)和ESI(−)模式)注入该系统。使用Agilent Mass Hunter定性分析软件(B.10.0)进行质谱控制、数据采集和数据分析。色谱分离采用德国Agilent公司的Eclipe Plus C18分析柱(100 × 2.1 mm,粒径1.8 μm)和C18保护柱(0.5 cm × 2.1 mm,粒径1.8 μm)。柱温保持在40℃,流速设置为0.5 mL/min。ESI(+)和ESI(-)模式均以水(LC-MS级)为流动相(A), ACN为流动相(B),甲酸为流动相改性剂(ESI(+)为0.1%,ESI(-)为0.01%)。梯度从0分钟开始,0 - 30% (B), 7分钟0 - 30% (B), 2分钟30-80% (B), 2分钟80-100% (B), 2分钟100% (B), 3分钟后回到初始状态。质谱仪的操作参数为:毛细管电压为3000 V(+)或- 3000 V(-),带am / z范围是25到1100。雾化器压力设置为40 psig,干燥气体流速固定为8 L/min,温度为300℃。350℃时,护套气流量为11 L/min。破碎器电压为110 V,撇渣器电压为45 V,八极器电压为750 V。MS/MS分析采用自动MS/MS模式,每循环5个前驱体,两次光谱后动态排除(0.5 min后释放),碰撞能量为20和40 V。为了获得适当的质量精度,光谱用离子校正m / z121.0509 (C5H4N4)及922.0098 (C18H18O6N3.P3.F24)在ESI(+)中,和米/z119.0363 (C5H4N4)和966.0007 (C18H18O6N3.P3.F24+甲酸)在ESI(−)中,同时泵入电离源。
质量控制
通过以下方式保证质量控制:i)序列的随机化;Ii)程序空白分析;iii)在不同顺序的样品前后注入池样品以平衡LC-MS系统;iv)注射标准混合物,检查保留时间、峰形、强度和质量精度。
数据处理
LC-MS原始数据文件首先使用Reifycs ABF(分析基础文件)转换器转换为ABF格式(可访问:http://www.reifycs.com/AbfConverter/)。然后使用MS-DIAL (v. 4.12)软件进行数据处理,用于反褶积、拾取峰值、对齐和识别43采用以下参数:保持时间开始,0分钟;保留时间结束,14分钟;质量范围开始,0 Da;质量范围端,1100 Da;MS1公差0.01 Da;平滑级别,3次扫描;最小峰宽,5次扫描;最小峰高,1000幅;质量片宽度,0.1 Da;反褶积的Sigma窗口值,0.1; accurate mass tolerance for MSP library, 0.01 Da; identification score cut off for MSP library, 80%; retention time tolerance for alignment, 0.1 min; MS1 tolerance for alignment, 0.015 Da. Peak height calculation was performed by combining data for different detected molecular species for each particular compound ([M+H]+[M + NH4)+[M + Na)+[M + K)+, (2 m + H)+, (2 m + NH4)+, (2 m + Na)+, (2 m + K)+加合物呈正模式,[M−H]−, (2 m−H)−[M + Cl)−[M + FA-H]−加合物为负模式)。用于注释的MSP文件由NIST20 MS/MS数据库、LipidBLAST质谱库中的MS/MS谱结合生成44,以及北美MassBank的数据库(MoNA,可在https://mona.fiehnlab.ucdavis.edu/downloads)。所有代谢物均按照代谢组学标准倡议(MSI)指南进行注释45,46为MSI水平2a(代谢产物与前体m/z和MS/MS谱库匹配)。
数据后处理和统计分析
对各ESI电离模式下获得的代谢物清单进行过滤,去除提取空白、Vacutainer®采血管空白、Ficoll-Hypaque空白中未知代谢物、最大高度低于1000单位的代谢物或最大高度低于平均高度3倍的代谢物。至少一组中超过50%的样品中存在的代谢物被保留了下来。缺失值按最小高度值的一半进行输入,数据使用生物信息学工具MS-FLO (https://msflo.fiehnlab.ucdavis.edu/#/)47。去除重复的代谢物和同位素,将同一化合物中不同加合物的高度进行组合,并使用随机森林归一化进行系统误差去除48使用池样本作为参考样本。
根据两种不同的实验设计进行统计分析。在第一种方法中,从住院患者收集的样本被一起分析,以寻找预后的代谢生物标志物。采用MetaboAnalyst 5.0网络软件对样本进行“Auto scaling”归一化后的多变量分析(PCA和PLS-DA)49。PLS-DA模型采用R的“留一”交叉验证法进行评价2和问2,获得投影变量重要性(VIP)得分,当VIP得分> 1.5时,认为VIP得分显著。采用Pearson相关系数(r)评价相关分析,获得热图表示,各组间比较采用非参数方差分析(Kruskal Wallis)检验。此外,采用非参数Mann-Whitney U检验计算并评价不同COVID-19阳性组(无症状、轻症、重症、死亡)与阴性对照组(非covid)之间的fold变化。当原始p值< 0.05时,认为代谢物显著改变。采用模糊c均值聚类算法研究不同阳性组与阴性对照组(非covid)代谢物折叠变化率的变化规律50。在此分析中,探索了不同的簇大小和模糊化参数组合,并找到了c = 8和m = 2的最优划分。这些值避免了空簇的出现,减少了到簇质心的最小距离。此外,对于集群分配,成员值的阈值设置为0.7。
第二个实验设计包括对轻度疾病组患者在两个不同时间点(入院时和出院后2-3个月)的血浆样本进行分析和比较,目的是寻找疾病恢复的代谢生物标志物。为了进行比较,采用了PCA、PLS-DA和配对非参数Mann-Whitney U检验。
数据可视化,丰富和通路分析
将COVID-19阳性样本与阴性对照比较后获得的数据矩阵合并生成联合数据集。对于ESI(+)和ESI(−)模式下检测到的代谢物,保留了相似性评分最高(来自MSP文件)、峰强度最高和/或峰形状更好的数据。
对于代谢网络的映射,InChiKey或化合物名称被导入到基于web的化学翻译服务(http://cts.fiehnlab.ucdavis.edu/batch)51获取PubChem Compound Identifiers (CID)和Kyoto Encyclopedia of Genes and Genomes Identifiers (KEGG ID)。简化的分子输入行输入系统(SMILES)代码是从MSP文件或PubChem化合物标识符交换服务(https://pubchem.ncbi.nlm.nih.gov/idexchange/idexchange.cgi),使用ChemRICH进行化学相似度富集计算52。使用MetaMapp进行KEGG反应物对和谷本相似度计算(阈值为0.7)53。将最终的网络图导入到Cytoscape 3.7.2中54,以及MetaboAnalyst生成的结果。使用Cytoscape中的yED有机布局算法将图形可视化。使用MBROLE 2.0进行代谢物富集分析。基于网络的软件55。导入与KEGG数据库匹配的显着改变的代谢物,并针对KEGG途径模块进行过代表性分析,并使用智人作为背景设置,被执行。p值小于0.05的注释被认为是显著富集。
参考文献
Aggarwal, S., Acharjee, A., Mukherjee, A., Baker, m.s.和Srivastava, S.多组学数据在了解COVID-19发病机制中宿主-病原体相互作用的作用。J.蛋白质组学。20., 1107-1132(2021)。
庞震,周刚,Chong, J. &夏杰。COVID-19全球代谢组学数据集的综合meta分析。代谢物11, 44(2021)。
洛奇。et al。SARS-CoV-2感染对血浆脂蛋白和代谢物与循环细胞因子相关的全身影响的核磁共振光谱窗口。J.蛋白质组学。20.中文信息学报,1382-1396(2021)。
Páez-Franco, j.c.。et al。代谢组学分析揭示了与COVID-19患者氧稳态改变相关的氨基酸代谢修饰。科学。代表。11, 6350(2021)。
郑,H。et al。代谢组学揭示了COVID-19非重症患者在康复过程中性别特异性代谢变化,并预测了从阳性到阴性的持续时间。第一版。结构体。Biotechnol。J。19, 1863-1873(2021)。
徐杰,等。COVID-19合并肺后遗症患者出院后3个月血浆代谢组学分析中国。感染。说。ciab147(2021)。
沈,B。et al。COVID-19患者血清的蛋白质组学和代谢组学特征。细胞182, 59-72(2020)。
Doğan, h.o.。et al。通过非靶向代谢组学了解COVID-19患者的病理生理变化。J. Med. Virol。93, 2340-2349(2021)。
吴,D。et al。与COVID-19相关的血浆代谢组学和脂质组学改变国家的。科学。牧师。7中文信息学报,1157-1168(2020)。
丹洛斯,f.x。et al。COVID-19患者的代谢组学分析揭示了阶段依赖和预后的生物标志物。细胞死亡病。12, 258(2021)。
托马斯,T.等。COVID-19感染改变犬尿氨酸和脂肪酸代谢,与IL-6水平和肾脏状态相关。JCI洞察力。5, e140327(2020)。
弗雷泽博士等。2019年冠状病毒危重症患者的代谢组学分析:诊断和预后生物标志物的鉴定暴击。保健空洞。2中文信息学报,027(2020)。
Blasco, H。et al。SARS-COV-2感染患者的特异性代谢组分析支持色氨酸-烟酰胺途径和胞嘧啶代谢的关键作用。科学。代表。10, 16824(2020)。
Sindelar等人。人血浆纵向代谢组学揭示了COVID-19疾病严重程度的可靠预后标志物。medRxiv。2020.https://doi.org/10.1101/2021.02.05.21251173。
肖,N。et al。综合细胞因子和代谢物分析揭示COVID-19患者免疫代谢重编程具有治疗意义。Commun Nat。12, 1-13(2021)。
Marin-Corral, J。et al。住院COVID-19患者的代谢特征与严重程度相关Int。科学通报;22, 4794(2021)。
Longo, N., Frigeni, M.和Pasquali, M.肉毒碱运输和脂肪酸氧化。Biochim。Biophys。学报1863, 2422-2435(2016)。
barberi E。et al。大规模血浆分析揭示了与宿主对SARS-CoV-2反应相关的新机制和分子。Int。科学通报;21, 1-25(2020)。
宋洁,林淑娟,方晓霞,曹伟。代谢失调在新冠肺炎发病机制中的组学驱动系统研究。细胞金属底座。32, 188-202(2020)。
Otsubo C。et al。长链酰基肉碱通过抑制肺表面活性物质降低肺功能。生物。化学。290中文信息学报,23897-23904(2015)。
Puchalska, P. & Crawford, P. A.酮体的多维作用。杂志。Behav。176, 139-148(2019)。
李,等。COVID-19感染可引起酮症和酮症酸中毒。糖尿病,ob。金属底座。22, 1935-1941(2020)。
Bruzzone, C.等。SARS-CoV-2感染导致血清代谢组学和脂质组学异常。iScience23中文信息学报,101645(2020)。
傅淑萍。et al。BHBA通过抑制NF- B激活来抑制lps诱导的BV-2细胞炎症。Mediat。Inflamm。2014, 98230(2014)。
Das、un花生四烯酸等不饱和脂肪酸及其代谢产物作为内源性抗菌分子的研究进展。J. Adv. Res。11, 57-66(2018)。
燕,B。et al。人冠状病毒感染细胞的脂质组学特征:冠状病毒复制过程中脂质代谢重塑的意义病毒11, 73(2019)。
Goc, A, Niedzwiecki, A. & Rath, M.多不饱和ω-3脂肪酸抑制ace2控制的SARS-CoV-2结合和细胞进入。科学。代表。11, 5207(2021)。
Vivar-Sierra,。et al。多不饱和脂肪酸作为潜在的SARS-CoV-2刺突蛋白封闭构象稳定剂的计算机研究:流行病学和计算方法。分子26, 711(2021)。
kon, A, Gitelman, J.和Inbar, M.不饱和游离脂肪酸灭活动物包膜病毒。拱门。性研究。66, 301-307(1980)。
施瓦兹,B。et al。前沿:人类严重的SARS-CoV-2感染的定义是血清脂质组发生变化,导致类二十烷类免疫介质失调。j . Immunol。206, 329-334(2021)。
Delafiori, J。et al。通过代谢组学和机器学习自动诊断和风险评估Covid-19。分析的化学。93中文信息学报,2471-2479(2021)。
穆勒,C。et al。胞质磷脂酶A(2) α的抑制损害了细胞培养中冠状病毒复制的早期步骤。j .性研究。92, e01463-e1517(2018)。
蔡,Y.等。犬尿酸是针对COVID-19的性别特异性免疫反应的基础。medRxiv。2020.https://doi.org/10.1101/2020.09.06.20189159。
Turski, W. A, Wnorowski, A., Turski, G. N., Turski, C. A.和Turski, L. AhR和IDO1在Covid-19发病机制和“系统性AhR激活综合征”中的作用:翻译回顾和治疗观点。备份文件夹。神经。>。38, 343-354(2020)。
patin, M, Wick, W.和Van Den Eynde, B. J.色氨酸在癌症中的分解代谢:超越IDO和色氨酸消耗。癌症Res。72, 5435-5440(2012)。
hajadj, J., Yatim, N., Barnabei, L., Corneau, A.和Boussier, J. COVID-19重症患者I型干扰素活性受损和炎症反应。科学369, 718-724(2020)。
孔芳,赛义夫,王强,等。胆汁酸在肠道病毒复制中的作用。动物说。1, 2(2021)。
赫罗尔德,b.c。et al。胆盐:预防性传播疾病的天然清洁剂。抗菌剂化学试剂。43, 745-751(1999)。
罗,L。et al。胆汁中的鹅去氧胆酸通过阻断病毒核糖核蛋白复合物的核输出抑制甲型流感病毒的复制。分子23, 3315(2018)。
Reese, V. C, Oropeza, C. E.和McLachlan, A.类维生素a、过氧化物酶体增殖体和胆汁酸对乙型肝炎病毒生物合成的独立激活。j .性研究。87, 991-997(2013)。
张,Y。et al。SARS-CoV-2劫持叶酸和单碳代谢以进行病毒复制。Commun Nat。12, 1676(2021)。
李,S. W。et al。质子泵抑制剂与COVID-19严重临床结局相关:一项倾向评分匹配的全国队列研究肠道70, 76-84(2021)。
Tsugawa, H。et al。MS- dial:数据独立的MS/MS反褶积,用于全面的代谢组分析。Nat方法。12, 523-526(2015)。
善良,T。et al。LipidBlast在硅串联质谱数据库脂质鉴定。Nat方法。10, 755-758(2013)。
Blaženović,我。et al。非靶向代谢组学中所有质谱的结构注释。分析的化学。91中文信息学报,2155-2162(2019)。
萨姆纳,l.w.。et al。建议的化学分析最低报告标准:化学分析工作组(CAWG)代谢组学标准倡议(MSI)。代谢组学3., 211-221(2007)。
德费利斯,b.c。et al。质谱特征列表优化器(MS-FLO):在非靶向液相色谱-质谱(LC-MS)数据处理中最大限度地减少假阳性峰报告的工具。分析的化学。89, 3250-3255(2017)。
粉丝,S。et al。随机森林用于规范化大规模非靶向脂组学数据的系统误差去除。分析的化学。91中文信息学报,3590-3596(2019)。
Pang, Z.等。MetaboAnalyst 5.0:缩小原始光谱和功能洞察之间的差距。核酸类。gkab382(2021)。
Futschik, M. & Carlisle, B.基因表达时间过程数据的噪声鲁棒聚类。j . Bioinform。第一版。医学杂志。4, 965-988(2005)。
Wohlgemuth, G, Haldiya, P. K, willighhagen, E., Kind, T. & Fiehn, O.化学翻译服务-一个基于网络的工具,以提高代谢组学报告的标准化。生物信息学26中文信息学报,2647-2648(2010)。
Barupal, D. K. & Fiehn, O.化学相似性富集分析(ChemRICH)作为代谢组学数据集的生化途径映射的替代方法。科学。代表。7, 1-11(2017)。
Barupal, d.k.。et al。MetaMapp:通过整合来自生化途径和化学和质谱相似性的信息来绘制和可视化代谢组学数据。BMC生物信息学13, 99(2012)。
香农,P。et al。Cytoscape:生物分子相互作用网络集成模型的软件环境。基因组Res。13中文信息学报,2498-2504 (2003)
López-Ibáñez, J, Pazos, F. & Chagoyen, M. MBROLE 20化合物功能富集。核酸类。44, w201-w204(2016)。
致谢
资金由西班牙高等调查委员会Científicas (CSIC-COV19-016/202020E155、SGL21-03-026和SGL2021-03-038)、Junta de Castilla y León (Proyectos COVID 07.04.467B04.74011.0和IBGM卓越计划ccl -2029-02)、Ayudas Atracción de Talento Modalidad 2(马德里社区和马德里大学Autónoma) BMD-5800、西班牙经济和竞争力部(MINECO) (AGL2017-89417-R项目)提供。A.V.在此感谢西班牙科学、创新和大学部授予他的“Juan de la Cierva”(IJC2018-037560-I)研究合同。
作者信息
作者及单位
贡献
交流电,D.B.和A.V.设计了这项研究。S.R.和A.O.招募患者,获取生物样本,获取临床资料。交流,D.B.和A.V.设计并执行实验。交流电和D.B.获得了资金。A.V.分析了数据。a.c., d.b. L.O.M.和A.V.写了这篇文章。所有作者都审阅了手稿。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益冲突。
额外的信息
出版商的注意
b施普林格《自然》杂志对已出版的地图和机构的管辖权要求保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/。
关于本文
引用本文
valdsamas, A, Moreno, lo, Rello, S.R.et al。4个不同临床阶段新冠肺炎患者代谢组学研究Sci代表12, 1650(2022)。https://doi.org/10.1038/s41598-022-05667-0
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-05667-0
这篇文章是由
小分子代谢物:生物标志物和治疗靶点的发现
信号转导和靶向治疗(2023)
血浆代谢组学和基因调控网络分析揭示非结构性SARS-CoV-2病毒蛋白在COVID-19患者代谢失调中的作用
科学报告(2022)
谷胱甘肽、多胺和溶血磷脂酰胆碱合成途径与循环促炎细胞因子相关
代谢组学(2022)