摘要
由于气泡不可预测的特性,改进沸腾是具有挑战性的。增强沸腾的一种方法是使用表面活性剂,它可以改变固体-液体和液体-蒸汽的界面。以往研究建立的传统智慧表明,传热强化在临界胶束浓度(CMC)附近是最佳的,这是一个取决于表面活性剂类型的平衡性质。然而,这些研究只测试了有限数量的表面活性剂在小浓度范围内。在这里,我们在最宽的浓度范围内测试了更多种类的非离子和阴离子表面活性剂,发现存在一个通用的、最佳的浓度范围,而不考虑CMC。为了解释这一点,我们证明了表面活性剂增强沸腾是由两个相互竞争的现象控制的:(1)表面活性剂在界面上的动态吸附和(2)在非常高的表面活性剂浓度下液体动态粘度的增加。这种动态吸附的时间受到气泡在沸腾表面上的毫秒寿命的限制,比观察CMC等平衡行为所需的时间短得多。在非常高的浓度下,增加的粘度抑制了气泡的快速增长,减少了热传递。我们通过一个简单的比例结合了吸附和粘度的影响,为沸腾应用提供了这种增强行为的简洁和有用的理解。
简介
沸腾是一种非常有效的多相传热过程,通过沸腾输送大量的能量。由于其有效性,沸腾起着至关重要的作用,并被广泛应用于各种应用(例如,电子冷却1、紧凑型热交换器和蒸发器2,3.,核反应堆4等)。尽管它无处不在,我们对它的了解却很有限5,6,7,8复杂的气泡动力学和其他物理现象。对于如何增强这一系列复杂的物理现象,我们的理解就更加有限了。强化的量化使用传热系数(HTC),定义为
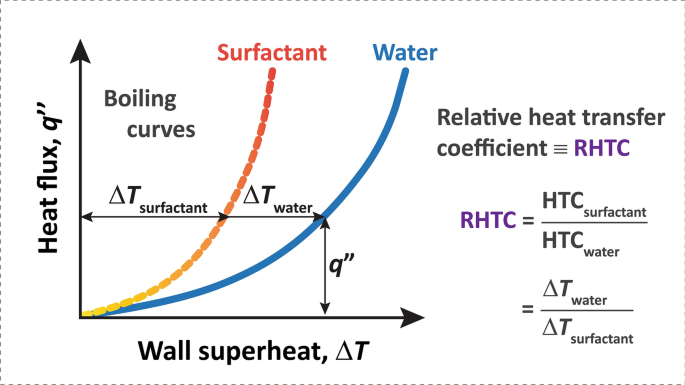
在这里,\(问^ {\ ' \ '}\)热通量是向着沸腾方向的吗\δT (\ \)壁面过热度是否定义为受热面温度、\ (T_{{\文本{年代}}}识别\),饱和温度,\ (T_{{{文本\{坐在}}}}\).近几十年来,许多方法都侧重于结合表面微纳米尺寸的特征,以增强气泡形核和表面润湿,防止干燥9,10,11,12,13,14,15,16.然而,这些广泛的表面修饰在大规模下可能非常昂贵16.一种潜在的低成本方法是添加少量的化学添加剂来改变界面行为:表面活性剂。在沸水中加入这些表面活性剂有时能使HTCs增强10-1000%17,18,19.然而,应该注意的是,增强的定义在不同的研究中是不同的,这可能导致了如此广泛的范围。因此,在图。1,我们定义了一个相对HTC (RHTC),以在我们的研究中提供一个一致的增强定义。在其他情况下,表面活性剂可以降低传热,这取决于表面活性剂的类型和浓度。因此,非常需要研究使用多少和什么类型的表面活性剂,需要从机理和分子的角度来理解。
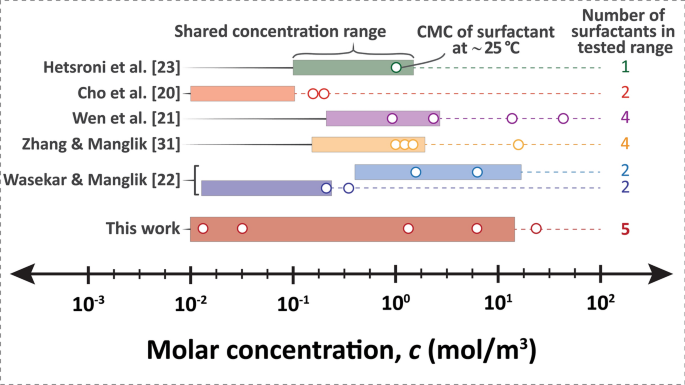
表面活性剂是两亲性分子,一旦溶解,吸附到界面,并改变液体的界面性质。研究表明,一般情况下,增加沸腾液体中表面活性剂的浓度可以在较低的壁过热时提供更多的传热,从而提高热传导率。然而,添加过多的表面活性剂也会降低HTC。非离子、阴离子和阳离子表面活性剂的这种增强和降解已被观察到17,20.,21,22,23,24,25,26,27,28,这表明无论其离子类型如何,表面活性剂的作用都是相似的。因此,表面活性剂的最佳浓度范围是什么是一个悬而未决的问题。先前的研究已经得出结论,这个最佳浓度取决于表面活性剂的类型,可能与临界胶束浓度(CMC)一致。22,24,29,30.,31即表面活性剂开始聚集成胶束结构的浓度。CMC是可预测的表面活性剂的标准平衡性质32或测量33适用于多种表面活性剂。具体来说,在浓度高于CMC时,如果有足够的时间,胶束将形成平衡浓度。然而,对于像沸腾这样高度动态的过程,我们质疑平衡描述的有效性。根据表面活性剂类型的不同,CMC可以跨越10个数量级8到102摩尔/ m3..尽管CMC的范围很大,但大多数研究17,20.,23,24,29通常使用表面活性剂(如十二烷基硫酸钠,Triton X-305, Habon G,十六烷基三甲基溴化铵等)与0.1-10 mol/m的cmc3..此外,许多现有的研究只研究单一的表面活性剂23,25,27,28,30.,34,35,36,37.因此,如果只对非常有限的一系列表面活性剂进行了狭窄的测试,那么最佳浓度与CMC一致这一结论的强度就会受到质疑。此外,以前的研究只调查了接近其CMC值的浓度(在三个数量级以内;无花果。2)——没有研究系统地观察过在很大浓度范围内的大量表面活性剂类型。
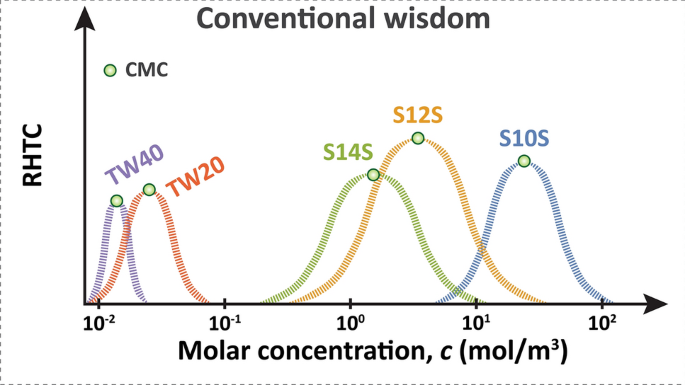
根据这些有限的浓度范围得出的结论(图。2),我们应该可以看到不同表面活性剂的CMC对应的HTC增强的最佳峰值(图。3.).
我们的工作报告了使用五种不同表面活性剂,即癸基硫酸钠(S10S)、十二烷基硫酸钠(S12S)、十四烷基硫酸钠(S14S)、吐温20 (TW20)和吐温40 (TW40)进行沸腾换热实验的结果。本研究的目的是测试RHTC中分离的最佳峰值的传统智慧(图。3.)在很大的浓度范围内。
沸腾的结果
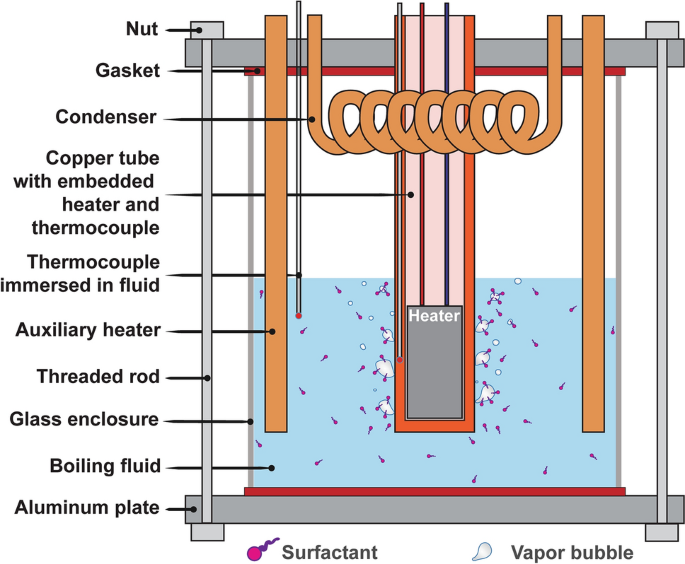
S10S、S12S、S14S、TW20和TW40表面活性剂的CMC范围为0.02 ~ 32 mol/m3.,跨越四个数量级,这比以往的研究(完整的CMC值,见表S.1,补充信息(SI))。此外,我们将浓度从0.01调整到14 mol/m3.(四个数量级)对于每一个表面活性剂(图。2),代表了与之前的工作相比表面活性剂的浓度变化和多样性最大。我们使用定制的沸腾室进行了超过150个池沸腾传热实验(详情见图)。10,S.1(SI)和方法部分;完全沸腾的结果如图。S.2SI)。
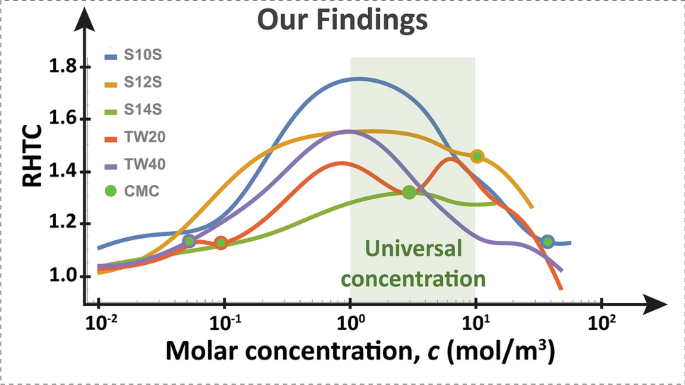
与之前的研究结果相反(图。3.),仅测量到RHTC的一个通用峰(图。4).也就是说,在不同的cmc表面活性剂上,它们都具有相似的HTC增强效应,其共同的最佳浓度范围在1-10 mol/m左右3..这个令人惊讶的结果,完全反驳了传统的关于平衡胶束化行为决定沸腾传热强化的智慧。人们预计TW40在其低CMC值(0.05 mol/m)附近有一个HTC峰值3.但我们发现它在1-10 mol/m的范围内达到峰值3..同样地,人们预计S10S的CMC比TW40大近1000倍,峰值在38 mol/m左右3.;然而,它也在1-10 mol/m的范围内达到峰值3..因此,我们发现可能存在一个与胶束化无关的强化传热的普遍浓度范围,而且一定有其他东西主要负责控制这种强化行为。
理论
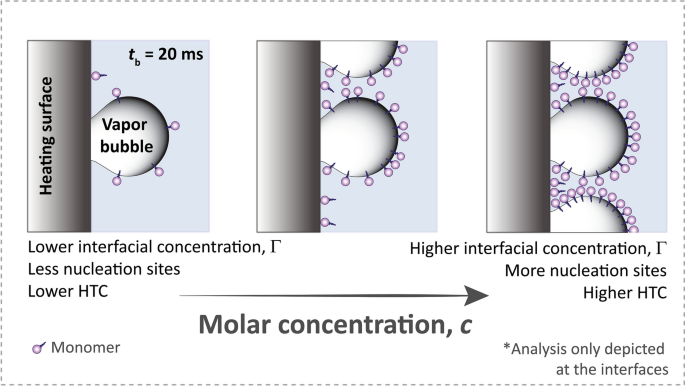
为了理解这种令人惊讶的普遍行为,我们开发了一个沸腾增强的动态描述,而不是基于CMC的平衡描述。由于在界面处通常有更多的表面活性剂(图5)。5)增强了我们之前测试的HTC38我们认为,宏达电的增强取决于在有限时间窗动态吸附中可吸附多少表面活性剂。这个时间窗对应于表面的气泡寿命,\ (t_{{\文本{b}}}识别\),根据科尔的研究估计39约为20毫秒(见理论)S.1, SI)为我们实验中遇到的沸腾条件。在这段时间内,表面活性剂从本体溶液扩散到界面。这种依赖时间的扩散行为适用于任何表面活性剂,而不考虑离子类型40.
和任何扩散问题一样,特征扩散时间尺度,\ (t_{{{文本\ {diff}}}} \),是长度的平方,\ (h ^ {2} \),除以扩散系数,\ (D \).根据Ferri & Stebe的说法40,这个长度为\(h = {\Gamma}_{{{\text{eq}}}} /c\)在哪里\ (c \)摩尔浓度和\({\伽马}_{{{文本\ {eq}}}} \)为Langmuir等温线确定的平衡表面浓度:\({\伽马}_{{{文本\ {eq}}}} ={\伽马}_{{{文本\{马克斯}}}}\压裂{{K_ c{{\文本{L}}}}} {{1 + K_ c{{\文本{L}}}}} \)在哪里\({\伽马}_{{{文本\{马克斯}}}}\)是每一个可能吸附位点被填充时的最大表面浓度(与表面活性剂分子截面积的倒数有关),\ (K_{{\文本{L}}} \)为Langmuir平衡吸附常数。因此,特征时间尺度为
在Eq. (2),当浓度高于特征朗缪尔浓度时,后一种近似成立,\(c \gg 1/K_{{\text{L}}}\),通常比CMC低几个数量级(见理论)S.2, SI,为完整推导)。\({\伽马}_{{{文本\{马克斯}}}}\),\ (K_{{\文本{L}}} \),\ (D \)分子性质随表面活性剂类型而改变(见表S.2, SI,为属性值)。然而,这两个\({\伽马}_{{{文本\{马克斯}}}}\)而且\ (D \)许多表面活性剂是否在一个数量级内变化20.,41;因此,给定一种特定的表面活性剂,扩散时间几乎完全取决于体积浓度。来自Eq. (2),\ (t_{{{文本\ {diff}}}} \)是成反比的\ \ (c ^ {2})比较气泡时间尺度与扩散时间尺度的比值,当\(t_{{\text{b}} /t_{{{\text{diff}}}} < 1\)时,表面活性剂向界面扩散较慢,吸附在界面上的表面活性剂较少。根据Eq. (2),低浓度时扩散缓慢。另一方面,如果\(t_{{\text{b}} /t_{{{\text{diff}}}} > 1\)时,扩散速度快,吸附在界面上的表面活性剂越多,对应的浓度越高(2).因此,在有限的时间窗口内吸附表面活性剂的量为\ (t_{{\文本{b}}}识别\)在扩散速率由摩尔浓度决定的情况下扩散输运受限。
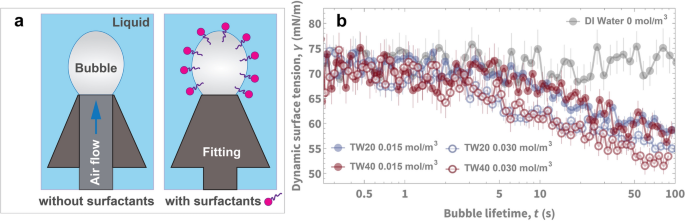
为了测试一个单独的机制是否会影响我们的沸腾数据,例如表面润湿性的变化,我们考虑了沸腾铜管随时间的长期表面降解变化。过去的研究发现了长期的氧化效应42和碳氢化合物吸附效应43会影响沸腾。在我们的测试中,我们发现沸腾前后动态接触角的变化不超过4.5°(见图5)。S.5SI)。我们还使用FE-SEM图像对沸腾表面进行了表面表征。S.6SI)。这些结果表明,表面润湿性没有发生重大变化,这将是影响我们实验结果的主要原因。除了永久的表面润湿性变化(长期的表面降解),我们还考虑了另一个润湿性方面:表面活性剂吸附在液-气和固-液界面上,改变了沸腾过程中的实际润湿性。这种表面活性剂介导的润湿效应很难描述,因为气泡动力学发生在毫秒级的时间尺度上。为了证明润湿性受时间依赖性的影响,我们进行了动态液-气表面张力测量(见图。6)在室温下的去离子水中被表面活性剂溶液包围的气泡上——这一物理场景类似于沸腾时气泡的形成。通过表征气泡的垂坠形状,我们测量了表面张力作为时间的函数。我们发现,对于两种不同类型的表面活性剂(TW20和TW40),在相同浓度(0.01 mol/m)下,它们的时间依赖性表面张力非常相似3.0.03 mol/m3.).结果如图5所示。6告诉我们,不同的表面活性剂确实以不同的浓度以相似的方式吸附在界面上,这为为什么沸腾时HTC行为出现普遍峰值提供了更多确凿的证据。为了进一步确认动态表面张力在比我们可以用实验测量的更快的时间尺度上的相似性,我们求解Ward-Tordai方程来模拟浓度高达100 mol/m时的动态表面张力3.在无花果。S.7,如果。
不同cmc和平衡表面张力的表面活性剂在相同浓度下,在短时间尺度上具有相似的动态吸附行为。我们表演(一个)动态垂泡实验测量,采用Young-Laplace拟合,(b)采用两种表面活性剂TW20和TW40在室温(25℃)下,在两种不同表面活性剂浓度的DI水中进行了时间依赖性表面张力的测试。TW20和TW40的cmc为0.05 mol/m3.0.02 mol/m3.,分别。在0.015 mol/m3.平衡表面张力分别为47.66±0.08 mN/m和43.99±0.09 mN/m。在0.03 mol/m3.平衡表面张力分别为44.22±0.09 mN/m和42.55±0.01 mN/m。尽管平衡表面张力不同,但两种表面活性剂具有相似的动态表面张力,这意味着在相同浓度下,它们具有相似的动态吸附行为。这种类似的动态吸附的时间尺度(扩散时间尺度)随着表面活性剂浓度的增加而减小。
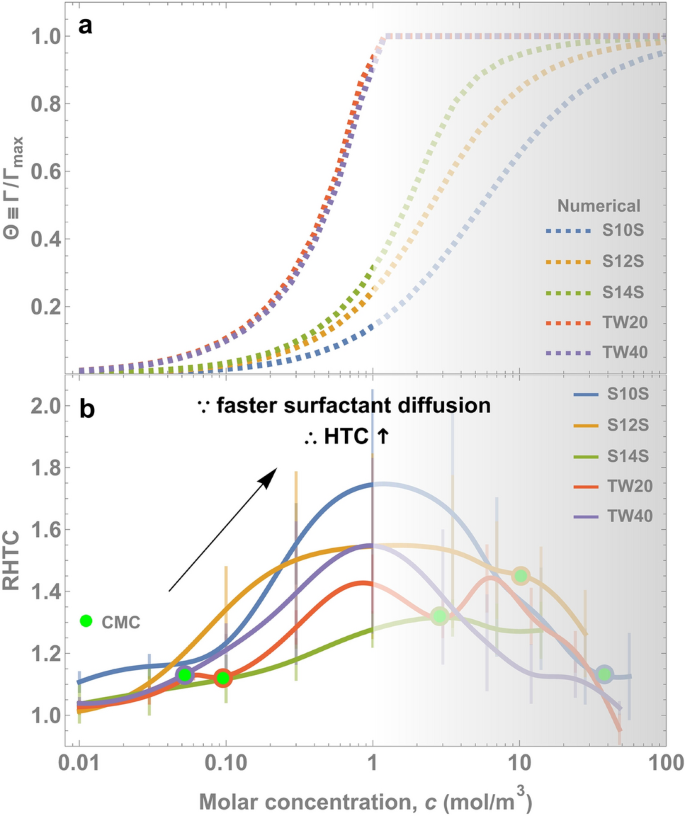
为了验证动态吸附的效果,我们计算了一个时间窗口内的精确吸附量,并将其与沸腾增强量进行了比较。我们解了沃德-托尔代方程44使用Li等人的算法。45计算动态吸附,其中表面活性剂的性质由我们之前的模型确定46.动态吸附无量纲表示为\(θ\枚\伽马\ \)/\({\伽马}_ {\ mathrm{马克斯}}\)以及利用表面活性剂的特性(见理论)S.3, SI),我们发现吸附确实与1 mol/m以下的HTC增强相一致3.(无花果。7A)所有表面活性剂都是如此。这种统一的增强行为(图。7解析:选B\({\伽马}_ {\ mathrm{马克斯}}\)而且\ (D \)许多表面活性剂是否在一个数量级内变化20.,41.结果,\ ({t} _ {\ mathrm {diff}} \)许多类型的表面活性剂对摩尔浓度的依赖性应该是相似的。
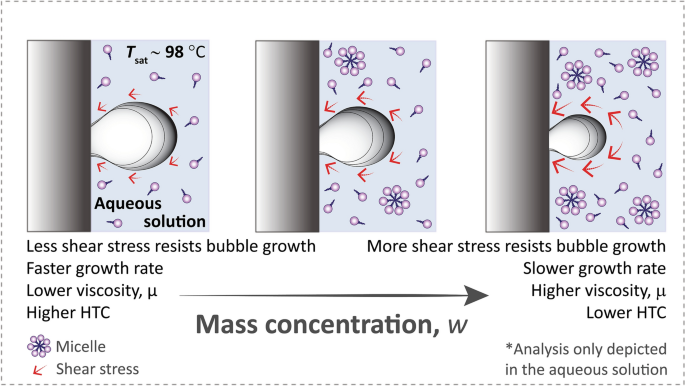
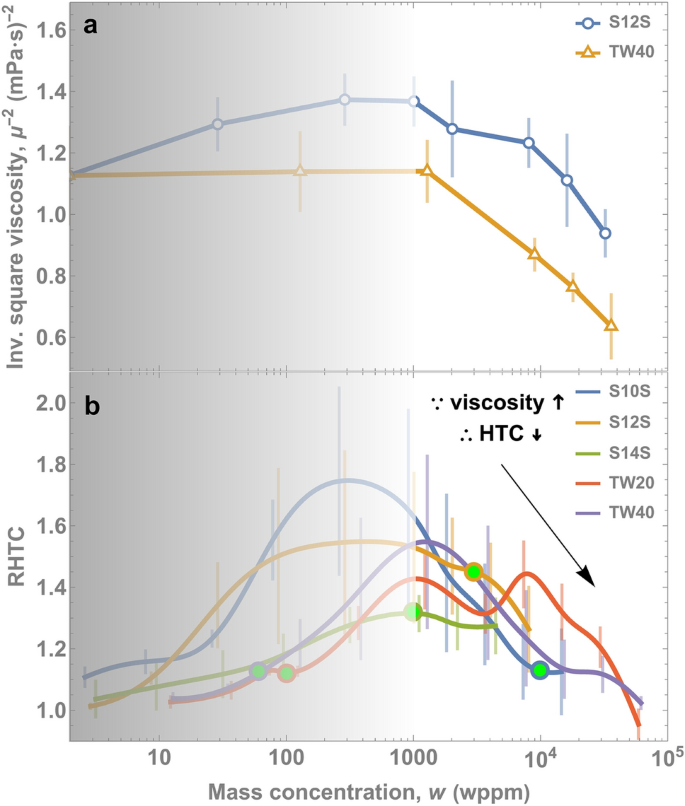
然而,这种增强不会永远持续下去。我们假设这种降解是由于粘度的增加,\μ(\ \)(无花果。8),因为表面活性剂的粘度随着浓度的增加而增加47,48和沸腾相关性表明低HTCs和高粘度49,50.具体来说,从Rohsenow相关中50, HTC与粘度的平方成反比:HTC\ \ propto \ ()\({\μ}^ {2}\).我们使用自定义粘度计,采用落球法(见方法和图)对不同浓度下TW40和S12S的粘度进行了评估。S.3SI)。我们证实了粘度在一定浓度以上确实增加了(图。S.4, SI)与之前的研究一致48.
为了说明这对HTC的影响,我们绘制了图表\({\μ}^ {2}\)在无花果。9a因为这应该与HTC成正比。的确,RHTC的下降在图中。8B是随着in的下降而变化的\({\μ}^ {2}\)在无花果。9A,支持我们的假设,增加的粘度会导致传热退化。
从这一点出发,我们通过图之间的定性相似性,建立了动态吸附与RHTC增强之间的联系,以及粘度与RHTC降解之间的联系。7A, b和9分别是A, b。为了进一步定量地确认这些联系,我们假设了一种受表面活性剂浓度影响的罗森诺沸腾相关的比例形式
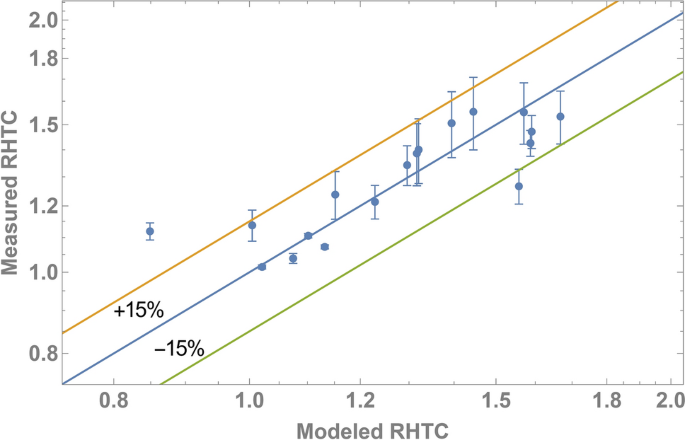
在这里,\ \ ()而且\ (b \)都是符合我们数据的正参数。方程(3.)有适当的限制,对于纯净水,\({\伽马}\离开(文本{c}}{\ \右)/{\伽马}_{{{文本\{马克斯}}}}= 0 \);的比例性降为罗森诺结果文本\ ({\ {HTC}} \ propto \压裂{1}{{\μ^{2}}}{\三角洲}T ^ {2} \).无量纲吸附,\({\伽马}\离开(文本{c}}{\ \右)/{\伽马}_{{{文本\{马克斯}}}}\),可以用Ward-Tordai方程求解。这两个\({\伽马}\离开(文本{c}}{\ \右)/{\伽马}_{{{文本\{马克斯}}}}\)而且\(\mu \左(c \右)\)是浓度的函数;\(\mu \左(c \右)\)对TW40和S12S进行了实验测定。因此,拟合比例与RHTC数据,我们能够找到一个最小二乘适合\ \ ()而且\ (b \)分别为0.77和0.18。如图所示。10时,我们可以使用Eq对RHTC进行建模。3.)误差在+ /−15%以内。这种良好的定量一致性有力地证实了表面活性剂在沸腾过程中发挥的双重作用:通过吸附增强剂和通过黏度降解剂。
(一个)质量浓度越高,粘度越高,符合Rohsenow相关性50宏达电∝μ-2.事实上,(b)随着粘度的增加,RHTC也相应下降。粘度的误差条(测量下降速度和滚珠轴承直径和密度的数据偏差的一个标准偏差)。有关错误传播的更多信息,请参见方法。
讨论
我们已经表明,与传统智慧相反,表面活性剂在沸腾中有一个相当均匀的最佳增强浓度范围。这个浓度范围与cmc无关,cmc是一个平衡性质。相反,HTC增强是由于气泡寿命有限的表面活性剂吸附,其浓度增加。这种限时吸附受描述动态质量传输的表面活性剂性质的控制:扩散系数和表面活性剂的最大表面浓度。动态表面张力测量如图所示。6,表明不同的表面活性剂确实在相似的浓度下以相似的方式吸附在界面上,这为为什么沸腾时HTC行为出现普遍峰值提供了更多确凿的证据。在很高的浓度下,HTC由于粘度的增加而降解。表面活性剂浓度高时,液体粘度的增加与传热的减少是同时发生的。9).这表明,粘性较大的体积溶液会抑制气泡的增长,从而导致气泡变小,增长速度变慢,如图所示。8,最终导致更少的传热,因为沸腾传热与蒸汽生成速率成正比。
我们通过可以添加到Rohsenow相关性的比例来量化吸附和粘度的综合效应。这种比例关系可以用的幂律表示\ \(压裂{{1 + 0.77 \离开({{\伽马}\离开(文本{c}}{\ \右)/{\伽马}_{{{文本\{马克斯}}}}}\右)^{0.18}}}{{\μ\离开(c \右)^ {2}}}\),表示分子上吸附的增强作用和分母上黏度的降解作用。我们的工作从机理和分子角度解决了表面活性剂如何增强或降低传热的重要问题。具体地说,我们强调表面活性剂增强沸腾是一个动态过程而不是一个平衡过程。从这项工作中获得的见解将为在大量的两相传热过程中结合表面活性剂增强沸腾的具体策略提供信息。
方法
池沸实验
煮沸实验是在常压(≈1atm)下用去离子水或表面活性剂水溶液在一个定制的煮沸室中进行的。11和无花果。S.1SI)。对于每个实验,热流密度从0到50 W/cm不等2.对于每个水溶液,我们评估10-12摩尔浓度,c,其中每种浓度测试三次(包括不含表面活性剂的沸腾液体;0摩尔/米3.代表去离子水),总计超过150个沸腾实验。加热表面用细砂纸仔细打磨,形成镜面般的表面光洁度(关于加热表面的详细视图,见图。S.5SI)。所有浸在沸水中的铜件都用去氧水和酒精清洗和漂洗。沸腾室的内部遵循同样的清洗程序。为了去除玻璃外壳上的有机/无机和微生物表面污染物,我们应用等离子体处理约15-30秒。我们在实验开始前(沸腾前)和测试结束后(沸腾后)评估了受热面的动态接触角。数字S.6结果表明,铜管表面的润湿性变化不明显。
粘度测量
我们用一个远离粘度计的摄像机以120帧/秒的帧率记录视频。S.3a).粘度计由3D打印的树脂部件、矩形硼硅酸盐玻璃外壳、玻璃容器背面的光源以提供足够的照明、热电偶用于测量液体的温度、磁性搅拌棒以混合液体中表面活性剂的水溶液(图)。S.3b).我们使用微移液管通过顶板上的小孔添加/去除水溶液,以达到所需的浓度值。对于粘度测量,我们使用(图。S.3B)落球(不锈钢轴承球)法。实验在24-25°C的室温下进行。我们使用一种图像处理技术,利用Wolfram Mathematica估计球轴承在一个固定区域(粉色矩形)的速度。一个定制的3D打印尺子用于像素校准和估计滚珠在设定区域内的移动距离。然后,我们根据记录的速度值估计流体的粘度。
误差计算的不确定性和传播性
图中的错误条。7b和9b表示相对HTC (RHTC)变化的一个标准偏差,由于热通量的平均值,\(问^ {\ ' \ '}\),
类似地,图中的不确定性条。9A代表粘度的一个标准偏差,\μ(\ \),计算落点速度误差的测量,\ \(ν\),滚珠轴承(直径,\ (d \),密度,ρ\ (\ \))
在本工作中,我们对每个浓度进行了三组实验,共计150多个沸腾实验。通过考虑每一种浓度下这三个实验的误差,我们评估了实验的运行到运行的可重复性。我们发现,温度变化为0.14±0.07°C,热流密度变化为0.57±0.06 W/cm2;因此,沸腾实验从一次运行到另一次运行是高度可重复的。我们还评估了实验的重复性,因为它们从表面活性剂到表面活性剂的变化。在一系列不同浓度的特定表面活性剂的实验之前,我们通过抛光和如上所述的清洁来更新表面。由于这一更新过程,接触角没有发生显著变化。S.5).对每种情况下的纯去离子水进行重复性测试,我们发现热流在2.8±1.6 W/cm内2.因此,一系列实验之间存在一定的重复性误差;然而,与我们测试的热流范围相比,这种热流的误差。
数据可用性
支持这项研究结果的数据可以在文章中找到,它补充信息,其中包含了本工作中使用的所有数据的JSON文件。
参考文献
坎德里卡,S. G. & Balasubramanian, P.流动沸腾与小通道和微通道中过渡、层流和深层流相关性的扩展。传热工程师。25, 86-93(2004)。
希弗罗,霍,X, Karayiannis, t.g.和Kenning, D. B. R.小直径管中R134a流动沸腾的传热相关性检验和模型。Int。J.热质传递。50, 5177-5193(2007)。
张伟,张晓明,张晓明。微通道流动沸腾换热的相关性研究。Int。J.热质传递。47, 5749-5763(2004)。
张文华,张文华,张文华,张文华,张文华,张文华。小通道中水沸腾临界热流密度的相关性研究。Int。J.热质传递。49, 1058-1072(2006)。
范勇,方俊。基于界面捕获方法的复杂气泡变形破碎动力学研究。Exp。第一版。多相流2021(33), 139-151(2020)。
泡沫谜题:从基础到应用。理论物理。启液体3., 110504(2018)。
王淑萍,张爱明,刘艳玲,张硕,崔鹏。气泡动力学及其应用。j .流体动力学。2018(30), 975-991(2018)。
赵洪杰,朱勇,王恩宁,朱勇。基于纳米工程材料的液-气相变传热研究。自然牧师脱线。2016(2), 1-17(2016)。
mahamudr - rahman, M, Pollack, J. & Mccarthy, M.使用低导电性材料增加沸腾传热。科学。代表。5, 1-11(2015)。
陈振宇,陈志明,陈志明。窄间隙不同模态相互作用沸腾提高流动沸腾临界热流密度。Int。J.热质传递。182, 121982(2022)。
Mata-Arenales, m.r., Sujith-Kumar, c.s., Kuo, l.s。&陈培华。池沸水中铜管表面粗糙度变化的影响。Int。J.热质传递。151, 119399(2020)。
许,c c。&陈培华。表面润湿性对纳米颗粒涂层沸腾换热临界热流的影响。Int。J.热质传递。55, 3713-3719(2012)。
Allred, t.p., Weibel, j.a . & Garimella, s.v.从超疏水表面实现高效沸腾。理论物理。启。120, 174501(2018)。
常压下圆柱管与水的池沸腾换热强化,第一部分:周向矩形开放微通道的实验结果。Int。J.热质传递。64, 1205-1215(2013)。
金俊生,吉拉尔,李俊生,尤绍明,表面粗糙度对疏水表面水沸腾换热的影响。Int。J.热质传递。118, 802-811(2018)。
梁国强。表面改性对池沸强化的研究进展。Int。J.热质传递。128, 892-933(2019)。
埃尔加南,法瓦尔,M. M. E.,阿卜杜勒-阿齐兹,R., Skr, M. H.和哈姆扎-哈利法,A.表面活性剂增强核状沸腾换热的实验研究。Ain Shams Eng。J。2, 195-209(2011)。
Dikici, B, Eno, E. & Compere, M.用环境友好的表面活性剂添加剂增强池沸腾。j .千卡。肛交。Calorim。116, 1367-1387(2014)。
程,梅韦斯,D.和卢克,A.表面活性剂和聚合物添加剂的沸腾现象:最新综述。Int。J.热质传递。50, 2744-2771(2007)。
赵洪杰,斯瑞斯特,维,布兰克施泰因,D.和王恩宁,了解triton x表面活性剂促进沸腾。在ASME 2013夏季传热会议与ASME 2013第七Int会议配套。能源可持续性会议和ASME 2013第11届会议。燃料电池科学,工程与技术,2013vol. 2(2013)。
温涛,罗建军,贾凯,吕亮。季铵型阳离子表面活性剂在铜表面强化水溶液的池沸换热。Int。J.热质传递。190, 122761(2022)。
Wasekar, V. M. & Manglik, R. M.添加剂分子量和离子性质对表面活性剂水溶液沸腾性能的影响。Int。J.热质传递。45, 483-493(2002)。
Hetsroni G。et al。表面活性剂对池沸腾中气泡生长、壁面热形态和传热的影响。Int。J.热质传递。44, 485-497(2001)。
张军,曼利克,张敏。表面活性剂水溶液中核池沸腾的添加剂吸附和界面特性。J.传热。127, 684-691(2005)。
Ammerman, c.n . & You s.m .表面活性剂加入水中引起的沸腾增强机制的测定。J.传热。118, 429-435(1996)。
邢明明,龚铮,王仁。全氟烷基表面活性剂溶液池沸腾换热实验研究。Int。J.热质传递。157, 119976(2020)。
井上田,Teruya, Y.,石井,M.和Monde, M.水和乙醇/水混合物中池沸腾传热的增强(表面活性剂的作用)。传热亚洲保留区。33, 229-244(2004)。
Najim, More, V., Thorat, A., Patil, S. & Savale, S.在金属丝加热器上使用创新的非离子表面活性剂增强池沸腾传热。Exp。小卡。流体科学。82, 375-380(2017)。
自成,郭佳强,邢南,钱伟。表面活性剂水溶液的沸腾换热。在第四届智能计算技术与自动化国际会议论文集,ICICTA 2011第2卷,第841-844页(2011)。
Hetsroni, G., Mosyak, A., Rozenblit, R., Pogrebnyak, E. & Segal, Z.垂直密闭空间中对环境影响可忽略不计的水和表面活性剂溶液的自然对流沸腾。Int。j . Multiph。流35, 20-33(2009)。
张军,曼利克,张瑞敏。阳离子表面活性剂的乙氧基化和分子量对水溶液中成核沸腾的影响。Int。J.热质传递。126, 34-42(2004)。
zeller, N. J. & Blankschtein, D.开发用户友好的计算机程序预测单一和混合表面活性剂体系的溶液性质。印第安纳州,Eng。化学。Res。34, 4150-4160(2002)。
吴,S。et al。用简单快速的滴定法测定表面活性剂的临界胶束浓度。肛交。化学。92, 4259-4265(2020)。
贾宏,徐磊,肖晓霞,钟凯。表面活性剂溶液在沟槽表面的沸腾换热研究。Int。J.热质传递。181, 121876(2021)。
尹军,肖晓霞,冯亮,钟凯,贾宏,表面活性剂溶液在双导电表面的沸腾特性实验研究。Int。J.热质传递。157, 119914(2020)。
豪达,R. K,帕塔克,M. & Kaleem Khan, M.生物表面活性剂在池沸换热强化中的应用前景。Int。J.热质传递。150, 119292(2020)。
郭德盛。et al。过冷池在水和非离子表面活性剂水溶液中沸腾过程中的气泡行为。Int。J.热质传递。159, 120087(2020)。
赵洪杰,米泽拉克,王忠平,王恩宁。在沸腾过程中使用带电表面活性剂调节气泡的开关。Commun Nat。6, 8599(2015)。
在大气压下气泡的频率和出发体积。AIChE J。13, 779-783(1967)。
哪种表面活性剂降低表面张力更快?扩散控制吸附的尺度论证。胶体界面科学。85, 61-97(2000)。
刘娟,张勇。短时间极限下空气/溶液界面亚胶束和胶束水溶液的扩散控制吸附动力学。韩国j化学。Eng。23, 699-703(2006)。
歌,Y。et al。通过原位氧化改变金属表面的池沸传热。Int。J.热质传递。185, 122320(2022)。
宋勇,张磊,刘志强,普雷斯顿,董军,王恩宁。空气中烃类吸附对池沸腾换热的影响。达成。理论物理。列托人。116, 253702(2020)。
张国强,张国强,张国强。解边界张力的时间依赖性I扩散在时间效应中的作用。j .化学。理论物理。14, 453-461(1946)。
李X,肖R,埃文斯G. M. &史蒂文森,P.非离子表面活性剂吸附Ward-Tordai方程的简单数值解。第一版。化学。Eng。34, 146-153(2010)。
赵洪杰,王恩宁,王恩宁。用统计力学方法预测表面活性剂溶液表面张力。朗缪尔34, 2386-2395(2018)。
王淑春,魏廷春,陈文波,曹宏坤,表面活性剂胶束对聚乙二醇溶液粘度和导电性的影响。j .化学。理论物理。120, 4980-4988(2004)。
王伟,王德明,雷廷格,魏,巴兹,等。聚甲基丙烯酸甲酯(PMMA)与电解质-表面活性剂水溶液接触时的Zeta电位。朗缪尔33, 10473-10482(2017)。
福斯特,H. K. & Zuber . N.蒸汽气泡动力学和沸腾传热。AIChE J。1, 531-535(1955)。
一种有关液体表面沸腾的传热数据的方法。J.流体工程74, 969-975(1951)。
确认
作者感谢Koshee Innovation和内华达大学拉斯维加斯分校(UNLV)通过启动基金和教师机会奖提供的资金支持。这篇文章的出版费用由UNLV大学图书馆开放文章基金支持。
作者信息
作者和隶属关系
贡献
M.R.M.和B.O.在设计、实验和数据管理方面贡献相同。D.L.和V.E.协助实验。mrm.和H.J.C.撰写了主要的手稿文本。H.J.C.构思并监督这项工作。
相应的作者
道德声明
相互竞争的利益
作者声明没有竞争利益。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构附属的管辖权要求保持中立。
权利与权限
开放获取本文遵循创作共用署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),该协议允许在任何媒体或格式中使用、分享、改编、分发和复制,只要您给予原作者和来源适当的署名,提供创作共用许可协议的链接,并说明是否有更改。本文中的图片或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果材料不包含在文章的创作共用许可中,并且您的预期用途不被法律法规允许或超出了允许的用途,您将需要直接从版权所有者那里获得许可。欲查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
玛塔,医学博士,奥尔蒂斯,B,卢哈尔,D。et al。动态吸附如何控制表面活性剂增强沸腾。Sci代表12, 18170(2022)。https://doi.org/10.1038/s41598-022-21313-1
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-21313-1