摘要
主要组织相容性复合体(MHC)是一组基因组成的脊椎动物免疫系统最重要的组成部分之一。因此,人们对描述MHC变异及其与多种物种适应度的关系非常感兴趣。由于MHC基因的特殊多态性,仔细的PCR引物设计对于捕获给定物种中存在的所有等位基因变异是至关重要的。因此,我们开发了内含子引物来扩增南极毛皮海豹MHC II类DQB外显子2全长267 bp的蛋白质编码序列。然后,我们对来自两个繁殖群体的母-子代间的MHC变异模式进行了表征,并从56个个体的771个克隆序列中检测出19个等位基因。个体内部和个体间的等位基因分布与孟德尔遗传的单拷贝经典DQB位点一致。MHC氨基酸相似性与全基因组亲缘性显著相关,但MHC杂合性与全基因组杂合性之间未发现相关性。最后,等位基因多样性比之前基于部分外显子序列的研究报告高几倍。这种差异似乎与等位基因特异性扩增偏倚有关,这意味着引物设计可以强烈影响MHC多样性的推断。
简介
主要组织相容性复合体(MHC)是颌骨脊椎动物免疫系统最重要的组成部分之一,包括超过280个基因,跨越人类基因组的几个百万酶1,2.许多研究已经证明了MHC基因型的功能重要性,它与许多物种的关键适应度成分的变化有关,如寄生虫易感性、生存、繁殖成功和配偶选择2,3.,4,5,6.因此,MHC基因是研究适应性遗传变异的重要候选基因。
由经典MHC基因编码的蛋白质结合来自寄生虫和病原体的外源肽,提交给t淋巴细胞,随后启动适应性免疫反应7.MHC基因家族包含两个主要的经典基因亚群,它们编码具有结构和功能相似性的免疫活性分子1.MHC I类和II类分子分别促进细胞内寄生虫如病毒和细胞外寄生虫如细菌的识别7.这两类分子都含有一个肽结合区(PBR),负责与外来肽结合。在MHC I类蛋白质中,PBR由两个α -链结构域定义,而一个α -链和一个β -链折叠在一起形成MHC II类蛋白质的PBR8.这两类MHC分子在大多数物种中都表现出异常的遗传变异性,这被认为是由病原体介导的平衡选择驱动的,在给定的种群中,每个MHC基因通常包含数十或数百个不同的等位变异2.
为了引发免疫级联,需要将MHC的PBR与抗原肽结合,因此单个MHC变体显示出对一系列肽的特异性,这些肽在固定位置上共享共同的氨基酸残基9.因此,MHC位点的杂合性可能通过增加可被识别和呈递给t细胞的抗原的多样性来增强对寄生虫和病原体的抵抗力10.因此,MHC总体上以高度多样性为特征,包括脊椎动物中描述的一些最多态的基因,这并不奇怪11.在人类中,已经有数千个等位基因被描述为最多态的MHC位点,导致核苷酸多样性超过全基因组平均水平两个数量级12,13,14.
这种模式在经典MHC基因的肽结合域上特别明显,例如MHC II类DQB和DRB位点的第二外显子,它们编码MHC II类PBR的功能重要的β-1结构域8.这些位点多态性的维持被认为是由病原体驱动的选择介导的,其中包括杂合子优势的各种机制15发散的等位基因优势16,17到负频率相关的选择11,18.通过MHC依赖的配偶选择进行的性选择似乎也是维持这些基因多样性的重要力量6,19,20..
然而,MHC基因的等位基因多样性模式在物种间表现出显著的差异。例如,亚洲黑熊在DRB上具有高度多态性,斯堪的纳维亚棕熊在DQB上具有相对高水平的多态性,而北极熊在两个基因上具有相当的多样性21,22,23,24.此外,包括独角鲸在内的几种海洋哺乳动物25南部和北部的象海豹26,27、长须鲸和长须鲸28和北极熊23似乎在DQB和/或DRB携带很少的变异。这一观察结果使一些人认为,海洋哺乳动物在海洋环境中接触到的病原体可能比陆地哺乳动物更少23,26.然而,包括座头鲸在内的一些物种29,加州海狮30.和crabeater海豹31这意味着物种特异性因素在形成MHC多样性的全球模式中发挥了重要作用。
从技术角度来看,由于用于扩增MHC等位基因的方法多种多样,从PCR引物设计的差异到大量不同的测序方法,比较不同物种间给定位点的多样性也具有挑战性,这些方法都代表着潜在的偏差来源32,33.引物设计的重要性尤其没有得到充分认识,许多研究者使用PCR引物开发并应用于之前对其他(或多或少相关的)物种的研究33.然而,这些引物可能并不总是放大感兴趣的物种中存在的所有变异,导致不可靠的基因分型33.出现这种情况主要有两个原因。首先,使用从部分外显子序列发展而来的引物将产生截断序列,这可能会排除外显子内引物结合位点侧面的可变位置。第二,引物结合位点内的遗传变异会因PCR扩增偏差而无意中导致目标等位基因的不完全检测,引物与模板不匹配会降低某些等位基因的扩增效率,最终导致等位基因多样性被低估34,35.
对MHC多样性的正确推断对于理解形成物种内部和物种间MHC变异的选择性力量显然是必不可少的33,36.然而,也有越来越多的人认识到有必要将基因组背景的潜在混淆效应纳入MHC研究。特别是,当种群内存在密切近交时,MHC杂合性可能与全基因组杂合性存在潜在的相关性37.这可能使解开MHC纯合性的影响与近交系个体中有害等位基因的暴露所导致的适应度损失具有挑战性38.此外,MHC基因的选择也会受到相关的有害突变的影响,这些突变可以由于高水平的局部杂合性而免受选择的影响39.最后,比较免疫遗传多样性和中性多样性可以为了解选择机制提供参考40.例如,相对于选择性中性位点,平衡选择倾向于增加MHC的群体内多样性,导致前者的群体结构更弱41而MHC上的多样化选择可能导致相反的模式42.
鳍足类动物非常适合研究MHC的适应性变异。尽管它们的大部分时间都在海上度过,但许多鳍类物种在陆地上高密度繁殖,在那里,由于同质物的密切接近和粪便物质的积累,它们可能会接触到各种寄生虫和病原体。此外,已经报道了鳍足类动物的多种适应度成分的杂合子-适应度相关性,包括寄生虫抗性43通过早期生存44,45伴侣的选择46和生殖成功47,48.这表明,许多健康因素受到个体遗传质量的影响,尽管其确切机制仍有待商榷49,50,51.最后,先前对鳍足类动物的研究表明,MHC基因的变异与幼鱼和成年鱼的死亡率有关52,53,54,寄生虫易感性55和生殖成功53这意味着MHC中存在强烈的自然(和潜在的性)选择。
南极海狗是一种高度一夫多妻制的鳍状动物56它们在亚南极岛屿上季节性繁殖,主要是西南大西洋的南乔治亚岛57.这个物种表现出极端的出生地点忠诚,雌性返回到其出生地点的一个体长内繁殖58,而雌雄成虫也会在季节和季节之间忠实于繁殖地59.在南乔治亚州的鸟岛进行的一项长期研究,从9个微卫星量化了杂合度与多种健康因素之间的联系,包括生存、体型和繁殖成功45,46,48,60.而基因组数据表明,这些关系可能是由于近亲繁殖萧条61,62在此基础上,MHC基因型对适应度变化的影响程度尚不清楚。可以说,MHC II类基因可能特别重要,因为细菌感染是领地雄性南极海狗死亡的主要原因63.
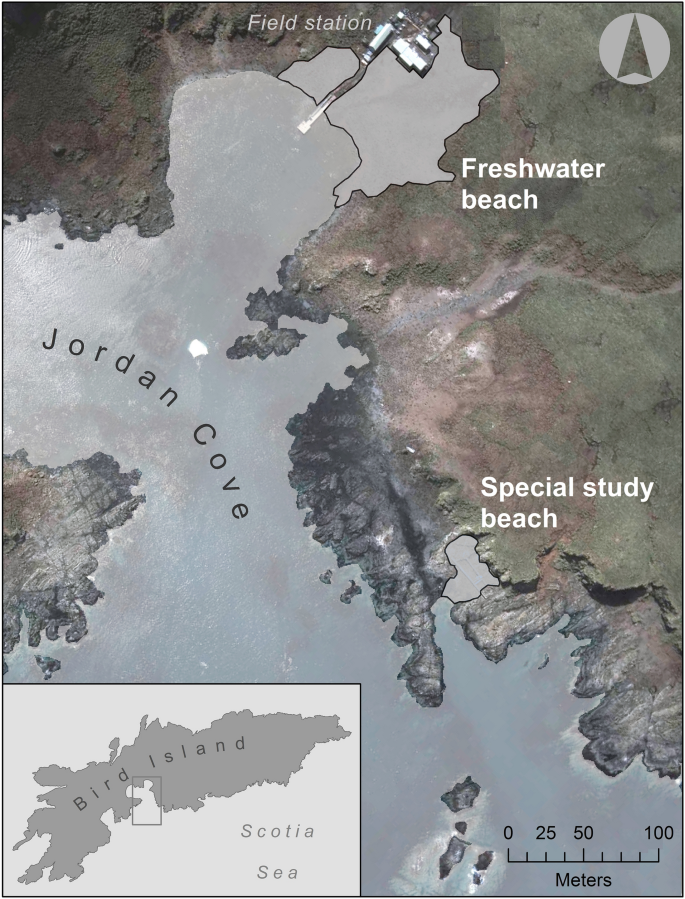
鸟岛上的两个南极海狗繁殖地64,65提供了一个机会来比较和对比MHC和中性分子标记的遗传结构和多样性模式。特别研究泳滩(SSB)与淡水泳滩(FWB)相距仅约200米(图1)。1),但在SSB繁殖的雌性的密度要高几倍(每米约1.2只vs.约0.3只)2分别)66.我们之前已经表明,SSB海豹皮肤微生物群落中致病菌的比例过高67这表明病原体驱动的选择压力可能会随着社会密度的变化而变化。因此可以想象,在SSB普遍存在的更拥挤的条件下,对特定MHC等位基因和/或MHC杂合性的选择可能更强。
南乔治亚鸟岛的地图,显示了两个南极海狗繁殖地的位置,特别研究海滩(SSB)和淡水海滩(FWB)。该数据是使用ArcGIS(版本10.3,ESRI, Redlands, CA, USA,https://www.esri.com/en-us/home)使用“自然地球数据”(https://www.naturalearthdata.com).
本研究设计了一对新颖的内含子引物,用于PCR扩增南极海狗MHC II类DQB外显子2全长蛋白编码序列。然后,我们使用经典的克隆和桑格测序方法来表征SSB和FWB的母-子对的等位基因多样性。近亲的加入减少了我们个体的有效样本量,但允许我们测试孟德尔错配,这是一种确定基因分型错误的成熟方法68.此外,同样的动物此前已经在41个微卫星上进行了基因分型69,使我们能够比较MHC的多样性模式和假定的中性遗传标记。我们假设:(i)密度依赖的选择压力可能导致MHC相对于中性位点的种群结构和/或遗传多样性的对比模式;(ii) MHC杂合性和全基因组杂合性之间的关系可能是我们研究人群中近亲繁殖存在变异的结果61,62.最后,Hoelzel等人之前的研究。70利用DQB外显子2内部的PCR引物扩增部分(141 bp)外显子序列,在鸟岛的13只南极海狗个体中发现了4个等位基因。这为我们在MHC多样性方面的研究设定了预期,尽管我们预计更大的个体样本量和全长外显子序列的结合可能会发现一些额外的等位基因。
结果
内含子PCR引物用于扩增一个459 bp的产物,其中包含完整的267 bp的MHC II类蛋白编码DQB外显子2序列,这些产物来自南乔治亚州鸟岛的两个繁殖群体的44对南极海狗母-后代(图。1).56只个体获得预期大小的PCR产物,包括20对母-子代,12只母未测序幼崽和4只母未测序幼崽(见补充表)1详情)。克隆和测序这些PCR产物产生了977个全长DQB外显子2序列的数据集。
DQB II等位基因的特征
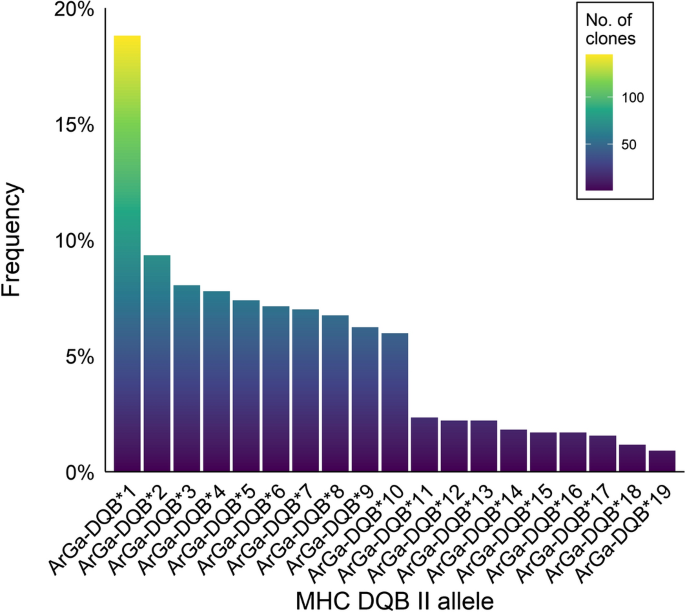
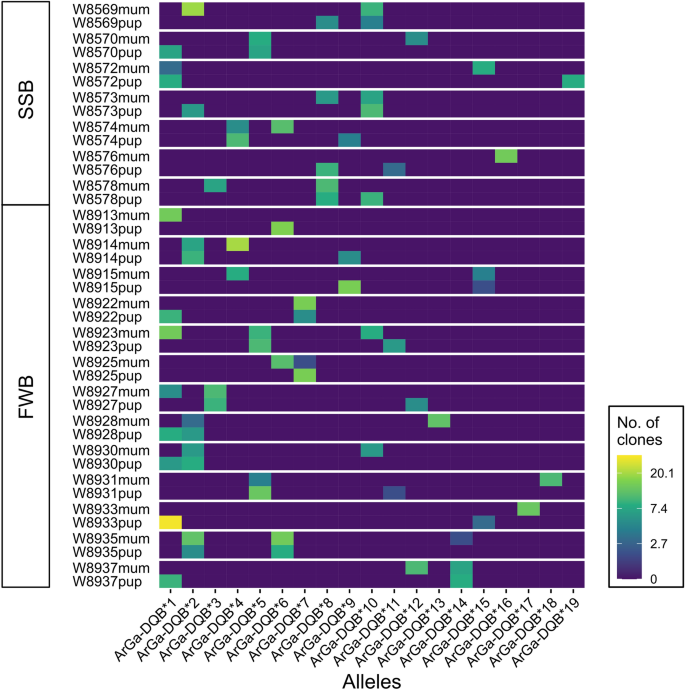
184个序列(9.3%)在整个数据集中出现过一次(即它们由一个克隆表示),另外10个序列(1.2%)出现过两次,但总是在同一个个体内。由于这些序列与更常见的序列相差一个(或最多两个)核苷酸,我们将它们归类为假定的人工制品,并将它们从数据集中过滤掉。这样总共剩下771个克隆序列(平均= 13.77,每个个体的范围= 7-32)。在这些序列中,我们鉴定出19个不同的ArGa-DQB等位基因,每个等位基因至少发生在两个个体中,并由至少7个克隆序列表示(平均= 40.6;无花果。2和补充表1).在我们最终的数据集中,除了两只动物外,所有动物都携带一个或两个ArGa-DQB等位基因(补充表1),与单个位点扩增一致。此外,对母鼠和幼鼠的基因型的比较显示,大多数配对(17/20,85.0%)至少共享一个等位基因(图1)。3.),表明这个位点遵循孟德尔遗传。
氨基酸分化与选择模式
所有19个ArGa-DQB等位基因序列转化为独特的氨基酸序列,包括整个外显子的89个氨基酸残基。氨基酸序列的比对显示没有帧移和过早停止密码子。序列比对发现核苷酸和氨基酸位置分别有34个和22个可变位点,后者包括13个可变的假定抗原结合位点(pss;补充图。1).然而,值得注意的是,pss是从与人类MHC的序列同源性中推断出来的,目前尚不清楚这些位点在抗原结合中的直接参与是否在哺乳动物中是保守的。在这些pABS密码子上,三个等位基因ArGa-DQB*01、ArGa-DQB*06和ArGa-DQB* 16和一对ArGa-DQB08*和ArGa-DQB*13分别是相同的。总体而言,配对氨基酸差异在pABS (d= 0.304, s.e = 0.079)比非pabs密码子(d= 0.066, s.e. = 0.023,t= 28.814,p< 0.001)。此外,非同义替换在pABS上发生的频率明显高于同义替换,而在非pABS密码子上则没有1),表明ABS是在平衡选择下进化的。根据这一点,最大似然系统发生树(补充图。2)揭示了ArGa-DQB等位基因在一定程度上的聚类,但也有多个南极海狗序列与其他物种的等位基因组合在一起,包括新西兰海狗(ArFo)、加利福尼亚海狮(ZaCa)和海象(OdRo),表明潜在的跨物种多态性。
菌落和遗传标记的比较
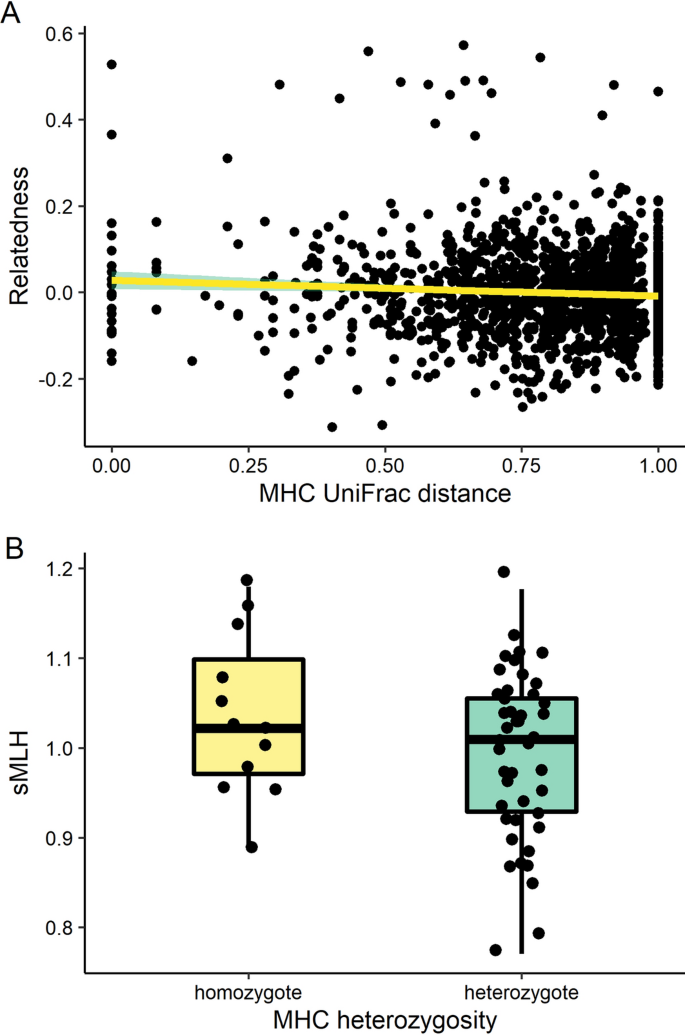
两个繁殖群体在MHC (F圣= 0.0054,p= 0.527)或41颗微卫星(F圣= 0.0028,p= 0.497)。两个群体的遗传多样性统计也相似(补充表2).在个体水平上,我们发现在MHC上的成对UniFrac距离和成对微卫星亲缘性(LME,F1538= 7.908,p= 0.005,无花果。4而MHC杂合度与微卫星杂合度无显著相关性(sMLH, Binomial GLM, χ21, 54= 64.50,p= 0.155,无花果。4B)。
与之前的研究比较
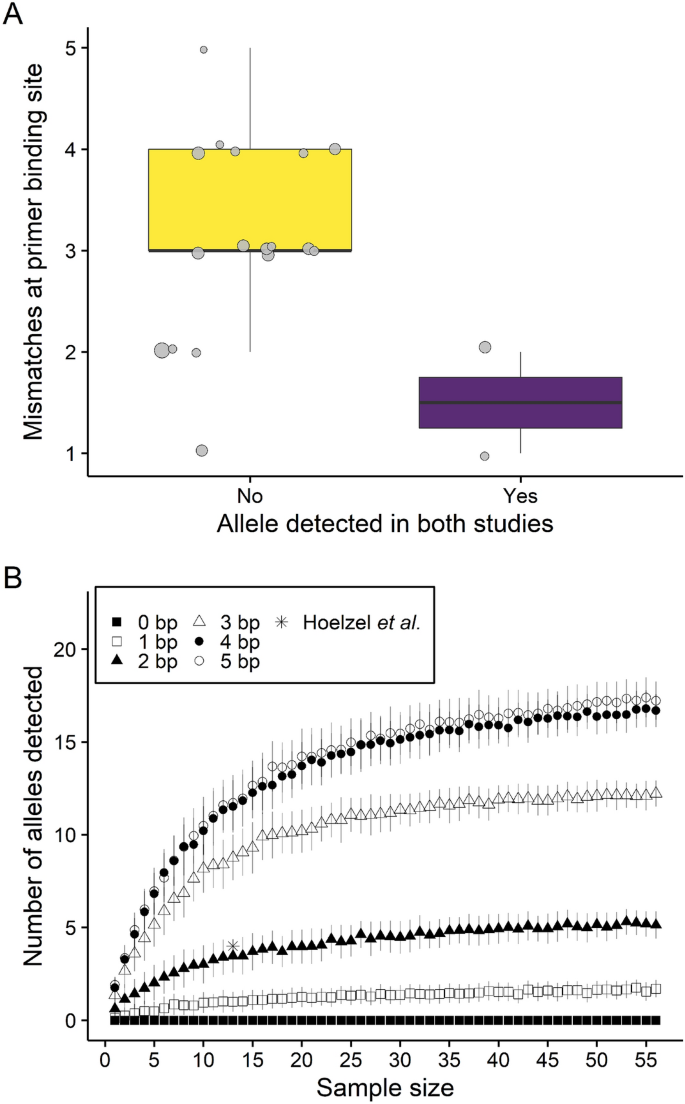
Hoelzel et al。70利用MHC II类DQB外显子2内部的PCR引物扩增了鸟岛13只南极海狗个体的4个部分(141 bp)外显子序列(其中为AFS1-4)。我们在我们的序列数据集中检测到两个这样的等位基因(AFS1 = ArGa-DQB*17和AFS2 = ArGa-DRB*06),但AFS3和AFS4在等位基因或推定的人工制品中都找不到。为了阐明两项研究在推测MHC多样性方面的差异,我们比较了Hoelzel等人使用的引物结合位点上核苷酸错配(汉明距离)的数量。70对于两项研究中共同存在的两个等位基因和仅在当前研究中发现的17个等位基因。数字5A和补充图。3.表明,新描述的等位基因在引物结合位点上的核苷酸错配比两项研究中普遍存在的等位基因多两倍。这可能表明引物结合位点的序列变化可能导致不同等位基因之间的扩增模式有偏差。为了探索核苷酸错配数量和等位基因扩增之间的联系,同时考虑到样本大小的变化,我们通过随机抽样替换的基因型计算我们数据集的等位基因检测曲线。数字5B为设置1-6个引物结合位点错配的不同阈值时,等位基因数与样本量的关系。随着样本量的增加,发现的等位基因总数迅速增加,直到在30-40个个体左右接近一个平台。对于13个个体的样本量,我们发现在检测到的等位基因数量之间显示出3个核苷酸错配与Hoelzel等人的经验值之间有合理的一致性。70,同时允许额外的不匹配导致检测到的等位基因数量增加。
讨论
我们开发了一对新的内含子PCR引物,用于扩增来自南乔治亚州鸟岛两个繁殖群的南极海狗母-后代MHC II类DQB外显子2的全长蛋白质编码序列。我们在56个个体中发现了19个ArGa-DQB等位基因,发现MHC多样性的水平出人意料地高。等位基因发现曲线表明,我们的结果与Hoelzel等人的结果之间存在差异。70不能完全归因于测序个体数量的差异。相反,目前研究中独特的许多等位基因与Hoelzel等人使用的引物结合位点的平均不匹配程度更高。70比两项研究中共有的少数等位基因更有效。一种可能的解释是引物结合位点的序列变化可能导致了等位基因扩增的偏态模式。
DQB基因发现
历史上,对非模式生物MHC基因测序的尝试往往依赖于从多个物种的部分外显子序列中设计的PCR引物。相比之下,我们能够使用南极海狗参考基因组设计内含子引物,以PCR扩增和测序全长MHC II类DQB外显子II。这似乎有助于发现比先前研究预期的更大的等位基因多样性70.具体来说,我们的研究结果表明,在南乔治亚州人群中至少存在19个ArGa-DQB等位基因。实际上,等位基因多样性可能更高,原因有二。首先,我们丢弃了由一个或两个克隆代表的序列,因为这些序列与更常见的序列主要有一个(或最多两个)核苷酸的差异,这表明它们中的大多数(如果不是全部的话)可能是PCR或测序产物,这是克隆PCR产物时的常见现象,如在MHC基因分型中71.然而,这种保守的方法可能已经导致排除了罕见的真正的等位基因,这些等位基因可能由于随机抽样效应而在我们的数据集中未被充分代表。其次,虽然我们的56个个体的样本量原则上应该允许等位基因的检测频率降低到1%左右,但真正的阈值可能更高,因为我们数据集中的许多个体都是密切相关的。因此,有可能在更大的不相关个体样本中检测到额外的等位基因,特别是如果我们可以包括来自整个物种全球分布的基因差异群体的样本62,72.
我们在目前的研究中报告的相对较高的等位基因多样性对于一夫多妻制、殖民繁殖的鳍状目来说并不一定是出乎意料的,在这种情况下,成年(但不是新生儿)死亡的主要原因是细菌感染63,73.为了研究自然选择是否能够维持这种多样性,有必要测试MHC基因型和适应性成分之间的联系,如生存、体型和繁殖成功,这些已经被认为是受该物种个体基因型影响的45,46,48,60.然而,南极海狗的MHC多样性也有可能与历史上较大的有效种群规模有关74.为了支持这一假设,一项对冰上繁殖海豹的比较研究报告称,在世界上最丰富的鳍足类食蟹海豹中,DQA等位基因多样性非常高(30个个体中有39个等位基因),而在韦德尔海豹和罗斯海豹中,多样性为中等,在豹海豹中最低31.此外,尽管由于历史上的封印,南极海狗的种群数量大幅减少,但在瓶颈期,有效种群数量可能保持在数百只72,75,76.相比之下,有记录的MHC多样性最低的鳍类动物——北方象海豹,被猎杀到只有几十个个体,这可能导致了基因漂移导致MHC等位基因的丢失27,70.
除了较高的等位基因丰富度外,我们还发现pbp中存在过量的非同义替换,这暗示了长期的平衡选择。这种模式并不出乎意料,并且与通过病原体介导的选择在进化过程中保持的等位基因多样性一致。与长期持有的观点相反,海洋哺乳动物面临较低的病原体压力26在美国,几项研究已经描述了MHC多样性对鳍足类动物的疾病易感性、生存和繁殖成功的强烈影响52,53,54,55.总的来说,这些研究表明自然选择(可能还有性选择)可能是鳍足类动物保持MHC多样性的重要力量。长期的平衡选择和/或对类似病原体的适应可能也有助于解释跨种多态性,这从鳍类物种的等位基因相似模式中可以明显看出。例如,ArGa-DQB*06和新西兰皮海豹的等位基因(AF111044.1)只不同一个核苷酸,并被翻译成相同的蛋白质序列,而一些等位基因已经在进一步的物种对中被交叉鉴定(例如加利福尼亚海狮和加拉帕戈斯海狮[AF503397-398, AF503400-402, AF503406和HE663128],南方象海豹和澳大利亚海狮[AF111038和KP127614.1])。
单拷贝孟德尔遗传位点的证据
MHC位点经常重复,鳍足类动物似乎也不例外。例如,灰海豹个体在DQB外显子2上携带多达4个等位基因,表明至少存在两个位点77而在加州海狮身上至少发现了7个DRB基因座30..相比之下,我们发现56个个体中有54个(96.5%)携带一个或两个ArGa-DQB等位基因,指向一个单拷贝的经典DQB位点。对大多数亲子对的孟德尔遗传的观察进一步支持了这一点。目前还不清楚为什么两个个体(都是母亲)各自扩增了三个等位基因。一种可能的解释是样品交叉污染,在这种情况下,有关个体的基因型(见补充表)1)就表明发生了两起独立的污染事件。不管确切的解释是什么,在这两种情况下,至少有一个母亲的等位基因与她的后代共享,这表明一些母亲和后代的等位基因被正确地描述了。另一种可能是MHC II类DQB外显子2的拷贝数变化。来自未来研究的更大的数据集可能会在这方面提供更多的信息。
更普遍地,我们发现母亲和后代之间的孟德尔不匹配率很低,20对中只有3对表现出不兼容的ArGa-DQB基因型。我们可以确信,这些不匹配不是由于母体-后代对在该领域被错误地识别78因为在目前的研究中,所有的母亲都在41个微卫星位点上与她们的幼崽相匹配。相反,这三位母亲似乎都是纯合的等位基因,而这种等位基因并没有与她们的后代共享。对这种模式最明显的解释是,这些母亲实际上是与后代共享的等位基因的杂合子,但由于随机等位基因缺失或由于PCR扩增偏倚,这些等位基因在我们的克隆数据集中没有被检测到,这可能导致某些等位基因的优先扩增。在使用能够筛选有限数量克隆的经典方法的研究中,两者都被认为是基因分型错误的来源36.
人口结构
用来推断MHC选择的一种方法是比较MHC基因和中性位点的群体结构强度。例如,在苏格兰灰海豹中,DQB外显子2在种群间表现出更强的分化,但比微卫星更弱的距离隔离模式,这被解释为栖息地特定的选择压力影响繁殖种群的遗传组成的证据77.因此,我们测试了两个社会密度不同的南极毛海豹群体之间的遗传差异。因为高的社会密度往往与接触寄生虫和病原体的风险增加有关79,我们假设来自这两个地方的动物可能在MHC经历了截然不同的选择压力。然而,我们在MHC和41个微卫星上都没有发现任何遗传差异,在这两种类型的标记上,种群结构可以忽略不计,遗传多样性具有可比性,无论是总体上还是当成人与后代分开考虑时。这种在中性标记上的分化的缺乏暗示了强烈的出生哲学58和成人网站的保真度59这种物种的数量不足以产生精细的种群结构。此外,来自两个群体的动物在MHC等位基因频率或MHC杂合性上没有任何明显差异,这表明在MHC上的选择强度可能不随社会密度的变化而变化。然而,我们在这方面的推断是有限的,因为我们的个体样本量有限,以及对该物种中病原体接触和免疫活性的密度依赖性模式的知识有限。
MHC基因型与基因组背景的关系
相对较少的非模式生物研究将MHC测序与全基因组分布式、选择性中性标记(如微卫星)的基因分型相结合38.因此,我们对MHC基因型与全基因组亲缘性和杂合性模式之间的关系的了解仍然有限,这对于理解配偶选择和近交系繁殖萧条具有重要意义。我们检测到从微卫星推断的基因亲缘关系和MHC的UniFrac距离之间微弱但显著的关联。这揭示了MHC基因型参与南极海狗遗传亲缘信号传递的可能性,这可能有助于解释该物种的雌性能够对不相关和杂合的伴侣进行择偶的能力46.然而,MHC杂合性与微卫星杂合性之间没有明显的关系,尽管微卫星携带着明确的身份不平衡信号69这表明它们捕捉到了研究种群内近亲繁殖的变异。尽管来自更多中性标记的数据可以让我们更加确信缺乏相关性,但从表面上看,这一发现表明MHC杂合性与近亲繁殖无关。这可能对解释适合度的变化有影响,因为近交系个体不一定在MHC上更纯合子。因此,如果在MHC上的选择有助于该物种的适应度变化,那么MHC基因型的任何影响都可能独立于近交萧条导致的适应度损失发生。
估计比较多样化
推测的MHC II类DQB外显子2的等位基因多样性大大高于此前报道的该物种70.虽然我们对这种差异没有明确的解释,但我们的序列数据清楚地表明,Hoelzel等人的引物结合位点。70在鸟岛的南极毛海豹中是不同的。此外,我们新描述的等位基因在Hoelzel等人的引物结合位点平均表现出更多的不匹配。70比两项研究中常见的等位基因要多。对这种模式的一种解释可能是偏等位基因扩增,这在目前的研究中似乎相对不重要,因为使用的引物退火到变量较少的侧面内含子。这与一项元条形码研究的发现一致,该研究可以解释不同节肢动物物种放大成功的80%左右的变化,通过物种特异性启动区域和通用引物之间的不匹配的数量35.另外,Hoelzel等人分析样本的确切地点和时间也不清楚。70虽然它们似乎来自长期研究群体(SSB),而且它们必须是在发表年份(即1999年)之前收集的。因此,推测出的MHC多样性的差异可能是来自不同时间点和地点的样本的反映,尽管这似乎不太可能,因为种群结构,至少在局部,看起来相当脆弱62,69,72.不管确切的解释是什么,我们的研究结果进一步支持了引物设计对多态基因等位基因多样性的准确评估至关重要的论点。重要的是,多物种对齐不一定能提供种内变异的信息。然而,这个问题可以通过预先筛选在预定引物结合位点的种内变异的焦点物种或群体来避免。由于全基因组重测序数据的不断增加,这种方法正变得越来越可行。
未来的视角
虽然克隆和桑格测序不能对大量的个体进行基因分型,但我们所采用的方法在研究的初步阶段是常见的,并产生了一个已知等位基因的目录,可用于验证用其他方法获得的结果33.我们的ArGa-DQB等位基因目录比我们最初预期的要大一些,但几行证据表明,即使不是所有的特征等位基因,大部分也可能是真实的。最明显的是,它们都是从多个个体中克隆出来的,除了少数例外,它们似乎符合孟德尔遗传。此外,核苷酸分化和系统发育聚类的总体模式与自然选择和跨种多态性的预期模式一致。未来的研究应该着眼于使用更大的个体样本来调查MHC基因型和适应度之间的关系,最好是在控制全基因组效应的同时,例如使用最近开发的85k SNP阵列61.另一个有前途的研究途径是测试MHC在化学交流中的作用69和配偶选择46.
方法
组织取样和DNA提取
样本来自南乔治亚州鸟岛(54°00′24.8″S, 38°03′04.1″W)的两个繁殖群落(SSB和FWB),共88只南极毛海豹个体(44对母幼)。2011年繁殖季节,作为英国南极调查局(BAS)长期监测和调查项目的年度例行程序的一部分进行了采样。Hoelzel等人分析样本的时间和地点尚不清楚。70收集的样本,尽管这些样本很可能来自于SSB,而且采样必须在1999年之前进行。在目前的研究中,用仔猪耳切钳从前鳍指间缘取皮肤样本,保存在- 20℃的20%二甲基亚硫酸钠饱和溶液中。随后使用改进的氯仿/异戊醇提取方案提取DNA81.
dqb特异性引物的开发
从多个鳍类物种中提取MHC II类DQB外显子2序列(见补充表)3.获取详细信息)并在BioEdit中对齐82.结果对齐后修剪到267 bp,对应整个蛋白质编码外显子2序列,并映射到南极毛皮海豹参考基因组(版本1.0)。83使用BLAST e值1e8一个字的大小是7。结果显示,该蛋白编码外显子2序列的所有267个核苷酸都匹配成功,且不存在缺口(Contig 48, 1,937,070-1,937,336)。然后设计内含子引物,利用Primer3Plus扩增全长的第二外显子84除了将熔化温度的最低和最高分别定义为60°C和65°C,并将GC含量限制在35-65%。该方法在第二外显子序列的保守侧区识别出正向引物和反向引物(ArGa-DQB_F: 5 ' - gctgttggttgggctgag, ArGa-DQB_R: 5 ' - CCACCTCAGCAGGAACAGTG)。这些引物使用BLAST对南极海狗参考基因组进行了唯一的映射,e值为10,单词大小为14,预计可以产生459 bp的单个产物。
PCR扩增、克隆和测序
PCR反应使用5 μL KAPA HiFi HotStart ReadyMix (KAPA Biosystems, Boston, united States)、1 μL基因组DNA和2 μL每个引物(1 μM),总体积为10 μL。使用TProfessional标准热循环仪(Biometra GmbH, Göttingen, Germany)进行热循环,包括在95°C下进行5分钟的初始变性步骤,然后在95°C下进行30秒变性30个循环;70℃退火1分钟,72℃延伸1分钟。最后一个延伸步骤在72℃下进行7分钟,随后冷却到4℃。所有样本PCR扩增三次,每个PCR产物分别取1 μL在标准的2%琼脂糖凝胶上扩增成功。
PCR产物用NucleoSpin进行纯化®提取II试剂盒(machery - nagel, Düren,德国),用1u taq -聚合酶和0.13 mM dNTPs(均为Qbiogene,海德堡,德国)孵育。我们将扩增的MHC片段克隆到电胜任大肠杆菌细胞(ElectrocompTM TOP10细胞,Invitrogen)使用TOPO TA克隆®测序试剂盒(Invitrogen)。使用标准T3或T7引物和BigDye在ABI 3100或ABI 3130自动测序仪(Applied Biosystems, Foster City, CA, USA)上对细菌质粒插入物进行测序®终结者v3.1周期测序试剂盒(应用生物系统)。
序列分析
使用MEGA 10.1.8版本对单个克隆核苷酸序列进行比对85.每个序列的测序跟踪文件都被手动检查是否有歧义核苷酸,并在必要的地方进行更正。然后将所有的核苷酸序列与南极海狗参考基因组的MHC II类DQB外显子2进行对齐,使用MEGA中的ClustalW实现(缺口打开惩罚15.00;间隙扩展惩罚6.66对两对齐和多次对齐),随后修剪到270 bp的长度。然后我们使用Biostrings包86由Bioconductor项目分发,构建定制函数来处理R中的序列数据。
群体分化与遗传多样性
我们生成了遗传多样性统计数据(私有等位基因的数量,等位基因丰富度,观察到的和预期的杂合度和F是)为两个使用近亲繁殖的蜂群87, adegenet88,素食89和hierfstat90.用计算的方法检测了两个菌落之间的遗传分化F圣分别为MHC和41颗微卫星,在Weir和cockham之后91hierfstat之内。通过排列原始数据9999次来确定统计显著性,以创建一个模拟的空分布F圣值和ade492.我们对所有个体的MHC UniFrac距离和微卫星相关性进行了成对量化。UniFrac是一种基于系统发育距离的对之间的总未共享分支长度的比例的距离度量。为了进行这一分析,我们首先使用MEGA中的邻居连接模型建立了本研究中识别的MHC II类DQB外显子2等位基因的系统发育树85而将p-距离来解析两个序列不同的核苷酸位点的比例。从41颗Queller和Goodnight的微卫星中计算成对的基因亲缘关系r使用Demerelate93.此外,我们利用inbreedR量化了MHC单倍型杂合性(1 =杂合,0 =纯合)以及微卫星的标准化多位点杂合性(sMLH)87.为了检验在MHC处的成对UniFrac距离和亲缘性之间的关联,我们构建了一个线性混合效应模型(LME),在该模型中,我们通过将两个被比较个体的身份作为随机效应来控制成对观察的非独立性。为了检验MHC杂合度和sMLH之间的关系,我们使用了二项广义线性模型(GLM)。统计学意义的确定使用F-test在LME和一个χ2-测试在GLM。
测试选择
核苷酸序列与加州海狮的全长DQB序列对齐,并修剪到Brown等人的第二外显子阅读框。8,得到267 bp的DQB外显子2序列。使用改进的带有Jukes-Cantor校正的内- gojobori模型估计MEGA中同义(dS)和非同义(dN)替换率。计算了整个外显子以及单独的假定抗原结合位点(pABS;24个密码子)和非pabs(65个密码子)。以Brown等人为参照,鉴定了paabs的密码子。8.然而,应该注意的是,这些假定的抗原结合位点在哺乳动物MHC II类分子之间的同源性仍然是假设的。通过使用基于密码子的z检验(999个自举复制)对中性选择和阳性选择进行检验,评估差异的显著性。
系统发育重建
MHC class II DQB外显子2序列来自南极海狗、各种其他鳍类动物和狗(犬属狼疮后裔)使用MEGA的ClustalW算法进行对齐。然后,我们用最大似然方法和Jukes-Cantor模型构建了一个系统发育树。
引物结合位点错配及等位基因检测模拟
我们将本研究中发现的等位基因的引物结合位点错配与Hoelzel等人发现的等位基因进行了比较。70.我们根据核苷酸与引物结合位点不匹配的数量(最大汉明距离)使用不同的阈值对等位基因进行分类。在自举方法中,我们对带有替换的经验基因型进行随机抽样,从1到56个样本,每个样本有999个替换,以计算在允许错配的指定阈值内检测到的等位基因的数量及其平均值和标准差。
动物伦理
根据英国南极考察队在南乔治亚岛实地活动的科学研究许可,并根据《濒危野生动植物种国际贸易公约》(CITES)收集和保留了样本。所有的现场程序都得到了英国南极调查动物福利和伦理审查机构的批准。PEA6)。
数据可用性
微卫星和MHC II类DQB外显子2基因型可通过Zenodo (https://doi.org/10.5281/zenodo.6534955).19个MHC等位基因的序列可通过Genbank获得(登录号为ON060886-ON060904)。
代码的可用性
用于分析数据的代码和附带的文档可作为Rmarkdown格式的PDF文件(电子补充材料,文件S1,https://github.com/tebbej/ArGa_MHC_DQB_R).
参考文献
Kumánovics, A. Takada, T. & Lindahl, K. F.哺乳动物MHC的基因组组织。为基础。启Immunol。21, 629 - 657。https://doi.org/10.1146/annurev.immunol.21.090501.080116(2003)。
Radwan, J., Babik, W., Kaufman, J., Lenz, T. L. & Winternitz, J. MHC多态性的进化理解进展。趋势麝猫。36, 298 - 311。https://doi.org/10.1016/j.tig.2020.01.008(2020)。
主要组织相容性复合体的进化生态学。遗传96, 7-21。https://doi.org/10.1038/sj.hdy.6800724(2006)。
伯纳切斯,L.和兰德里,C.对非模式脊椎动物的MHC研究:15年来我们对自然选择学到了什么?j .另一个星球。医学杂志。16, 363 - 377(2003)。
免疫基因变异(MHC)在进化生态学和保护中的重要性。前面。黑旋风。216。https://doi.org/10.1186/1742-9994-2-16(2005)。
配对偏好与主要组织相容性复合体基因的进化。点。Nat。153, 145 - 164。https://doi.org/10.1086/303166(1999)。
Neefjes, jonsma, m.l.m, Paul, P. & Bakke, O.对MHC I类和MHC II类抗原呈递的系统理解。启Immunol Nat。11, 823 - 836。https://doi.org/10.1038/nri3084(2011)。
布朗,j . H。et al。人II类组织相容性抗原HLA-DR1的三维结构。自然364, 33-39。https://doi.org/10.1038/364033a0(1993)。
Lafuente, E. & Reche, P. mhc肽结合预测:一个系统和全面的概述。咕咕叫。制药。Des。15, 3209 - 3220。https://doi.org/10.2174/138161209789105162(2009)。
Penn, D. J, Damjanovich, K. & Potts, W. K. MHC杂合性对多株感染具有选择性优势。Proc。国家的。学会科学。美国的一个。99, 11260 - 11264。https://doi.org/10.1073/pnas.162006499(2002)。
Hughes, a.l., Hughes, m.k, Howell, c.y. & Nei, M.哺乳动物II类主要组织相容性复合体位点的自然选择。费罗斯。反式。r . Soc。Lond。爵士。B-Biol。科学。345, 359 - 367(1994)。
Gaudieri, S., Dawkins, R. L., Habara, K., Kulski, J. K.和Gojobori, T.在人类主要组织相容性复合体中的SNP谱揭示了核苷酸多样性的极端和中断水平。基因组Res。10, 1579 - 1586。https://doi.org/10.1101/gr.127200(2000)。
加里根,D.和赫德里克,P. W.检测自适应分子多态性:从MHC的教训。进化57, 1707 - 1722。https://doi.org/10.2307/3448697(2003)。
罗宾逊,J。et al。区分功能多态性与> 10000 HLA-A, -B和-C等位基因序列的随机变异。公共科学图书馆麝猫。13, e1006862。https://doi.org/10.1371/journal.pgen.1006862(2017)。
主要组织相容性复合体抗原的生物学作用。《柳叶刀》305, 1406 - 1409。https://doi.org/10.1016/s0140 - 6736 (75) 92610 - 0(1975)。
Wakeland,公司e·K。et al。MHC II类基因的祖先多态性:发散等位基因优势。Immunol。Res。9, 115 - 122。https://doi.org/10.1007/bf02918202(1990)。
MHC ii抗原结合的计算预测支持发散的等位基因优势,并解释了跨物种多态性。进化65, 2380 - 2390。https://doi.org/10.1111/j.1558-5646.2011.01288.x(2011)。
MHC基因座的超显性与频率依赖性选择。遗传学132, 861 - 864。https://doi.org/10.1093/genetics/132.3.861(1992)。
乔丹,W. C.布鲁福德,M. W.配偶选择与MHC的新视角。遗传81, 239 - 245。https://doi.org/10.1038/sj.hdy.6884280(1998)。
主要组织相容性复合体、性选择和配偶选择。为基础。启生态。另一个星球。系统。37, 159 - 186(2006)。
Goda, N., Mano, T., Kosintsev, P., Vorobiev, A. & Masuda, R.棕熊MHC II类DRB基因的等位基因多样性(熊属arctos)和Ursidae科内DRB序列的比较。组织抗原76, 404 - 410。https://doi.org/10.1111/j.1399-0039.2010.01528.x(2010)。
Kuduk, K。et al。棕熊主要组织相容性复合体I类和II类基因的进化。BMC另一个星球。医学杂志。12, 197年。https://doi.org/10.1186/1471-2148-12-197(2012)。
韦伯,d S。et al。北极熊低MHC变异:面对北极变暖的影响?动画。Conserv。16, 671 - 683(2013)。
Yasukochi, Y.,黑崎,T., Yoneda, M.,小池,H. & Satta, Y.日本黑熊MHC II类DQB多样性熊属主干多糖类化合物.BMC Evolut。医学杂志。12, 230年。https://doi.org/10.1186/1471-2148-12-230(2012)。
穆雷,B. W,马利克,S. &怀特,B. N.白鲸主要组织相容性复合体位点DQ β的序列变异(Delphinapterus莱夫卡斯岛).摩尔。杂志。另一个星球。https://doi.org/10.1093/oxfordjournals.molbev.a040238(1995)。
Slade, R. W. Limited南方象海豹的MHC多态性:对MHC进化和海洋哺乳动物种群生物学的影响。Proc,杂志。科学。249, 163 - 171。https://doi.org/10.1098/rspb.1992.0099(1992)。
韦伯,D. S,斯图尔特,B. S, Schienman, J. &雷曼,N.北方象海豹三个II类位点的主要组织相容性复合体变异。摩尔。生态。13, 711 - 718。https://doi.org/10.1111/j.1365-294x.2004.02095.x(2004)。
Trowsdale, J., Groves, V. & Arnason, A.鲸鱼的MHC多态性有限。免疫遗传学29, 19到24。https://doi.org/10.1007/bf02341609(1989)。
贝克,c . S。et al。须鲸(须鲸亚目)MHC DQB和drb样基因的多样性和复制。免疫遗传学58, 283 - 296。https://doi.org/10.1007/s00251-006-0080-y(2006)。
鲍文,L。et al。加州海狮体内MHC-DRB区域构型变化所产生的第II类多样性(Zalophus californianus).免疫遗传学56, 12日到27日。https://doi.org/10.1007/s00251-004-0655-4(2004)。
雷曼,N.,德克尔,D. J.和斯图尔特,B. S.南极酸种主要组织相容性复合体II类等位基因变异的分歧模式。j .哺乳动物。85, 1215 - 1224(2004)。
lt, J., Van Oosterhout, C. & Bentzen, P.对多基因家族从头基因分型的NGS分析的评论。摩尔。生态。23, 3957 - 3972。https://doi.org/10.1111/mec.12843(2014)。
非模式脊椎动物的MHC基因分型方法。摩尔生态Resour10, 237 - 251。https://doi.org/10.1111/j.1755-0998.2009.02788.x(2010)。
Marmesat, E., Soriano, L., Mazzoni, c.j, Sommer, S. & Godoy, J. A.利用高通量测序方法在多基因家族中进行全等位基因调用的PCR策略。《公共科学图书馆•综合》11, e0157402。https://doi.org/10.1371/journal.pone.0157402(2016)。
Piñol, J., Mir, G., Gomez-Polo, P. & Agustí, N.万能和阻塞引物错配限制了高通量DNA测序用于节肢动物定量元条形码的使用。摩尔。生态。Resour。15, 819 - 830。https://doi.org/10.1111/1755-0998.12355(2015)。
Sommer, S., Courtiol, A. & Mazzoni, C. J.使用下一代测序对非模式生物进行MHC基因分型:处理人工制品和等位基因缺失的新方法。BMC染色体组。14542(2013)。
罗伯茨,S. C,黑尔,M. L. &皮特里,M.杂合性与遗传相似性度量之间的相关性:理解配偶选择的意义。j .另一个星球。医学杂志。19, 558 - 569。https://doi.org/10.1111/j.1420-9101.2005.01003.x(2006)。
Thoß, M., Ilmonen, P., Musolf, K. & Penn, D.。主要组织相容性复合体杂合性提高繁殖成功率。摩尔。生态。20., 1546 - 1557。https://doi.org/10.1111/j.1365-294x.2011.05009.x(2011)。
MHC进化的新理论:超越免疫基因的选择。Proc。r . Soc。B:生物。科学。276, 657 - 665。https://doi.org/10.1098/rspb.2008.1299(2009)。
斯普金,L. G. &理查森,D. S.病原体如何驱动遗传多样性:MHC,机制和误解。Proc Sci杂志277, 979 - 988。https://doi.org/10.1098/rspb.2009.2084(2010)。
席鲁普,魏可曼斯,张文华,等。平衡选择下多等位基因位点细分对变异的影响。麝猫。Res。76, 51 - 62。https://doi.org/10.1017/s0016672300004535(2000)。
李文华,李文华,李文华,等。局部选择、平衡多态性和背景选择对细分群体遗传多样性平衡模式的影响。麝猫。Res。70, 155 - 174。https://doi.org/10.1017/s0016672397002954(1997)。
Acevedo-Whitehouse, K, Gulland, F, greg, D. & Amos, W.近亲繁殖:加利福尼亚海狮的疾病易感性。自然422, 35岁。https://doi.org/10.1038/422035a(2003)。
科特曼,D. W.,鲍恩,W. D.和赖特,J. M.港湾海豹幼崽的出生体重和新生儿存活率与微卫星测量的遗传变异呈正相关。Proc,杂志。科学。265, 803 - 809。https://doi.org/10.1098/rspb.1998.0363(1998)。
福卡达,J. &霍夫曼,J. I.气候变化在下降的海狗种群中选择了杂合性。自然511, 462 - 465。https://doi.org/10.1038/nature13542(2014)。
霍夫曼,福卡达,特拉森,P. N. &阿莫斯,W.雌性海狗对杂合子和无亲缘关系的雄性海狗表现出积极的选择。自然445, 912 - 914(2007)。
阿摩司,W。et al。亲缘关系对生育成功的影响。Proc,杂志。科学。268, 2021 - 2027。https://doi.org/10.1098/rspb.2001.1751(2001)。
霍夫曼,J. I.,博伊德,I. L.和阿莫斯,W.探索南极海狗亲缘关系和雄性繁殖成功之间的关系Arctocephalus gazella.进化58, 2087 - 2099(2004)。
近亲繁殖的微卫星测量:一个元分析。进化57, 971 - 983。https://doi.org/10.1111/j.0014-3820.2003.tb00309.x(2003)。
查普曼,J. R.,中川,S.,科尔特曼,D. W., Slate, J.和Sheldon, B. C.动物群体杂合性-适应度相关性的定量综述。摩尔。生态。18, 2746 - 2765。https://doi.org/10.1111/j.1365-294X.2009.04247.x(2009)。
Szulkin, M., Bierne, N., David, P.杂合子-适合度相关性:重新评估的时间。进化64, 1202 - 1217。https://doi.org/10.1111/j.1558-5646.2010.00966.x(2010)。
da Assunção Soares Franco, M., Hoffman, J. I., Harwood, J. & Amos, W.灰海豹MHC基因型和近确定性死亡率。科学。代表。2659(2012)。
Lenz, T., Müller, B., Trillmich, F. & Wolf, J. B. W. MHC-DRB的发散等位基因优势通过直接和母系基因型效应及其对等位基因池组成和交配的影响。Proc。r . Soc。Lond。爵士。B-Biol。科学。280, 20130714(2013)。
奥斯本a·J。et al。MHC DRB的杂合子优势可能影响对传染病的反应。摩尔。生态。24, 1419 - 1432。https://doi.org/10.1111/mec.13128(2015)。
Acevedo-Whitehouse, K, Gulland, F. m.d. & Bowen, L. MHC II类DRB多样性预测抗原识别,并与加州海狮自然感染的疾病严重程度相关钩端螺旋体interrogans.感染。麝猫。另一个星球。57, 158 - 165(2018)。
霍夫曼,J. I.,博伊德,I. L.和阿莫斯,W.南极毛海豹的雄性生殖策略和母性地位的重要性Arctocephalus gazella.进化57, 1917 - 1930。https://doi.org/10.1111/j.0014-3820.2003.tb00598.x(2003)。
繁殖的南极毛海豹幼崽的生产和分布(Arctocephalus gazella)在南乔治亚州。Antarct。科学。5, 17-24。https://doi.org/10.1017/s0954102093000045(1993)。
南极雌性海狗的极端出生亲缘关系(英文版)Arctocephalus gazella).Mamm。医学杂志。77, 71 - 73。https://doi.org/10.1016/j.mambio.2011.09.002(2012)。
霍夫曼,J. I.,特拉森,P. N.和阿莫斯,W.基因标记揭示了南极领地雄性毛海豹的极端位点忠诚Arctocephalus gazella.摩尔。生态。15, 3841 - 3847。https://doi.org/10.1111/j.1365-294X.2006.03053.x(2006)。
霍夫曼,J. I.,福卡达,J.和阿莫斯,W.长牙:南极海狗的犬齿大小和杂合性之间的强正相关Arctocephalus gazella.j .她。101, 527 - 538(2010)。
Humble, E., Paijmans, A. J., Forcada, J. & Hoffman, J. I.一个85K SNP阵列在南极海狗繁殖群体中发现了近亲繁殖和神秘的亲缘关系。G3:基因组基因| |麝猫。10, 2787 - 2799。https://doi.org/10.1101/2020.04.01.020123(2020)。
谦虚,E。et al。RAD测序和杂交南极毛皮海豹基因组组装揭示了快速衰减的连锁不平衡,全球种群结构和近亲繁殖的证据。G3(贝塞斯达)8, 2709 - 2722。https://doi.org/10.1534/g3.118.200171(2018)。
成年雄性南极毛海豹的病理学和细菌学,Arctocephalus gazella在南乔治亚州的伯德岛去世。Br。兽医。J。145, 263 - 275(1989)。
内格尔,R。et al。南极海豹幼崽的运动模式和活动水平是由新生环境决定的。科学。代表。1114323(2021)。
内格尔,R。et al。Allee效应在海狗数量下降中的证据。Proc。r . Soc。B:生物。科学。288, 20202882。https://doi.org/10.1098/rspb.2020.2882(2021)。
梅泽,K.,冯·恩格尔哈特,N.,福卡达,J. &霍夫曼,J.。母亲和后代的激素水平反映了海狗的产前社会环境:胎儿编程的潜力?《公共科学图书馆•综合》11e0145352(2016)。
粗俗的,年代。et al。海狗的微生物群是由社会和物理环境塑造的,表现出母亲和后代的相似性,并与宿主的遗传质量有关。摩尔。生态。28, 2406 - 2422。https://doi.org/10.1111/mec.15070(2019)。
霍夫曼,J. I. & Amos, W.微卫星基因分型错误:父亲排斥的检测方法、常见来源和后果。摩尔。生态。14, 599 - 612。https://doi.org/10.1111/j.1365-294X.2004.02419.x(2005)。
Stoffel, m·A。et al。皮毛海豹的气味编码了群体成员、母代相似度、亲缘关系和遗传质量。Proc。国家的。学会科学。美国112E5005-E5012(2015)。
侯泽尔,斯蒂芬斯,J. C.和O 'brien, S. J.四种鳍足类动物MHC DQB位点的分子遗传多样性与进化。摩尔。杂志。另一个星球。16, 611 - 618(1999)。
Lenz, T. L. & Becker, S.减少PCR人工产物形成的简单方法导致了可靠的MHC基因分型和进化分析中其他高多态性位点的影响。基因427, 117 - 123。https://doi.org/10.1016/j.gene.2008.09.013(2008)。
Paijmans, a·J。et al。极地脊椎动物极度剥削的遗传遗产。科学。代表。https://doi.org/10.1038/s41598-020-61560-8(2020)。
Litzke, V., Ottensmann, M., Heitzmann, L., Forcada, J. & Hoffman, J. I.中性位点和免疫位点的杂合性与南极毛海豹微生物感染引起的新生儿死亡率无关。生态。另一个星球。9, 7985 - 7996(2019)。
快活的,c R。et al。鳍足类动物生态进化尺度上遗传变异的决定因素。Nat,生态。另一个星球。4, 1095 - 1104(2020)。
霍夫曼,j . I。et al。南极毛海豹的人口结构重建支持磷虾过剩假说。基因规格。发布极性基因。极地染色体组。13541(2022)。
霍夫曼,格兰特,s.m,福卡达,J. &菲利普斯,c.d.重度开发的海洋哺乳动物历史瓶颈的贝叶斯推断。摩尔。生态。20., 3989 - 4008。https://doi.org/10.1111/j.1365-294X.2011.05248.x(2011)。
K. Cammen, Hoffman, J. I., Knapp, L. A., Harwood, J. & Amos, W.东大西洋灰海豹主要组织相容性复合体的地理变异(Halichoerus grypus).摩尔。生态。20., 740 - 752。https://doi.org/10.1111/j.1365-294X.2010.04975.x(2011)。
霍夫曼,J. I. &阿莫斯,W.亲缘选择是否影响南极海狗的养育行为(Arctocephalus gazella) ?。Proc。r . Soc。伦敦爵士。B-Biol。科学。272, 2017 - 2022(2005)。
阿内伯格,斯考平,A,格伦费尔,B.和里德,A. F.宿主密度作为寄生虫群落丰度的决定因素。Proc。r . Soc。B-Biol。科学。265, 1283 - 1289(1998)。
鲍文,L。et al。在自由放养的加利福尼亚海狮群体中,泌尿生殖器官癌高发病率的免疫遗传学基础(Zalophus californianus).免疫遗传学56, 846 - 848(2005)。
萨姆布鲁克,J.弗里奇,E. F. &曼尼提斯,T.;分子克隆:实验室手册第二版。(冷泉港实验室出版社,1989)。
BioEdit:一个用户友好的生物序列比对编辑器和分析程序,适用于windows 95/98/NT。诊断。酸协会。爵士。41, 95 - 98(1999)。
谦虚,E。et al。一份皮毛海豹基因组草案为影响SNP验证的因素以及如何减轻这些因素提供了见解。摩尔。生态。Resour。16, 909 - 921。https://doi.org/10.1111/1755-0998.12502(2016)。
Untergasser,。et al。Primer3:新的功能和接口。诊断。酸Res。40e115(2012)。
Kumar, S., Stecher, G.和Tamura, K. MEGA7:用于更大数据集的分子进化遗传学分析7.0版本。摩尔。杂志。另一个星球。33, 1870 - 1874。https://doi.org/10.1093/molbev/msw054(2016)。
Pagès, H., Aboyoun, P., Gentleman, R. & DebRoy, S.生物串:生物串的有效操作。R包版本2.62.0。https://bioconductor.org/packages/Biostrings.(2021)。
Stoffel, m·A。et al。inbreedR:一个R包,用于基于遗传标记的近亲繁殖分析。生态方法。另一个星球。7, 1331 - 1339(2016)。
Jombart, T. adegenet:遗传标记多变量分析的R包。生物信息学24, 1403 - 1405。https://doi.org/10.1093/bioinformatics/btn129(2008)。
Dixon, P. VEGAN,一个社区生态的R函数包。j .蔬菜。科学。14, 927 - 930(2003)。
Goudet, J. HIERFSTAT,一个用于R计算和测试分层的包F统计数据。摩尔。生态。笔记5, 184 - 186(2005)。
用于人口结构分析的估计f统计量。进化38, 1358 - 1370。https://doi.org/10.1111/j.1558-5646.1984.tb05657.x(1984)。
迪里,S. &杜福尔,A.-B。ade4包:为生态学家实现对偶图。Softw j . Stat。22(2007), 1 - 20。
Kraemer, P. & Gerlach, G. Demerelate :计算基于共显性二倍体遗传标记的亲缘分析的个体间亲缘性。摩尔。生态。Resour。17, 1371 - 1377。https://doi.org/10.1111/1755-0998.12666(2017)。
确认
该研究是由德国研究基金会(DFG,德国研究基金会)在Sonderforschungsbereich (NC3.项目编号为316099922和396774617-TRR 212)和优先方案“南极研究与北极冰区的比较调查”(项目编号为42411918)。它还得到了自然环境研究委员会和英国南极考察生态系统项目的核心资金支持。这项工作有助于英国南极调查局、自然环境研究委员会的生态系统项目,也是地球极地科学计划的一部分。我们感谢Luke Eberhart-Hertel制作Fig。1.
资金
由Projekt DEAL支持和组织的开放获取资金。
作者信息
作者和联系
贡献
构思研究:J.I.H.样品采集和物流:J.F.实验室工作:K.H.和M.O.,由R.T和J.I.H.投入。贡献物流、试剂和资金:J.I.H.、J.F.、r.t.和B.A.C.。分析数据:j.t.、M.O.和A.E.。解释结果:j.t.、M.O.、A.E.、J.I.H.、r.t.、B.A.C.和T.L.L.。撰写论文:J.I.H.、j.t.、M.O.和T.L.L.。
相应的作者
道德声明
相互竞争的利益
作者声明没有竞争利益。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构附属的管辖权要求保持中立。
权利和权限
开放获取本文遵循创作共用署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),该协议允许在任何媒体或格式中使用、分享、改编、分发和复制,只要您给予原作者和来源适当的署名,提供创作共用许可协议的链接,并说明是否有更改。本文中的图片或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果材料不包含在文章的创作共用许可中,并且您的预期用途不被法律法规允许或超出了允许的用途,您将需要直接从版权所有者那里获得许可。欲查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于这篇文章
引用这篇文章
德贝,J.,奥滕斯曼,M.,海文斯坦,K.。et al。内含子引物出人意料地揭示了南极海狗的主要组织相容性复合体多样性。Sci代表1217933(2022)。https://doi.org/10.1038/s41598-022-21658-7
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-21658-7