摘要
硅谱分析用于鉴定活性化合物和指导传统药物的合理使用。以前对埃塞俄比亚本土芦荟的研究主要集中在植物化学成分和传统用途的记录上。在这项研究中,我们评估了埃塞俄比亚本土芦荟植物化学物质的ADMET和药物相似特性,并使用Discovery Studio进行了基于药效团的分析,以预测治疗靶点。利用KEGG通路、基因本体和网络分析对靶点进行检测。在CODA网络中,采用随机行走带重启算法进行网络传播,寻找与目标相关的疾病。结果,82个人类靶点被预测并发现参与了一些分子功能和生物过程。这些靶标还与免疫系统、代谢系统、神经系统、肌肉骨骼系统、消化系统、血液系统、传染病、口腔和牙科以及先天性代谢紊乱的各种癌症和疾病有关。207个KEGG通路中靶点丰富,主要通路为类固醇激素生物合成代谢、脂质和动脉粥样硬化、化学致癌和癌症通路。总之,硅靶捕鱼和网络分析揭示了植物化学物质的治疗活性,表明埃塞俄比亚土著芦荟对与许多疾病相关的许多基因和信号通路具有多药理学作用。
介绍
世界各地的医疗保健系统正面临流行病、慢性病、人口老龄化和医疗费用不断上升的问题。患者和医疗保健提供者都要求振兴医疗保健服务。这包括改善获得传统、补充和替代医学(TCAM)从业人员、产品和服务的机会,特别是在初级卫生保健方面1。几个世纪以来,天然产物的生物活性成分被广泛用于治疗各种疾病,由于其潜在的愈合作用,被认为是有前途的替代治疗剂2。在过去三十年中,天然产物药物的使用有了显著增加,全球80%的人在基本医疗保健的某些方面依赖天然产物药物3.。几千年来,在许多不同的文化中,利用植物作为天然产物的来源和传统医学系统的基础,已经被广泛地记录下来2,4,5。
芦荟属植物是历史记载中最常见的传统药用植物6。据文献记载,芦荟属植物74%的用途是药用,其中芦荟液被频繁使用7。几千年来,芦荟叶一直被用作治疗皮肤病、烧伤和便秘的主要药物8。此外,还有许多含有芦荟的商业产品,如泻药、健康饮料和滋补品、剃须后凝胶、漱口水和牙膏、护发液和洗发水以及皮肤保湿凝胶9,10。在埃塞俄比亚,沉香因其治疗特性以及确保生计、促进经济增长和保护生物多样性而具有重要意义9。埃塞俄比亚有46个已知的芦荟物种和3个亚种,是芦荟生物多样性的可能中心之一。在这些物种中,67.3%是本土物种11,12。在埃塞俄比亚,已经确定了三个区域流行中心10(1)大裂谷北部、中部高地和西部有特有种和种下类群芦荟adigratana,答:ankoberensis,答:benishangulana,答:camperi,答:clarkei,答:debrana,答:线虫,答:monticola,答:percrassa,一个。pulcherrima,答:schelpei,答:sinana,答:steudneri,答:trigonantha,答:weloensis;(2)东部高地和低地有特有种芦荟bertemariae,答:harlana,答:mcloughlinii,答:megalacantha无性系种群。alticola,答:pirottae;答:下毛竹;和答:trichosantha无性系种群。Longiflora;(3)南部高地、低地和裂谷芦荟elkerriana,答:friisii,答:ghibensis,答:gilbertii无性系种群。gilbertii,答:gilbertii无性系种群。megalacanthoides,答:jacksonii,答:kefaensis,答:otallensis,答:tewoldei,答:welmelensis,答:yavellana。
由于芦荟具有长期广泛的药用价值,鉴定其植物化学成分的工作正在进行。芦荟的叶和根是各种有趣的次生代谢产物的储存库,包括生物碱、蒽醌、前蒽醌、蒽酮、双蒽醌、色素、类黄酮、香豆素和吡酮8。然而,主要的有效成分、相关疾病及其作用方式,特别是土著埃塞俄比亚芦荟的作用方式,还没有得到很好的了解。这阻碍了它们在药物开发中的广泛应用。
寻找生物活性化合物来帮助治疗疾病是药物开发过程的目标。过去,新药发现过程始于随机筛选和对天然产物对已知疾病的作用的经验观察。目前,高通量筛选(HTS)改进了这一过程,使成千上万的化合物针对分子靶点或细胞检测的筛选过程非常迅速13。此外,研究人员正在不断研究新的方法来提高药物发现过程的效率14。利用计算机辅助药物设计(CADD),通常被称为计算机方法,是提高新药开发有效性的一种策略。通过使用分子模型,可以虚拟筛选大量化合物的药物相似特性及其与药理靶点的相互作用,CADD减少了药物开发时间和总体研究费用13。化合物硅活性分析是一种新兴的计算方法,用于预测生物活性化合物最可能的靶标,从而预测不良反应、副作用和药物再利用15。它可以应用于许多不同的领域,包括药物重新定位,天然产物分析和多靶点方法16。除了传统的药物开发之外,目前正在对已经建立的药物的新用途进行研究。旧药物的计算机分析可以帮助重新定位这些旧药物的新用途17,18。从基于表型的筛选(包括经验知识)中产生的化合物通常具有完全未知的作用机制(MoA)。基于药效团的天然产物活性分析能够预测其作用机制,并指导适当规划体内和体外实验。此外,以前未知的具有有趣的化学支架的铅治疗性天然产物可以被描述16。这将有助于根据它们预测的目标轮廓来确定化合物的优先级。了解和预测多药理学的协同作用也是计算机靶点谱分析的主要应用之一19。
基于药效团模型的埃塞俄比亚本土芦荟化合物的硅谱分析在本研究中完成。药效团是对生物大分子识别配体所需的分子特征(空间和电子)的抽象描述,影响其生物过程20.。具有相似药效团模式的结构不同的分子可能被生物靶标的相同结合位点识别,从而具有相似的生物学特征21。药效团模型通常用于几种药物(活性化合物)已经确定,但靶蛋白或受体的三维(3D)结构未知的情况。药物被叠加以确定它们的共同特性,提供一个描述配体-受体结合的药效团模型22。分子中任何具有与分子识别相关的特定性质的原子或基团都可以还原为药效团性质23。这些分子模式可以是氢键供体或受体、阳离子、阴离子、芳香或疏水,以及任何可能的组合24。对于一组活性分子,药效团鉴定包括两个步骤:分析分子以确定其药效团性质,即可以与受体相互作用的原子;对齐分子的活性构象以找到相应特征的最佳叠加22。
在这项研究中,ADMET分析和药效团模型为基础的硅靶预测从埃塞俄比亚土著芦荟植物化学物质进行。目的:明确芦荟相关疾病,揭示芦荟植物化学物质、基因本体(GO)、KEGG通路的治疗作用机制25,并对预测目标进行了网络分析。据我们所知,还没有使用计算机化的综合目标捕捞方法来确定埃塞俄比亚土著芦荟植物化学物质的药理潜力。
结果与讨论
埃塞俄比亚本土芦荟植物化学物质理化、药物相似性和ADMET相关特性的评价
物理化学性质影响分子的药效学和药代动力学。分子的吸收、分布、代谢、排泄和毒性(ADMET)特性是成功开发药物和其他工业化学品的重要因素26,27。利用从PubChem数据库中编译的物理化学特性28和SwissADME web服务器29,评估了植物化学物质的药物相似性。利用admetSAR web server -一个包含从大量不同文献中整理的admet相关特性的数据库,预测了埃塞俄比亚土著芦荟植物化学物质的admet相关特性27。在对植物化学物质进行硅谱分析之前,我们使用admetSAR的数据排除了潜在的有害物质,如AMES诱变剂、致癌物和hERG抑制剂。
我们用了利平斯基的5法则30.和韦伯法则31评估埃塞俄比亚本土芦荟植物化学物质的药物相似特性。然而,应该指出的是,许多最成功的药物并不符合这些准则32。对于天然产物或天然产物衍生物的口服药物,常见的是违反2或3条五法则33。如表所示1,大多数植物化学物质符合Veber的规则标准和五项规则(最多违反三项规则)。因此,在埃塞俄比亚土著芦荟中发现的植物化学物质显示出足够的药物相似性和物理化学特征,表明它们具有治疗药物的潜力。
与adme相关的性质,如分子量(MW),辛醇-水分配系数(Log)P)、拓扑极性表面积(TPSA)、水溶性、胃肠吸收(GIA)、血脑屏障(BBB)通透性见表2。当候选药物的TPSA高于140时,其吸收不良Å2这是上市药物的基准31,34,35。TPSA与质量呈正相关,质量大于500 g/mol的分子TPSA在0 ~ 140之间35。埃塞俄比亚土著芦荟的大部分植物化学物质的TPSA值和GIA值是可以接受的。日志p值和Abbott生物利用度评分均大于零,表明植物化学物质具有丰富的生物利用度,并能有效地穿过细胞膜36。GIA和血脑屏障通透性是药物广泛使用的重要特性。有许多先前的研究,以改善分子的胃肠道渗透,口服给药,吸收不良的药物37。绝大多数来自埃塞俄比亚本土芦荟的植物化学物质显示出可接受的GIA并穿过血脑屏障。
通透性糖蛋白(P-gp)影响着许多外源药物或化学物质的ADMET特性,因此研究转运蛋白与药物分子之间的相互作用具有重要意义38。它作为一个单向的外排泵,将其底物从细胞内挤压到细胞外,从而限制了细胞对化合物的摄取和代谢39,40。从表3.结果表明,除叶绿醇外,其余植物化学物质均不是p -糖蛋白的底物,显示出它们作为潜在治疗剂的理想特性。
细胞色素P450s (CYPs)是一类含血红素的酶,是体外解毒和药物代谢所必需的。细胞色素P450酶可被药物抑制或诱导,导致临床显著的药物-药物相互作用,可引起意想不到的不良反应或治疗失败。抑制剂阻断一种或多种CYP450酶的代谢活性,而诱导剂通过增加酶合成来增加CYP450酶的活性。因此,在开已知是CYP450抑制剂或诱导剂的药物时应注意。靶药物可能需要替换或调整剂量,以解释代谢的潜在减少或增加41。
基于药效团模型的埃塞俄比亚本土芦荟植物化学物质的硅谱分析
分析结果显示在两个HTML表格中,分别是MoleculeFits和PharmacophoreFits。评价配体和药效团适合度的两个指标是拟合值和形状相似性。从配体剖析器中选择目标,使用等于或大于0.5的拟合值标准。
最后绘制了458个药效团模型。这些模型属于272个具有唯一UniProt-ID的靶蛋白/基因。其中82个目标与人类有关,CODA42采用网络进行进一步分析。1885对具有目标短名称、基因和蛋白id UniProt-ID的植物化学靶标对的完整列表见(补充表S)1在线)。
利用KEGG、GO和网络分析推断其药理作用
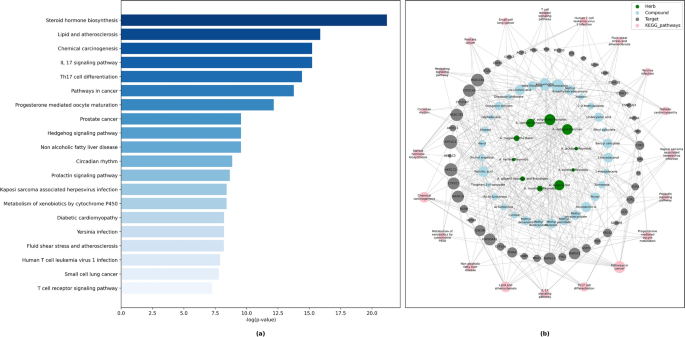
本研究利用药效团模型,将10种芦荟中的35种化合物成功定位到82个人类相关靶点上。207 KEGG通路25丰富了埃塞俄比亚本土芦荟植物化学物质的82个靶点(补充表S2在线)。根据调整后的p值小于或等于0.05,筛选出104条KEGG通路。数字1a显示前20条显著富集的KEGG通路。使用python NetworkX库2.5构建的药物靶标通路网络表明,47个基因与前20个KEGG通路显著相关。该网络中的大多数候选基因都参与了7个主要的KEGG通路,即类固醇激素生物合成代谢、脂质和动脉粥样硬化、化学致癌、IL-17信号通路、Th17细胞分化和癌症通路中的通路(图2)。1b). KEGG富集分析突出了植物化学物质可以有效发挥其治疗潜力的靶点和途径。类固醇激素在调节水盐平衡、代谢和应激反应以及启动和维持性别分化和生殖方面发挥着重要作用43。先前的研究表明,芦荟可以作为一种传递激素的生物载体44。有证据表明,炎症在动脉粥样硬化的发生、发展和结局中起着重要作用。由于其抗炎特性,芦荟可能是预防动脉粥样硬化进展的良好候选者45。芦荟中的植物化学物质,特别是芦荟大黄素,在多种人类癌细胞系中具有多种抗增殖和抗癌特性,经常影响多种重要的信号通路。最显著的作用是抑制细胞增殖、细胞迁移和侵袭、细胞周期阻滞、诱导细胞死亡、线粒体膜和氧化还原干扰以及调节免疫信号。芦荟大黄素的作用并不是在所有细胞系中普遍存在,并因细胞类型而异46,47。无论是把芦荟作为一个整体来看,还是从它的化合物来看,有各种各样的文章都说芦荟是一种药用植物,已经被证明对对抗多种癌症有益47。然而,芦荟植物化学物质对潜在分子靶点的确切作用机制仍有待研究。
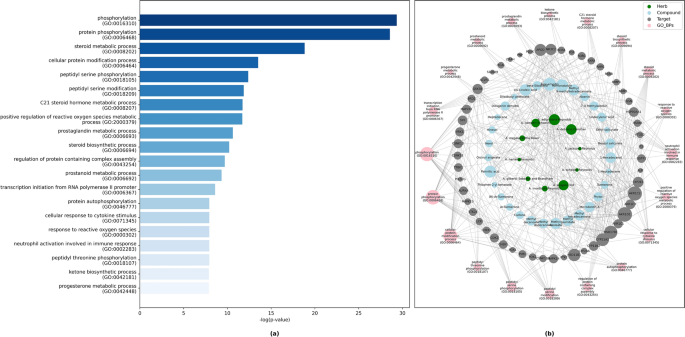
去分析48是发现生物过程、细胞成分和基因分子功能的有用工具吗49。共鉴定出与82个预测靶蛋白/基因相关的1376个生物过程(bp)、213个分子功能(MFs)和101个细胞组分(CCs)(补充表S)2在线)。基于P-值小于或等于0.05,过滤211 bp, 58 mf和9 cc。对前20个bp的功能富集分析表明,大部分靶点与蛋白质磷酸化修饰过程、类固醇代谢过程等相关,如图所示。2a.此外,使用python NetworkX库版本2.5构建的药物-靶点-生物过程网络显示,55个靶点主要富集前20个bp(图2)。2b)。
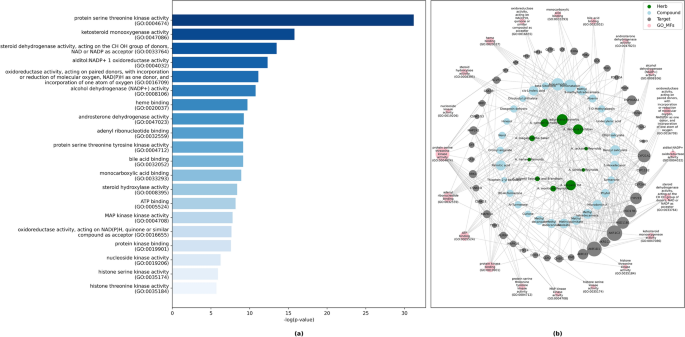
前20个功能富集的mf如图所示。3.。在主要的20个mf中,蛋白丝氨酸/酪氨酸激酶活性和酮类固醇单加氧酶活性主要由55个靶基因表达(图2)。3.一)。3.b显示了药物-靶标-生物过程网络,其中45个基因主要富集于前20个mf。
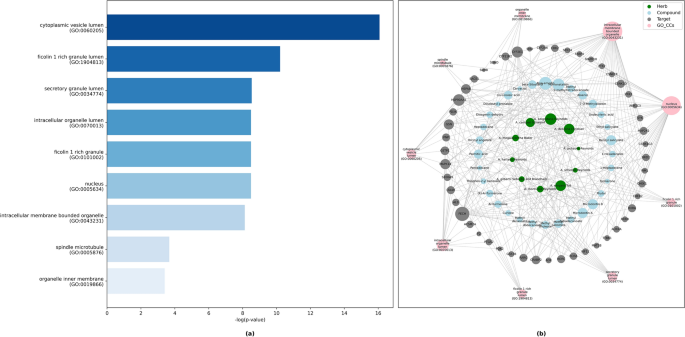
此外,cc广泛分布于细胞质囊泡的管腔、富含ficolin-1的颗粒、分泌颗粒等(图2)。4A和b)。
此外,我们对本研究中使用的10种芦荟进行了KEGG通路、GO和网络分析。有关数字载于补充图S1网上。15个基因与答:adigratanaReynolds’s的植物化学物质在KEGG的4个主要途径中富集,即类固醇激素生物合成、化学致癌、细胞色素p450对外源物的代谢和自然杀伤细胞介导的细胞毒性。功能富集分析表明答:adigratana雷诺兹植物化学物质与类固醇代谢和生物合成过程、黄体酮代谢过程、糖皮质激素代谢和生物合成过程以及活性氧代谢过程的正调控有关。此外,酮类固醇单加氧酶活性、类固醇脱氢酶活性、糖醇:NADP + 1-氧化还原酶活性、氧化还原酶活性和乙醇脱氢酶(NADP +)活性是主要的MFs相关因子答:adigratana雷诺兹的植物化学物质。类似地,预测了23个目标的植物化学物质答:camperiSchweinf。这些靶点富集在类固醇激素生物合成、化学致癌、Th17细胞分化、昼夜节律、孕激素介导的卵母细胞成熟、细胞衰老、p53信号通路、小细胞肺癌、IL-17信号通路等KEGG通路中。该芦荟植物化学靶点的主要富集bp包括:类固醇代谢过程、类固醇生物合成过程、蛋白质磷酸化、RNA聚合酶II启动子转录起始、磷酸化、dna模板转录起始、糖皮质激素生物合成过程、糖皮质激素代谢过程和细胞碳水化合物代谢过程的调控。此外,与该芦荟植物化学物质相关的主要MFs有:蛋白丝氨酸/苏氨酸激酶活性、类固醇脱氢酶活性、血红素结合、酮类固醇单加氧酶活性、氧化还原酶活性、类固醇羟化酶活性和氧甾醇结合。类似地,来自其他芦荟物种的植物化学物质也有相关的KEGG通路、bp和cc,如图5所示1网上。
通过比较前20个生物过程和途径富集数据,发现42个共同靶点,与这些靶点相关的前10个途径是类固醇激素生物合成、脂质和动脉粥样硬化、化学致癌、IL-17信号通路、癌症途径、Th17细胞分化、孕激素介导的卵母细胞成熟、前列腺癌、卡波西肉瘤相关疱疹病毒感染和人t细胞白血病病毒1感染。
埃塞俄比亚本土芦荟的潜在治疗作用
根据药理学分析,来自埃塞俄比亚土著芦荟的植物化学物质与癌症(66个目标)、内分泌疾病(16个目标)、代谢疾病(15个目标)、免疫系统疾病(5个目标)、神经系统疾病(11个目标)、先天性代谢障碍(3个目标)、肌肉骨骼疾病(3个目标)、消化系统疾病(3个目标)、血液病(2个目标)、传染病(3个目标)、口腔和牙科疾病(1个目标)有关。其中一些药理活性与传统报道的芦荟药用有关。
从我们的分析中,我们发现大约10种癌症类型,即腺癌、乳腺癌、胶质瘤、乳腺恶性肿瘤、前列腺恶性肿瘤、乳腺肿瘤、食管鳞状细胞癌、白血病和黑色素瘤与65个靶点有关,这些靶点与本研究中使用的10种芦荟中的34种化合物有关。补充表S3.在线提供了关于埃塞俄比亚土著芦荟中每种植物化学物质的预测目标和疾病的信息。
答:adigratana雷诺兹植物化学物质被预测对几种癌症(腺癌、乳腺癌、前列腺恶性肿瘤和前列腺肿瘤)、内分泌和代谢疾病(糖尿病、非胰岛素依赖型肥胖)、免疫系统疾病(结肠炎、炎症性肠病和溃疡)、消化系统疾病(溃疡)和感染性疾病(溃疡和结肠炎)具有治疗作用。在埃塞俄比亚北部,答:adigratana雷诺兹传统上用于治疗各种疾病,包括伤口、感染和炎症50。以前的体内和体外研究也支持使用答:adigratana雷诺兹在传统医学中证实了它的抗炎特性,这至少部分与叶子中芦荟素A/B和microdontin A/B的存在有关50。
答:camperiSchweinf。植物化学物质被预测对癌症(腺癌、乳腺癌、乳腺恶性肿瘤、前列腺恶性肿瘤、乳腺肿瘤、前列腺肿瘤)以及内分泌和代谢疾病(糖尿病-非胰岛素依赖、胰岛素抵抗、病态肥胖、肥胖和病态肥胖)具有治疗作用。虽然关于这种植物的传统用途的资料很少,但据称它可用于伤口愈合和疟疾治疗51。
本研究推断的活性植物化学物质的潜在治疗活性需要进一步通过体内和体外科学实验来研究。
蛋白质-蛋白质相互作用(PPI)网络,分子对接和分子动力学(MD)模拟
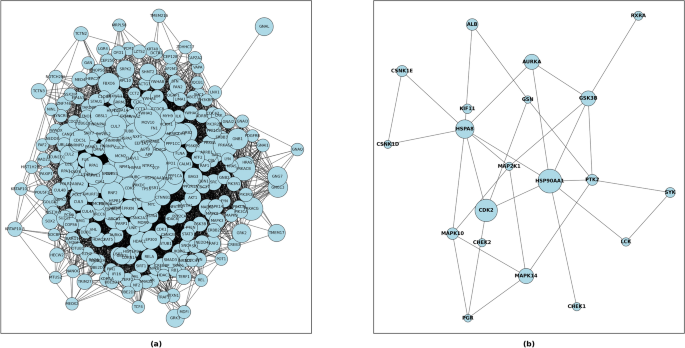
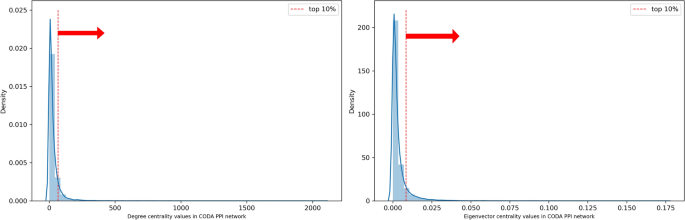
CODA PPI网络共有17358个蛋白节点(图2)。5A)和度中心性和特征向量中心性的分布进行了检验。前1、5、10%节点的度中心性值分别大于等于243、101、67。1、5%和10%的节点特征向量中心性值分别大于等于0.0313、0.0138和0.008。20个预测靶标(CDK2、HSPAA1、HSPA8、AURKA、MAPK14、GSK3B、MAPK10、PTK2、CSNK1E、SYK、CHEK1、MAP2K1、KIF11、ALB、RXRA、GSN、CHEK2、PGR、CSNK1D和LSK)的度和特征向量中心性均在前10%。5b).其中,靶点CDK2、HSPAA1、HSPA8、AURKA、MAPK14的度和特征向量中心性均位于前1%(图2)。6).
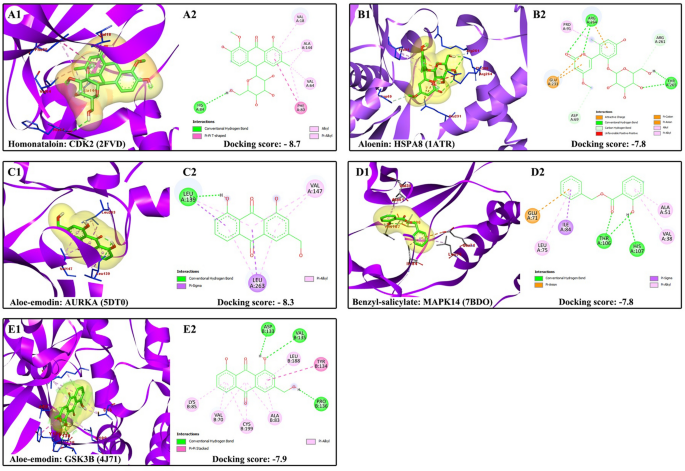
对接结果显示配体与靶蛋白成功结合,显著降低了(p≤0.05)的结合能与PubChem中的随机化合物与PDB中的随机靶标的对接分数相比,证实了本研究中药效团模型预测的相互作用。所选植物化学物质与靶点的结合亲和能、相互作用氨基酸残基、对接中心和对接大小如表所示4。数字7展示了从埃塞俄比亚本土芦荟中随机选择的植物化学物质与预测靶标的PPI网络中的枢纽基因/蛋白质之间相互作用的3D和2D姿态视图。
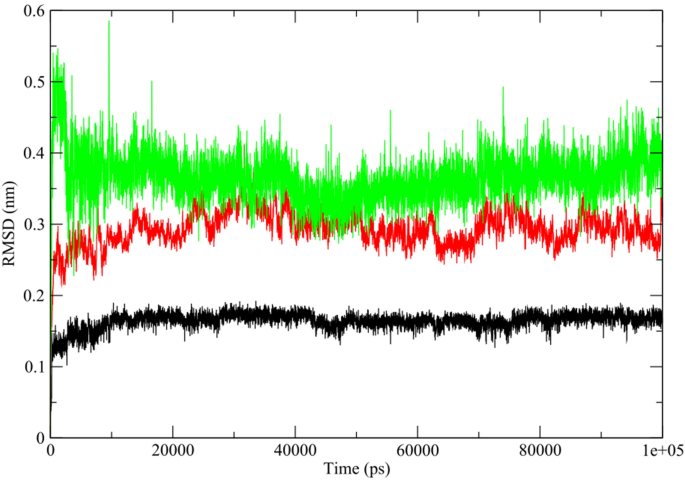
根据对接分析,我们选择单胞脂素作为配体进行MD模拟,因为它与靶蛋白CDK2的结合能评分相对最低(- 8.7 kcal/mol)。利用均方根偏差(RMSD)参数分析了蛋白质-配体复合物在100 ns以上的运动轨迹,以考察结合配体的蛋白质的稳定性。为了考察靶蛋白与配体相互作用后的构象变化,我们计算了蛋白-配体复合物、配体和靶蛋白相对于起始结构的RMSD,如图所示。8。清楚地表明,蛋白质-配体复合物的原子均方根误差(RMSD),蛋白质和配体具有相同的波动模式,在最初的0.25 ns内稳定增加,然后稳定直到模拟结束。蛋白的均方根偏差(RMSD)(图2)8,红色)略高于配体(图2)。8(黑色)在模拟过程中。此外,蛋白质-配体复合物的RMSD(图2)。8(绿色)比蛋白质和配体的高,说明配体结合后复合物中蛋白质发生了构象变化。有趣的是,在模拟期间,蛋白质-配体复合物表现出非常低的波动,这表明该复合物是稳定的,配体仍然适合受体的结合袋(见补充视频S)1在线)。
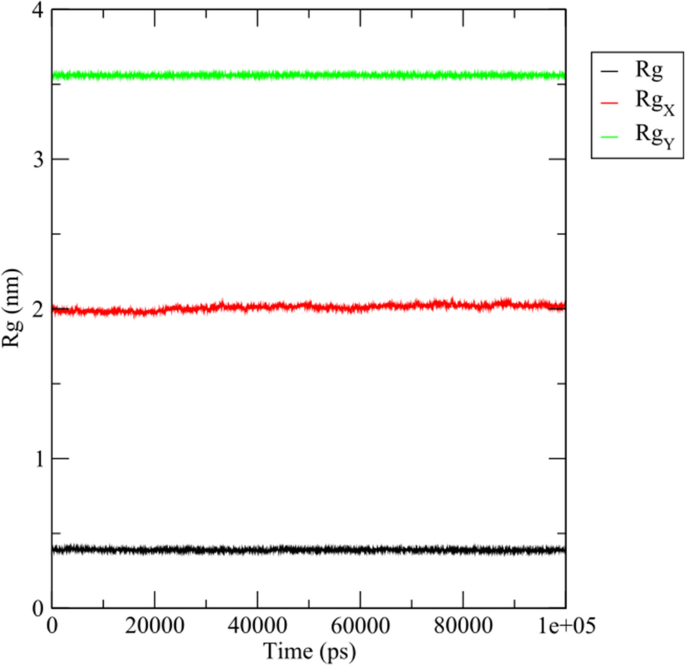
旋转半径(Rg)的时间发展为蛋白质崩溃动力学提供了一个很好的分析。52。为了确定蛋白质是否紧凑,测量了系统的旋转半径,并创建了一个图表,显示它们与模拟时间的关系53如图所示。9。与RMSD图相似,在整个模拟过程中,配体、蛋白质和蛋白质-配体复合物系统的Rg没有发生明显变化,说明在模拟过程中,结合区对它们的结构影响不大。
方法
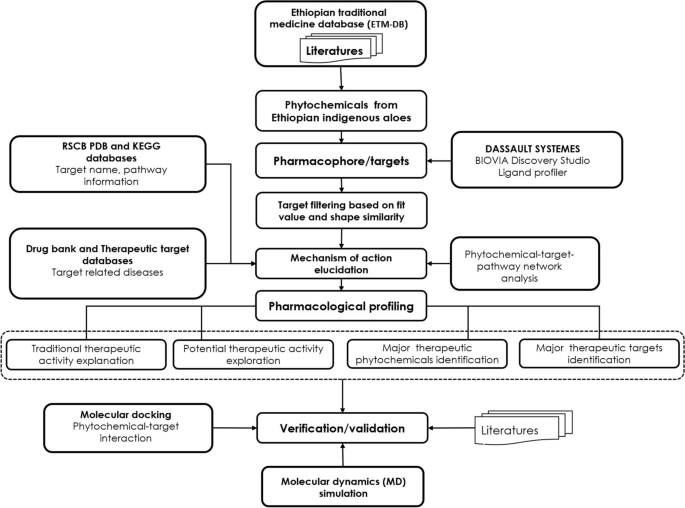
在这项研究中,基于药效团模型的配体分析被用于目标捕捞,以预测埃塞俄比亚本土芦荟化合物的潜在靶标。数字10展示了本研究的工作流程。首先,通过文献检索对埃塞俄比亚土著沉香进行鉴定,并从文献和埃塞俄比亚传统草药和植物化学物质数据库(ETM-DB)中手动编译其植物化学物质(化合物)。54。植物化学物质的三维(3D)结构数据文件(SDF)从PubChem数据库中收集55。植物化学物质的理化性质从PubChem数据库和SwissADME网站服务器检索29。用admetSAR对植物化学物质进行毒性过滤。然后,我们使用了PharmaDB药效团和Discovery Studio的目标数据库56对植物化学物质进行目标捕捞。根据预先设定的拟合值(0.5)的阈值挑选出命中药效团模型。在分析了命中目标及其相关途径和疾病,以及植物化学物质与目标之间的相互作用后,构建了埃塞俄比亚土著芦荟植物化学物质行动网络。此外,还进行了分子对接,以完善结合模式并验证研究结果。最后,通过分子动力学(MD)模拟了蛋白质-配体复合物的最佳结合相互作用。
埃塞俄比亚本土芦荟植物化学成分的收集
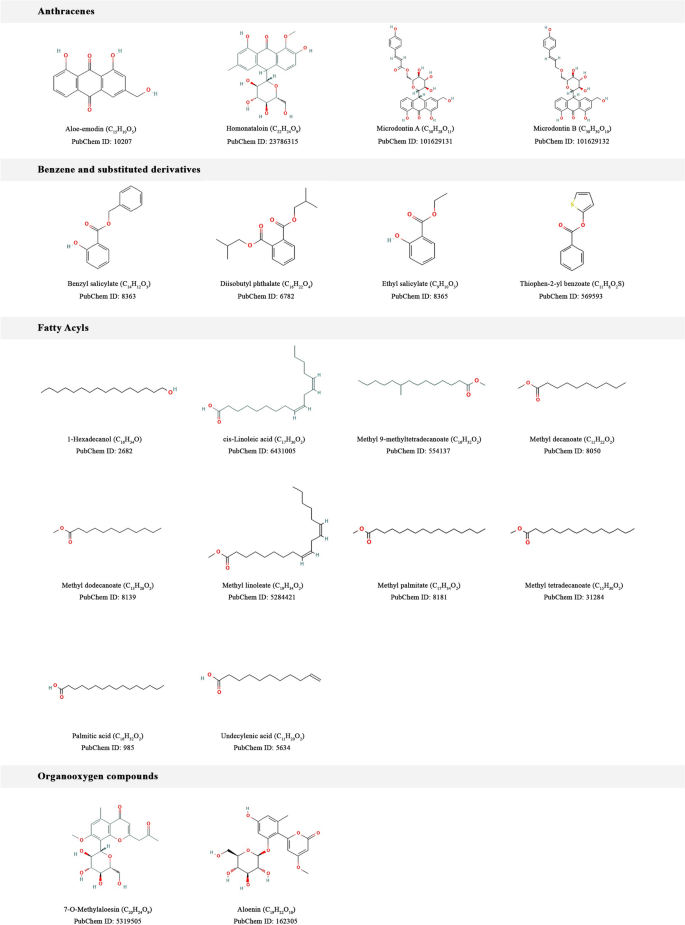
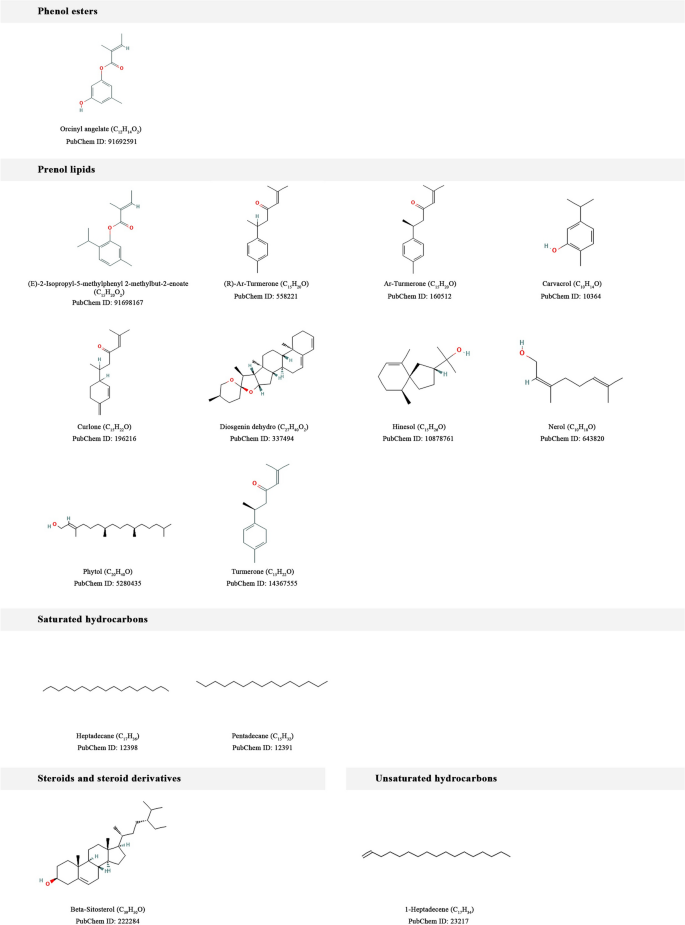
从我们自己的数据库中收集了埃塞俄比亚土著芦荟的植物化学成分54还有文学作品。因此,我们在去除潜在毒性化合物并评估其ADMET和药物相似特性后,从10种埃塞俄比亚本土芦荟中收集了35种化合物。然后,利用计算目标捕鱼成功地预测了植物化学物质的目标。图中列出了35种植物化学物质的二维化学结构和化合物类别。11。这35种植物化学物质使用ClassyFire(具有全面可计算分类法的自动化学分类)进行分类。57分为蒽、苯及其取代衍生物、脂肪酰基、有机氧化合物、酚酯、醇脂、饱和烃、类固醇及其衍生物、不饱和烃等9个化合物类。
埃塞俄比亚土著沉香植物化学物质理化、药物相似性和ADMET特性的评价
植物化学物质的理化性质从PubChem数据库检索28和SwissADME web服务器29。SwissADME是一个免费的网络工具,用于评估小分子的药代动力学,药物相似性和药物化学友好性。我们使用pubchempy——一个python库,用于与PubChem数据库交互,从PubChem数据库中检索与植物化学物质相关的信息。
利用理化性质预测了植物化学物质的药物相似性。药物相似性与影响分子药效学和药代动力学的分子特性有关58。这些分子性质与一些基本的结构或物理化学性质(如测井)有关p(分配系数),分子量(MW),拓扑极性表面积(TPSA),氢键受体和供体在一个分子中计数。为潜在药物选择配体有几套标准。最著名的是利平斯基30.确定在批准的化合物中经常观察到的共同特性。作者提出了类药物分子的“5规则”(小于5个氢键供体,小于10个氢键受体,小于500道尔顿(g/mol)分子量,小于5 log)p(有机相和水相之间的分配系数))。另外,韦伯法则31提出仅满足10个或更少的可旋转键和极性表面积等于或小于140 Å这两个标准的化合物2在大鼠体内具有良好的口服生物利用度。然而,许多最成功的药物不符合这些指南,在应用这些指南时应小心32。此外,大多数来自天然产物的化合物并不总是遵循现代药物设计中常用的规则,包括利平斯基的“五法则”21我们使用的化合物违反了两个或更多的规则5,这是药物化学家和工业在药物开发中使用的59为本研究植物化学物质的药物相似性评价提供参考。
从admetSAR web服务器预测ADMET属性27使用BeautifulSoup(一个用于从HTML和XML文件中提取数据的Python库)从化合物的简化分子输入行输入系统(SMILES)字符串作为输入。我们去除了潜在的有毒化合物,如AMES诱变剂、致癌物和人类乙醚相关基因(hERG)抑制剂。抑制人乙醚离子通道可能导致心脏毒性,因此,有必要筛选所有潜在的候选药物,以防止阻断hERG通道的风险60。艾姆斯试验是筛选潜在基因毒性致癌物的灵敏工具61。
基于药效团模型的埃塞俄比亚本土芦荟植物化学物质的硅谱分析
药效团模型表示触发所需药理作用的靶配体结合位点16。本研究中使用的药效团模型来源于蛋白质-配体三维复合结构以及小生物活性有机分子的结构数据62。药效团可作为低维靶标用于靶标预测任务63。我们使用BIOVIA Discovery Studio对芦荟植物化学物质的潜在靶点进行了基于药效团的预测56。Discovery Studio是一个交互式计算化学和分子建模软件包,具有广泛的建模和仿真功能56。我们使用了“配体分析器”协议,这是BIOVIA Discovery Studio中的自动配体分析。BIOVIA Discovery Studio提供基于药物团的自动活动分析和报告16。Discovery Studio 4.5配备了PharmaDB药效团数据库,该数据库包含来自sc-PDB数据集的8000个蛋白质配体复合物的约68,000个药效团,该数据集本身是PDB中发现的结合位点的3D结构的集合64。结合位点是从晶体结构中提取出来的,在晶体结构中可以识别出蛋白质腔和小分子配体之间的复合物15。
对于Input PharmaDB Pharmacophores配体分析的参数设置,选择所有具有binding pocket形状的药效团模型进行虚拟筛选,默认设置。采用刚性模式作为分子映射算法。使用每个查询配体的构象生成器组件的BEST设置生成一个构象数据库(3D SDF文件格式)。在将这些配体映射到药效团模型以增加选择性时,允许所有分子特征。最小特征间距离设置为0.5 Å。对于每个查询配体,通过降低拟合值对目标进行排序。目标是根据他们的UniProt ID提名的。UniProt是Universal Protein Database程序的缩写,由Swiss-Prot、TrEMBL和PIR-PSD数据库组成,是目前包含信息量最大的数据资源和蛋白质结构的数据库65。有关该蛋白质的更多信息,包括蛋白质名称、基因名称、生物体、序列信息、分类、家族和结构域以及相关的分子功能和生物过程,可使用UniProt ID从UniProt网站(http://www.uniprot.org/).该数据库还可以根据PDB ID、KEGG ID等信息进行搜索,链接到其他数据库。在这项工作中,对于每个目标,从PDB中收集目标名称、UniProt条目名称和UniProt ID信息64和UniProt数据库65。
利用KEGG、GO和网络分析推断其药理作用
为了研究埃塞俄比亚土着沉香的治疗效果,对82个预测靶点的京都基因与基因组百科(KEGG)途径和基因本体(GO)进行了分析。为了确定化合物、靶点、途径和生物过程之间的复杂关系,我们在内部基因集名为“KEGG_2021_Human”的gseapy python文库中使用enrichment函数进行了富集测试。情境导向关联(CODA)中的网络分析42得到与每个预测靶点相关的疾病。在CODA的异构生物网络中,采用随机行走与重启(RWR)算法进行网络传播。CODA是一个包含从分子水平到表型水平的多种类型生物相互作用的综合数据库。我们利用CODA中所有类型的生物相互作用构建了一个异构网络,以观察信息流从靶点开始聚合到网络中的疾病节点。运行算法后,我们根据RWR分数对网络中的疾病节点进行排名。然后使用KEGG应用程序编程接口(API)将疾病映射到高级疾病类别-一个rest风格的API到KEGG数据库资源。
蛋白质-蛋白质相互作用(PPI)网络,分子对接和分子动力学(MD)模拟
利用CODA构建了蛋白质相互作用(PPI)网络42,共包含17358个蛋白节点。在CODA的分子关系中,选择了具有左实体型和右实体型基因产物的蛋白质。然后用基因符号表示所有节点,以便更好地解释。为了获得PPI网络中的枢纽目标,使用了两种网络中心性(度中心性和特征向量中心性)。还有另外两种更具代表性的网络中心性度量,如亲密中心性和中间中心性。然而,在本研究中没有考虑紧密性和中间性中心性,因为它们关注的是网络的整体鲁棒性,而不是相邻节点之间的关系66。因此,我们将枢纽目标视为PPI网络中前10%度和特征向量中心性值内的节点。
此外,还进行了分子对接研究,以证实药效团模型预测的蛋白质-配体相互作用。盲对接是通过扫描蛋白质靶标的整个表面来检测肽配体可能的结合位点和模式67。在这项研究中,我们采用了盲对接,因为我们没有关于植物化学物质与预测靶标结合方式的信息。从蛋白质数据库(Protein Data Bank, PDB)中检索PPI网络枢纽蛋白中随机选取的5个蛋白的PDB文件(由CODA网络分析获得),并从PubChem数据库中获取配体的3D SDF文件。分子对接是通过CB-Dock2 web服务器(http://clab.labshare.cn/cb-dock/php/index.php),是蛋白质与配体盲对接的服务器,集空腔检测、对接和同源模板匹配于一体。CB-Dock自动识别结合位点,计算中心和大小,根据查询配体定制对接盒大小,然后与AutoDock Vina进行分子对接68。然后,使用Discovery Studio Visualizer对蛋白质-配体复合物的三维和二维姿态进行分析和可视化。
此外,我们使用单样本单侧t检验将我们选择的靶标和蛋白质的对接分数与PubChem中随机化合物与PDB中随机靶标的对接分数进行比较,以统计显示结合是显著的(P≤0.05)。
在所选择的植物化学物质中,与细胞周期蛋白依赖性激酶2 (Cyclin Dependent Kinase 2, CDK2)靶蛋白结合的配体homonataloin表现出最好的结合相互作用和自由能。因此,选择它对目标蛋白进行100纳秒(ns)的分子动力学(MD)模拟,以确认其稳定的结合亲和力。采用GROningen MAchine for Chemical simulations (GROMACS) 2021.4软件包进行MD模拟69CHARMM27全原子力场在哪里70用于蛋白质拓扑制备,官方SwissParam (https://www.swissparam.ch/)71用于配体拓扑的制备。使用的溶剂化方法是默认的简单点电荷(SPC)水模型的三斜盒,其中应用了显式溶剂周期边界条件。用钠离子和氯离子对溶剂化配合物进行了电荷中和。通过5000步的最陡下降法,对系统进行能量最小化,以解决任何空间冲突或不适当的几何形状。利用NVT对系统进行均衡处理,保证了合理的启动结构;使用Berendsen恒温器在恒定数量的粒子,体积和温度(NVT)下平衡100皮秒(ps)72。此外,使用Parrinello-Rahman气压计在恒压(等温-等压(NPT)集合)下再进行100 ps的重新平衡,每个平衡轮的时间步长为2飞秒(fs)73。最后,在恒温300 K、恒压1 atm条件下,以2 fs的时间步长进行了100 ns的MD生产阶段。对于MD轨迹分析,使用GROMACS的“trjconv”功能将复合物重新居中并重新包裹在单元胞内。然后,根据初始位置和旋转半径(Rg),利用蛋白质、配体和蛋白质-配体复合物的RMSD分析轨迹。使用绘图与数据高级计算与探索(Grace)工具进行数据绘图(https://plasma-gate.weizmann.ac.il/Grace/).
计算环境
BIOVIA Discovery Studio软件程序安装在Windows 10上。在一台Windows 10计算机(英特尔酷睿i5-4690 CPU @ 3.50 GHz, 3501 MHz, 4核和4逻辑处理器)上以自动方式对植物化学物质进行了分析。RAM的配置是:4个插槽,其中3个插槽各有8 GB RAM和1个插槽4 GB RAM,总共28 GB, DDR3和1600 MHz的速度。网络分析(随机行走与重启算法)、KEGG路径富集和GO分析在服务器CentOS计算机上进行,Intel Xeon CPU E5-2680 v3 @ 2.50 GHz, 48核。RAM的配置是:16个插槽,32gb RAM, DDR4。MD模拟使用:Linux系统(Ubuntu 2021.4-2)计算机(Intel Core i7-10,700 CPU @ 2.90 GHz × 16, Mesa Intel UHD Graphics 630 (CML GT2) / llvmpipe (LLVM 13.0.1, 256位,64.0 GB RAM))。
结论
计算机分析为鉴定活性化合物、预测化合物的生物活性以及指导传统药物的合理化使用提供了一种快速的方法。计算目标钓鱼是一种新的药物研究方法,有助于研究药物与疾病之间的关系。利用admetSAR和SwissADME在线服务器,对埃塞俄比亚本土芦荟植物化学物质的ADMET和药物相似特征进行了评估。然后,利用硅药效团模型预测了潜在的治疗靶点,并揭示了广泛的相关治疗潜力。
研究结果表明,埃塞俄比亚本土芦荟中的植物化学物质是潜在的治疗分子,具有82个相关靶点,这些靶点在许多KEGG途径和GO术语中富集。结果表明,这些植物化学物质具有广泛的治疗靶点,并有可能调节重要的生物途径,如类固醇激素生物合成代谢、脂质和动脉粥样硬化、化学致癌、IL-17信号通路、Th17细胞分化和癌症途径等。此外,本研究表明,植物化学物质可能被用作许多癌症的潜在治疗剂,以及内分泌、代谢、免疫、神经、消化、肌肉骨骼和血液系统疾病,以及先天性代谢紊乱、传染病、口腔和牙齿疾病。尤其是芦荟答:debrana基督教和答:megalacantha贝克认为癌症与内分泌疾病有关;答:gilbertiiSebsebe和Brandham,答:monticola雷诺兹,答:schelpei雷诺兹与先天性代谢障碍有关;答:adigratana雷诺兹和答:线虫托德与消化系统疾病有关;等等。这一信息表明,预计这些芦荟对治疗上述疾病有效。为了进一步证实这些作用,植物化学物质的药理作用有待于进一步的对照实验研究。
数据可用性
所有相关数据都在论文和支持信息文件中。
参考文献
Medcalf, A., Bhattacharya, S., Momen, H., Saavedra, M. & Jones, M.全民健康 :全民健康覆盖之旅。(东方黑天鹅私人有限公司2015)。
Mushtaq, S., Abbasi, b.h., Uzair, B. & Abbasi, R.天然产物作为新型治疗药物的储存库。EXCLI J。17中文信息学报,420-451(2018)。
越来越多的草药使用:与不良反应有关的问题和监测安全性的挑战。前面。神经。4, 1-10(2014)。
Cragg, g.m.和Newman, d.j.下一个千年的天然产物药物发现。制药。医学杂志。39, 8-17(2001)。
Newman, D. J. & Cragg, g.m.在1981年1月1日至2019年9月的近四十年中,天然产品作为新药的来源。J.纳特。83中文信息学报,770-803(2020)。
Rainsford, k.d., Powanda, m.c.和Whitehouse, m.w.。新型天然产物:治疗疼痛、关节炎和胃肠道疾病。药物研究进展卷70(施普林格巴塞尔,2015年)。
Grace, O. M., Simmonds, M. S. J., Smith, G. F.和Van Wyk, A.芦荟L. (Asphodelaceae):综述。经济学。机器人。63, 167-178(2009)。
Dagne, E., Bisrat, D., Viljoen, A.和Van Wyk, b.e .。芦荟的化学成分。咕咕叫。Org。化学。4, 1055-1078(2005)。
Belayneh, A, desmissew, S, Bussa, n.f.和Bisrat, D.埃塞俄比亚东非大裂谷区南部和东部芦荟的民族医药和生物文化重要性。Heliyon6, e04344(2020)。
重要贸易回顾:东非芦荟。9.2文档。2附件4。:CITES植物委员会第14次会议,纳米比亚温得和克16 - 20(2004)。
desmissew, S., Nordal, I.和Stabbetorp, O. E.埃塞俄比亚和厄立特里亚芦荟属植物区系的特有特征和分布模式。医学杂志。Skr。(2001)。
爱德华兹,S., Nemomissa, S.和Hedberg, I.。埃塞俄比亚和厄立特里亚的植物群(亚的斯亚贝巴大学,2003)。
Maia, E. H. B., Assis, L. C., de Oliveira, T. A., da Silva, A. M. & Taranto, A. G.基于结构的虚拟筛选:从经典到人工智能。前面。化学。8, 343(2020)。
Hillisch, A, Pineda, L. F. & Hilgenfeld, R.同源模型在药物发现过程中的效用。药物。今天9, 659-669(2004)。
Meslamani, J。et al。基于蛋白质配体的药物载体:计算配体分析的产生和效用评估。j .化学。正无穷。模型。52中文信息学报,943-955(2012)。
作为活动分析工具的3D药效团。药物。今天抛光工艺。7, e205-e211(2010)。
Campillos, M, Kuhn, M, Gavin, a - c。,Jensen, L. J. & Bork, P. Drug target identification using side-effect similarity.科学321, 263-266(2008)。
Dubus, E., Ijjaali, I., Barberan, O.和Petitet, F.使用硅化合物分析的药物重新定位。未来医学。化学。1, 1723-1736(2009)。
Anighoro, A., Bajorath, J.和Rastelli, G. .多种药理学:药物发现的挑战和机遇。医学化学。57中文信息学报,7874-7887(2014)。
Wermuth, c.g, Ganellin, c.r, Lindberg, P. & Mitscher, l.a.术语的化学家在药物化学中使用的术语。纯粹的达成。化学。70, 1129-1143(1998)。
Seidel, T., Wieder, O., Garon, A. & Langer, T.,天然产物启发药物设计中药效团概念的应用。摩尔。通知。39, e2000059-e2000059(2020)。
张晓明,张晓明,张晓明,等。药物药效团鉴定程序的比较:Catalyst, DISCO和GASP。j .第一版。辅助。摩尔,Des。16, 653-681(2002)。
清,X。et al。药效团模型:在药物发现中的进展、限制和当前效用。j .受体。配体通道Res。7, 81-92(2014)。
计算机辅助药物设计中药效团概念的历史与演变。咕咕叫。上面。地中海,化学。2, 1321-1332(2005)。
Kanehisa, M. & Goto, S. KEGG:京都基因和基因组百科全书。核酸类。28, 27-30(2000)。
Lucas, A. J, spproston, J. L, Barton, P. & Riley, R. J.评估人类ADME特性,药代动力学参数和药物发现的可能临床剂量。当今专家。药物。14中文信息学报,1313-1327(2019)。
程,F。et al。AdmetSAR:一个全面的来源和免费的工具,用于评估化学ADMET性质。j .化学。正无穷。模型。52中文信息学报,3099-3105(2012)。
金,S。et al。PubChem物质和化合物数据库。核酸类。44, d1202-d1213(2015)。
Daina, A., Michielin, O.和Zoete, V. SwissADME:一个评估小分子药代动力学,药物相似性和药物化学友好性的免费网络工具。科学。代表。7, 42717(2017)。
Lipinski, C. A, Lombardo, F, Dominy, B. W. & Feeney, P. J.在药物发现和开发环境中估计溶解度和渗透率的实验和计算方法。药物输送牧师。64, 4-17(2012)。
韦伯博士。et al。影响候选药物口服生物利用度的分子特性。医学化学。45, 2615-2623(2002)。
Cosconati, S。et al。基于autodock的虚拟筛选:理论与实践。当今专家。药物。5, 597-607(2010)。
Shannalee R. Martinez, Maresha S. Gay, L. Z. BDDCS, 5法则和可药物性。药物输送牧师。176, 139-148(2016)。
Palm, K., Stenberg, P., Luthman, K. & Artursson, P.,极性分子表面特性预测人类对药物的肠道吸收。制药。Res。14, 568-571(1997)。
使用多元方法表征细胞毒性海洋代谢物的药物样化学空间。ACSω4中文信息学报,5402-5411(2019)。
杜克,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,陈晓明,等。口服药物空间超越5法则:来自药物和临床候选药物的见解。化学。医学杂志。21, 1115-1142(2014)。
Azman, M, Sabri, A. H, Anjani, Q. K, Mustaffa, M. F. & Hamid, K. A.肠道吸收研究:改善口服药物输送的挑战和吸收增强策略。药品15, 1-24(2022)。
Shirasaka, Y., Sakane, T.和Yamashita, S. p -糖蛋白表达水平对药物对细胞膜渗透性的影响。j .制药。科学。97; 553-565(2008)。
p -糖蛋白对最佳药物递送的抑制作用。药物靶点见解7, 27-34(2013)。
艾勒,s.g.。et al。p糖蛋白的结构揭示了多特异性药物结合的分子基础。科学323, 1718-1722(2009)。
Lynch, T. & Price, A.细胞色素P450代谢对药物反应、相互作用和不良反应的影响。点。Fam公司。医生76; 391-396(2007)。
Yu H。et al。结语:整合多层次情境导向的药物效应分析关联。科学。代表。7, 7519(2017)。
希弗,L。et al。人类类固醇的生物合成、代谢和排泄是不同的反映血清和尿液类固醇代谢组:一个全面的综述。J.类固醇生物化学。摩尔。杂志。194, 105439(2019)。
Davis Robert, H.使用芦荟作为生物载体的方法。美国专利,US 5,708,038(1998)。
Dana, N., Javanmard, s.h, Asgary, S., Asnaashari, H. & Abdian, N.芦荟叶凝胶对高胆固醇血症家兔脂肪条纹形成的影响。医学科学杂志。掉了。伊斯法罕大学医学科学17, 439-442(2012)。
桑德斯,B。et al。芦荟大黄素抗癌作用的系统综述。j .中国。Transl。Res。3., 283-296(2018)。
Manirakiza, A, Irakoze, L. & Manirakiza, S.芦荟及其对癌症的影响:叙述性文献综述。东非治愈。> J。5, 1-16(2021)。
哈里斯,文学硕士。et al。基因本体数据库和信息学资源。核酸类。32, d258-d261(2004)。
财团,T。g.o.基因本体论资源:20年,依然强大。核酸类。47, d330-d338(2019)。
Tsegay, M., Tewabe, Y., Bisrat, D.和Asres, K. .芦荟叶胶中两种药物的体内抗炎活性。阿比西尼亚的。制药。J。34, 1-8(2018)。
Fentaw E。et al。的使用和可持续性芦荟埃塞俄比亚中部和北部高地的L.(藤科)。【南非】J.博特。147, 1042-1050(2022)。
詹,F。et al。了解β-乳球蛋白与辣椒素的相互作用:多光谱、热力学、分子对接和分子动力学模拟方法。Hydrocoll食物。105, 105767(2020)。
Sahihi, M. & Ghayeb, Y.分子动力学模拟和分子对接的研究:柑橘类黄酮和牛β-乳球蛋白的相互作用。第一版。医学杂志。地中海。51, 44-50(2014)。
Bultum, l.e., Woyessa, a.m.和Lee, D. ETM-DB:整合埃塞俄比亚传统草药和植物化学物质数据库。BMC补。交错的。地中海。191-11(2019)。
Bolton, E. E., Wang, Y., Thiessen, P. A. & Bryant, S. H. PubChem的物质和化合物。为基础。众议员第一版。化学。4中文信息学报,217-241(2008)。
达索系统公司股价。BIOVIA,探索工作室。(2021)。
斯坦贝克,C。et al。classfire:自动化学分类与一个全面的,可计算的分类法。j . Cheminform。8, 1-20(2016)。
Mishra, H., Singh, N., Lahiri, T. & Misra, K.一项预测小分子药物相似性的分子描述符的比较研究。Bioinform。3.; 384-388(2009)。
Benet, L. Z., Hosey, C. M., Ursu, O. & Oprea, T. I. BDDCS, 5规则与可用药性。药物输送牧师。101, 89-98(2016)。
Hanser, T., Steinmetz, F. P., Plante, J., Rippmann, F. & Krier, M.通过不同(Q)SAR方法和数据来源的协同组合来避免药物设计中的herg责任:一个工业环境中的案例研究。j . Cheminform。11, 9(2019)。
遗传毒理学测试。在非临床药物开发毒理学综合指南。129-154 (Elsevier, 2017)。
Sydow D。et al。计算目标预测的进展与挑战。j .化学。正无穷。模型。https://doi.org/10.1021/acs.jcim.8b00832(2019)。
麦格雷格,M. J.和M. M.药效团指纹图谱。2.在小学图书馆设计中的应用。j .化学。正无穷。第一版。科学。40, 117-125(2000)。
Meslamani, J, Rognan, D. & Kellenberger, E. sc-PDB:一个用于识别蛋白质中“可药物”结合位点变异和多样性的数据库。生物信息学27, 1324-1326(2011)。
UniProt:通用蛋白质知识库。核酸类。46, 2699(2018)。
MD Aksam, V. K, Chandrasekaran, V. M. & Pandurangan, S.人类丝裂原活化蛋白激酶(MAPK)通路网络的枢纽节点:特征和潜在的药物靶点。信息学医学解锁9, 173-180(2017)。
药物大小的化合物与多达一千个残基的蛋白质的盲对接。2月。580, 1447-1450(2006)。
刘,Y。et al。CB-Dock:一个用于空腔检测引导蛋白质与配体盲对接的web服务器。学报杂志。罪。41中文信息学报,138-144(2020)。
亚伯拉罕,m.j.。et al。GROMACS:通过从笔记本电脑到超级计算机的多级并行性进行高性能分子模拟。SoftwareX1 - 2, 19-25(2015)。
Bjelkmar, P., Larsson, P., Cuendet, M. A., Hess, B. & Lindahl, E. GROMACS中CHARMM力场的实现:来自校正图、虚拟相互作用位点和水模型的蛋白质稳定性影响分析。j .化学。理论第一版。6, 459-466(2010)。
Zoete, V., Cuendet, M. A., Grosdidier, A.和Michielin, O. SwissParam:小有机分子的快速力场生成工具。j .第一版。化学。32, 2359-2368(2011)。
Golo, V. L. & Shaĭtan, K. V. Berendsen恒温器的动态吸引子和生物大分子的慢动力学。Biofizika47, 611-617(2002)。
Tuble, S. C, Anwar, J. & Gale, J. D.一种用于马氏体相变分子模拟的力场方法,在能量和结构上存在细微差异。j。化学。Soc。126, 396-405(2004)。
致谢
本研究由韩国政府科学与信息通信技术部(MSIT)资助的韩国国家研究基金会(NRF)生物与医疗技术发展计划(2022M3A9B6017511)支持。这项工作也得到了韩国政府资助的韩国国家研究基金会(NRF)的部分支持,MSIT (2020R1A2C3005453)。
作者信息
作者及单位
贡献
L.E.B.构思和设计研究,撰写手稿,进行实验和分析数据;G.B.T.设计了这项研究;G.K.处理和分析数据,O.K.进行数据处理和可视化,D.L.设计研究并监督整个项目。所有作者都审阅了手稿。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益冲突。
额外的信息
出版商的注意
b施普林格《自然》杂志对已出版的地图和机构的管辖权要求保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,该协议允许以任何媒介或格式使用、共享、改编、分发和复制,只要您适当地注明原作者和来源,提供知识共享许可协议的链接,并注明是否进行了更改。本文中的图像或其他第三方材料包含在文章的知识共享许可协议中,除非在材料的署名中另有说明。如果材料未包含在文章的知识共享许可中,并且您的预期用途不被法律法规允许或超过允许的用途,您将需要直接获得版权所有者的许可。如欲查阅本许可证副本,请浏览http://creativecommons.org/licenses/by/4.0/。
关于本文
引用本文
Bultum, l.e., Tolossa, g.b., Kim, G。et al。利用药效团模型分析埃塞俄比亚本土芦荟植物化学物质的硅活性和ADMET谱。Sci代表12, 22221(2022)。https://doi.org/10.1038/s41598-022-26446-x
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-26446-x