摘要
我们测量了口腔病原体产生挥发性有机化合物(VOCs)的变化Porphyromonasgingivalis在体外用抗生素阿莫西林治疗时。我们还测量了VOC的产量P。gingivalis在有或没有补充血红素的情况下生长的.在浮游细菌生长迟滞期,用不同剂量阿莫西林处理浮游细菌培养。在培养基中分别添加和不添加血红素对浮游细菌进行培养。采用质子转移-飞行反应时间质谱法(PTR-ToF-MS)测定VOCs浓度,并采用固相微萃取(SPME)采样,采用气相色谱-质谱法(GC-MS)进行分子鉴定。细胞生长P。gingivalis用波长为600 nm (OD)的光密度测量来估计600).我们发现,使用阿莫西林进行抗生素处理后,甲硫醇、硫化氢和几种短至中链脂肪酸的产生减少了。发现随着抗生素处理而增加的化合物是丁酸和吲哚。在不添加血红素的培养物中,吲哚和中链脂肪酸的产量显著降低。研究发现,当没有补充血红素时,乙酸的产量会增加。我们的结果表明,抗生素治疗和补充hemin可用性的代谢效应都反映在产生的VOCsP。gingivalis并且可以作为细菌细胞生长和对威胁反应的标记。从人类样本中分析这些挥发物,如呼出的气,可以在未来用于快速监测对抗菌治疗的反应。
简介
Porphyromonasgingivalis是一种革兰氏阴性口腔细菌,参与牙周炎的发展和恶化,牙周炎是一种破坏支持牙齿的软组织和骨组织的炎症性疾病。牙周炎是许多其他全身性疾病的危险因素P。gingivalis是否与糖尿病、阿尔茨海默病、心血管疾病、癌症和不良妊娠结局有关1.通常这些疾病在恶性循环中相互恶化,口腔炎症导致全身健康恶化,从而导致免疫反应减弱和更多炎症2.P。gingivalis也与牙齿脓肿有关,如果大量细菌进入血液,就会导致败血症3..早期至重度牙周炎,包括I-III期,建议用口腔清洁治疗,如刮除或磨平牙根表面,而不常规使用全身抗生素或辅助治疗4.然而,晚期牙周炎可能需要外科手术,如移植或移除皮瓣,以及抗生素5.然而,抗生素的过度使用和抗生素耐药性的增加已成为现代社会的最大问题之一。新的、更具体的针对细菌感染的方法不断被开发出来,以对抗这种疾病,但这种治疗方法的高成本和低可用性鼓励了传统抗生素的使用,特别是在发展中国家。快速识别病原体对靶向治疗至关重要。传统上,这是通过培养或聚合酶链反应(PCR)方法来完成的,这可能很耗时。这既可以延长治疗时间,也可以鼓励使用广谱抗生素。此外,抗生素治疗的进展通常只能通过评估患者的症状来监测。一种快速识别和监测细菌感染的方法可以帮助减少不必要的广谱抗生素的使用,同时确保治疗的成功。分析细菌产生的挥发性有机化合物(VOCs)已被认为是一种从呼气、血液、尿液或唾液顶隙等样本中识别病原体的快速方法6,7,8,9,10,11,12.
阿莫西林是一种广谱青霉素类抗生素,可抑制细菌细胞壁生物合成。它是治疗口腔感染和晚期牙周炎最常用的抗生素之一,通常与β-内酰胺药物联合使用以克服耐药性13.它还与甲硝唑等其他抗生素联合使用,以增强抗菌效果5,13.在体内和体外实验中,人们普遍认为阿莫西林与β-内酰胺类药物或甲硝唑联合使用对牙周病原体极为有效5,13,14,15.然而,也有证据表明许多牙周病原体对阿莫西林有耐药性16,17,单用青霉素类抗生素对牙周菌群无明显影响18亚致死浓度的阿莫西林可增加生物膜的形成19.在蛋白质组学和基因表达研究之外,研究抗生素对代谢产物的影响P。gingivalis是稀缺的,而那些研究抗生素对挥发性代谢物影响的人更是如此。然而,关于抗生素和其他环境因素对细菌代谢产物影响的研究存在于一些物种,如埃希氏杆菌属杆菌、分枝杆菌smegmatis,葡萄球菌葡萄球菌,假单胞菌绿脓杆菌20.,21,22,23,24,25,26,27,28,29.细胞外血红素是影响小鼠正常代谢的重要环境因子P。gingivalis30.以及在hemin-poor条件下P。gingivalis毒性降低31.液相研究调查血红素对代谢产物的影响P。gingivalis已经执行过31,但没有关于挥发性代谢物的研究。如果抗生素治疗或环境因素改变了voc谱P。gingivalis在体外,体内人体样品的voc谱也可以看到变化。这为监测细菌感染对抗菌治疗的反应提供了新的可能性。
我们之前已经确定了一些由口腔致病菌产生的最重要的挥发性有机化合物,包括P。gingivalis6,7.这些化合物包括几种硫化合物,如甲硫醇、硫化氢、2-甲基丙硫醇、二甲基二硫化物、二甲基三硫化物、二甲基四硫化物和年代-甲基硫酯,以及几种短链和中链脂肪酸,几种异戊酯,6-甲基-1,2,3,4-四氢喹啉和1-甲基-1,2,3,4-四氢异喹啉6,7.在当前的研究中,我们想要研究环境因素的变化是否对生产的VOCs产生影响P。gingivalis以及这些变化是否可以用来评估细菌的生存能力或毒性。我们选择血红素和阿莫西林作为环境变量,因为它们对代谢的影响P。gingivalis虽然它们对挥发性有机化合物产生的影响还不清楚。采用质子转移-反应飞行时间质谱(PTR-ToF-MS)和固相微萃取(SPME)结合气相色谱-质谱(GC-MS)对VOCs进行鉴定和测定。我们研究了浮游培养产生的挥发物的变化P。gingivalis在存在阿莫西林和补充血红素不可用时。我们的目的是确定受阿莫西林和补充血红素的可用性影响最显著的化合物,并评估它们作为细菌对抗菌治疗反应的标记物的潜力。在这篇文章中,我们还讨论了可能的代谢来源的变化vocs生产P。gingivalis.
材料与方法
初始细菌培养
的参考应变P。gingivalisATCC 33277(血清型Pg a)来源于美国类型培养集(American Type Culture Collection, ATCC)。所使用的培养方法我们已经在前面描述过了6,7.参考菌株储存在−80°C的冷冻脱脂牛奶中。菌株在布氏菌血琼脂(BBLTM, 211086)板上划纹激活,添加马血(5% v/v)、血红素(5mg /L)和维生素K (1mg /L)。初始培养物在厌氧气体混合物(5% CO)中培养2, 10% h285% N2孵育后,将3.0 mL磷酸盐缓冲盐水(PBS)移液管移到琼脂板上,将细菌块从琼脂上轻轻刮入5 mL Falcon™管中。所得到的细菌悬浮液通过轻轻移液均质。将500 μ L的细菌悬浮液移液到5.0 mL胰蛋白酶大豆肉汤(TSB, ATCC 2722)中,并添加血红素(5mg /L)和维生素K (1mg /L)。该细菌培养物在37°C下无搅拌厌氧培养,直到600 nm处的光密度达到1.0(第0批),这大约相当于109细胞/毫升。
阴性和阳性对照
本研究阴性对照为新鲜TSB (ATCC 2772),不添加任何细菌。在50 mL瓶中制备10 mL TSB的3个副本,用于阴性对照测量。阳性对照是将1.25 mL前一节所述的细菌培养物(第0批)加入10 mL新鲜TSB (ATCC 2722)中,装在50 mL瓶中。同时制备3份阳性对照。
抗生素治疗
将阿莫西林(Sigma Aldrich)溶解于极少量(1 ~ 2滴)1m NaOH溶液中。测量中使用的阿莫西林的最终浓度从这批中用灭菌水稀释。使用OD测量细菌生长曲线600用来估计滞后,指数和细菌生长的固定阶段。分别测定0、15、30 h的时间点。在这些时间点的培养中加入阿莫西林试验浓度,以研究抗生素治疗在细菌生命周期不同阶段的效果。因此,VOC测量选择滞后期,因为阿莫西林对细菌生长的影响最大。根据不同阿莫西林浓度下的生长曲线,选择15和150µg/mL两种暴露浓度进行VOC的测定。将1.25 mL细菌培养物(第0批)加入10 mL含阿莫西林的新鲜TSB中,在50 mL瓶中制备3个重复培养物,用于VOC的测量。
限制性补充血红素
将1.25 mL细菌(第0批)添加到10 mL不添加hemin的新鲜TSB (ATCC 2722(−hemin))中,在50 mL瓶子中制备第一传代培养。制备三份。使用OD测量细菌生长曲线600有或没有补充的hemin存在可以从补充信息中找到(图。S4).在添加和不添加血红素的培养物中观察到细菌负荷没有显著差异,然而,在缺乏补充血红素的培养物中,细菌生长达到指数和固定阶段的时间稍晚。
VOCs的测量和识别
PTR-ToF-MS的方法和操作条件我们已经介绍过6,7.测量从m / z17到239,H3.O+作为试剂离子。所使用仪器的质量分辨率(PTR-TOF 1000, Ionicon)为1500(全宽半最大)。PTR-ToF-MS操作条件如下:E / N)的116 Td(对应漂管电压为500v);漂移管压力2.20 mbar;H2O流量5.0标准立方厘米每分钟(sccm);离子源电流3.0 mA;进口流量为65立方厘米。漂移管和入口温度保持在70°C。采样频率为1频谱/秒。此外,还有一个单独的传感器用于CO的测量2(Vaisala, GMP251)。为了获得准确的浓度,PTR-ToF-MS仪器应分别校准每种化合物,在细菌样品的情况下,这是大量的。在本研究中,PTR-ToF-MS仪器没有针对每种分析化合物进行专门校准,因此,本工作中提出的浓度应被认为是估计值。
气相色谱-质谱联用方法和操作条件我们之前也有过介绍7.简单地说,使用了电子电离(EI)结合四极质谱仪(Agilent 5973N MSD)的gc仪器(Agilent 6890 A)。色谱柱(DB-1701, J&W Scientific)长度为30 m,内径为0.25 mm,薄膜厚度为0.15µm。保持2分钟后,温度从40°C上升到250°C(10°C/min)。采用无分裂注射,注射后无分裂时间为2min。注射口保持在240°C。载气(99.996%氦气,林德气)流量为1.0 mL/min。GC-MS转移线保持在250℃。在20 ~ 300 u的质量扫描范围内进行测量,电离能为70 eV,离子源温度为230℃,四极温度为150℃。用聚二甲基硅氧烷/二乙烯基苯SPME Arrow (CTC Analytics AG, Zwingen, Switzerland)对细菌培养物顶部空间的挥发物进行采样。 The National Institute of Standards and Technology NIST14 Mass Spectral Library and Analysis Tools were used for the tentative identification of compounds from the measured mass spectra. Most compounds were also further identified using reference samples (Sigma Aldrich).
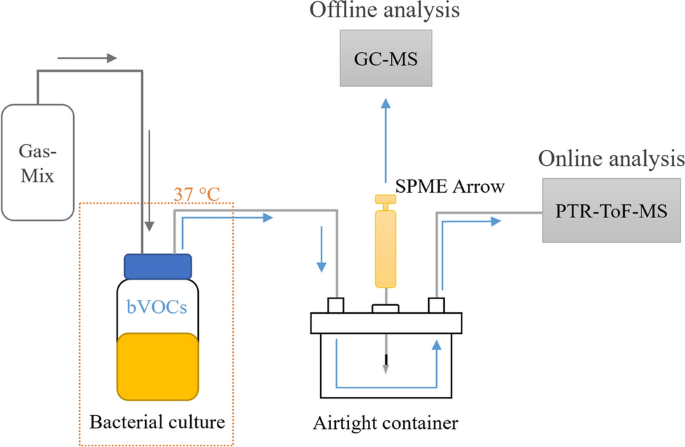
数字1描述了本研究中使用PTR-ToF-MS和GC-MS测量细菌VOC的完整设置。PTR-ToF-MS连续测量100 h,每次测量20 min。70立方厘米的厌氧气体混合物流量被引导通过细菌培养。GC-MS测量样品在0和100小时采集并离线分析。在测量过程中,培养条件保持在37℃和常压下。
通过计算3份重复样品的平均浓度和标准差进行统计学评价。
结果
生长曲线的例子P。gingivalis在不同浓度的阿莫西林,以及阿莫西林在细菌生长的不同阶段的杀菌性能,在补充资料(图。S1).生长曲线的例子P。gingivalis在添加和不添加血红素的情况下培养的细胞也在补充信息中显示(图。S4).的顶空间识别的化合物的完整列表P。gingivalis使用GC-MS,不包括由TSB产生的化合物,在补充信息(表S1).相应的PTR-MS信号,以及理论质子化质量也在表中S1.一个VOC只由TSB产生的例子,而不是由P。gingivalis,也在补充信息中显示(图。S3).
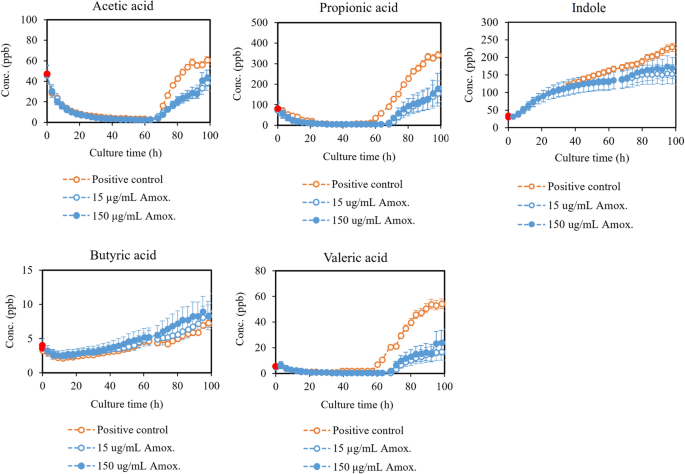
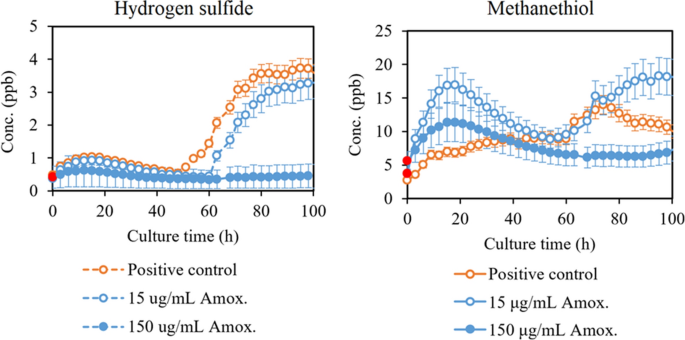
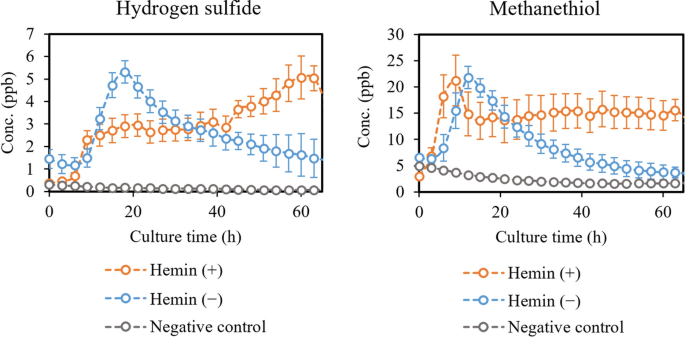
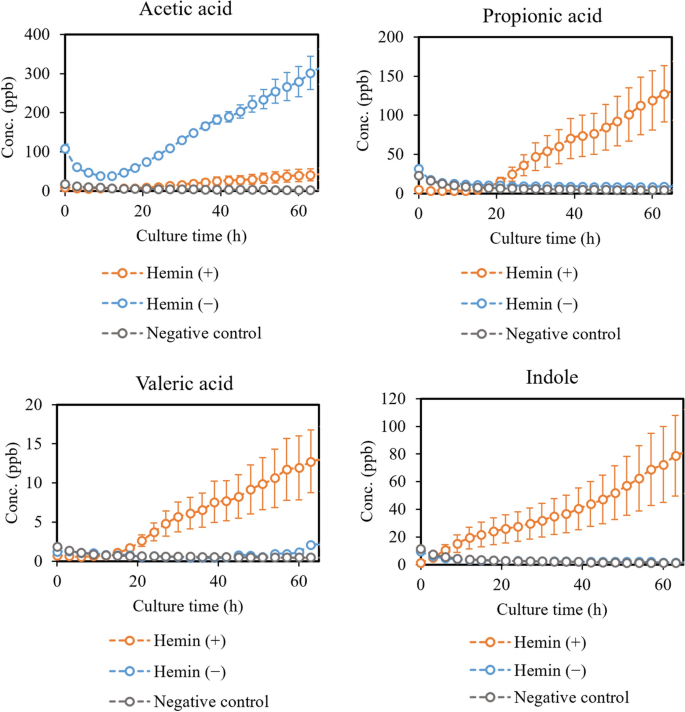
在这里,我们介绍了受抗生素治疗和补充hemin可用性显著影响的VOCs的生产概况。数字2为阿莫西林对挥发性中链脂肪酸和吲哚的总影响。3.在甲硫醇和硫化氢上,当抗生素在培养开始时加入。此外,生长校正终点(90 h)浓度(Conc。(含量/ OD600)列于表1.
数字4介绍了添加血红素对硫化物硫化氢和甲硫醇的影响。数字5研究了补充血红素对所选中、短链脂肪酸和吲哚的影响。生长无显著性差异P。gingivalis添加和不添加血红素(补充信息图。S4),因此,没有进行生长校正。
讨论
阿莫西林的作用
如前所述,研究抗生素对代谢产物的影响P。gingivalis是稀缺的。然而,对其他物种的研究已经完成,比如E。杆菌、M。smegmatis,年代。葡萄球菌,P。绿脓杆菌20.,21,22,23,24,25,26,27,28,29,其中一些研究挥发性代谢物。然而,使用不同的抗生素和分析技术阻碍了结果之间的比较。此外,许多早期的研究集中在基于单点VOC谱(离线方法测量)分离抗生素耐药菌株和非耐药菌株。只有少数早期研究调查了抗生素对挥发性代谢物的实时影响,检查了生长校正浓度,或讨论了所建议的标记化合物的代谢意义22,23.在本节中,我们将抗生素对细菌代谢物影响的最相关的早期研究结果与我们的结果进行比较P。gingivalis。
在液相研究中,Belenky等人表明,特别是中链脂肪酸产生E。杆菌在使用氨苄西林(一种与阿莫西林同属一类的抗生素)治疗后会减少27.他们还发现碳水化合物和能量代谢物(如丙酮酸)的相对浓度增加了。氨苄西林处理的细菌细胞对半胱氨酸、赖氨酸、蛋氨酸和色氨酸的利用率也增加,这表明这些氨基酸的产物也增加了。这些产品包括硫化氢、甲硫醇、吲哚和氨。事实上,Han等人的另一项早期液相研究发现,细胞外吲哚的产生增加E。杆菌用氨苄青霉素治疗28.此外,Wiesner等人的一项研究检测了挥发性代谢物,发现甲烷硫醇的产量下降时E。杆菌而且年代。葡萄球菌分别用氨苄西林和唑西林治疗21.唑西林是青霉素类的另一种抗生素。另一项由Allardyce等人进行的气相研究发现,几种硫化合物的产量下降,包括甲硫醇和硫化氢、乙酸和吲哚E。杆菌用庆大霉素治疗25.他们还发现氨和二甲基硫化物的产量下降年代。葡萄球菌用氟氯西林治疗氟氯西林是青霉素类抗生素,庆大霉素不是。
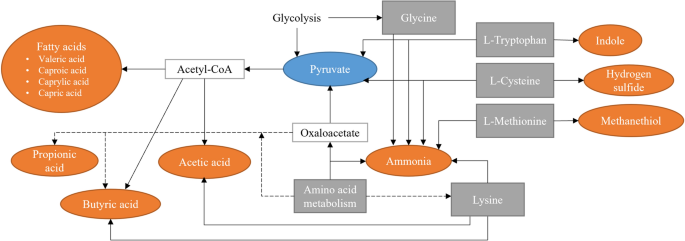
我们的结果证实了之前的大部分发现。我们发现,总的来说,阿莫西林降低了挥发性脂肪酸的产生P。gingivalis.这些化合物包括短链和中链脂肪酸,如乙酸、丙酸、戊酸、2-甲基己酸和辛酸。有趣的是,丁酸的产生被发现增加阿莫西林的存在。它是唯一一种发现对抗生素治疗有积极反应的挥发性脂肪酸。P。gingivalis能产生多种短链脂肪酸31,它们既与细胞毒性有关,也与有益作用有关,这取决于环境32,33.其中一些脂肪酸尤其对肠道健康有益,而它们在慢性牙周炎患者的龈沟液中的作用则是负面的34.浓度似乎与牙周病的严重程度相关34.丙酸、丁酸、异丁酸、戊酸和异己酸也在病变部位的牙菌斑中被发现35.研究还表明,许多不同类型的细胞,包括口腔上皮细胞,对这些酸很敏感35,36.因此,我们假设短链脂肪酸是牙周病原体引起宿主细胞脱离、细菌渗透和组织破坏的重要毒力因素35.特别是丁酸已被证明可诱导严重的细胞毒性作用,其次是丙酸和戊酸37.事实上,McKee等人表明,在所有测试中,毒性最强的细菌产生的这些细胞毒性代谢物浓度最高P。gingivalis菌株31.因此,在阿莫西林的存在下,挥发性丁酸的产量增加可能是一种抵消P。gingivalis对环境的威胁.其他脂肪酸和丁酸之间的区别的一个可能的原因是P。gingivalis丁酸有几种可能的产生途径,而其他脂肪酸主要通过乙酰辅酶A(乙酰辅酶A)产生,如图所示。6.由于抗生素胁迫,糖酵解活性与氨基酸利用的变化可能导致VOC产量的差异。脂肪酸是许多细菌物种以及人体的常见代谢物,这使得它们单独成为较差的生物标志物。然而,挥发性脂肪酸浓度的综合变化可用于监测抗菌治疗的效果。特别是丁酸与其他脂肪酸的关系有待进一步研究。
根据我们的结果,当阿莫西林不存在时,挥发性吲哚的实时产量更高。然而,当用细胞密度校正时,阿莫西林处理的培养物的终点浓度更高。这些结果支持了早期的一些发现27,28.从图中可以看出,吲哚是色氨酸代谢的产物。6.不同种类的细菌生产吲哚已被广泛研究28,41.除其他外,它与信号传递、耐药性和生物膜形成有关41.Han等人证明了这一点E。杆菌增加吲哚的产生以应对抗生素治疗,并提高细胞存活率28.吲哚还被证明可以增加那些自身不产生吲哚的细菌的耐药性28,41,对人体上皮细胞也有有益的作用28,41.因此,吲哚似乎是细胞中和或增强对威胁抵抗力的一种方式。因此,挥发性吲哚有潜力作为抗生素治疗下细菌活力的标记物。氨,另一个产物的色氨酸代谢和其他常见的代谢途径,也发现略有减少阿莫西林的存在。然而,质子化氨的PTR-MS信号受到离子源贡献的影响,这扭曲了记录的浓度。因此,本文不进一步讨论氨。氨是人类呼出气体的常见成分,主要来源于口腔细菌的脲酶活性42,这使得氨成为一种不理想的细菌生物标志物。
我们还发现硫化氢的生产由P。gingivalis通过阿莫西林治疗减少,这从实时测量和细胞密度校正终点浓度中都是明显的。阿莫西林对甲硫醇生产的影响不太清楚,只有在阿莫西林浓度大时才有明显的减少。然而,根据细菌生长曲线,在我们的培养体系中,15µg/mL的阿莫西林对细菌生长的抑制作用很小,而150µg/mL的阿莫西林则使细菌生长下降了70%。因此,未经处理的培养物和用较小浓度阿莫西林处理的培养物可能具有类似的产生某些化合物的能力。阿莫西林处理极有可能降低甲硫醇的产量,但其减少量与硫化氢不同。P。gingivalis酶法生产甲硫醇l-蛋氨酸和硫化氢l半胱氨酸43.此外,l-半胱氨酸可以转化为l-同型半胱氨酸和进一步l-甲硫氨酸,产生甲硫醇。中村等人表明,甲硫醇的生产由P。gingivalis实际上不依赖于细胞外的存在吗l-蛋氨酸,但硫化氢的生产依赖于l半胱氨酸44.将这些发现与我们的结果结合起来表明,在阿莫西林存在时硫化氢产量的减少很可能是由于(1)酶活性转向甲硫醇生产,或(2)细胞外利用率的增加l-半胱氨酸导致快速消耗。在阿莫西林存在的情况下,甲硫醇的产量不会像硫化氢那样减少,这一事实进一步证实了这一点。我们的结果表明,特别是硫化氢产量的变化,或硫化氢和甲硫醇的比例的变化,是生存能力的指标P。gingivalis在阿莫西林存在的情况下。此外,我们的结果证实了早期的发现,当细菌被抗生素治疗时,硫化氢和甲硫醇的产量总体上下降21,25.
所讨论的VOCs的产生与不同的细菌生长阶段相一致,结合Figs的实时生产概况就很清楚了。2而且3.和相应的生长曲线(补充信息图S1).吲哚和丁酸在细菌生长过程中产生,而其他短链和中链脂肪酸则在细胞开始裂解的后期静止和死亡阶段释放。甲硫醇和硫化氢在指数相活跃生成,但在固定相它们的水平下降。在培养的后半段,还可以观察到甲醇和硫化氢对细胞死亡的影响以及由此产生的VOCs的释放。根据这些结果,可以通过细菌产生的VOCs来监测不同的细菌生长阶段。例如,挥发性吲哚、硫化氢和甲硫醇的联合生产可作为活跃生长的指标,而大多数检测到的短链和中链脂肪酸与细胞死亡有关。
限制补充血红素的影响
据我们所知,调查铁源限制对细菌影响的气相研究很少或不存在。因此,在本节中,我们将相关液相研究的结果与我们的结果进行比较P。gingivalis.McKee等人发现,短链到中链脂肪酸,如丁酸和丙酸,是由P。gingivalis在血红素过量的情况下,含量更高31.据报道,在没有补充血红素的情况下,乙酸是唯一产生量较高的脂肪酸。我们的结果证实了这些发现,尽管是在气相中测量的。我们还从顶空中发现少量戊酸、己酸、辛酸和癸酸。在hemin丰富的条件下,它们增加。如前所述,的毒性P。gingivalis是否与细胞毒性化合物有关,如丁酸31,34,35,36,37.它还表明,最致命的影响是在hemin丰富的条件下实现的31.因此,缺乏外部铁源似乎降低毒力P。gingivalis重要的是,除其他外,因为短链和中链脂肪酸的产量减少。我们的结果表明,缺乏外部铁源会使这些毒力因子的产生降低到阴性对照的水平,除醋酸外。塌中链脂肪酸的产生P。gingivalis与乙酸的增加相结合是环境压力下细菌代谢转移的一个有希望的标志。
McKee等人发现P。gingivalis在hemin有限的条件下使用的细胞外色氨酸(消耗25%)比在hemin丰富的条件下(消耗50%)少31,这表明在hemin受限的情况下,吲哚的产生减少。我们的顶空测量结果证实了这一点。事实上,在我们的测量中,当没有补充血红素时,挥发性吲哚降低到阴性对照的水平。吲哚的缺乏是代谢分化的明确指标P。gingivalis与富hemin条件相比,不添加hemin的培养。特别是,因为在这些条件下,细菌生长之间没有发现重大差异。当没有补充血红素时,色氨酸利用率下降的一个可能原因当然是铁的缺乏。一些报告表明,在细菌和人类中,色氨酸代谢和铁之间存在联系45,46,但没有证据证明这一点P。gingivalis.蛋白质组学需要进一步研究这一问题。有趣的是,根据我们的结果,血红素和阿莫西林的作用是相反的。P。gingivalis在抗生素压力下产生更多的吲哚,但当补充的hemin不存在时,吲哚的生产崩溃。这进一步表明,当没有足够的铁时,色氨酸通路可能会受到严重干扰,而其他应激源则有不同的影响。
如前所述,甲硫醇和硫化氢是由蛋氨酸和半胱氨酸的酶分解产生的,尽管效率不同,对这些氨基酸的细胞外需求也不同。我们发现,在添加和不添加血红素的情况下,挥发性甲硫醇和硫化氢的最高水平相对相似,而在培养结束时观察到差异。根据McKee等人的研究,半胱氨酸被有效地利用P。gingivalis在hemin有限的情况下(消耗73%)和在hemin丰富的情况下(消耗55%)31.硫化氢的产生取决于细胞外半胱氨酸的数量,这意味着在hemin有限的条件下,它的有效利用会比hemin过量的情况下更早地达到硫化氢的最大浓度。这得到了我们的研究结果的支持,在培养的前20小时内,硫化氢会有效产生,之后随着半胱氨酸的耗尽,硫化氢会下降。在hemin过剩时,硫化氢在整个培养过程中持续产生。甲硫醇也观察到类似的趋势,尽管据报道它不依赖于细胞外蛋氨酸的量44.根据McKee等人的研究,蛋氨酸只被P。gingivalis血红素过量(消耗27%)31.也许P。gingivalis在无法利用细胞外蛋氨酸时,当补充的hemin不可用时,因此,细胞内蛋氨酸在细菌生长过程中被耗尽。这将导致在我们的结果中看到的甲硫醇产量的迅速下降。在富含hemin的条件下,利用细胞外蛋氨酸,这导致在整个培养过程中稳定生产甲硫醇。甲硫醇和硫化氢生产的区别P。gingivalis添加或不添加血红素的培养物不如添加脂肪酸和吲哚的培养物清晰。此外,这些硫化合物对补充血红素可用性的反应不像对抗生素应激那样强烈。
虽然细菌负荷会影响VOCs的产生量,但它不是唯一的因素。由细菌应激反应引起的代谢变化或利用内部铁库的需要也会影响所产生的VOCs的数量和组成。为了生存,P。gingivalis可能利用细胞内铁蛋白或从相关的原卟啉合成卟啉环,当hemin不可用时,但这些过程很可能比hemin过剩的过程需要更多的能量30.,47.引起的能量代谢的变化P。gingivalis可能会改变挥发性有机化合物的产量,但细菌的整体生长不会受到严重影响。在这项研究中,在第一代中限制补充hemin并没有观察到与生长相关的显著影响,但是VOC的产量却发生了明显的变化,如图所示。4而且5.根据这些结果,P。gingivalis通过改变其代谢来适应补充血红素的缺乏,这可以在产生的VOCs中观察到。因此,所讨论的VOCs是胁迫响应的标志P。gingivalis这在体外实验中尚未得到证实。
从生长曲线可以看出(补充信息图。S4),在没有补充hemin的情况下,细菌生长的指数期和静止期会稍晚一些。在早期的研究中也观察到这种现象,结果很可能是由于细胞需要使用细胞内铁储存库来生长48,49.如前所述,这可能比利用细胞外血红素消耗更多的能量,而细胞外血红素会略微减缓生长。同样,不同的细菌生长阶段和某些VOCs的产生之间的联系从图中的实时产量曲线中可以清楚地看出。4而且5,得到相应的生长曲线(补充信息图S4).就像前一节讨论的那样,在整个培养过程中产生吲哚,而硫化氢和甲硫醇更明显地与指数相联系。短链和中链脂肪酸的生成与稳态相一致,细胞裂解也有一定的作用。
结论
据我们所知,对任何细菌种类的挥发性代谢物进行的干预研究很少20.,21,22,23,24,25,26,50.此外,我们的研究首次调查了抗生素治疗和补充hemin限制对致病性口服厌氧菌特异性产生的挥发性化合物的影响P。gingivalis.我们的研究也是第一个证明如何通过细菌挥发性指纹的变化来实时检测细菌生长和代谢的研究之一。
我们的研究结果表明P。gingivalis在体外用阿莫西林改变其挥发性代谢物的组成。特别是醋酸、丙酸和戊酸在抗生素治疗后减少,硫化氢和甲硫醇也是如此。与此相反,阿莫西林处理时吲哚和丁酸增加。我们还表明,补充hemin的可用性影响挥发性代谢产物P。gingivalis显著。当补充的血红素不可用时,吲哚的生产几乎被否定,大多数短链和中链脂肪酸的生产也是如此。然而,醋酸在这些条件下明显增加。挥发性代谢物的变化很可能与细菌代谢紊乱有关,这是由对环境威胁的应激反应引起的。限制补充血红素通过改变细菌的代谢来影响挥发性代谢物的产生,而抗生素治疗也通过限制生长来影响挥发性代谢物的产生。此外,hemin的有效性对VOCs释放的影响P。gingivalis明显比阿莫西林更强。这一发现支持了使用铁结合化合物(如乳铁蛋白)治疗牙周炎的潜力51,50,51,54.
我们的结果表明,挥发性指纹图谱的变化P。gingivalis和一般的细菌,可以在未来用于估计抗菌治疗的有效性或作为细菌生长的标记物。最重要的是,由于这些代谢物是挥发性的,它们可以从人类呼出的气或唾液顶空等样本中测量,而不需要传统的细菌培养。这反过来又为快速病原体检测和非侵入性诊断提供了新的可能性。
数据可用性
在这项研究中分析的所有相关数据包括在这篇发表的文章及其补充信息文件中。在当前研究期间产生的原始测量数据可根据合理要求从通讯作者处获得。
参考文献
梅,F。et al。Porphyromonasgingivalis及其系统影响:现状。病原体9, 944(2020)。
普雷肖,下午。et al。牙周炎和糖尿病:双向关系。Diabetologia5, 21-31(2012)。
罗伯逊,D. &史密斯,A. J.急性牙脓肿的微生物学。微生物学。58, 155-162(2009)。
Sanz, M。et al。I-III期牙周炎的治疗——EFP S3级临床实践指南。j .中国。Periodontol。47, 4-60(2020)。
Graziani F。et al。牙周炎的非手术和手术治疗:一种疾病有多少种选择?Periodontol。2000(75), 152-188(2017)。
Roslund, K。et al。用质子转移反应质谱和气相色谱质谱鉴定口腔细菌挥发性体外生物标志物。科学。代表。11, 6897(2021)。
Roslund, K。et al。口腔致病菌体外产生挥发性化合物的在线分析。呼吸储备。14, 016010(2020)。
德雷斯,C。et al。GC-IMS顶空分析可以在标准血液培养中早期识别细菌生长和快速病原体分化。达成。Microbiol。Biotechnol。103, 9091-9101(2019)。
Monedeiro F。et al。用HS-SPME-GC/MS技术评估口臭和颌下腔脓肿时唾液VOC谱。分子24, 2977(2019)。
坎帕内拉,B。et al。用于挥发性唾液代谢物分析的HS-SPME-GC-MS方法,以及在间接评估肠道菌群的案例研究中的应用。肛交。Bioanal。化学。411, 7551-7562(2019)。
巴蒂,c。et al。挥发性有机化合物(VOC)分析及代谢组学检测免疫血小板减少症(ITP)患者尿顶空微生物代谢产物的差异中国。詹。学报。461, 61-68(2016)。
卡佩里,L。et al。电子鼻在尿样临床诊断中的应用综述。传感器16, 1708(2016)。
系统性抗生素在牙周治疗中的应用。欧斯特。凹痕。J。54, 96-101(2009)。
Takeshita, M。et al。器官培养组织中抗生素对牙周细菌的作用。中国。经验,削弱。Res。3., 5-12 (2017)
Belibasakis, G. N. & Thurnheer, T.体外牙龈下生物膜抗生素有效性的验证。j . Periodontol。85, 343-348(2014)。
Ardila C.-M。& Bedoya-García, j.a。抗微生物药物耐药性Aggregatibacteractinomycetemcomitans,Porphyromonasgingivalis而且Tannerella连翘牙周炎患者。j .水珠。Antimicrob。抗拒。22, 215-218(2020)。
Serrano C。et al。经常使用抗生素的牙周病原体对抗生素的耐药性。Acta Odontol。Latinoam。22, 99-104(2009)。
人,E。et al。全身抗生素影响牙周参数和口腔微生物群,但不影响血清学指标。前面。细胞。感染。Microbiol。11, 774665(2021)。
贝尔纳迪,S。et al。亚抑制性抗生素浓度促进临床生物膜的形成肠球菌粪隔离。抗生素。10, 874(2021)。
聪明,一个。et al。嗅出耐药性-使用挥发性代谢物谱快速识别尿路感染引起细菌及其抗生素敏感性。j .制药。生物医学。肛交。167, 59-65(2019)。
威斯纳,K。et al。通过顶空气体分析监测细菌生长和快速评估抗生素敏感性。Proc。英格。87, 332-335(2014)。
克雷斯波,E。et al。质子转移反应质谱检测挥发性代谢物排放的快速变化分枝杆菌smegmatis在加入特定的抗菌剂后。j . Microbiol。方法86, 8-15(2011)。
李海华,朱海燕。耐药菌的鉴别葡萄球菌葡萄球菌采用二次电喷雾电离串联质谱法。肛交。化学。90, 12108-12115(2018)。
Buszewski B。et al。生物银纳米颗粒对不同菌株代谢的影响体现在其VOCs谱上。呼吸储备。12, 027105(2018)。
阿勒代斯et al。用离子流管质谱法快速评估血液培养中的细菌生长和抗生素敏感性。成岩作用。Microbiol。感染。说。55, 255-261(2006)。
Drabiń平方公里列阵,N。et al。固相微萃取-气相色谱-质谱/金属氧化物传感器系统在尿路感染性抗生素敏感性检测中的应用埃希氏杆菌属杆菌-原理论证研究。医学科学67, 1-9(2022)。
还会,P。et al。杀菌抗生素引起毒性代谢紊乱,导致细胞损伤。细胞的代表。13, 968-980(2015)。
韩,t.h.。et al。影响吲哚生产的环境因素埃希氏杆菌属杆菌.Microbiol >,162, 108-116(2011)。
Kuczyńska-Wiś尼克,D。et al。促进氧化应激的抗生素抑制氧化应激的形成埃希氏杆菌属杆菌生物膜通过吲哚信号。Microbiol >,161, 847-853(2010)。
铁和血红素的利用Porphyromonasgingivalis.《。牧师。29, 119-144(2005)。
麦基,a.s.。et al。血红素对大鼠生理和毒力的影响拟杆菌gingivalisW50。感染。Immun。52, 349-355(1986)。
细菌挥发性化合物:在交流、合作和竞争中的功能。为基础。启Microbiol。74, 409-430(2020)。
Veselova, m.a., Plyuta, v.a. & Khmel, i.a.细菌来源的挥发性化合物:结构,生物合成和生物活性。微生物学88, 261-274(2019)。
陆,R。et al。非手术牙周治疗对全身性侵袭性牙周炎患者龈沟液中短链脂肪酸水平的影响j . Periodont。Res。49, 574-583(2014)。
Pöllänen, M. T., Salonen, J. I. & Uitto, V. J.牙齿-上皮界面在健康和疾病中的结构和功能。Periodontol。2000(3), 12-31(2003)。
短链脂肪酸对人类口腔上皮细胞的影响和对牙周病的潜在影响:体外研究的系统综述。Int。理学。21, 4895(2020)。
Scragg m.a., Cannon, S. J. & Williams, D. M.牙周病原体产生的短链脂肪酸对两种培养成纤维细胞系的细胞毒作用的比较。活细胞。生态。健康说。7, 83-90(1994)。
为了解细胞生物的起源和进化。蛋白质科学。28, 1947-1951(2019)。
金久,M. &后藤,S. KEGG:京都基因和基因组百科全书。核酸测定。28, 27-30(2000)。
纳尔逊,k。E。et al。口腔致病菌全基因组序列Porphyromonasgingivalis应变W83。j . Bacteriol。185, 5591-5601(2003)。
李,黄永发。李,J.吲哚作为微生物群落的细胞间信号。《。牧师。34, 426-444(2010)。
陈,W。et al。口呼氨气的起源。呼吸储备。8, 036003(2014)。
舒尔茨,S.和迪克夏特,J. S.细菌挥发物:小生物体的气味。奈特·普罗德代表24, 814-842(2007)。
中村,S。et al。Porphyromonasgingivalis硫化氢增强甲基硫醇诱导的小鼠脓肿形成的致病性。微生物学164, 529-539(2018)。
Pokorzynski, N. D., Brinkworth, A. J. & Carabeo, R.色氨酸挽救途径的二部铁依赖性转录调控衣原体trachomatis.Elife8, e42295(2019)。
Wenninger, J。et al。在缺铁和不缺铁的个体中观察到色氨酸和铁代谢之间的联系。科学。代表。9, 14548(2019)。
拉特纳亚克,d。et al。专性厌氧菌中的铁蛋白Porphyromonasgingivalis:纯化、基因克隆及突变体研究。Microbiol。146, 1119-1127(2000)。
吴,J。et al。一种新的转录激活剂对血红素结合蛋白的调控Porphyromonasgingivalis.j . Bacteriol。191, 115-122(2009)。
Kiyama-Kishikawa, M。et al。血红素限制下的基因表达谱和特征Porphyromonasgingivalis.口腔科学。47, 191-197(2005)。
Drabiń平方公里列阵,N。et al。从快速鉴定到耐药性测试:挥发性化合物谱作为一种新型的抗生素敏感性检测诊断工具。趋势肛门。化学。115, 1-12(2019)。
Berlutti F。et al。乳铁蛋白与口腔疾病:牙周炎研究现状与展望。安。Stomatol。(罗马)2, 10-18(2011)。
若林史江、H。et al。牙周炎,牙周病细菌和乳铁蛋白。Biometals23, 419-424(2010)。
克鲁皮斯基,a.m.和Bogucki, Z.乳铁蛋白在牙科使用的临床方面。口腔生物科学。63, 129-133(2021)。
陈,Y。et al。牛乳铁蛋白抑制牙周炎正畸大鼠模型中的牙槽骨破坏。安。阿娜特。237, 151744(2021)。
确认
KR感谢Alfred Kordelin基金会,Wilhelm and Else Stockmann基金会和赫尔辛基大学CHEMS博士项目的资助。PHG得到了Folkhälsan研究基金会、芬兰科学院(275614,316664)、诺和诺德基金会(#NNF OC0013659)、赫尔辛基大学医院研究基金以及威廉和埃尔斯·斯托克曼基金会的支持。由赫尔辛基大学图书馆资助的开放获取。
作者信息
作者及隶属关系
贡献
k.r.、m.m.、P.P.和M.L.提出了研究思路和假设;k.r.、m.m.、p.p.、M.L.和K.H.设计了实验;K.R.进行细菌培养;K.R.和K.J.进行PTR-MS测量;k.r., K.H.和M.U.进行了GC-MS测量;k.r.、M.M.和M.U.分析了数据;K.R.写了手稿;所有作者都审阅了手稿。
相应的作者
道德声明
相互竞争的利益
PHG已收到来自安斯泰来、阿斯利康、拜耳、勃林格殷格翰、礼来、爱乐水、健酶、Medscape、MSD、蒙迪制药、诺华、诺和诺德、PeerVoice、赛诺菲和Sciarc的讲座费。他是AbbVie, Astellas, Astra Zeneca, Bayer, Boehringer Ingelheim, Eli Lilly, Janssen, Medscape, MSD, Mundipharma, Novartis, Novo Nordisk和Sanofi的顾问委员会成员。其他作者宣称没有利益冲突。
额外的信息
出版商的注意
施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
罗斯隆德,K., Uosukainen, M., Järvik, K。et al。抗生素治疗和补充hemin可用性影响产生的挥发性有机化合物P。gingivalis体外。Sci代表12, 22534(2022)。https://doi.org/10.1038/s41598-022-26497-0
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s41598-022-26497-0