摘要
糖尿病神经病变是糖尿病最常见的慢性并发症之一,高达一半的糖尿病患者在病程中会发生糖尿病神经病变。值得注意的是,新出现的证据表明,血糖变化与糖尿病并发症的发病机制有关,并已成为糖尿病神经病变的一个可能的独立危险因素。在这篇综述中,我们描述了临床实践中常用的评估血糖变异性的指标,并总结了血糖变异性在糖尿病神经病变(包括心血管自主神经病变、糖尿病周围神经病变和认知障碍)中的作用和相关机制。此外,我们还探讨了糖尿病神经病变潜在的药物和非药物治疗方法,旨在为糖尿病神经病变的治疗提供思路。
简介
随着人们生活水平的提高和竞争压力的增加,糖尿病及糖尿病相关并发症的患者越来越多1.糖尿病神经病变(DN)是糖尿病最常见的长期并发症之一,具有显著的发病率和死亡率。它包括周围神经病变和自主神经病变,估计影响超过60%的糖尿病患者2.
尽管传统上认为慢性高血糖是糖尿病相关并发症的主要危险因素,但也有研究表明,频繁或大幅度的血糖波动可能独立导致糖尿病相关并发症。除糖化血红蛋白(HbA1c)外,血糖变异性(GV)可能是糖尿病并发症的另一个独立危险因素3..多项大规模临床研究发现,GV程度越高,糖尿病慢性并发症的发生率越高4.例如,一项包括38名2型糖尿病(T2DM)患者的广泛HbA1c对照队列研究发现,即使在HbA1c水平正常的情况下,高GV也对DN有害5.近年来,GV作为评价血糖控制的指标受到广泛关注。GV定义为血糖波动程度,很少由单一因素引起,被认为是糖尿病并发症的潜在独立危险因素3.,6,7,8.同样,来自T2DM的研究结果支持GV与糖尿病视网膜病变的发生或进展之间存在显著的正相关9,10心血管疾病和死亡率11,12,13.值得注意的是,GV往往是评估T2DM患者未来微血管和大血管并发症风险的更好的血糖参数3.,14,15.
在此,我们详细阐述了GV在DN中的作用和相关机制,包括心血管自主神经病变(CAN)、糖尿病周围神经病变(DPN)和认知障碍。同时,我们也探讨了GV潜在的药物和非药物治疗方法,旨在为糖尿病合并DN的治疗提供新的策略。
全球价值链评估
如何在不引起低血糖的情况下降低平均血糖水平和餐后高血糖,是糖尿病患者终生面临的优化问题16.在过去的十年中,GV与HbA1c一起被越来越多地视为血糖控制的主要标志17,18,19.随着人们对GV重要性的日益关注,在临床试验中提出了许多表征GV的指标。变异系数(CV)和标准差(SD)是GV连续血糖监测(CGM)指标的共识值16,20..其他一些目前使用的指标包括血糖漂移平均振幅(MAGE)、连续整体净升糖作用、平均日差值、高血糖指数、低血糖指数、糖尿病方程中的血糖风险评估16,21,22,23,24,25,26,27.然而,目前对评估全球价值链的标准方法还没有达成共识。值得注意的是,《糖尿病先进技术与治疗国际共识》建议在临床实践中使用CV评估GV,临界值为36%28.
除了自我血糖监测外,主要支持糖尿病患者的自我管理和用药调整,这里我们强调CGM29.糖化血红蛋白(HbA1c)反映了最初60-90天的整体血糖控制情况,自1993年以来一直被认为是评估糖尿病管理结果的金标准30..然而,由于忽视了血糖水平波动(GV),越来越多的人认识到HbA1c作为血糖控制的局限性。CGM系统的发展,提高了地球辐射的分析和解释水平31.CGM提供了血糖控制的几个方面的详细信息,包括GV32.值得注意的是,在HbA1c水平正常的情况下,CGM可以可靠地检测出潜在的餐后高血糖33.此外,CGM还可以系统地记录每日血糖水平,使数据更具有代表性,而不影响正常的日常生活34.最近,CGM已被证明是临床前1型糖尿病(T1DM)中GV的有用指标。35,36.综上所述,CGM系统能够准确测量短期GV,并研究葡萄糖波动在糖尿病相关并发症发展中的作用3..
据报道,这些指标之间有很大的相关性37,38.例如,先前一项纳入88名日本糖尿病患者的研究显示,CGM获得的血糖控制指数、日差均值、持续总体净升糖作用、MAGE等GV指数与SD葡萄糖密切相关39.相反,最近的一项回顾性研究发现,每日GV和就诊GV与临床参数有不同的相关性,两者之间几乎没有联系40.因此,有必要通过进一步的分析来明确全球价值链各指标之间的关系。
GV和CAN
众所周知,自主神经活动与葡萄糖代谢之间存在双向调节46,47.糖尿病患者普遍存在自主神经失衡,可发展为糖尿病自主神经病变48.值得注意的是,最近的证据表明GV参与了伴有T1DM的CAN。一项纳入密歇根大学卫生系统44例T1DM患者的初步研究发现,反映低血糖应激的GV指标、低血糖指数、低血糖曲线下面积与心率变异性低功率和高频功率(CAN指标)呈显著负相关,提示GV可能与CAN有关49.同样,Nyiraty等人发现,通过SD和平均绝对葡萄糖计算的GV标记物与T1DM患者CAN的严重程度相关50.然而,在一项包括133名18 - 24岁T1DM年轻人的横断面观察性研究中,Christensen等人报道,在对危险因素和多项测试进行调整后,只有较高的MAGE与心率变异性测量值略有增加有关,这表明GV可能不是患有T1DM的年轻人的CAN危险因素51.
此外,有报道表明,GV被认为是T2DM患者CAN的重要危险因素。例如,先前的一项研究报道,在T2DM患者中,通过心率变异性评估空腹交感神经活动在醒来前后的波动与短期GV呈正相关46.同样,韩国的一项前瞻性研究显示,短期和长期GV,如CGM-SD、CGM-CV、HbA1c的SD、HbA1c的log CV等,与T2DM患者有无CAN的相关性显著高于无T2DM患者,表明GV与T2DM患者有无CAN独立相关52.与此同时,一项包括681例T2DM患者的回顾性队列研究报告称,CAN与用SD测量的HbA1c变异性较高的风险显著相关53.此外,压力反射敏感性作为CAN在T2DM中的敏感指标,被发现与T2DM患者以就诊间HbA1c变异性为代表的长期GV呈负相关54.类似地,Lai等人表明,用SD测量的HbA1c变异性不仅与CAN的存在密切相关,而且与CAN的严重程度密切相关55.但值得注意的是,在一项由39名女性和48名男性组成的非胰岛素治疗的T2DM队列研究中,CAN指标包括正常间期标准差、连续差值均方根、总功率、呼气吸气比等仅在女性中与MAGE的增加显著相关,提示GV对T2DM患者的CAN有性别特异性的影响56(表1).因此,需要进一步的前瞻性研究来证实GV和CAN在T1DM和T2DM中的作用。
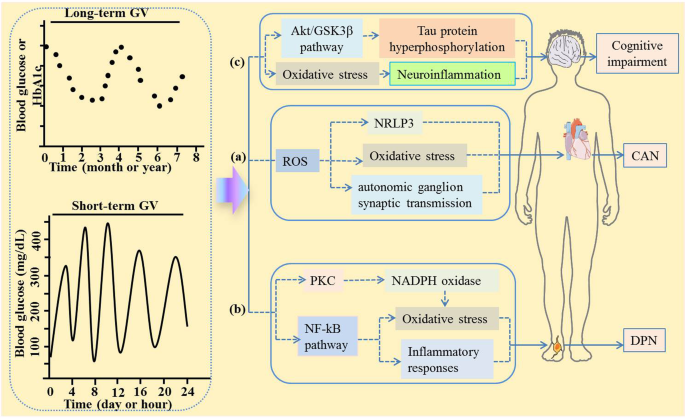
受限于目前的知识,CAN的发病机制还不完全清楚。然而,新出现的证据表明,CAN可能是由炎症反应和氧化应激引起的GV变化引起的。1)57,58,59.一方面,糖尿病早期出现自主神经功能障碍,可能伴随着各种炎症细胞因子的改变,包括白细胞介素-657.另一方面,先前体外研究的结果表明,急性血糖波动通过线粒体电子传递链上活性氧的过量产生,诱发了更大的氧化应激触发效应60.此外,活性氧的增加激活了NRLP3炎症小体通过氧化nAch受体α3亚基抑制自主神经节突触传递,从而导致糖尿病性CAN58.
GV和DPN
DPN是长期糖尿病常见的慢性并发症,其发病率随着糖尿病整体发病率的增加而增加。DPN与神经性疼痛、足部溃疡、随后的坏疽和截肢有关,严重影响患者的生活质量。近年来,越来越多的证据表明GV是DPN合并T1DM的危险因素。在对100例T1DM患者的11年随访中,血糖的标准偏差被证明是DPN患病率的独立预测因子1.此外,Kwai等发现MAGE与运动和感觉轴突功能改变的兴奋性标记物(如超兴奋性、强度持续时间常数、最小I/V斜率等)密切相关,表明GV可能是轴突退行性变的关键中介因子,也是T1DM伴DPN发生的一个促成因素61.更重要的是,一项横断面研究发现,与无DPN的患者相比,DPN患者的HbA1c变异性更高,包括HbA1c- sd和HbA1c- cv62.与这一结果一致的是,一项系统的文献综述揭示了HbA1c变异性的增加可以作为足部DPN的生物标志物63.
同时,多项横断面研究表明,在T2DM患者中,HbA1c的变异性与DPN密切相关64,65,66.另一项观察性队列研究纳入了90例伴有/不伴有DPN的T2DM患者,发现MAGE与HbA1c控制良好的DPN显著相关67.类似地,Hu等人。68纳入了982例T2DM患者,他们接受了DPN筛查并接受了持续葡萄糖监测系统的监测,并证明了MAGE是2型糖尿病患者DPN的重要独立因素。此外,在台湾进行的一项回顾性病例对照研究显示,T2DM成人中更大的长期GV与DPN明显相关69.有趣的是,值得注意的是,GV也与T2DM中疼痛性DPN的风险密切相关。一项包括275例伴或不伴DPN疼痛的T2DM以及351例无DPN的T2DM患者的病例对照回顾性研究显示,多变量调整后,空腹血糖- cv与DPN疼痛风险显著相关64.不久之后,相似的结果发现,增加餐后血糖暴露,定义为高HbA1c和接近正常的空腹血糖水平,显著增加了T2DM患者疼痛性DPN的风险70.最近,Yang等人发现,与无痛组相比,轻度/中度/重度疼痛组以范围内时间表示的GV显著降低,这表明范围内时间可作为疼痛性DPN的一项有价值的临床评价指标71(表2).
到目前为止,关于GV对DPN影响的信息很少。但不可忽视的是,GV诱导DPN的机制之一是通过激活蛋白激酶C依赖的NADPH氧化酶,从而进一步导致氧化应激72.同时,gv诱导的雪旺氏细胞凋亡可能参与了这一过程73.值得注意的是,新兴的临床前研究表明,GV可以削弱坐骨神经的运动神经传导速度,并破坏坐骨神经髓鞘和轴突的微结构74.此外,GV显著降低超氧化物歧化酶的表达,提高丙二醛、TNF-a、白细胞介素-6和NF-kB的表达水平。综上所述,上述研究表明,GV通过激活NF-kB通路诱导氧化应激和炎症反应,从而引起DPN(图。1 b)74.
GV和认知障碍
除了CAN和DPN, GV对认知障碍(如阿尔茨海默病和血管性痴呆)的影响也得到了解决75.值得注意的是,老年2型糖尿病患者认知障碍的发生率是正常人的两倍。既往临床研究表明,MAGE与老年T2DM患者的迷你精神状态检查、认知综合评分和脑萎缩有显著相关性76,77.此外,Kim等人进行的横断面研究显示,HbA1c的SD或CV较高与轻度精神状态检查低显著相关78.此外,乙肝糖化血红蛋白≥8%的老年糖尿病患者认知能力较差79.值得注意的是,神经影像学研究检查了T2DM认知障碍的神经相关性,发现白质高强度可能是所观察到的认知改变的基础。事实上,以色列糖尿病和认知衰退研究的一项调查显示,HbA1c变异性与APOE4载体白质高强度体积显著相关80.不久之后,类似的结果表明,在多种族的华盛顿高地因伍德哥伦比亚老化项目中,GV与更高数量的白质高强度体积相关81.与这些结果一致,Tamura等人在横断面研究中发现,高糖蛋白/HbA1c是高GV的标志,是大白质高强度体积的重要决定因素82.此外,AGP在糖尿病相关痴呆中表现出明显不同,而在与糖尿病相关的阿尔茨海默病中则没有,这表明糖尿病相关痴呆组可能更容易受到GV对大脑的有害影响83(表3.).需要强调的是,有报道称T1DM患者也有认知障碍84.例如,在一个包括18个糖尿病研究中心的T1DM交换临床网络中,48%的参与者有临床显著的认知障碍。此外,较高的HbA1c和持续血糖监测平均夜间血糖均与临床显著认知障碍的发生率增加相关85.综上所述,这些结果表明GV可能是糖尿病患者认知障碍的一个因素。
越来越多的证据表明,GV显著增加氧化应激,导致神经炎症和认知障碍86.随着对GV危险因素研究的不断深入,神经病理学和神经影像学为认知障碍的发生提供了重要的机制线索。值得注意的是,Tau蛋白异常过度磷酸化被认为在认知障碍中起关键作用87.进一步支持GV影响认知障碍风险的观点来自Yang等人进行的另一项研究。74.在该研究中,作者观察到波动性高血糖大鼠模型的学习和记忆能力均被破坏,其机制可能是GV抑制了Akt/GSK3β通路,使海马中的Tau蛋白过度磷酸化,从而引起认知障碍。此外,Xia等人观察到过多的GV与认知障碍以及左额中回的度中心性显著降低有关(图2)。1 c)88.
后备疗法
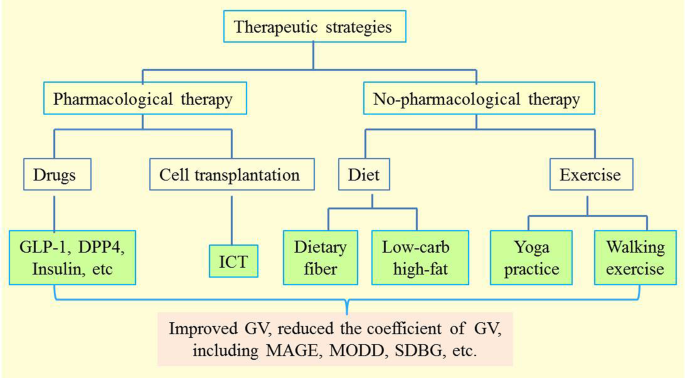
营养治疗在糖尿病的管理中是必不可少的,其中饮食碳水化合物的摄入是餐后高血糖和GV的主要因素。研究表明,在碳水化合物之前摄入脂质和蛋白质可以通过减缓胃排空和增强胰岛素分泌来显著改善糖耐量90,91.有趣的是,Chang等人发现,非常低碳水化合物、高脂肪的早餐可以显著降低24小时的MAGE和SD水平,并改善T2DM患者的GV92.此外,膳食纤维已被证明可以降低糖尿病患者餐后GV。在评估富含纤维的荞麦和玉米面食对餐后GV的急性影响时,Vetrani等人。93显示患有T1DM的受试者在食用富含纤维的荞麦面食后,餐后GV有更高的稳定性。此外,值得注意的是,作为均衡饮食的一部分,使用适量的蔗糖不会影响T1DM患者的GV或胰岛素需求94.因此,控制饮食顺序或选择更天然的膳食纤维食物可以改善糖尿病患者的GV。此外,运动训练,包括有氧运动、阻力运动和联合运动,也可以降低T2DM的GV95.在一项观察性研究中,Van Dijk等人表明,长时间的步行运动可以大大降低TIDM患者的每日胰岛素给药量,但不一定会损害24小时GV96.值得注意的是,瑜伽辅助治疗2型糖尿病有多种益处,包括降低空腹血糖、餐后血糖、氧化应激和促炎标志物61.同样,在另一项研究中,Vijayakumar等人评估了2型糖尿病患者进行一周瑜伽练习后,GV显著降低,血糖目标持续时间延长97.
药物治疗
虽然不同的糖尿病治疗方法可能降低HbA1c的程度相似,但其降低GV的效果可能存在显著差异98.高血糖是糖尿病临床表现及相关并发症的主要原因,通过药物治疗降低血糖水平是糖尿病管理的基石。
胰高血糖素样肽-1 (GLP-1)受体激动剂
口服降糖药二甲双胍是T2DM的一线治疗方法。当T2DM患者仅接受二甲双胍且血糖控制不佳时,可选择使用GLP-1受体激动剂和基础胰岛素作为抗糖尿病药物99,One hundred..与西方国家相比,艾塞那肽在中国是一种广泛使用的短期GLP-1受体激动剂101.艾塞那肽不仅显著降低了平均血糖值的标准差和最大血糖偏移幅度,而且显著降低了最高和平均血糖水平101.
胰岛素
在胰岛素强化治疗的糖尿病患者中,常观察到GV引起的代谢控制不稳定和低血糖的高风险106.因此,胰岛素在糖尿病患者中的有效性和安全性的证据是一个优先考虑的问题。degludec (IDeg)是一种新型的超长效基础胰岛素,已在一项涉及广泛糖尿病患者的综合研究中进行了广泛的测试107,108,109.一项临床试验表明,在胰岛素缺乏的T2DM患者中,IDeg在血糖控制方面取得了与Iglar相似的改善,并且在接受IDeg的患者中,每日空腹血糖的变化较小110.有趣的是,另一项观察性纵向研究也报告了类似的结果64.大量证据表明,IDeg不仅能够降低T2DM患者的GV,而且对T1DM患者也有效。Iga等人。111发现在IDeg组和IGlar组之间,糖化血红蛋白、胰岛素总用量、体重变化以及基础与丸剂比均无差异。值得注意的是,在IDeg治疗期间,空腹间质GV在CGM曲线上的日变异性明显小于IGlar治疗期间111.
在非住院糖尿病患者中,已有大量关于基础-丸剂方案中IDeg的有效性和安全性的文献,而对住院患者使用IDeg治疗的影响的研究很少。一项观察性纵向回顾性研究表明,在需要营养支持的T2DM住院患者中,IDeg具有维持稳定血糖水平和降低GV的潜力112.
细胞移植
细胞移植作为一种解决DN潜在原因的可能方法正在被研究113,114.115自体骨髓单个核细胞移植可显著改善DPN的体征和症状。一直以来,另一组116发现自体骨髓单个核细胞移植可改善T2DM患者的糖尿病感觉运动多神经病变,提示自体骨髓单个核细胞移植可能是一种有效且有前景的治疗DPN的方法。值得注意的是,胰岛细胞移植是对T1DM和严重低血糖有耐药性的患者的另一种有前景的治疗方法117.胰岛细胞移植可通过改善血糖控制和降低GV来减少并发症117,118.一项前瞻性交叉研究的结果表明,与强化药物治疗相比,胰岛细胞移植可以减缓糖尿病视网膜病变和肾病的进展119.此外,Azmi等发现T1DM患者胰肾同时移植后糖化血红蛋白、神经病变症状和腓神经传导速度均有改善120.然而,还需要进一步的临床研究来证实细胞移植治疗DN的安全性和有效性。
联合治疗
Misra等人报道了一名KCNJ11-G334V突变的年轻女性,在接受高剂量磺脲类药物联合胰岛素治疗时,血糖控制有显著改善121.值得注意的是,这种联合治疗也导致了GV和低血糖意识的显著改善。同样,一项概念验证研究证实了用餐时间艾塞那肽治疗高危胰岛素需求人群的有效性和安全性,并证明使用这种方法可以降低GV98.一项双盲随机2期研究表明,恩格列净显著降低了GV,增加了在葡萄糖靶范围内的时间,而不增加在低血糖状态下的时间122.Nomoto等提出达格列净联合注射胰岛素治疗在胰岛素治疗上不表现出葡萄糖波动优于二肽基肽酶4抑制剂123.如果降低血糖波动是治疗的优先事项,使用GLP-1的方案比单独使用基础胰岛素更可取,因为高于范围的时间更短,GV也更低124.特别是,只有当GLP-1是治疗方案的一部分时,GV才会下降124.然而,在卡塔尔研究的一项前瞻性亚研究中,Ponirakis等人发现艾塞那肽加吡格列酮或胰岛素治疗可降低糖化血红蛋白,促进小纤维再生,但对超过1年的神经性疼痛没有影响125.
引人注目的是,最近的一项研究报道,给糖尿病小鼠注射羟胆酸可以改善空腹GLP-1分泌和葡萄糖稳态。随后,在一个临床队列中,进一步证实血清中低浓度的胆酸与糖尿病有关126.因此,低胆酸有望成为治疗糖尿病GV的另一种新药,从而改善DN。此外,在血糖控制方面,T2DM治疗的目的是将HbA1c降低到目标水平,降低GV,以避免低血糖和餐后葡萄糖的大幅波动127.因此,通过早期发现自主神经失衡,重视糖尿病控制,消除神经病变危险因素,可以减缓DN的发生48.
总结和进一步展望
目前,在常规临床实践中评估GV仍然是一个挑战。事实上,全球价值链的评估并没有黄金标准。因此,采用最佳的GV评估方法,为改善血糖控制提供最相关的反馈,对于临床实践至关重要128.此外,如何避免低血糖、降低平均血糖水平和餐后高血糖是糖尿病患者终身面临的优化问题16.如果降低GV,就可以实现这种优化。因此,在过去的十年中,GV与HbA1c一起被越来越多地视为血糖控制的主要标志17,18,19.然而,对于相同的血浆胰岛素浓度,降糖效果可能不同,这取决于胰岛素敏感性,甚至在静脉注射后。在相对较短的时间内,个体内部和个体之间的胰岛素敏感性差异很大,导致糖尿病患者的代谢效应不同106.因此,非药物治疗已成为改善血液GV的有效途径。总之,DN是糖尿病最常见的长期并发症之一,良好的GV控制可能是预防此类并发症的关键。
报告总结
有关研究设计的进一步资料,请参阅自然研究报告摘要链接到这篇文章。
数据可用性
本研究没有使用数据,因此没有数据可用。
参考文献
Bragd, J.等人。通过血糖自我监测计算出的血糖变异性能否预测10年内1型糖尿病并发症的发生?糖尿病金属底座。34, 612-616(2008)。
Vinik, A. I., Maser, R. E., Mitchell, B. D. & Freeman, R.糖尿病自主神经病变。糖尿病护理26, 1553-1579(2003)。
米,S. H.等。未确诊糖尿病患者血糖变异性和糖化血红蛋白作为冠状动脉疾病危险因素的比较下巴。地中海J。125, 38-43(2012)。
Nalysnyk, L., Hernandez-Medina, M. & Krishnarajah, G.糖尿病患者的血糖变异性和并发症:来自文献系统回顾的证据。糖尿病ob。金属底座。12, 288-298(2010)。
Ishibashi, F., Taniguchi, M., Kosaka, A., Uetake, H. & Tavakoli, M. 2型糖尿病患者HbA(1c)正常化后神经病变预后的改善。糖尿病护理42, 110-118(2019)。
Kohnert K.-D。,Heinke, P., Vogt, L. & Salzsieder, E. Utility of different glycemic control metrics for optimizing management of diabetes.J.糖尿病6, 17-29(2015)。
Suh, S. & Kim, J. H.血糖变化:我们如何测量它,为什么它很重要?糖尿病金属底座。J。39, 273-282(2015)。
服务,F. J.等。血糖波动的平均振幅,糖尿病不稳定性的衡量指标。糖尿病19, 644-655(1970)。
gimono - orna, J. A., Castro-Alonso, F. J., bone - juliani, B. & Lou-Arnal, L. M.空腹血糖变异性作为2型糖尿病患者视网膜病变的危险因素。J.糖尿病并发症。17, 78 - 81。
Picconi, F.等人。视网膜Müller细胞对葡萄糖变异的反应。内分泌65, 542-549(2019)。
卡瓦尔特,F.等人。在2型糖尿病中,餐后血糖比空腹血糖更能预测心血管事件,特别是在女性中:来自圣路易斯冈萨加糖尿病研究的经验教训。j .中国。性。金属底座。91, 813-819(2006)。
Zoppini, G.等人。体重、脉压和血糖的变异性可以很好地预测老年2型糖尿病患者的总死亡率。维罗纳糖尿病研究。糖尿病/金属底座。牧师》。24, 624-628(2008)。
Bruginski, D., Précoma, D., Sabbag, A. & Olandowski, M.血糖变化率和低血糖对巴西老年患者死亡率和住院时间的影响。咕咕叫。糖尿病牧师。16, 171-180(2020)。
Cardoso, C. R. L., Leite, N. C., Moram, C. B. M. & Salles, g.f.长期访视血糖变异性作为2型糖尿病患者微血管和大血管并发症的预测因素:里约热内卢里约热内卢2型糖尿病队列研究。心血管Diabetol。17, 33(2018)。
Pu, Z.等。入院时急性血糖变异性预测冠状动脉疾病住院患者的预后:一项荟萃分析内分泌67, 526-534(2020)。
血糖控制指标——从HbA(1c)到持续血糖监测。内分泌。13, 425-436(2017)。
血糖变异性与糖尿病并发症:重要吗?当然了!糖尿病护理38, 1610-1614(2015)。
葡萄糖变异性:它的重要性以及如何测量它。糖尿病62, 1405-1408(2013)。
Siegelaar, S. E, Holleman, F., Hoekstra, J. B. & DeVries, J. H.葡萄糖变异;这重要吗?Endocr。牧师。31, 171-182(2010)。
Nusca, A.等。血糖变化在糖尿病心血管并发症发展中的作用。糖尿病金属底座。牧师》。34, e3047(2018)。
乔希,A.等人。糖尿病自我管理教育计划中血糖变化的模式。医学科学。7,未定义(2019)。
Chakarova, N., Dimova, R., Grozeva, G. & Tankova, T.糖尿病前期受试者血糖变异性评估。糖尿病临床研究。Pract。151, 56-64(2019)。
Monnier, L., Colette, C. & Owens, D. R.简单指标在血糖可变性评估中的应用。糖尿病金属底座。44, 313-319(2018)。
Umpierrez, g.e. & Kovatchev, b.p.血糖变异性:如何测量及其对2型糖尿病的临床意义。点。医学科学356, 518-527(2018)。
周铮,孙斌,黄松,朱春华,边敏。血糖变化:不良临床结局及如何改善?心血管Diabetol。19, 102(2020)。
Fabris, C, Patek, S. D. & Breton, m.d.。CGM衍生的风险指数可以与基于smbg的指数互换吗?糖尿病科学。抛光工艺。10, 50-59(2015)。
Molnar, G. D., Taylor, W. F. & Ho, M.连续监测血糖的每日变化:糖尿病不稳定性的进一步测量。Diabetologia8, 342-348(1972)。
Danne, T.等人。使用连续血糖监测的国际共识。糖尿病护理40, 1631-1640(2017)。
血糖控制指标——从HbA到持续血糖监测。内分泌。13, 425-436(2017)。
Nathan, D. M.等人。糖尿病强化治疗对胰岛素依赖型糖尿病长期并发症发生和进展的影响心血管病。j .地中海。329, 977-986(1993)。
Jin, H. Y. Lee, K. A. & Park, T. S.血糖变化对糖尿病周围神经病变的影响。内分泌53, 643-648(2016)。
Leelarathna, L.等。用一种新的复合连续血糖监测指标评价血糖控制。糖尿病科学。抛光工艺。14, 277-283(2020)。
Klonoff, d.c.等人。持续血糖监测:内分泌学会临床实践指南。j .中国。性。金属底座。96, 2968-2979(2011)。
劳,G. R.等人。经治疗的妊娠糖尿病患者夜间血糖控制不佳与胎龄大有关。糖尿病护理42, 810-815(2019)。
Helminen, O.等人。持续血糖监测和糖化血红蛋白在1型糖尿病高危儿童糖代谢评估中的应用糖尿病临床研究。Pract。120, 89-96(2016)。
范·达伦,A.等人。(即将发生的)1型糖尿病中血糖变异性与高血糖钳源性功能变量之间的关系。Diabetologia58, 2753-2764(2015)。
测量血糖变化的挑战。糖尿病科学。抛光工艺。6, 712-715(2012)。
血糖变异性和氧化应激:糖尿病和心血管疾病之间的联系?Int。理学。15, 18381-18406(2014)。
Saisho, Y.等。连续血糖监测得出的不同血糖变异性指标之间的关系。Prim. Care糖尿病9, 290-296(2015)。
土屋,T.等。2型糖尿病患者每日和就诊间血糖变异性的关系Endocr。J。67, 877-881(2020)。
糖尿病自主神经病变。Handb。中国。神经。126, 63-79(2014)。
李伟,黄娥,高寿。1型糖尿病与认知障碍:一项系统综述。阿尔茨海默病。57, 29-36(2017)。
费尔德曼,E. L.,内夫,K. A.,詹森,T. S.和班尼特,D. L. H.糖尿病神经病变的新视野:机制,生物能学和疼痛。神经元93, 1296-1313(2017)。
Du, W.等。STAT3磷酸化在糖尿病周围神经病变的雪旺细胞中以hdac1依赖和不依赖的方式介导高糖受损细胞自噬。美国实验生物学学会联合会J。33, 8008-8021(2019)。
刘玉萍,邵淑娟,郭宏德。高糖诱导糖尿病周围神经病变雪旺细胞凋亡。生命科学。248, 117459(2020)。
Matsushita, Y.等。在2型糖尿病患者中,起床前后交感神经活动的波动不仅与早晨的血糖变化呈正相关,而且与每日的血糖变化也呈正相关。糖尿病临床研究。公关。152, 1-8(2019)。
胰岛细胞质量和功能的神经调节。糖尿病ob。金属底座。16补充1, 87-95(2014)。
糖尿病自主神经失衡和血糖变化。糖尿病科学。抛光工艺。6, 1207-1215(2012)。
Jaiswal等人。1型糖尿病患者心血管自主功能受损与低血糖的关系糖尿病护理37, 2616-2621(2014)。
Nyiraty, S.等。1型糖尿病患者的心血管自主神经病变与血糖变异性:是否存在相关性?前面。性。9, 174(2018)。
Christensen, m.m.b., Hommel, e.e., Jørgensen, m.e., Fleischer, J. & Hansen, c.s.年轻成人1型糖尿病的血糖变异性和糖尿病神经病变。前面。性。11, 644(2020)。
君,J. E.等。2型糖尿病患者血糖变异性与糖尿病心血管自主神经病变的关系。Cardiovasc Diabetol。14, 70(2015)。
杨,Y.等。心血管自主神经病变预示2型糖尿病患者糖化血红蛋白变异性较高。糖尿病金属底座。J。42, 496-512(2018)。
Matsutani, D.等。在2型糖尿病中,访诊间HbA1c变异性与独立于HbA1c值的压力反射敏感性呈负相关。Cardiovasc Diabetol。17, 100(2018)。
Lai, Y. R.等。在糖尿病病程较长2型糖尿病患者中,糖化血红蛋白的变异性与心血管自主神经病变的严重程度密切相关。前面。>。13, 458(2019)。
弗莱舍,J.等。血糖变异性与2型糖尿病女性心脏自主调节降低有关。糖尿病护理38, 682-688(2015)。
Lieb, d.c., Parson, h.k., Mamikunian, G. & Vinik, a.i.:新诊断和确诊糖尿病的心脏自主神经失衡与脂肪组织炎症标志物相关。糖尿病研究。2012, 878760(2012)。
沙,m.s. &布朗利,M.糖尿病心血管疾病的分子和细胞机制。中国保监会,Res。118, 1808-1829(2016)。
糖尿病患者心血管自主神经病变的影响、诊断和管理的最新进展:什么是定义,什么是新的,什么是未满足的。糖尿病金属底座。J。43, 3-30(2019)。
Piconi, L.等人。持续和间歇性高糖通过线粒体超氧化物过剩促进内皮细胞凋亡。糖尿病金属底座。牧师》。22, 198-203(2006)。
Kwai, n.c., Arnold, R, Poynten, a.m.和Krishnan, a.v. 1型糖尿病血糖变异性和周围神经功能障碍之间的关系。肌肉神经54, 967-969(2016)。
平托,m.v.等。糖化血红蛋白变异性和长期血糖控制与1型糖尿病患者周围神经病变有关。Diabetol。金属底座。Syndr。12, 85(2020)。
Casadei, G., Filippini, M. & Brognara, L.糖化血红蛋白(HbA1c)作为糖尿病足周围神经病变的生物标志物。疾病9,https://doi.org/10.3390/diseases9010016(2021)。
Pai yw ., Lin c.h ., Lee i.t. & Chang m.h .空腹血糖的变异性与2型糖尿病患者疼痛性糖尿病周围神经病变的风险。糖尿病金属底座。44, 129-134(2018)。
Lai, Y. R.等。在2型糖尿病患者中,糖化血红蛋白的变异性与周围神经病变的严重程度密切相关。前面。>。13, 90(2019)。
苏,J. B.等。2型糖尿病患者糖化血红蛋白变异性与糖尿病周围神经病变Cardiovasc。Diabetol。17, 47(2018)。
徐峰,等。糖化血红蛋白控制良好的2型糖尿病患者血糖变异性与糖尿病周围神经病变的关系Diabetol。金属底座。Syndr。6, 139(2014)。
胡,y.m.等。通过持续血糖监测评估2型糖尿病患者糖尿病周围神经病变与血糖变异性的关系。内分泌60, 292-300(2018)。
白玉文,林春华,林淑云,李一田,张明辉。2型糖尿病患者糖尿病周围神经病变新发现危险因素的再确认:一项病例对照研究。《公共科学图书馆•综合》14, e0220175(2019)。
Pai, Y. W.等。疼痛性糖尿病周围神经病变的血糖控制不仅仅是空腹血糖和糖化血红蛋白。糖尿病金属底座。47, 101158(2021)。
杨,J.等。持续血糖监测评估的时间范围与疼痛性糖尿病多发性神经病的相关性。糖尿病调查。12, 828-836(2021)。
Quagliaro, L.等人。间歇性高糖增强与人脐静脉内皮细胞氧化应激相关的凋亡:蛋白激酶C和NAD(P) h氧化酶激活的作用糖尿病52, 2795-2804(2003)。
孙丽琪等。α硫辛酸对暴露于持续或间歇性高糖的雪旺氏细胞的保护作用。物化学。制药。84, 961-973(2012)。
杨,J.等。血糖变异性的机制加速糖尿病大鼠糖尿病中枢神经病变和糖尿病周围神经病变。物化学。Biophys。Commun >,510, 35-41(2019)。
Świątoniowska-Lonc, N., polazynski, J., tazynski, W. & jankowska - polazynska, B.认知障碍对2型糖尿病患者坚持治疗和自我护理的影响。糖尿病金属底座。Syndr。ob。14, 193-203(2021)。
里佐,m.r.等人。老年2型糖尿病患者每日急性血糖波动与认知功能的关系糖尿病护理33, 2169-2174(2010)。
Cui, X., Abduljalil, A., Manor, B. D., Peng, C. K. & Novak, V.多尺度血糖变化:与2型糖尿病患者灰质萎缩和认知能力下降有关。《公共科学图书馆•综合》9, e86284(2014)。
金,C.等人。老年2型糖尿病患者访视血糖变异性与认知功能的相关性:一项横断面研究《公共科学图书馆•综合》10, e0132118(2015)。
Mimenza-Alvarado, A. J.等人。血糖控制不良对老年2型糖尿病患者认知能力的影响:墨西哥健康与老龄化研究BMC Geriatr。20., 424(2020)。
利夫尼等人。2型糖尿病APOE4基因型携带者血糖控制的长期变异性与白质高强度相关。糖尿病护理39, 1056-1059(2016)。
Reitz, C.等人。多民族老年队列中血糖异常与大脑结构变化的关系。j。Geriatr。Soc。65, 277-285(2017)。
田村,Y.等。老年糖尿病患者白质高与认知障碍、功能障碍和高糖蛋白/糖血红蛋白比值相关。前方衰老神经科学。9, 220(2017)。
小川,Y.等。糖尿病相关痴呆的动态血糖谱。Geriatr。Gerontol。Int。19, 282-286(2019)。
Bispham, J. A. Hughes, A. S. Driscoll, K. A. & McAuliffe-Fogarty, A. H. 1型糖尿病衰老的新挑战。咕咕叫。新代表。20., 15(2020)。
Chaytor, n.s.等人。老年1型糖尿病患者的临床显著认知障碍。J.糖尿病并发症33, 91-97(2019)。
瓦特,C,桑切斯-兰格尔,E. &黄,J. J.血糖变异性和中枢神经系统炎症:回顾联系。营养物质12,https://doi.org/10.3390/nu12123906(2020)。
张q等。CK2磷酸化I(2)(PP2A)/SET介导tau病理和认知障碍。前面。摩尔。>。11, 146(2018)。
夏,W.等。葡萄糖波动与大脑功能结构紊乱和认知障碍有关。阿尔茨海默病。74, 603-613(2020)。
考克斯,a.a.等人。低剂量脉冲白介素-6作为糖尿病周围神经病变的治疗选择。前面。性。8, 89(2017)。
Ma, J.等。饮食控制型2型糖尿病患者碳水化合物餐后蛋白质预负荷对胃排空、血糖和肠道激素的影响糖尿病护理32, 1600-1602(2009)。
Tricò, D.等。通过一个小的蛋白质和脂质预负荷改善葡萄糖耐量的机制。Diabetologia58, 2503-2512(2015)。
Chang, c.r, Francois, M. E. & Little, J. P.限制早餐碳水化合物足以减少24小时的餐后高血糖暴露和改善血糖变化。点。j .中国。减轻。109, 1302-1309(2019)。
Vetrani, C.等人。与玉米面食相比,富含纤维的荞麦面食可以改善1型糖尿病和乳糜泻患者的血糖反应:急性随机对照试验糖尿病临床研究。公关。149, 156-162(2019)。
Souto, D. L.等。蔗糖会影响1型糖尿病患者的血糖变异性吗?先导交叉临床研究。营养179 - 184,https://doi.org/10.1016/j.nut.2018.05.009(2018)。
费格拉,F. R.等。有氧运动和联合运动可以降低2型糖尿病的血糖变异性:交叉随机试验《公共科学图书馆•综合》8, e57733(2013)。
范戴克,J. W.等。1型糖尿病患者在连续几天长时间步行运动期间的血糖控制。糖尿病临床研究。公关。117, 74-81(2016)。
Vijayakumar, V., Mavathur, R., Sharma, M. N. K. & Kannan, S.瑜伽可降低2型糖尿病患者的血糖变化:一项初步研究的结果。糖尿病科学。抛光工艺。13, 803-804(2019)。
平糖试验调查员。在一项为期26周的随机比较中,速效胰岛素与GLP-1激动剂在高心血管风险的2型糖尿病患者的用餐时间治疗中的血糖变异性。糖尿病护理39, 973-981(2016)。
加伯,A.等。美国临床内分泌学家协会和美国内分泌学会关于综合2型糖尿病管理算法的共识声明- 2017年执行摘要。Endocr。Pract。23, 207-238(2017)。
Eng, C., Kramer, C. K., Zinman, B. & Retnakaran, R.胰高血糖素样肽-1受体激动剂和基础胰岛素联合治疗2型糖尿病:系统综述和荟萃分析。《柳叶刀》384, 2228-2234(2014)。
阴,t。t。等。艾塞那肽与甘精胰岛素治疗中国2型糖尿病患者血糖变异性的比较:一项随机对照试验。糖尿病其他。9, 1253-1267(2018)。
Koyanagawa, N.等。通过持续血糖监测比较维格列汀和西格列汀对2型糖尿病患者的疗效。Endocr。J。63, 747-753(2016)。
金,G.等人。在二甲双胍治疗中加入维格列汀或格列美脲对2型糖尿病患者的疗效和安全性。当今专家。Pharmacother。18, 1179-1186(2017)。
Vianna, a.g.d.等人。一项随机对照试验,比较磺脲类格列齐特MR(修饰释放)和DPP-4抑制剂维格列汀对巴西2型糖尿病女性血糖变异性的影响,并通过持续血糖监测(CGM)进行控制。糖尿病临床研究。Pract。139, 357-365(2018)。
Nishimura, R., Osonoi, T., Koike, Y., Miyata, K. & Shimasaki, Y.一项关于trelagliptin和阿格列汀对2型糖尿病患者血糖变异性影响的随机试点研究。放置其他。36, 3096-3109(2019)。
Rodacki, M., Carvalho, R. M. & Zajdenverg, L.超长胰岛素degludec对血糖变化的潜在影响。糖尿病临床研究。公关。133, 92-103(2017)。
加伯,A. J.等人。degludec是一种超长效基础胰岛素,与甘精胰岛素在2型糖尿病餐时天冬胰岛素基础丸治疗中的对比(BEGIN基础丸2型):一项3期、随机、开放标签、治疗-靶点非劣效性试验。《柳叶刀》379, 1498-1507(2012)。
Zinman, B.等。degludec胰岛素与甘精胰岛素在未使用胰岛素的2型糖尿病患者中的对比:一项为期1年的随机靶向治疗试验(BEGIN Once Long)糖尿病护理35, 2464-2471(2012)。
Meneghini, L.等。在2型糖尿病患者中,以可变的每日一次给药间隔给予胰岛素的有效性和安全性与甘精胰岛素和每日同一时间给予胰岛素的有效性和安全性:一项为期26周、随机、开放标签、平行组、治疗-靶点试验。糖尿病护理36, 858-864(2013)。
麻生,y等人。degludec胰岛素和甘精胰岛素对insulin-naïve日本2型糖尿病患者血糖控制和每日空腹血糖变异性的影响:我得到了试验。糖尿病临床研究。Pract。130, 237-243(2017)。
Iga, R. & Uchino, H. 1型糖尿病患者清晨注射degludec和甘精碱时血糖变化:一项开放标签随机对照试验。8, 783 - 792,https://doi.org/10.1007/s13300-017-0269-0(2017)。
法塔蒂,G.等人。德葡dec胰岛素对需要肠外/肠内营养的2型糖尿病住院患者的影响:一项观察性研究放置其他。35, 809-816(2018)。
刘,W.等。自体骨髓干细胞治疗代谢综合征糖尿病神经病变。生物医学。Int >,2017, 8945310(2017)。
李志刚,李志刚,李志刚。糖尿病神经病变的细胞移植治疗。日本Rinsho68补充9, 627-631(2010)。
毛,H.等。自体骨髓单个核细胞移植治疗难治性糖尿病周围神经病变的疗效观察。下巴。地中海。J。132, 11-16(2019)。
魏,W.等。自体骨髓单个核细胞移植治疗通过旁分泌和免疫调节机制改善难治性糖尿病感觉运动多神经病变患者的症状:一项对照研究细胞Transpl。29, 963689720949258(2020)。
霍姆斯-沃克,D. J.等人。胰岛移植与连续皮下胰岛素输注或每日多次胰岛素注射相比,具有更好的血糖控制和更少的低血糖。移植101, 1268-1275(2017)。
贝尔图兹,F.等人。胰岛移植对血糖变异性的长期影响。细胞移植。27, 840-846(2018)。
汤普森博士等人。与强化药物治疗相比,胰岛细胞移植可减少糖尿病微血管并发症的进展。移植91, 373-378(2011)。
Azmi, S.等人。1型糖尿病患者胰肾联合移植后早期神经纤维再生Diabetologia62, 1478-1487(2019)。
Misra, S.等。永久性新生儿糖尿病:磺脲类药物联合胰岛素可能是一种有效的治疗方法。Diabet。地中海。https://doi.org/10.1111/dme.13758(2018)。
Famulla, S.等。恩格列净辅助胰岛素治疗1型糖尿病患者的葡萄糖暴露和变异性:来自4周随机安慰剂对照试验(EASE-1)的连续葡萄糖监测数据糖尿病抛光工艺。其他。19, 49-60(2017)。
野本,H.等。一项随机对照试验比较了达格列净和DPP-4抑制剂对2型糖尿病胰岛素患者血糖变异性和代谢参数的影响。Diabetol。金属底座。Syndr。9, 54(2017)。
卡尔森,a.l.等人。甘精胰岛素和艾塞那肽单独和联合应用的评价:一项持续血糖监测和动态血糖分析的随机临床试验。Endocr。Pract。25, 306-314(2019)。
Ponirakis, G.等人。艾塞那肽联合吡格列酮或基础注射胰岛素治疗糖尿病神经病变的效果:卡塔尔研究的一个亚研究。BMJ开放糖尿病护理8,https://doi.org/10.1136/bmjdrc-2020-001420(2020)。
郑,X.等。胆酸物种通过独特的TGR5和FXR信号机制改善葡萄糖稳态。细胞金属底座。https://doi.org/10.1016/j.cmet.2020.11.017(2020)。
Zenari, L. & Marangoni, A.控制2型糖尿病患者血糖变异性的首选策略是什么?糖尿病,ob。金属底座。零, 17-25(2013)。
Kovatchev, B. P., Otto, E., Cox, D., Gonder-Frederick, L. & Clarke, W.糖尿病血糖变异性新测量方法的评估。糖尿病护理29, 2433-2438(2006)。
确认
基金资助:国家自然科学基金项目82104307 (S.B.)和湖南省自然科学基金项目2021JJ40865 (S.B.)。
作者信息
作者及隶属关系
贡献
z.x.c和Y.X.对概念和手稿的撰写做出了贡献;Z.C.S.和S.B.修订并监督整个项目。
相应的作者
道德声明
相互竞争的利益
作者声明没有利益竞争。
同行评审信息
通信生物学感谢Rayaz Malik和Yoshifumo Saisho对这项工作的同行评审所做的贡献。主要处理编辑:Gabriela Da Silva Xavier和Karli Montague-Cardoso。同行评审报告是可用的。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
张,X,杨,X,孙,B。et al。糖尿病神经病变中血糖变化的前景:一项全面综述。Commun杂志4, 1366(2021)。https://doi.org/10.1038/s42003-021-02896-3
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s42003-021-02896-3
这篇文章被引用
2型糖尿病和神经性疼痛患者认知功能的相关因素,情绪和睡眠障碍在这种关系中的作用
科学报告(2022)
持续血糖监测在糖尿病周围神经病变管理中的新兴作用:一项叙述综述
糖尿病的治疗(2022)