文摘gydF4y2Ba
DDX3X是哺乳动物RNA解旋酶调节RNA代谢,癌症,先天免疫和几个RNA病毒。我们发现,单纯疱疹病毒1,核DNA复制病毒,重定向DDX3X核膜,令人惊讶的是调节退出新装配的病毒颗粒。DDX3X损耗也会导致病毒粒子的累积在细胞核内的突出。从力学上看,我们表明,DDX3X身体上和功能上与病毒编码的核出口复杂交互内核膜。DDX3X还结合和刺激公司在成熟的颗粒pUs3,疱疹激酶,促进整个外核膜病毒,核泄漏。总而言之,RNA解旋酶的数据突显出两个意想不到的角色在通过单纯疱疹病毒颗粒通过核膜。这揭示了一个高度复杂的DDX3X和病毒之间的相互作用,并提供新的目标病毒传播的机会。gydF4y2Ba
介绍gydF4y2Ba
DDX3X ATP-dependent RNA解旋酶,属于家庭出局区gydF4y2Ba1gydF4y2Ba。它与许多细胞蛋白相互作用,调节RNA代谢,细胞循环,细胞凋亡和展品都致癌基因和肿瘤抑制基因活动gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3gydF4y2Ba。DDX3X也是一个重要的球员感应的先天免疫和细胞因子/趋化因子生产gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba。不出意料,DDX3X调节几个RNA病毒,赞成和抗病毒的后果gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba,gydF4y2Ba15gydF4y2Ba,gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba。然而,DDX3X的含义并不局限于RNA病毒,因为它是包含在乙型肝炎病毒粒子,消极的调节DNA基因组和抑制逆转录的牛痘病毒传播gydF4y2Ba18gydF4y2Ba,gydF4y2Ba19gydF4y2Ba。DDX3X也纳入至少三个不同的疱疹病毒,即单纯疱疹病毒1(1型单纯疱疹病毒),假狂犬病病毒(减压阀)和人类巨细胞病毒()血巨细胞病毒gydF4y2Ba20.gydF4y2Ba,gydF4y2Ba21gydF4y2Ba,gydF4y2Ba22gydF4y2Ba,gydF4y2Ba23gydF4y2Ba,gydF4y2Ba24gydF4y2Ba。尽管我们以前报道,DDX3X感染1型单纯疱疹病毒粒子的最优生产需要调制,不足为奇的是,病毒基因转录和翻译gydF4y2Ba25gydF4y2Ba,或者为什么蛋白质是如何融入成熟病毒粒子是未知的。DDX3X因此多功能蛋白质,RNA和DNA病毒的影响,这也使得它成为一个有吸引力的治疗目标。gydF4y2Ba
1型单纯疱疹病毒是人类疱疹病毒与一堆的相关条件gydF4y2Ba26gydF4y2Ba。这个包裹DNA病毒复制其基因组组装新的核衣壳gydF4y2Ba27gydF4y2Ba,gydF4y2Ba28gydF4y2Ba。生产至少四种类型的病毒颗粒感染细胞的细胞核。这始于原壳体,充满了脚手架蛋白,核酸和thermo-unstable,有空。乳沟,支架部分释放病毒基因组的衣壳,而衣壳获得一个二十面体形状,产生所谓的C-capsids。这些伴随的过程不是绝对的和流产病毒性中间体也产生,包括isocahedral A-capsids缺乏的脚手架和B-capsids仍然保留了脚手架gydF4y2Ba28gydF4y2Ba。C-capsids优先出口的核——或B-nuclear衣壳但推动这种选择性的机制没有完全理解gydF4y2Ba29日gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba,gydF4y2Ba31日gydF4y2Ba,gydF4y2Ba32gydF4y2Ba,gydF4y2Ba33gydF4y2Ba,gydF4y2Ba34gydF4y2Ba,gydF4y2Ba35gydF4y2Ba,gydF4y2Ba36gydF4y2Ba。因为这些C-capsids(125海里)通过核孔太大,进入细胞质的非常规路线gydF4y2Ba30.gydF4y2Ba第一个通过内核膜涉及他们的萌芽,产生包膜细胞核周围的病毒粒子。这些短暂的病毒粒子保险丝外核膜,de-envelopment一步释放无包膜衣壳进入细胞质。衣壳然后获得最后的信封之前从细胞间细胞表面gydF4y2Ba37gydF4y2Ba,gydF4y2Ba38gydF4y2Ba。gydF4y2Ba
的聚氨酯gydF4y2BalgydF4y2Ba31、聚氨酯gydF4y2BalgydF4y2Ba34病毒蛋白质是至关重要的病毒成分,形成一个所谓的核出口复杂(NEC)促进衣壳核出芽通过内核膜和刺激体外形成囊泡gydF4y2Ba35gydF4y2Ba,gydF4y2Ba39gydF4y2Ba,gydF4y2Ba40gydF4y2Ba,gydF4y2Ba41gydF4y2Ba,gydF4y2Ba42gydF4y2Ba,gydF4y2Ba43gydF4y2Ba,gydF4y2Ba44gydF4y2Ba,gydF4y2Ba45gydF4y2Ba,gydF4y2Ba46gydF4y2Ba,gydF4y2Ba47gydF4y2Ba,gydF4y2Ba48gydF4y2Ba,gydF4y2Ba49gydF4y2Ba,gydF4y2Ba50gydF4y2Ba,gydF4y2Ba51gydF4y2Ba,gydF4y2Ba52gydF4y2Ba,gydF4y2Ba53gydF4y2Ba。NEC组件检测到核衣壳,核膜和细胞核周围的病毒粒子,但缺席成熟细胞外的病毒gydF4y2Ba21gydF4y2Ba,gydF4y2Ba36gydF4y2Ba,gydF4y2Ba43gydF4y2Ba,gydF4y2Ba54gydF4y2Ba,gydF4y2Ba55gydF4y2Ba,gydF4y2Ba56gydF4y2Ba。聚氨酯gydF4y2BalgydF4y2Ba31、聚氨酯gydF4y2BalgydF4y2Ba34都是病毒pU的基质gydF4y2Ba年代gydF4y2Ba3病毒激酶的酶活性改变原子核周围NEC的平稳分布组件gydF4y2Ba43gydF4y2Ba,gydF4y2Ba45gydF4y2Ba。虽然这些磷酸化事件最初被认为主要的后续版本的NEC包膜病毒的细胞核周围的空间gydF4y2Ba42gydF4y2Ba,gydF4y2Ba45gydF4y2Ba,gydF4y2Ba57gydF4y2Ba,gydF4y2Ba58gydF4y2Ba,gydF4y2Ba59gydF4y2Ba,最近的发现表明,NEC磷酸化可能作为负调节控制膜的萌芽直至C-capsids NEC停靠gydF4y2Ba60gydF4y2Ba,gydF4y2Ba61年gydF4y2Ba,gydF4y2Ba62年gydF4y2Ba。有趣的是,删除pUgydF4y2Ba年代gydF4y2Ba3并不妨碍最初萌芽一步而导致核包膜细胞核周围的病毒粒子的累积形成疝,指向病毒激酶的双重角色在病毒出口细胞核,细胞核周围的空间gydF4y2Ba42gydF4y2Ba,gydF4y2Ba45gydF4y2Ba,gydF4y2Ba63年gydF4y2Ba。细胞第9、TorsinA SUN2, ESCRT三世组件CHMP4B和阿历克斯,VAPB CD98、蛋白激酶C和D以及SCL35E1另外一直与疱疹病毒核出口gydF4y2Ba64年gydF4y2Ba,gydF4y2Ba65年gydF4y2Ba,gydF4y2Ba66年gydF4y2Ba,gydF4y2Ba67年gydF4y2Ba,gydF4y2Ba68年gydF4y2Ba,gydF4y2Ba69年gydF4y2Ba,gydF4y2Ba70年gydF4y2Ba,gydF4y2Ba71年gydF4y2Ba,gydF4y2Ba72年gydF4y2Ba,gydF4y2Ba73年gydF4y2Ba,gydF4y2Ba74年gydF4y2Ba。然而许多分子的细节这复杂的核出口途径仍有待澄清。gydF4y2Ba
鉴于1型单纯疱疹病毒粒子及其DDX3X整合调节病毒基因表达的能力gydF4y2Ba21gydF4y2Ba,gydF4y2Ba23gydF4y2Ba,gydF4y2Ba25gydF4y2Ba荧光显微镜,我们最初的病毒可能会遇到DDX3X定义。尽管DDX3X主要积累在未感染细胞的胞质如预期的那样,病毒出奇的重定向细胞核膜蛋白。RNA干扰和电磁干扰的研究暗示,这是功能相关自DDX3X损耗导致核包膜细胞核周围的病毒粒子的积累形成疝类似报道1型单纯疱疹病毒或减压阀突变体缺乏病毒聚氨酯gydF4y2Ba年代gydF4y2Ba3激酶或那些模拟既定的磷酸化pUgydF4y2BalgydF4y2Ba31日gydF4y2Ba59gydF4y2Ba。解释如何参与DDX3X 1型单纯疱疹病毒的核出口,我们确定了DDX3X绑定合作伙伴通过质谱1型单纯疱疹病毒感染的细胞,这揭示了15种不同的病毒蛋白。其中,聚氨酯gydF4y2BalgydF4y2Ba31日是特别感兴趣的特定作用的核出口的核relocalisation DDX3X。绑定DDX3X聚氨酯gydF4y2BalgydF4y2Ba31日证实了co-immunoprecipitation,免疫荧光和病毒突变体。最有趣的是,DDX3X核膜本地化不仅NEC和聚氨酯gydF4y2Ba年代gydF4y2Ba3依赖而且C-capsid依赖,NEC核本地化DDX3X独立的。此外,DDX3X co-localised大衣壳核外围焦点,其存在是DDX3X和C-capsid依赖,暗示功能DDX3X之间的联系,C-capsids和NEC。进一步分析了EM表示这是细胞核周围的病毒粒子位于两个核之间的膜。他们还透露,DDX3X是正常水平的成熟病毒粒子将所需的聚氨酯gydF4y2Ba年代gydF4y2Ba3,两种蛋白质浓缩核细胞膜相互作用,解释了为什么DDX3X或聚氨酯gydF4y2Ba年代gydF4y2Ba3损耗导致相似的表型。总之,这表明DDX3X与病毒核合作出口机械和聚氨酯gydF4y2Ba年代gydF4y2Ba3病毒激酶在1型单纯疱疹病毒细胞核退出。这些令人兴奋的发现强调意想不到的功能为哺乳动物核成熟过程中RNA解旋酶DNA病毒,将开辟新的研究途径。gydF4y2Ba
结果gydF4y2Ba
1型单纯疱疹病毒重定向DDX3X核膜gydF4y2Ba
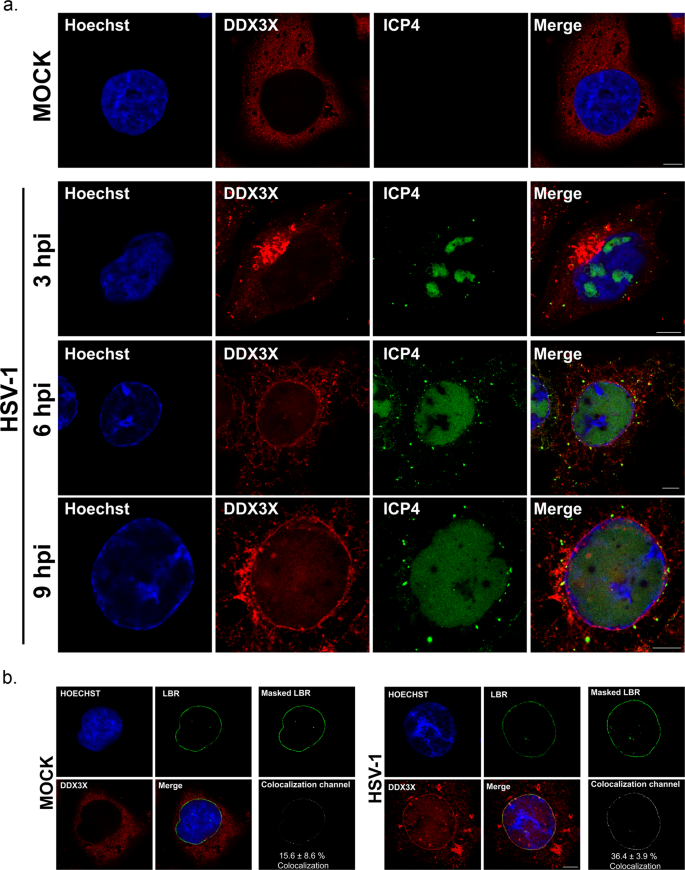
我们之前报道,DDX3X存在于成熟的1型单纯疱疹病毒粒子和最优1型单纯疱疹病毒的传播,需要消耗的DDX3X减少细胞外病毒产量50 - 70%。减少最初归因于其调节病毒基因表达的能力,这是预期的RNA解旋酶gydF4y2Ba21gydF4y2Ba,gydF4y2Ba23gydF4y2Ba,gydF4y2Ba25gydF4y2Ba。定义在病毒第一次遇到DDX3X可能合并,我们检查了本地化DDX3X HSV感染期间使用我们的标准17gydF4y2Ba+gydF4y2Ba实验室的压力。正如预期的gydF4y2Ba75年gydF4y2Ba,质核穿梭DDX3X主要是胞质扩散的细胞无毒性和一些核斑点(无花果。gydF4y2Ba1gydF4y2Ba;模拟)。然而,DDX3X relocalised细胞核附近聚集在感染早期(无花果。gydF4y2Ba1gydF4y2Ba;感染后3小时以内(hpi)),符合其在一定条件下形成压力颗粒的能力gydF4y2Ba76年gydF4y2Ba。6居民,大部分这些最初总量逐步消散,取而代之的是核边缘含有斑点的染色。这是特别明显的现病史9和现在在80 - 85%的细胞(图gydF4y2Ba1gydF4y2Ba),当时大部分的新生产1型单纯疱疹病毒核衣壳退出。这个relocalisation量化,我们标记细胞和抗体针对lamin-B受体(LBR),一个内核膜标记。DDX3X当时发现膜在15.6%±8.6未感染的细胞,这一比例翻了一番,达到36.4%±3.9在感染细胞gydF4y2BapgydF4y2Ba值为0.0367(图。gydF4y2Ba1 bgydF4y2Ba)。1型单纯疱疹病毒因此明显重定向的一些DDX3X在感染后期核膜。gydF4y2Ba
一个gydF4y2Ba海拉细胞种植在盖玻片是模拟治疗或野生型菌株感染17gydF4y2Ba+gydF4y2Ba病毒的莫伊5。感染是停在3、6、9 h感染后(hpi)。免疫荧光细胞被固定和加工(DDX3X:红色;ICP4:绿色;赫斯特33342年:蓝色)。样本使用、显微成像。酒吧代表5µm规模。图片代表三个独立的实验。gydF4y2BabgydF4y2Ba量化的DDX3X relocalisation原子核是由播种海拉细胞在盖玻片和模拟治疗或野生型菌株感染17gydF4y2Ba+gydF4y2Ba病毒的莫伊5。在现病史9,细胞被固定和加工双颜色、显微镜使用anti-DDX3X(红色)和anti-LBR(绿色)抗体。在三个独立的实验中,12个随机整个细胞(z-stacks)成像的条件。接下来,图像处理与伊万里瓷器软件计算的数量DDX3X上发现一个蒙面LBR通道。酒吧代表5µm规模。意味着±标准差(两国的学生gydF4y2BaTgydF4y2Ba测试;gydF4y2BapgydF4y2Ba= 0.0367)。gydF4y2Ba
DDX3X调节细胞核周围的病毒粒子堆积gydF4y2Ba
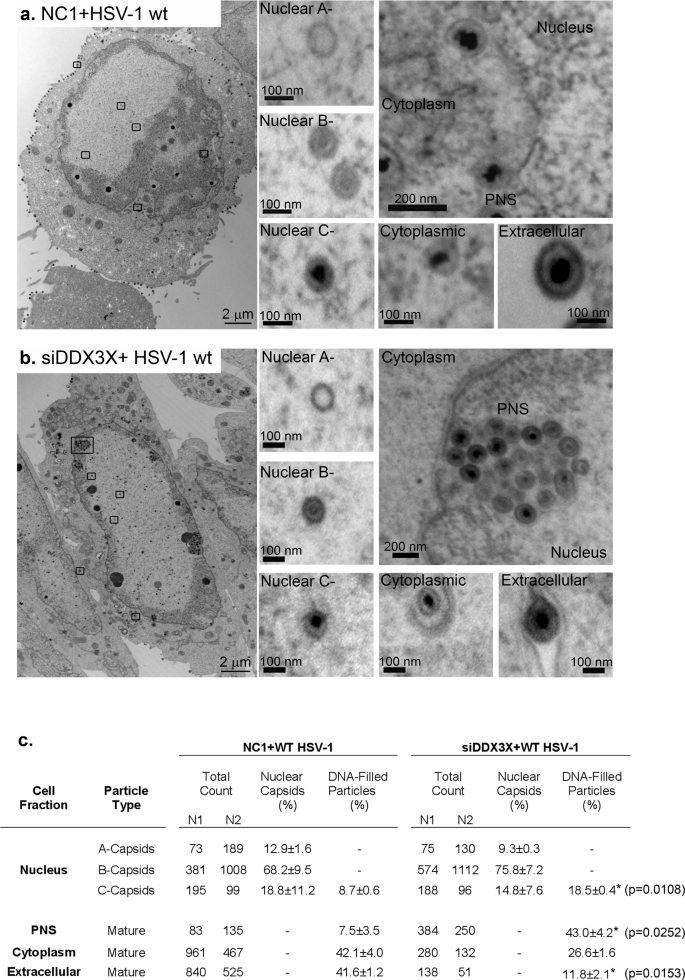
鉴于DDX3X的重新定位,我们想知道这是功能相关的病毒。我们之前报道,DDX3X所需最优病毒基因的表达与下游影响病毒基因组拷贝,衣壳组装和感染性粒子丰富gydF4y2Ba25gydF4y2Ba。调查如果另外解旋酶影响的核出口,我们进行了详细的分析1型单纯疱疹病毒的出口途径通过电子显微镜在RNA干扰的背景下针对DDX3X,使用上述17gydF4y2Ba+gydF4y2Ba病毒毒株。我们还依赖于先前的siRNA试剂之前证明是有效地减少DDX3X水平细胞蛋白质水平抑制(70%)和抑制DDX3X公司成熟细胞外的病毒粒子减少(> 90%)对细胞生存能力没有显著影响细胞的生存能力(80%)gydF4y2Ba23gydF4y2Ba,gydF4y2Ba25gydF4y2Ba。正如预期的那样,所有的病毒中间体,包括A - B - C-nuclear衣壳,细胞核周围的病毒粒子和细胞质衣壳以及成熟的细胞外的病毒粒子中可检测野生型感染的正常水平的DDX3X(无花果。gydF4y2Ba2gydF4y2Ba)。最有趣的是,DDX3X枯竭导致减少大量的病毒颗粒在等离子体膜和野生型包膜病毒颗粒的积累在核形成疝(无花果。gydF4y2Ba2 bgydF4y2Ba)。虽然没有核衣壳的相对丰度的差异(见%核衣壳)DDX3X枯竭时,有一个显著的积累成熟C-capsids(两个)和细胞核周围的病毒粒子(6倍)的细胞外的病毒颗粒在考虑充满dna病毒颗粒(无花果。gydF4y2Ba2摄氏度gydF4y2Ba)。因此,DDX3X细胞核周围的病毒粒子的累积的影响。这让人想起表型观察到的聚氨酯gydF4y2Ba年代gydF4y2Ba3,调节NEC函数在病毒出芽但导致细胞核周围的病毒粒子的堆积形成疝时缺陷(见介绍)。我们也注意到在细胞核中保留C-capsids略大(DDX3X耗尽细胞增加两倍),还提出一个可能的角色在核衣壳DDX3X萌芽,虽然这没有达到统计学意义。总的来说,这表明,DDX3X是所需的最佳释放1型单纯疱疹病毒核衣壳,哺乳动物的RNA解旋酶的不可预见的作用。gydF4y2Ba
海拉细胞被播种在6-well盘子和处理gydF4y2Ba一个gydF4y2Ba控制新NC1或gydF4y2BabgydF4y2BasiDDX3X 48 h然后感染野生型菌株17gydF4y2Ba+gydF4y2Ba病毒的莫伊5。在12 hpi,细胞被固定和准备电子显微镜(见方法)。整个图像显示细胞的观点与缩放,B - C-nuclear衣壳以及病毒颗粒在细胞质和细胞表面。gydF4y2BacgydF4y2Ba14从每个受感染细胞被随机选择条件在两个独立的实验(N1;N2)。A - B - C-nuclear衣壳以及病毒颗粒在细胞核周围的空间(pn),细胞质和细胞外空间计算。百分比(±标准错误的手段)指的是相对大量的核衣壳核衣壳(%)或包含病毒基因组的病毒颗粒总数(%充满dna粒子,即。C-capsids细胞核周围的病毒粒子,细胞质病毒颗粒,细胞外的病毒)。两国的学生gydF4y2BaTgydF4y2Ba测试被执行。*gydF4y2BapgydF4y2Ba< 0.05和* *gydF4y2BapgydF4y2Ba< 0.01。gydF4y2Ba
DDX3X有多个潜在的病毒伙伴gydF4y2Ba
破译DDX3X如何改变病毒的核出口,我们假设DDX3X,直接或间接地与至少一个病毒蛋白相互作用与途径。确定这样的合作伙伴,我们开发了一个稳定细胞系表达蛋白G标记DDX3X执行拉痛苦。这个细胞系表现出类似的表达水平和本地化内生DDX3X,由免疫印迹和免疫荧光(图gydF4y2Ba1gydF4y2Ba)。这是在我们以前的报告标记DDX3X通常表现在模拟海拉细胞治疗或1型单纯疱疹病毒感染gydF4y2Ba25gydF4y2Ba。然后我们被感染的细胞和细胞溶解产物收集4或12 hpi区分早期(没有衣壳制成)和晚期(新装配的病毒颗粒的释放)的感染阶段。自从DDX3X功能与细胞蛋白的数组(uniprot.org),我们使用未受感染的细胞作为控制。使用一式三份独立的质谱分析和严格的条件(95%肽和蛋白质的信心,2肽最小和检测在所有3实验),四个病毒蛋白质在现病史4唯一标识,另外四个在12和7的快乐与DDX3X在两个时间点(图gydF4y2Ba2gydF4y2Ba)。大约一半的目标是皮蛋白质(40%),27%的非结构化病毒蛋白质衣壳蛋白(图包膜糖蛋白20%和13%。SgydF4y2Ba2 bgydF4y2Ba)gydF4y2Ba21gydF4y2Ba。不仅仅这些蛋白质是病毒颗粒,co-purified DDX3X因为许多其他病毒粒子组件缺席的样本,包括主要衣壳蛋白VP5非常丰富。gydF4y2Ba
与NEC DDX3X形式复杂gydF4y2Ba
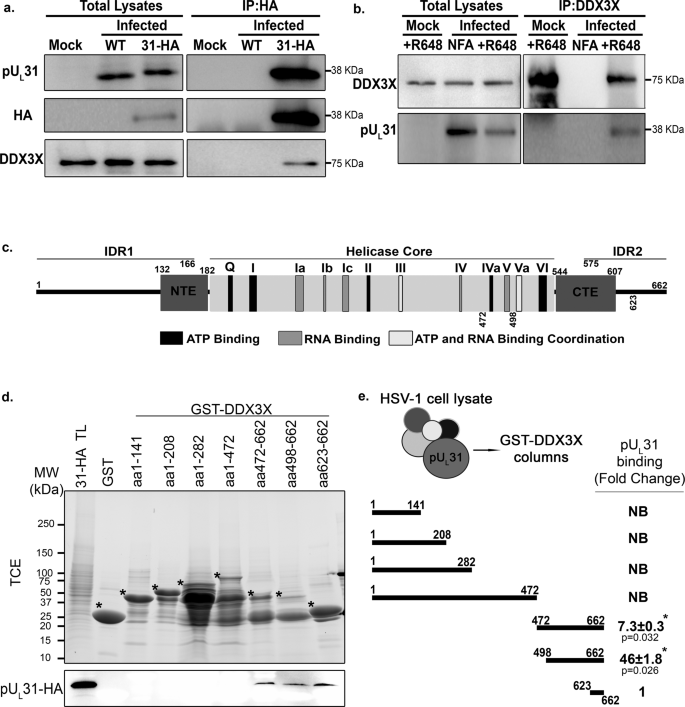
鉴于DDX3X核细胞膜的存在和调制的病毒核出口,NEC的识别组件聚氨酯gydF4y2BalgydF4y2Ba31日为DDX3X约束力的合作伙伴是有趣的因为NEC参与衣壳内核膜包。因此,我们在互惠co-IP交互实验进行验证。我们采取一个重组病毒编码HA-tagged pUgydF4y2BalgydF4y2Ba31因为聚氨酯gydF4y2BalgydF4y2Ba31日IP抗体表现不佳。注意这个突变是在F 1型单纯疱疹病毒株的背景。控制,细胞模拟治疗或野生型菌株F病毒感染(无哈标签)。然后我们纯化聚氨酯gydF4y2BalgydF4y2Ba31日使用商用anti-HA琼脂糖珠,免疫印迹检查DDX3X的存在。确认的数据形成一个复杂的(DDX3X co-IP HA抗体)的特异性抗体(DDX3X只是存在于细胞感染重组病毒和聚氨酯gydF4y2BalgydF4y2Ba31和HA抗体检测到这些蛋白质在模拟或野生型感染细胞溶解产物(图)。gydF4y2Ba3gydF4y2Ba)。相反的条件下,细胞被感染野生型病毒,内生DDX3X检索与DDX3X R648多克隆抗体gydF4y2Ba77年gydF4y2Ba和聚氨酯gydF4y2BalgydF4y2Ba31日受到西方墨点法。正如所料,聚氨酯gydF4y2BalgydF4y2Ba31日检测DDX3X丰富时,但不缺乏主要的抗体(图。gydF4y2Ba3 bgydF4y2Ba)。验证在核膜的交互,在感染细胞进行免疫荧光研究,标签(1型单纯疱疹病毒gydF4y2BaUgydF4y2BalgydF4y2Ba31日gydF4y2Ba病毒ha)和聚氨酯gydF4y2BalgydF4y2Ba34 (NEC和核膜标记)。结果证实了上述发现,DDX3X部分co-localises聚氨酯gydF4y2BalgydF4y2Ba核被膜(图31。SgydF4y2Ba3gydF4y2Ba)。此外,这进一步扩展我们的发现1型单纯疱疹F株以上。gydF4y2Ba
交互使用co-IP DDX3X和pUL31评估。gydF4y2Ba一个gydF4y2Ba海拉细胞被mock-treated或野生型菌株F病毒感染(负控制)或HA-tagged pUgydF4y2BalgydF4y2Ba31日病毒的莫伊现病史5 12。细胞是细胞溶解和HA-tagged pUgydF4y2BalgydF4y2Ba31日拉下使用anti-HA琼脂糖珠。总溶解产物和洗出液被调查分析了世行聚氨酯gydF4y2BalgydF4y2Ba31日(反公顷或聚氨酯gydF4y2BalgydF4y2Ba31日)和DDX3X(反DDX3兔子R648多克隆血清)显示左边的屁股。gydF4y2BabgydF4y2Ba反向co-IP也表现了海拉细胞mock-treated或感染如上所述,而是沉淀DDX3X(反DDX3兔子R648多克隆血清琼脂糖珠和蛋白质)。DDX3X和聚氨酯gydF4y2BalgydF4y2Ba31日在洗出液进行评估通过免疫印迹使用anti-DDX3X R648或anti-pUgydF4y2BalgydF4y2Ba31这些墨迹图左侧所示。gydF4y2BacgydF4y2Ba示意图DDX3X地图显示其不同领域和主题(改编自gydF4y2Ba103年gydF4y2Ba)。印尼盾,《和CTE代表内在无序域,分别N -和c端扩展。解旋酶的核心(残留182 - 544)代表了最低限度DDX3X活跃的部分。守恒DDX3X图案都是颜色编码的定义上的传奇人物。这些图案调节ATP和RNA绑定或两个函数之间的协调。gydF4y2BadgydF4y2Ba重组GST-tagged DDX3X构造或销售税单独控制了谷胱甘肽琼脂糖4 b珠子。海拉受感染的溶解产物(HA-tagged pUgydF4y2BalgydF4y2Ba31个病毒,莫伊的24 hpi) van buren消费税加载谷胱甘肽琼脂糖珠然后孵化与各种丰富GST-DDX3X构造3 h。珠子被煮在样品缓冲释放诱饵。分析了样品在5 - 20%包含0.5% TCE梯度sds - page。珠的水平约束GST-tagged结构分析了紫外线照射面板(TCE) ChemiDoc (BioRad)。绑定的聚氨酯gydF4y2BalgydF4y2Ba31日被西方墨点法评估使用HA-tag抗体(下半部分)。明星突出每个销售税构造的位置。TL代表总溶解产物珠子之前加载。gydF4y2BaegydF4y2Ba量化的聚氨酯gydF4y2BalgydF4y2Ba31日绑定到每个DDX3X构造的珠子(画示意图)。绑定被正常化计算HA-tagged pUL31免疫印迹信号为每个销售税TCE信号妄想。褶皱的变化是衡量任意设置绑定GST-DDX3X aa 623 - 662。没有绑定定义是NB(没有绑定)。±标准错误的手段(两国的学生gydF4y2BaTgydF4y2Ba测试;*gydF4y2BapgydF4y2Ba< 0.05)。图代表了四个独立的实验。gydF4y2Ba
我们下一个映射DDX3X残留物(见地图在无花果。gydF4y2Ba3 cgydF4y2Ba)与聚氨酯形成一个复杂的需要gydF4y2BalgydF4y2Ba31日,利用提供的一组细菌结构优雅Arvind Patel博士和表达不同的销售税标记DDX3X碎片gydF4y2Ba78年gydF4y2Ba。在方法部分详细和传说,感染细胞溶解产物经过DDX3X片段固定在琼脂糖珠和免疫印迹分析聚氨酯gydF4y2BalgydF4y2Ba31日结合这些碎片。注意,尽管表达的不同片段在相似的水平(图gydF4y2Ba4gydF4y2Ba),他们一定会谷胱甘肽琼脂糖珠有不同的效率(图。gydF4y2Ba3 dgydF4y2Ba),大概是因为他们的独特的三维折叠或溶解度。为了避免任何偏见,我们监控DDX3X绑定的珠子通过合并2,2,2-Trichloroethanol (TCE)在sds - page凝胶,使总蛋白成像在紫外光照前转移到PVDF膜检测聚氨酯gydF4y2BalgydF4y2Ba31日通过免疫印迹gydF4y2Ba79年gydF4y2Ba,gydF4y2Ba80年gydF4y2Ba。这使得估计pU成为可能gydF4y2BalgydF4y2Ba31 DDX3X或控制销售税信号比率在同一凝胶(无花果。gydF4y2Ba3 egydF4y2Ba)。这些实验表明,聚氨酯gydF4y2BalgydF4y2Ba31只绑定到DDX3X羧基末端,主要通过498 - 662片段(图。gydF4y2Ba3 d egydF4y2Ba)。虽然这个绑定可以间接的为我们使用受感染的细胞溶解产物作为聚氨酯的来源gydF4y2BalgydF4y2Ba31日,这些实验证实DDX3X和NEC之间的物理相互作用。gydF4y2Ba
DDX3X核膜招聘是依赖于NEC的gydF4y2Ba
我们想知道是什么驱使DDX3X核膜在1型单纯疱疹病毒感染。我们猜测,聚氨酯gydF4y2BalgydF4y2Ba5月31日捕获DDX3X核细胞膜和评估如果聚氨酯的缺失gydF4y2BalgydF4y2Ba31日将改变DDX3X的胞内定位。事实上,一个聚氨酯感染gydF4y2BalgydF4y2Ba31日删除突变病毒招募大大减少DDX3X核细胞膜(无花果。SgydF4y2Ba5gydF4y2Ba)。由于溶性聚氨酯gydF4y2BalgydF4y2Ba31日与内核膜peripherically相关通过其与蛋白质pU积分gydF4y2BalgydF4y2Ba34gydF4y2Ba43gydF4y2Ba,pU的突变体耗尽gydF4y2BalgydF4y2Ba34毫不奇怪了相同的表型对DDX3X本地化(无花果。SgydF4y2Ba5gydF4y2Ba)。应该注意的是,聚氨酯gydF4y2BalgydF4y2Ba34本地化有点不安,pU的缺失gydF4y2BalgydF4y2Ba31日。因此,聚氨酯gydF4y2BalgydF4y2Ba34部分核膜结合但分布在一个ER-like舱pU的缺失gydF4y2BalgydF4y2Ba31,暗示一些错误的膜定位,滚子和同事的表型之前报道gydF4y2Ba43gydF4y2Ba。聚氨酯的角色gydF4y2Ba年代gydF4y2Ba3在NEC核出口机器,我们也对其影响DDX3X核本地化。有趣的是,gydF4y2BaUgydF4y2Ba年代gydF4y2Ba3gydF4y2Ba删除病毒变异同样招募DDX3X少有效核膜(图gydF4y2Ba5gydF4y2Ba),这表明磷酸化的NEC组件或在核膜光滑的定位可能导致DDX3X招聘到核细胞膜上。相比之下,损耗的细胞相关DDX3X通过RNA干扰没有影响的核本地化NEC组件(图gydF4y2Ba6gydF4y2Ba)。这些发现是最符合模型,pUgydF4y2BalgydF4y2Ba31日捕获DDX3X核膜。gydF4y2Ba
DDX3X促进大VP5疫源地的形成核外围gydF4y2Ba
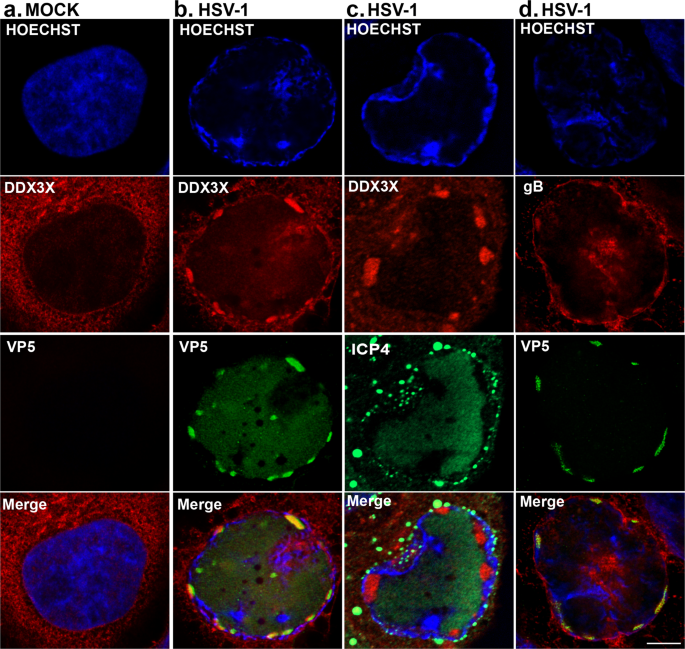
虽然上述EM研究强调的作用DDX3X de-envelopment阶段核病毒衣壳,可能积累的成熟在核衣壳是令人费解的。详细评估NEC和DDX3X之间的物理相互作用如何影响病毒核出口,我们进行高分辨率、共焦显微镜DDX3X和病毒衣壳,与抗体检测针对VP5主要衣壳组件。正如所料,DDX3X基本上是细胞质的细胞无毒性和部分重定向到细胞核的病毒在感染后期(无花果。gydF4y2Ba4 a、bgydF4y2Ba)。出乎意料,DDX3X co-localised VP5在大型稍微拉长在核衣壳病灶边缘(> 1µm和4µm)但是不是更加分散或小圆VP5焦点(0.5 1µm)。量化的数据从六个细胞在每个三个独立的实验中显示,100%的这些大VP5疫源地DDX3X是积极的。这些大的衣壳疫源地,可见在~ 20%的受感染的细胞,没有co-localise ICP4(无花果。gydF4y2Ba4摄氏度gydF4y2Ba),病毒复制区域的标志gydF4y2Ba81年gydF4y2Ba,但偶尔染色阳性病毒包膜蛋白gB,暗示核衣壳是密切同信封或者细胞核周围的包膜病毒粒子(图表示。gydF4y2Ba4 dgydF4y2Ba)。gydF4y2Ba
海拉细胞播种在盖玻片gydF4y2Ba一个gydF4y2Bamock-treated或gydF4y2Ba罪犯gydF4y2Ba野生型菌株感染17gydF4y2Ba+gydF4y2Ba病毒的莫伊现病史5为9。细胞被固定和标签gydF4y2Ba一个gydF4y2Ba,gydF4y2BabgydF4y2BaDDX3X(红色)和VP5(绿色)gydF4y2BacgydF4y2BaDDX3X(红色)和ICP4(绿色)gydF4y2BadgydF4y2BagB(红色)和VP5(绿色)。所有原子核都沾染了赫斯特33342年(蓝色)。使用双彩色高分辨率、显微镜细胞成像。酒吧代表5µm规模。的图片是代表三个独立的实验。gydF4y2Ba
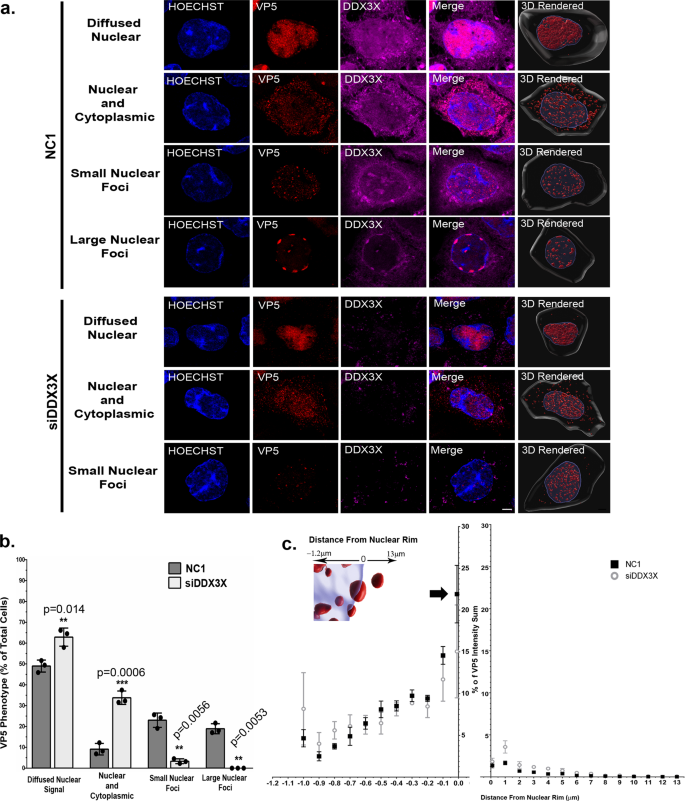
评估如果DDX3X-dependent衣壳大疫源地,我们重复了这个实验在宿主蛋白的存在与否。在感染细胞的新NC1 siRNA对待,我们观察和量化四种不同VP5分布模式(扩散核、核和胞质、小核疫源地和上述大型核焦点),所有最好的(图中可见呈现图像。gydF4y2Ba5gydF4y2Ba)。DDX3X耗尽细胞的VP5染色模式通常更加分散的显著损失大部分小焦点和缺乏大细长焦点(无花果。gydF4y2Ba5 a、bgydF4y2Ba)。DDX3X因此似乎对衣壳聚合物的生成至关重要。鉴于这些大型的邻近衣壳与核外围聚集,我们想知道如果DDX3X改变的细胞内分布VP5焦点通过测量距离核外围。然而,分析显示,DDX3X没有改变VP5焦点的定位(图。gydF4y2Ba5度gydF4y2Ba)。有趣的是,大部分的大型VP5聚集在靠近核膜的20 - 25%的总量在0附近µm轴(见大箭头图。gydF4y2Ba5度gydF4y2Ba)。我们得出结论,DDX3X所需的起源更大的核外围聚集,但不是他们的交通从另一个位置。gydF4y2Ba
一个gydF4y2Ba海拉细胞种植在盖玻片和25 nM siDDX3X转染或新控制siRNA (NC1) 48 h。细胞被感染野生型菌株17gydF4y2Ba+gydF4y2Ba病毒的莫伊现病史5为9。DDX3X固定细胞被标记(红色)和VP5(红色)和细胞核染色使用赫斯特33342(蓝色)。这个面板显示了不同的代表图片VP5表型观察和他们的3 d渲染插图(见方法)。所呈现的图像(Z-stacks获得传统共焦显微镜)。酒吧代表5µm规模。gydF4y2BabgydF4y2Ba八个随机图像(包含约200个细胞)为每个条件量化分析了上述VP5表型。酒吧表示方式和手段的标准误差。两国的学生gydF4y2BaTgydF4y2Ba测试,* *gydF4y2BapgydF4y2Ba< 0.01;* * *gydF4y2BapgydF4y2Ba< 0.001;NS:不重要。gydF4y2BacgydF4y2Ba二十随机细胞/表型(六个细胞越丰富的小型核疫源地siDDX3X治疗细胞)分析了伊万里瓷器软件比较VP5信号的分布(%强度之和)与他们的距离核边缘(µM)。每个点代表三个独立的实验和误差的均值表明标准差的意思。所以统计差异被发现gydF4y2BacgydF4y2Ba。gydF4y2Ba
DDX3X调节C-capsid崭露头角的gydF4y2Ba
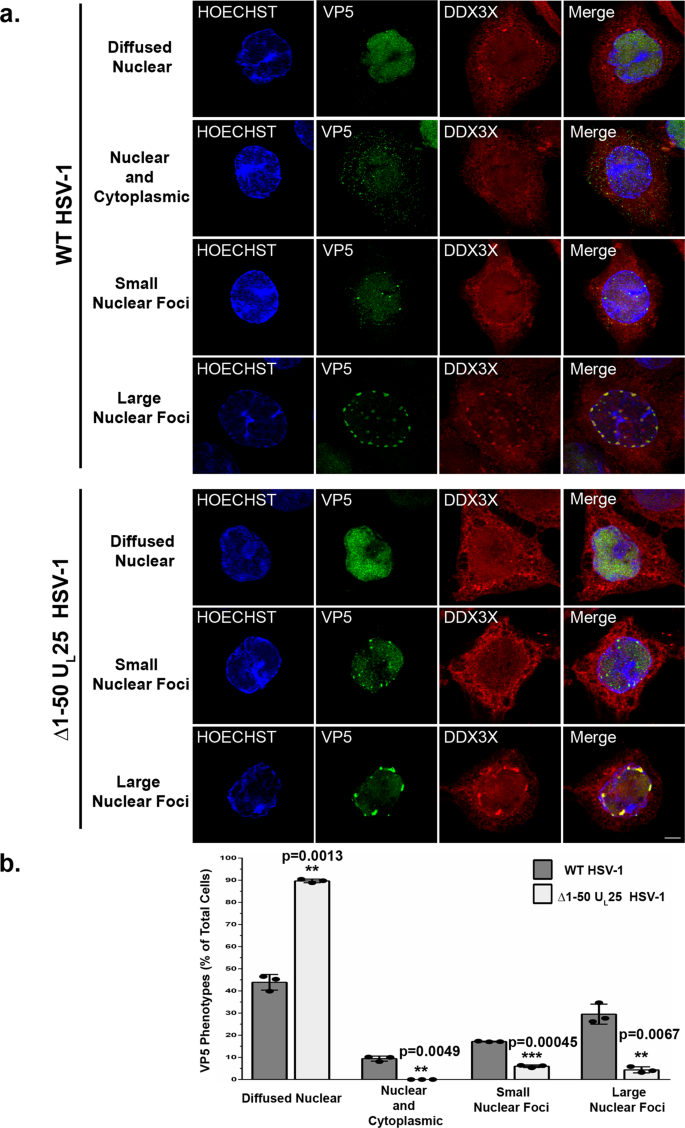
DDX3X-dependent形成核衣壳大疫源地的外围,有别于病毒复制隔间提出问题是否这些核衣壳是退出。这不是简单的1型单纯疱疹病毒产生四种不同的核衣壳(见介绍)。探索如果这些大型衣壳聚合C-capsids,我们比较了VP5表达式模式由野生型病毒与病毒变异vFH421编码生成的1型单纯疱疹病毒Δ1-50 UgydF4y2BalgydF4y2Ba25日,生产高度C-capsid水平降低,但仍有效地使其他类型的衣壳gydF4y2Ba34gydF4y2Ba,gydF4y2Ba36gydF4y2Ba,gydF4y2Ba82年gydF4y2Ba,gydF4y2Ba83年gydF4y2Ba。注意,这些突变体是基于科斯的压力,所以我们比较他们相应的野生型父母的压力。图gydF4y2Ba6gydF4y2Ba(前面板)显示再次通常分布的四个VP5表达谱在野生型感染细胞,表明这些表型也程度第三个1型单纯疱疹病毒。然而,在细胞感染病毒突变,无论大小,VP5核焦点在统计学上减少,只有5%的细胞表现出大疫源地VP5和DDX3X colocalised(无花果。gydF4y2Ba6 a、bgydF4y2Ba)。虽然有些残余病灶持续,我们认为他们可能代表有限的A - B -核衣壳,摆脱原子核gydF4y2Ba29日gydF4y2Ba。有趣的是,聚氨酯gydF4y2BalgydF4y2Ba34本地化是缺乏强烈不安的核衣壳和显示一个在细胞核内的染色。尽管意想不到的跨膜蛋白,聚氨酯gydF4y2BalgydF4y2Ba34在纯化的蛋白质组学研究还发现1型单纯疱疹病毒核衣壳(即使用女士而不是抗体),从而采用正交确认这种奇怪的观察,我们无法解释gydF4y2Ba36gydF4y2Ba。尽管如此,这一总体表明,大型VP5疫源地DDX3X和C-capsid依赖一致的再一次与一个角色DDX3X在1型单纯疱疹病毒核出口。gydF4y2Ba
一个gydF4y2Ba海拉细胞被mock-treated或感染病毒变异的莫伊5∆1-50 UgydF4y2BalgydF4y2Ba25(只会让A和B核衣壳)或相应的科斯野生型病毒。在现病史9,免疫荧光细胞被固定和加工(DDX3X:红色;VP5:绿色;赫斯特33342年核染色:蓝色)。传统的共焦显微镜图像获得的。酒吧代表5µm规模。gydF4y2BabgydF4y2Ba10个随机图像(~ 200细胞/条件)被用来量化不同VP5表型。三个独立实验的百分比方式以及它们的标准差(两国的学生gydF4y2BaTgydF4y2Ba测试;* * *gydF4y2BapgydF4y2Ba< 0.001)。gydF4y2Ba
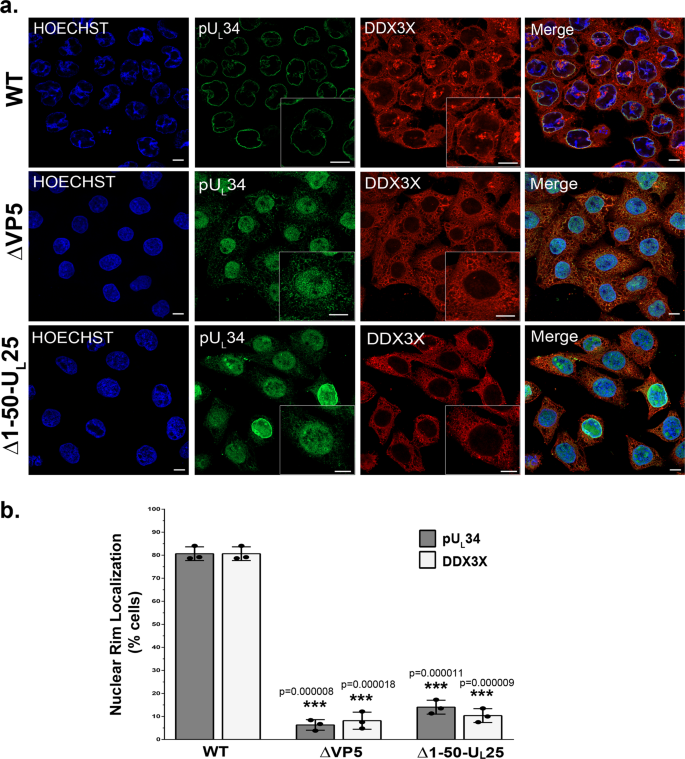
为了更好地理解的机制DDX3X调节1型单纯疱疹病毒核衣壳出口,我们下一个评估如果C-capsids所需DDX3X核本地化。这是评估突变病毒的上下文中,无法完全组装病毒衣壳(变异缺乏主要衣壳蛋白VP5gydF4y2Ba84年gydF4y2Ba)或只组装和B -但不是C-nuclear衣壳(Δ1-50 UgydF4y2BalgydF4y2Ba25)。图gydF4y2Ba7gydF4y2Ba表明ΔVP5病毒突变体没有重定向pUgydF4y2BalgydF4y2Ba34核膜。在这种背景下,DDX3X也不足为奇的是,缺席以来核膜NEC新兵在那里(无花果。gydF4y2Ba7gydF4y2Ba)。最有趣的是,这些表型也发现在细胞感染C-capsid缺陷病毒(Δ1-50 UgydF4y2BalgydF4y2Ba25),表明这些表型C-capsid驱动的。gydF4y2Ba
一个gydF4y2Ba海拉细胞播种在盖玻片mock-treated或感染的莫伊5与∆VP5或∆1-50 UgydF4y2BalgydF4y2Ba科斯25突变病毒或相应的野生型病毒。细胞被固定在9 hpi和标签DDX3X(红色),聚氨酯gydF4y2BalgydF4y2Ba34(绿色)和赫斯特33342染色细胞核(蓝色)。放大框添加强调DDX3X和聚氨酯gydF4y2BalgydF4y2Ba在每个条件34本地化。所有酒吧代表5µm规模。gydF4y2BabgydF4y2Ba量化的核聚氨酯gydF4y2BalgydF4y2Ba34和DDX3X使用100随机细胞状态。酒吧表示均值和标准差的手段(两国的学生gydF4y2BaTgydF4y2Ba测试;* * *gydF4y2BapgydF4y2Ba< 0.001)。代表三个独立实验的数据。gydF4y2Ba
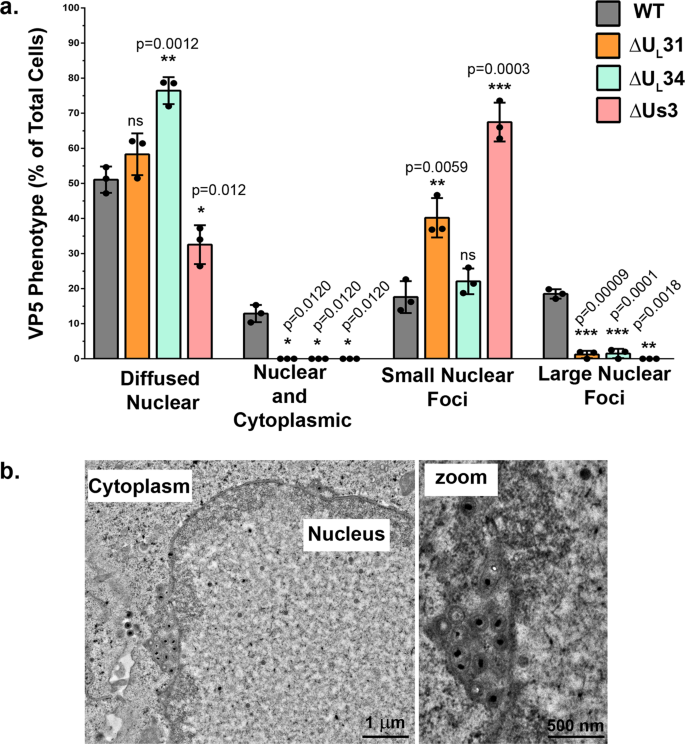
一个有趣的方面是大VP5疫源地见上图先于衣壳与NEC的联系。为了验证这一点,我们诉诸于共焦显微镜和Z栈中gydF4y2BaUgydF4y2BalgydF4y2Ba31日gydF4y2Ba,gydF4y2BaUgydF4y2BalgydF4y2Ba34gydF4y2Ba或gydF4y2BaUgydF4y2Ba年代gydF4y2Ba3gydF4y2Ba缺乏病毒突变体。量化的结果表明,尽管大型VP5核病灶可见之前在野生型感染细胞约20%,这一比例在很大程度上是和统计上显著降低NEC中断(无花果。SgydF4y2Ba7gydF4y2Ba和无花果。gydF4y2Ba8gydF4y2Ba)。因此,形成大的细长的衣壳焦点在NEC的缺乏阻碍了,暗示衣壳第一次遇到NEC然后凝聚。更直接的调查表型,感染细胞受到电子显微镜的重新塑造。野生型感染细胞后仔细检查,只细长的病毒聚合> 1µm核外围的包膜C-capsids在细胞核周围的空间(无花果。gydF4y2Ba8 bgydF4y2Ba)。有趣的是,这些衣壳的存在焦点在细胞核周围的空间容易解释他们的细长的本性,被困两核之间的膜。总的来说,这些实验表明DDX3X中也扮演了重要的角色在核膜1型单纯疱疹病毒粒子细胞核周围的形态发生,即。,during capsid budding at the inner nuclear membrane, in addition to its implication during the subsequent capsid de-envelopment at the outer nuclear membrane.
一个gydF4y2Ba海拉细胞种植在感染前盖玻片。24小时后,细胞被感染了∆UgydF4y2Ba年代gydF4y2Ba3、∆UgydF4y2BalgydF4y2Ba31、∆UgydF4y2BalgydF4y2Ba34突变病毒或相应的野生型病毒(F应变)的莫伊5。在现病史9细胞治疗传统共焦显微镜和DDX3X贴上标签,VP5和聚氨酯gydF4y2BalgydF4y2Ba34(见图gydF4y2Ba7gydF4y2Ba如果图像)。至少100个细胞/条件分析了量化细胞内VP5分布。百分比的平均值和标准偏差的3个人实验。两国的学生gydF4y2BaTgydF4y2Ba测试被执行,而野生型病毒(*gydF4y2BapgydF4y2Ba< 0.05,* *gydF4y2BapgydF4y2Ba< 0.01和* * *gydF4y2BapgydF4y2Ba< 0.001)。gydF4y2BabgydF4y2Ba海拉细胞被感染野生型菌株17gydF4y2Ba+gydF4y2Ba病毒的莫伊5 9 h。接下来,细胞被固定为电子显微镜和治疗。几个细胞被透射电子显微镜成像使用。的图片是代表三个独立的实验。gydF4y2Ba
DDX3X纯化核衣壳上缺席gydF4y2Ba
在衣壳内核膜萌芽,一个吸引人的场景是DDX3X可能桥C-capsids核膜的绑定病毒衣壳组件。这可以是聚氨酯gydF4y2BalgydF4y2Ba31日,目前在核衣壳gydF4y2Ba36gydF4y2Ba,gydF4y2Ba54gydF4y2Ba,gydF4y2Ba55gydF4y2Ba,或者病毒蛋白的结构确定在本研究DDX3X绑定合作伙伴(无花果gydF4y2Ba2gydF4y2Ba核衣壳),其中一些被报道gydF4y2Ba36gydF4y2Ba,gydF4y2Ba85年gydF4y2Ba,gydF4y2Ba86年gydF4y2Ba。直接探测这个选项,总衣壳从感染纯化细胞核在生理盐条件下保持皮蛋白质衣壳gydF4y2Ba86年gydF4y2Ba。积极的控制,我们还监控细胞外的病毒粒子,它以前将DDX3X显示gydF4y2Ba23gydF4y2Ba。西方墨点法的确证实了在细胞外DDX3X病毒粒子的存在,但不是在核衣壳(图gydF4y2Ba8gydF4y2Ba)。这是符合我们最近的质谱研究没有揭示DDX3X在纯化的存在,B -或C-nuclear衣壳gydF4y2Ba36gydF4y2Ba。虽然我们不能排除DDX3X从衣壳在净化掉了下来,它似乎更有可能,蛋白质不招募衣壳之前他们的交互与NEC, DDX3X,而与传入C-capsids核膜。gydF4y2Ba
DDX3X促进聚氨酯gydF4y2Ba年代gydF4y2Ba3并入病毒颗粒gydF4y2Ba
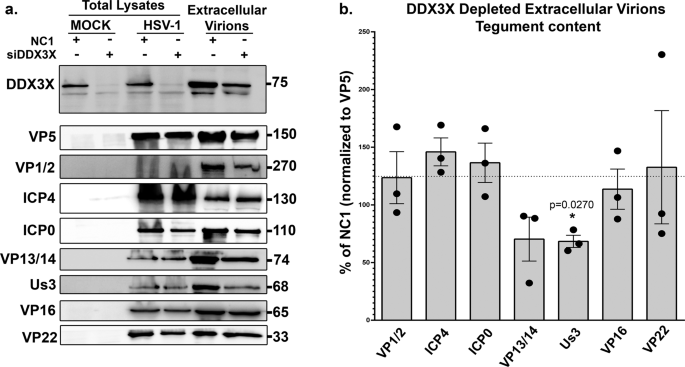
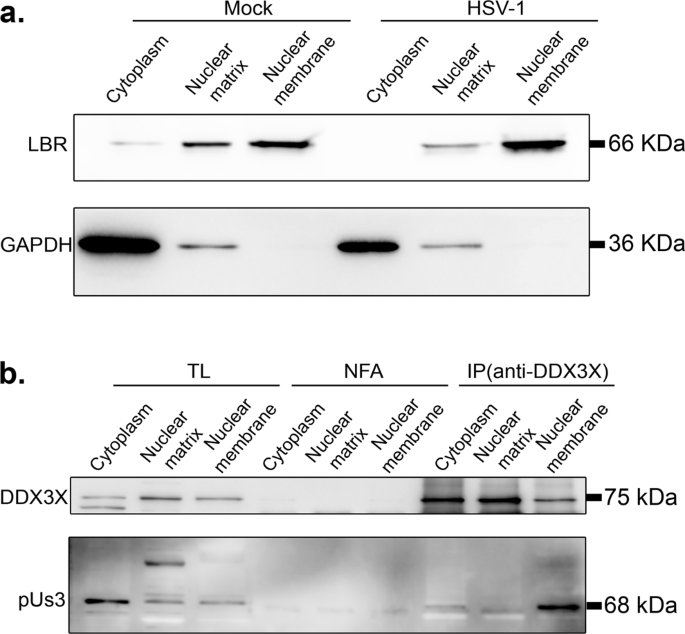
迄今为止,DDX3X似乎促进新病毒衣壳组装的通道通过内部和外部的核细胞膜。在前一种情况中,我们显示高于DDX3X刺激C-capsid崭露头角的通过在核膜与NEC交互,导致细胞核周围的包膜病毒粒子的形成。然而,DDX3X如何也促进细胞核周围的病毒粒子堆积是令人费解的。我们假设DDX3X可能招募关键蛋白在病毒颗粒在萌芽,需要后续阶段的感染。感兴趣的,新组装顺序1型单纯疱疹病毒衣壳成熟的招聘各种皮蛋白质在细胞核内,细胞质或最后的包络gydF4y2Ba38gydF4y2Ba。破译DDX3X如何促进细胞核周围的病毒粒子的融合与外核膜,我们认为探索细胞核周围的病毒粒子的外皮的内容,但这将需要他们的净化,一项艰巨的任务只之前通过一个实验室gydF4y2Ba87年gydF4y2Ba。自纯度仍不能轻易解决的一个问题,我们监控的外皮组成病毒出口的最终产品,即成熟DDX3X耗尽细胞产生的细胞外成熟的病毒粒子。随着聚氨酯gydF4y2BalgydF4y2Ba31、聚氨酯gydF4y2BalgydF4y2Ba34不成熟的细胞外成分病毒粒子,他们省略了分析gydF4y2Ba21gydF4y2Ba,gydF4y2Ba45gydF4y2Ba。七皮蛋白质免疫印迹检测,大部分显示病毒在细胞之间没有显著差异处理的新控制核或那些来自siDDX3X治疗细胞(VP1/2 (pUgydF4y2BalgydF4y2Ba36)、ICP4 ICP0 VP13/14 (pUgydF4y2BalgydF4y2Ba47),VP16 (pUgydF4y2BalgydF4y2Ba48)和VP22 (pUgydF4y2BalgydF4y2Ba49))。然而,显著降低聚氨酯被发现gydF4y2Ba年代gydF4y2Ba3在DDX3X损耗(无花果。gydF4y2Ba9gydF4y2Ba)。这是非常令人兴奋和高度有关聚氨酯的双重角色gydF4y2Ba年代gydF4y2Ba3在1型单纯疱疹病毒通过两个核出口膜(本地化NEC和融合的细胞核周围的病毒粒子外核膜)。因此,我们如果pU探测gydF4y2Ba年代gydF4y2Ba3与DDX3X但也许侦测在我们的蛋白质组学方法(图。SgydF4y2Ba2gydF4y2Ba)。最初实验使用总细胞溶解产物未能发现每我们的女士实验等交互(数据现在如图所示)。然而,由于溶性聚氨酯gydF4y2Ba年代gydF4y2Ba3和DDX3X核膜蛋白存在(gydF4y2Ba58gydF4y2Ba这项研究),我们下一个纯化核生化反应膜。虽然不完美,但数据显示,一个高效的分离细胞质和核分数以及强烈的核浓缩膜基于各自的细胞标记(图。gydF4y2Ba10gydF4y2Ba)。最有趣的是,免疫沉淀反应的DDX3X聚氨酯gydF4y2Ba年代gydF4y2Ba3从感染的细胞,但只有在核膜分数和充其量只差在其他分数(无花果。gydF4y2Ba10 bgydF4y2Ba)。这些数据推断DDX3X促进聚氨酯gydF4y2Ba年代gydF4y2Ba3招聘到病毒颗粒,大概在衣壳对接/出芽病毒激酶将使后续的细胞核周围的病毒粒子释放到细胞质中。gydF4y2Ba
一个gydF4y2Ba海拉细胞被种植在245毫米板和处理控制的新NC1或siDDX3X 48 h。转染细胞mock-treated或野生型菌株感染17gydF4y2Ba+gydF4y2Ba病毒。现病史在24,上层清液含有成熟的病毒粒子收集和集中在60000 x g。他们下一个分析5 - 20%梯度sds - page及免疫印迹,使用针对各种病毒被膜蛋白的抗体。总溶解产物相同的细胞裂解缓冲中收集和分析并行作为负(模拟细胞)和积极的(感染细胞)抗体控制。证实了DDX3X损耗的细胞和病毒粒子探测DDX3X相同的样本。gydF4y2BabgydF4y2Ba图像实验室5.0版本被用来量化西方的屁股(注意,检测的蛋白质是一种乐器4-log线性范围,而不是在x射线胶片)。VP5作为加载控制,使用规范化的数据感染样本。酒吧显示三个独立实验的手段和标准误差的手段(两国的学生gydF4y2BaTgydF4y2Ba测试;*gydF4y2BapgydF4y2Ba< 0.05)。聚氨酯gydF4y2Ba年代gydF4y2Ba3是唯一统计不同的外皮DDX3X枯竭的病毒粒子。gydF4y2Ba
讨论gydF4y2Ba
RNA解旋酶DDX3X主要与细胞的RNA代谢有关,RNA病毒的干扰素反应和调制。然而,我们和其他人已经报道,DDX3X纳入成熟病毒颗粒对乙型肝炎病毒,1型单纯疱疹病毒,减压阀和,血巨细胞病毒都是基于DNA病毒gydF4y2Ba18gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba,gydF4y2Ba21gydF4y2Ba,gydF4y2Ba22gydF4y2Ba,gydF4y2Ba88年gydF4y2Ba。我们也曾发表,DDX3X调节1型单纯疱疹病毒基因组复制和下游基因表达影响数字,衣壳组装和感染性粒子interferon-independent地gydF4y2Ba23gydF4y2Ba,gydF4y2Ba25gydF4y2Ba。这个扩展的作用范围DDX3X RNA和DNA病毒。然而,它是不清楚,为什么DNA病毒招募细胞解旋酶。探测这些关键方面,目前的研究显示,1型单纯疱疹病毒遇到DDX3X核膜,它通过与病毒相互作用促进病毒核出口核出口复杂和聚氨酯gydF4y2Ba年代gydF4y2Ba3所示。自从DDX3X似乎并不需要感染细胞gydF4y2Ba25gydF4y2Ba因此,DDX3X在成熟的病毒粒子的存在残余的角色在病毒生命周期的这一步。这是最为有趣的一个发现RNA解旋酶。gydF4y2Ba
核外围,DDX3X晋升大VP5疫源地的积累在所有三个菌株进行这项研究(17gydF4y2Ba+gydF4y2BaF和KOS)。因为这些焦点没有co-localise ICP4,病毒复制的经典标志隔间gydF4y2Ba81年gydF4y2Ba,只有形成C-nuclear衣壳的存在,我们最初认为他们可能是成熟的dna中核衣壳准备退出。然而,共焦显微镜显示这些衣壳焦点部分co-localised信封gB病毒蛋白和要求NEC,暗示他们密切不是核膜或已经达到细胞核周围的空间,后者最终证实了电子显微镜。这些发现表明,DDX3X需要最优衣壳内核膜出芽。gydF4y2Ba
蛋白质组学分析发现潜在的病毒蛋白质驾驶DDX3X核膜和促进衣壳萌芽内核膜15种不同的病毒蛋白。其中聚氨酯gydF4y2BalgydF4y2Ba31日,一个组件的NEC调节1型单纯疱疹病毒核出芽。组建一个DDX3X-pUgydF4y2BalgydF4y2Ba31复杂的正交证实了互惠co-immunoprecipitation和荧光显微镜和映射到羧基DDX3X的尾巴。此外,DDX3X核招聘依赖于整个NEC机械包括溶性聚氨酯gydF4y2BalgydF4y2Ba31个蛋白质,也是聚氨酯gydF4y2BalgydF4y2Ba34岁的跨膜蛋白,对锚pU至关重要gydF4y2BalgydF4y2Ba31日核膜以及聚氨酯gydF4y2Ba年代gydF4y2Ba3影响核的病毒激酶NEC的本地化。在这一点上,我们不能排除间接绑定DDX3X聚氨酯gydF4y2BalgydF4y2Ba通过聚氨酯31,这可能发生gydF4y2BalgydF4y2Ba34。显著减少DDX3X核本地化观察没有聚氨酯gydF4y2BalgydF4y2Ba31日,而聚氨酯gydF4y2BalgydF4y2Ba34保持核捆绑,然而支持一些聚氨酯gydF4y2BalgydF4y2Ba31日暗示。聚氨酯的有趣的缺席gydF4y2BalgydF4y2Ba34在目前MS分析DDX3X伙伴,尽管它通常绑定到聚氨酯gydF4y2BalgydF4y2Ba31日,进一步印证了这一观点。相比之下,女士分析确定了聚氨酯gydF4y2BalgydF4y2Ba47岁的一种蛋白质,这种蛋白质与NEC和交互调节1型单纯疱疹病毒核出口gydF4y2Ba89年gydF4y2Ba。这将是最有趣的解决其潜在作用也NEC磷酸化DDX3X核结合的重要性。相比之下,NEC核本地化DDX3X独立,说明NEC新兵DDX3X而不是反之亦然。我们的数据还显示,DDX3X核本地化和选择性释放自相关的C -衣壳在功能上是相互依存的。我们认为DDX3X是否会使膜NEC和核衣壳,一个函数,有趣的是已经提出了pUgydF4y2BalgydF4y2Ba31日gydF4y2Ba55gydF4y2Ba,但排除了这个场景DDX3X缺席核衣壳。DDX3X,而似乎桥即将离任的衣壳NEC直接在核膜上由于与NEC的交互和多个衣壳/皮组件被作为女士DDX3X约束力的合作伙伴。随着这些很少看到瞬态病毒中间体,它们迅速达到膜结合细胞核周围的空间一次。gydF4y2Ba
一个不可预见的观察从这项研究是聚氨酯gydF4y2BalgydF4y2Ba34核定位取决于C-capsids的存在。这是违反直觉的,唯一的过度NEC在转染细胞足以驱动到核细胞膜gydF4y2Ba43gydF4y2Ba,gydF4y2Ba46gydF4y2Ba,gydF4y2Ba90年gydF4y2Ba,gydF4y2Ba91年gydF4y2Ba。然而,情况显然更复杂的感染细胞的核定位NEC由聚氨酯调制gydF4y2Ba年代gydF4y2Ba3、聚氨酯gydF4y2BalgydF4y2Ba31日,甚至在转染细胞细胞类型的依赖gydF4y2Ba43gydF4y2Ba,gydF4y2Ba45gydF4y2Ba,gydF4y2Ba59gydF4y2Ba,gydF4y2Ba92年gydF4y2Ba。此外,在转染细胞或在体外实验中使用人工膜,NEC刺激控制囊泡的形成,在感染细胞缺失gydF4y2Ba48gydF4y2Ba,gydF4y2Ba49gydF4y2Ba,gydF4y2Ba50gydF4y2Ba。随之而来,NEC通常是严格控制过程中感染。同意这种观点,它最近表明capsid-associated pUgydF4y2BalgydF4y2Ba25岁是一个重要的球员,赞成的pentamerization NEC,从而激活其膜变形的潜力gydF4y2Ba35gydF4y2Ba。班菲尔德和他的同事们也表明病毒内膜蛋白pU优雅gydF4y2BalgydF4y2Ba21抵消pU的激酶活性gydF4y2Ba年代gydF4y2Ba3通过绑定蛋白磷酸酶1,进而激活NECgydF4y2Ba60gydF4y2Ba,gydF4y2Ba62年gydF4y2Ba。他们还报道,pU皮蛋白质gydF4y2BalgydF4y2Ba16在NEC的定位有牵连gydF4y2Ba93年gydF4y2Ba。因此NEC转染细胞明显缺乏关键的控制组件。在这种情况下,它是有关聚氨酯gydF4y2BalgydF4y2Ba34本地化取决于核衣壳的存在gydF4y2Ba51gydF4y2Ba,仍然是最好的信号打开NEC崭露头角的机械。这也是符合低温电子显微镜数据显示在核膜capsid-dependent NEC招聘gydF4y2Ba51gydF4y2Ba。gydF4y2Ba
病毒出口途径的深入的分析表明,DDX3X损耗导致核形成疝细胞核周围的病毒粒子的累积,即内陷,让人想起那些见过聚氨酯gydF4y2Ba年代gydF4y2Ba3激酶死亡或缺失突变体和聚氨酯gydF4y2BalgydF4y2Ba31个突变体gydF4y2Ba42gydF4y2Ba,gydF4y2Ba45gydF4y2Ba,gydF4y2Ba58gydF4y2Ba,gydF4y2Ba59gydF4y2Ba,gydF4y2Ba60gydF4y2Ba。怎么DDX3X也影响第二步1型单纯疱疹病毒的核出口需要被显示DDX3X解决pU的最佳招聘吗gydF4y2Ba年代gydF4y2Ba3成熟的病毒粒子,通过提供证据的身体交互浓缩核细胞膜上。这与先前的报道是一致的聚氨酯gydF4y2Ba年代gydF4y2Ba3是缺席核衣壳但由NEC招募了核细胞膜和细胞核周围的病毒粒子的存在gydF4y2Ba36gydF4y2Ba,gydF4y2Ba45gydF4y2Ba,gydF4y2Ba58gydF4y2Ba。这突显出一个机制DDX3X促进聚氨酯的合并gydF4y2Ba年代gydF4y2Ba3在病毒颗粒相互作用的病毒通过内核膜味蕾,从而促进随后的聚氨酯gydF4y2Ba年代gydF4y2Ba3介导融合的细胞核周围的病毒粒子外核膜,聚氨酯gydF4y2Ba年代gydF4y2Ba3是已知的行为。这些发现强调了协调通过病毒衣壳在两核细胞膜。gydF4y2Ba
总的来说,本研究强调不可预见的角色DDX3X 1型单纯疱疹病毒核衣壳出口通过(1)与病毒核出口机器的交互;(2)通过刺激形成的大型细长C-capsids焦点在细胞核周围的空间;(3)通过刺激pUgydF4y2Ba年代gydF4y2Ba3招聘到病毒颗粒从而(4)促进病毒粒子释放的细胞核周围的空间。这些都是完全不同的从传统角色与RNA解旋酶有关,这将开辟新的研究途径和创新手段来控制病毒复制。gydF4y2Ba
方法gydF4y2Ba
细胞和病毒gydF4y2Ba
海拉(女人类宫颈;写明ATCC CCL-2)、维罗(雌性非洲绿猴肾;写明ATCC ccl - 81)和HEK293 Flp-In(女性人类肾脏;杰森年轻,麦吉尔大学)细胞在DMEM(杜尔贝科的修改鹰介质)补充了2毫米L -谷氨酰胺在5%的股份有限公司gydF4y2Ba2gydF4y2Ba和5%牛血清(BGS)的增长。17 + 1型单纯疱疹亲代野生型病毒株F和科斯(由Beate Sodeik汉诺威医学院)和血凝素(HA)标记gydF4y2BaUgydF4y2BalgydF4y2Ba31日gydF4y2Ba病毒命名vJB90 (F应变;从乔尔·贝恩斯获得;gydF4y2Ba54gydF4y2Ba)在维洛细胞种植和滴定。1型单纯疱疹病毒突变体和补充细胞系Prashant德赛的礼物(K5∆Z;科斯应变;VP5-null病毒gydF4y2Ba84年gydF4y2Ba),弗雷德Homa (vFH421;科斯应变第一50氨基酸的缺乏gydF4y2BaUgydF4y2BalgydF4y2Ba25gydF4y2Ba只生产一个——和B-nuclear衣壳gydF4y2Ba34gydF4y2Ba,gydF4y2Ba82年gydF4y2Ba,gydF4y2Ba83年gydF4y2Ba)、乔尔·贝恩斯(v3161;gydF4y2BaUgydF4y2BalgydF4y2Ba31日gydF4y2Ba空病毒gydF4y2Ba92年gydF4y2Ba)和理查德辊(vRR1072;F应变gydF4y2BaUgydF4y2BalgydF4y2Ba34gydF4y2Ba空病毒和vRR1202;gydF4y2Ba卖价gydF4y2Ba空病毒gydF4y2Ba58gydF4y2Ba)。所有病毒突变体被放大在补充细胞系和滴定相比,维洛细胞和各自的野生型病毒毒株。细胞系都定期测试和为支原体阴性。gydF4y2Ba
抗体gydF4y2Ba
抗体的几个实验室慷慨地提供了一些用于这项研究。这些包括反DDX3X兔子R648多克隆血清(1:10 0如果;1:10,000 WB和施用IP)从阿尔温德•帕特尔gydF4y2Ba77年gydF4y2Ba和anti-pUgydF4y2BalgydF4y2Ba34个鸡多克隆血清从理查德辊(如果1:50 0)gydF4y2Ba43gydF4y2Ba。乔尔·贝恩斯提供pUgydF4y2BalgydF4y2Ba31日兔多克隆(WB 1:1000)和anti-VP22鸡多克隆血清(1:10,000 WB)gydF4y2Ba43gydF4y2Ba,gydF4y2Ba94年gydF4y2Ba。吉尔艾略特提供anti-VP13/14兔多克隆血清(WB 1:5000)gydF4y2Ba95年gydF4y2Ba海伦娜布朗anti-VP16鼠标单克隆抗体(WB 1:1000)gydF4y2Ba96年gydF4y2Ba伯纳德Roizman anti-pUs3兔多克隆血清(Bernard Roizman;在世行1:4000)gydF4y2Ba97年gydF4y2Ba和Beate Sodeik Ari Helenius都给了我们一些抗兔多克隆血清1型单纯疱疹病毒衣壳(WB 1:1000)gydF4y2Ba98年gydF4y2Ba。布鲁斯·班菲尔德为我们提供了pUs3老鼠多克隆血清反应对1型单纯疱疹病毒和HSV-2 (WB 1:50 0)gydF4y2Ba99年gydF4y2Ba。商用主要抗体也使用:Anti-VP5鼠标单克隆(东海岸生物;1:1000 WB) LBR鼠标单克隆抗体(Abcam猫# ab232731;如果1:50),GAPDH鼠标单克隆抗体(微孔σ;1:10,000 WB)γ-Tubulin鼠标单克隆抗体(微孔σ;1:5000 WB) HA-tag鼠标单克隆抗体(圣克鲁斯;如果在世行和1:1000 1:10 0),鼠标单克隆ICP4 (Abcam;如果1:200和1:1000 WB)和ICP0 (Abcam;在世行1:50 0)。HRPO-Conjugated二级抗体被用于1:1000的浓度和从Bethyl购买实验室(山羊anti-Rabbit),杰克逊ImmunoResearch(山羊anti-Mouse)或Cedarlane(驴anti-Chicken)。 For immunofluorescence, Goat anti-Chicken Alexa Fluor 488, Goat anti-Rabbit Alexa Fluor 568, Chicken anti-Mouse Alexa Fluor 488 and Donkey anti-Mouse Alexa Fluor 647 were purchased from Molecular Probes and used at a 1:1000 dilution. For STED microscopy, Goat-Anti-Rabbit-IgG-Atto 647 N (Sigma-Aldrich) and Goat anti-Mouse IgG (H + L) cross-adsorbed secondary antibody, Alexa Fluor 594 (Thermo Fisher Scientific) were used at the 1:100 dilution.
代DDX3X稳定的细胞系gydF4y2Ba
HEK293细胞Flp-In, pOG44和pcDNA5 / FRT杰森博士提供的质粒是慷慨地年轻(麦吉尔大学)和用于生成细胞稳定表达GS-DDX3X (DDX3X融合蛋白G)根据热费希尔的指导方针。简单地说,pGS-DDX3X GS-DDX3X被切断从核的抵抗力gydF4y2Ba25gydF4y2Ba和克隆到pcDNA5 / FRT。HEK293细胞Flp-In然后co-transfected pcDNA5 / FRT——GS-DDX3X和pOG44(1:10比例)。稳定细胞选择使用200µg /毫升潮霉素B大约4周。这个新创建的细胞系是可用的。gydF4y2Ba
隔离和蛋白质组学DDX3X病毒约束力的合作伙伴gydF4y2Ba
HEK293 Flp-In GS-DDX3X表达细胞生长在150毫米的菜肴,mock-treated或1型单纯疱疹病毒感染野生型菌株17gydF4y2Ba+gydF4y2Ba在感染复数(MOI) 5 4 h或12 h。细胞一细胞溶解3毫升的裂解缓冲(50毫米Tris-HCl pH值8.0,150毫米氯化钠,NP-40 1%, 10%甘油)1 h在4gydF4y2BaogydF4y2Bac溶解产物包含tagged-DDX3X丰富了GS-DDX3X使用免疫球蛋白g琼脂糖6快流亲和树脂(通用电气医疗集团)。简单,3毫升的总溶解产物孵化100µL免疫球蛋白琼脂糖在一夜之间在4gydF4y2BaogydF4y2Bac .免疫球蛋白琼脂糖被离心分离的材料为800×gydF4y2BaggydF4y2Ba了2分钟,然后洗了三次裂解缓冲。洗脱的免疫球蛋白g琼脂糖是由沸腾(95°C)的100年珠µL Laemmli样品缓冲(SDS 50 mM Tris-HCl, pH值6.8,2%,0.1%溴酚蓝、10%甘油和2%β-mercaptoethanol)为5分钟。洗出液分离5 - 15%梯度sds - page凝胶和乐队通过胶体Coomassie染色显示。染色协议的灵感来自于Coomassie染色美国赛瓦公司提供的一些修改。例如,凝胶是固定的(10%乙酸和乙醇40% Milli-Q水)在室温下过夜。解我(0.2%考马斯亮蓝g - 250 (BioRad) 90%甲醇)和解决方案二(20%乙酸Milli-Q水)1:1的比例混合,用于染色的凝胶在室温下20分钟。5分钟的凝胶被迅速使退色固定缓冲区。这些凝胶与第二个解决方案是使退色(10%冰乙酸和甲醇20% Milli-Q水),直到所需的对比。最后,在Milli-Q水凝胶被洗两次。准备样品的蛋白质组学,凝胶切成三个部分:之间的免疫球蛋白重链,上面下面的免疫球蛋白g重型和轻型链和免疫球蛋白轻链。 These sections were conserved in Eppendorf tubes at −80 °C until their analysis.
凝胶部分萎缩在50%乙腈(ACN),重组与10毫米50 mM碳酸氢铵TCEP(三羟甲基氨基甲烷(2-carboxyethyl)液磷化氢盐酸盐;热费希尔科学、圣何塞,CA)和涡1 h在37°C。氯乙酰氨烷基化与执行55毫米(Sigma-Aldrich)一小时与涡流37°C。样本在37°C下消化8 h 1µg ACN的胰蛋白酶和缩氨酸随后提取使用90%。提取的多肽干下来,随着在acn 5% - 0.2%甲酸(FA)。消化肽被装载在一个自制的C4 precolumn(优化技术)和自制的反相柱分离(150μm身份证150毫米),56分钟梯度从10 FA acn 30% - 0.2%和600 nl /分钟流量EasynLC 1000(热费希尔科学、圣何塞,CA)连接到一个LTQ-Orbitrap融合(热费希尔科学、圣何塞,CA)。全光谱女士都获得了分辨率为60000,其次是串联(MS-MS)光谱采集最丰富的繁殖前体离子最多3 s。collision-induced离解(CID) 30%的碰撞能量进行了串联实验。山峰X(滑铁卢,生物信息学解决方案)和连接UniProt人类疱疹病毒数据库被用来处理数据。质量公差在前体Da 0.01 10 ppm和碎片离子的选择。 Variable selected post-translational modifications were carbamidomethyl (C), oxidation (M), deamidation (NQ), and phosphorylation (STY). The obtained data were analyzed with Scaffold 4.3.0 (protein threshold, 95%, with at least 2 peptides identified and a false-discovery rate of 0.1% for peptides). The data are available via ProteomeXchange with identifier PXD03940.
Co-immunoprecipitationsgydF4y2Ba
确认物理DDX3X和聚氨酯之间的互动gydF4y2BalgydF4y2Ba31日,海拉细胞被种植在100毫米盘子,mock-treated或HA-tagged感染gydF4y2BaUgydF4y2BalgydF4y2Ba31日gydF4y2Ba病毒(vJB90)或野生型菌株17gydF4y2Ba+gydF4y2Ba莫伊的5 12 h。细胞细胞溶解在1.5毫升里帕缓冲区(50毫米三羟甲基氨基甲烷、液pH值7.5,150毫米氯化钠,1毫米EDTA, 1% Triton x - 100)gydF4y2BaOne hundred.gydF4y2Ba在4°C 30分钟。溶菌产物都用近10×1 s脉冲强度的8 Microcup-horn超声发生器在4°C。用的溶菌产物事先批准使用鼠标pre-immune血清和50µl蛋白琼脂糖。对免疫沉淀反应HA-pUgydF4y2BalgydF4y2Ba31、新鲜50µl整除的皮尔斯anti-HA琼脂糖(热Fisher)在一夜之间被封锁在里帕缓冲区使用1% BSA在4°C。阻塞,珠子和事先批准在4°C溶解产物一起孵化3 h。珠子被离心12000×颗粒状gydF4y2BaggydF4y2Ba十年代,然后洗了三次里帕缓冲区。Bead-bound蛋白质被筛选了50µl沸腾的珠子的样品缓冲为5分钟。另外,免疫沉淀反应DDX3X,溶解产物事先批准使用一只兔子pre-immune血清(Susanne水斗友情提供)和100µL蛋白琼脂糖(微孔σ)1 h在4°C。同时,一夜之间,100µL蛋白质琼脂糖被孵化与反DDX3兔子R648多克隆血清在4°C。事先批准的溶解产物被添加到anti-DDX3 R648共轭琼脂糖珠和3 h在4°C。控制,感染的事先批准的溶解产物是孵化珠子没有主要的抗体(第一抗体(NFA))。珠子与裂解缓冲洗了三次。洗提bead-bound蛋白质,珠子煮5分钟(95°C)在100年µL Laemmli样品的缓冲区。所有样品都是通过免疫印迹分析如下详细。gydF4y2Ba
为了区分具体的手机网站,DDX3X pUs3互动,我们分次细胞细胞质、核矩阵和核细胞膜co-IP之前。为此,海拉细胞被播种在150毫米菜肴感染前24小时,然后感染17 + 5或模拟的莫伊治疗。12 hpi,细胞被resuspending细胞溶解3毫升的温和的裂解缓冲(10毫米三羟甲基氨基甲烷、液pH值7.4,150毫米氯化钠,MgCl 2毫米gydF4y2Ba2gydF4y2Ba1毫米EDTA, 1毫米Igepal DDT和0.5%)和孵化冰上10分钟,其次是涡流30年代。溶菌产物被离心机500×gydF4y2BaggydF4y2Ba5分钟分离细胞质和细胞核。一旦上层的收获,核颗粒在裂解缓冲resuspended没有任何洗涤剂(50毫米三羟甲基氨基甲烷、液pH值7.5,150毫米氯化钠,1毫米EDTA)和三个冻融循环执行打破核和释放核矩阵。这种混合然后在2500×离心机gydF4y2BaggydF4y2Ba10分钟的核膜分离矩阵。最后,颗粒(核细胞膜)在前面提到的缓冲区里帕resuspended,孵化冰上30分钟。其次是三个段落通过27½G针剪切细胞基因组。分数被免疫印迹检测纯度GAPDH和LBR。感染的分数被用于执行对DDX3X使用IP anti-DDX3X R648如上解释道。最后,总溶解产物和洗出液检查世行DDX3X pUs3和浓缩。gydF4y2Ba
聚氨酯的映射gydF4y2BalgydF4y2Ba31和重组GST-tagged DDX3X碎片gydF4y2Ba
DDX3X是632氨基酸(aa)的蛋白质。pGEX-DDX3X细菌结构表达各种DDX3X片段被慷慨地提供的阿尔温德•帕特尔博士。其中包括pGEX-4T-DDX3X aa1 - 141, pGEX-4T-DDX3X aa1 - 208, pGEX-4T-DDX3X aa1 - 282, pGEX-4T-DDX3X aa1 - 472, pGEX-6P-DDX3X aa472 - 662, pGEX-6P-DDX3X aa498 - 662和pGEX-6P-DDX3X aa623 - 662。gydF4y2Ba
BL21-CodonPlus (DE3) -RIPL细菌(安捷伦科技)表达GST-tagged DDX3X碎片前面所提到的,和相应的空pGEX-6P-1向量(由马里诺Zerial博士)是生长在40毫升Luria-Bertani(磅)37°C到ODgydF4y2Ba600年gydF4y2Ba达到0.4。片段的表达诱导使用1毫米的β-异丙酯d-1-thiogalactopyranoside (IPTG) 37°C 4 h。样本离心机在4000 xgydF4y2BaggydF4y2Ba在4°C为20分钟。细菌颗粒resuspended在细菌裂解缓冲(20毫米Tris-HCl pH值7.5,500毫米氯化钠,EDTA 1毫米,1毫米EDTA,蛋白酶抑制剂和1毫克/毫升的溶菌酶(σ))在4°C 1 h。样本随后用在Fisherbrand超声发生器和一个探测器(3 x 5 s的脉冲和5 s在8然后7 x脉冲强度的5 s和5 s在强度7)的溶解产物清除了8500 xgydF4y2BaggydF4y2Ba在4°C和孵化20分钟4°C 3 h 100µL谷胱甘肽琼脂糖4 b (Cytiva)。与此同时,海拉细胞被播种在150毫米菜(约7×10gydF4y2Ba6gydF4y2Ba细胞每GST-tagged构造),感染了31-HA病毒的莫伊5 24 h,然后在里帕缓冲细胞溶解。细胞溶解产物事先批准在销售税(绑定到谷胱甘肽琼脂糖)对3 h。事先批准的细胞溶解产物被平分秋色的谷胱甘肽琼脂糖GST-tagged构造。样本孵化3 h在4°C。最后,琼脂糖洗3次裂解缓冲和颗粒状在500 xgydF4y2BaggydF4y2Ba。释放诱饵,琼脂糖煮100年µL Laemmli样本缓冲区。所有样本被西方墨点法分析如下表示。gydF4y2Ba
西方墨点法gydF4y2Ba
为西方墨点法准备样品,我们执行BCA化验(皮尔斯BCA试验设备;热费希尔科学)或布拉德福德Bio-Rad蛋白质化验以确定蛋白质浓度。一般来说,25µg每个样本加载5 - 15% sds - page梯度凝胶。可视化的总蛋白质,0.5%的2,2,2-Trichloroethanol (TCE);σ)纳入凝胶是用光催化ChemiDoc (BioRad)使用没有污点凝胶应用程序(590/110滤波器和45 s(激活)。下转移到蛋白质是聚乙二烯二氟化物薄膜(PVDF)然后封锁了牛奶中阻断缓冲区(13.7毫米脱脂奶粉5%氯化钠,氯化钾0.27毫米,0.2毫米KHgydF4y2Ba2gydF4y2Ba阿宝gydF4y2Ba4gydF4y2Ba1毫米Na2HPOgydF4y2Ba4gydF4y2Ba,0.1%的渐变20)在室温下1 h。随后,阻塞pvdf与适当的反应主要在BSA抗体稀释阻断缓冲区(5%牛血清白蛋白在13.7毫米氯化钠,氯化钾0.27毫米,0.2毫米KHgydF4y2Ba2gydF4y2Ba阿宝gydF4y2Ba4gydF4y2Ba1毫米Na2HPOgydF4y2Ba4gydF4y2Ba一夜之间,0.1%渐变20)4gydF4y2BaogydF4y2Bac .最后,反应了pvdf HRPO-conjugated二级抗体稀释5%牛奶阻断缓冲区并使用清晰显示西方ECL衬底(Bio-Rad) Syngene凝胶文档(凝胶doc)系统。表示,图像量化使用图像软件(NIH) J。gydF4y2Ba
标准共焦荧光显微镜gydF4y2Ba
细胞被播种在圆形玻璃盖玻片(Fisherbrand)根据每个实验装置和治疗。然后他们被固定在4%多聚甲醛(PFA)磷酸盐(PBS)在室温下15分钟。下面提到的所有试剂准备基于免疫荧光(如果)协议提供的细胞信号的技术。固定样本被封锁在室温下1 h如果阻断缓冲区(正常血清1 x PBS, 5%和0.3% Triton x - 100)。一夜之后,细胞反应在4°C与适当的主要抗体稀释抗体稀释缓冲(1 x PBS、1% BSA和0.3% Triton™x - 100)。细胞被洗了三次1 x PBS,然后用适当的二次孵化抗体如果抗体稀释缓冲在室温下1 h。细胞终于洗了三次使用1 x PBS和被安装在玻璃幻灯片Dako包含0.1µg /毫升赫斯特33342年(Sigma-Aldrich)。使用LSM800成像进行了共焦显微镜(蔡司)或莱卡TCS SP8-DLS (TCS SP8激光扫描共焦显微镜与DLS光表模块)。gydF4y2Ba
受激发射损耗显微术(发生的)gydF4y2Ba
海拉细胞被种植在精密覆盖眼镜# 1.5 h厚度(ThorLabs)。各种治疗后根据具体实验协议,细胞被固定在4%的PFA在室温下15分钟。使用的缓冲区阻塞和抗体稀释是一样的标准共焦荧光显微镜所提到的,但主要抗体被用于双重浓度高于传统共焦荧光显微镜,以确保目标的有效检测。所有样本孵化主要抗体在一夜之间在4°C。、兼容二次抗体是在室温下孵化2 h。盖玻片被安装在显微镜幻灯片包含0.1µg /毫升赫斯特33342年延长玻璃不变色(热费希尔科学)。样品在室温下干燥过夜。成像是激光扫描共焦显微镜(徕卡TCS SP8)配备白光激光激发波长之间的470和670 nm和两个损耗激光在592和775海里。这些图像进一步处理在拉斯维加斯闪电模式X软件以提高分辨率。gydF4y2Ba
分析DDX3X和LBR colocalisation与伊万里瓷器软件gydF4y2Ba
海拉细胞播种在盖玻片mock-treated或野生型菌株感染17 + 5的莫伊9 h。DDX3X (Goat-Anti-Rabbit-Atto 647 N)和LBR(山羊anti-Mouse-Alexa萤石594)上面都贴上(、显微镜)和核沾染了0.1µg /毫升赫斯特33342年。Z-stack图像了徕卡TCS SP8-STED使用HC PL APO 100 x / 1.40 CS2与激光强度调整目标,以避免信号饱和。对于每一个条件,12个随机细胞成像。下面的分析都是9.8.0然后在伊万里瓷器上执行软件版本。首先,表面向导选择过程LBR信号。首先,在阈值的选择,选择背景减法< 0.1µm对象将被消除。接下来,任何信号低于50像素点被淘汰的表面。最后,LBR信号的强度的意思是设置为500,根据视觉的观察来达到最干净的表面。所有这三个参数都保持相同的图像在整个分析。 A binary mask was created on the LBR surface. The only processing step for the DDX3X channel was a background subtraction to eliminate objects <0.1 µm. To avoid any inaccuracy in the colocalisation measurement, only few middle z-stacks (based on the number of stacks which can vary between images) where a clear nuclear rim shape was observed were chosen. Finally. using the Coloc wizard in Imaris a colocalisation channel was built. In the “coloc” estimated statistics, the number represented in the % of ROI colocalised was chosen to demonstrate the percentage of DDX3X signal found on the masked signal of LBR surface.
与伊万里瓷器软件VP5表型分析gydF4y2Ba
海拉细胞播种在盖玻片转染了25 nM siDDX3X (Dharmacon猫# d - 006874 - 01 - 0002)或NC1 (IDT) 48 h如前所述gydF4y2Ba25gydF4y2Ba然后mock-treated或野生型菌株感染17gydF4y2Ba+gydF4y2Ba莫伊的5 9 h。VP5和DDX3X上面贴上(标准共焦显微镜)和核沾染了0.1µg /毫升赫斯特33342年。Z-stack照片拍摄在徕卡TCS SP8-DLS使用HC PL APO CS2 63 x / 1.40石油客观和12位深度与激光强度调整以避免信号饱和。对于每一个条件,从六到八20细胞随机选择图片。下面的分析都是9.7.2然后在伊万里瓷器上执行软件版本。首先,表面向导选择过程VP5信号。表面平滑使用高斯滤波器和背景减法选项。阈值调整,是一个小光环可以观察到在表面和触摸对象分离通过调整种子点直径。最后,任何信号低于五体素表面被淘汰。定义核,我们使用了高斯滤波器与所有其他参数保持不变。 Cell boundaries were delimited with the click-draw option. The DDX3X signal was used to draw a border around each cell. Object to object statistics were enabled to analyze the VP5 signal (signal intensity sum) and position (µg) in relation to the nuclear envelope. The VP5 % intensity sum is the ratio of each object to the total VP5 signal in the cell. These sums were then averaged over 20 cells in each of three independent experiments.
细胞外的病毒粒子和核衣壳净化gydF4y2Ba
成熟的1型单纯疱疹病毒粒子释放细胞外介质和核衣壳从海拉细胞纯化如前所述gydF4y2Ba101年gydF4y2Ba。简而言之,产生细胞外的病毒粒子,海拉细胞被感染野生型菌株17gydF4y2Ba+gydF4y2Ba现病史的莫伊5 24。细胞外介质在0.45µm过滤器过滤,然后集中在60000 xgydF4y2BaggydF4y2Ba。核衣壳,完整的核是孤立的从这些感染细胞和核衣壳释放三个周期的核冻结/解冻gydF4y2Ba29日gydF4y2Ba,gydF4y2Ba31日gydF4y2Ba,gydF4y2Ba86年gydF4y2Ba。总核衣壳是由离心浓缩35%蔗糖垫在100000 xgydF4y2BaggydF4y2Ba。gydF4y2Ba
电子显微镜gydF4y2Ba
海拉细胞播种6-well板块在11000个细胞的浓度在每口井的24小时之前治疗处理25 nM siDDX3X或NC1新控制48 h。随后,转染海拉细胞被模拟治疗或野生型菌株感染17gydF4y2Ba+gydF4y2Ba莫伊的5 9到12 h。细胞被洗两次0.1钠甲次砷酸盐缓冲(pH值7.2)然后固定1 h 4°C(2.5%戊二醛、2%多聚甲醛,0.1甲次砷酸盐缓冲,pH值7.2)。固定样本洗两次0.1甲次砷酸盐缓冲,pH值7.2,刮,颗粒状的离心3300×gydF4y2BaggydF4y2Ba。颗粒在post-fixation resuspended缓冲区(1%四氧化锇、0.1甲次砷酸盐缓冲)1 h在4°C。后来,逐渐脱水的细胞进行使用乙醇为30%,50%,70%,95%,100%。最后,使用丙烯氧化,细胞permeabilized然后嵌入在环氧树脂(环氧树脂812;dodecenyl琥珀酸酐(DDSA) nadic甲基酐(NMA) +三(二甲氨基甲基)苯酚(DMP-30))。薄片与莱卡(MZ6)准备Ultracut开普敦大学超微切片机(80 - 90纳米厚度)和成像表现菲利普斯300或飞利浦Tecnai 12透射电子显微镜。gydF4y2Ba
皮细胞外vrions内容gydF4y2Ba
海拉细胞被播种在6 245毫米平方菜前24小时感染。一旦细胞融合达到了90%,他们感染野生型菌株17gydF4y2Ba+gydF4y2Ba病毒的莫伊5 18 h。受感染的上层清液收集和拉,透过0.45 -μm醋酸纤维素过滤(配角),然后在500×离心机gydF4y2BaggydF4y2Ba5分钟在4°C。细胞外的病毒粒子的颗粒状从上层清液离心20000×gydF4y2BaggydF4y2Ba1 h在4°C。MNT的颗粒被(30毫米morpholineethanesulfonic酸,100毫米氯化钠,和20毫米Tris-HCl, pH值7.4)的新一轮20000×gydF4y2BaggydF4y2Ba1 h在4°C。洗颗粒在MNT resuspended一夜之间在4°C最大化病毒复苏。约25µg细胞外的病毒粒子,模拟和感染的总溶解产物(海拉细胞模拟治疗或野生型菌株感染17gydF4y2Ba+gydF4y2Ba病毒的莫伊5 18 h,然后细胞溶解在里帕缓冲区)被西方墨点法分析使用一个银行病毒抗体。gydF4y2Ba
统计和再现性gydF4y2Ba
在适用情况下,蛋白质丰富和荧光强度归一化的值计算控制所述图传说,分析两国在每个学生的gydF4y2BaTgydF4y2Ba测试(双尾分布和同方差的)Excel (Microsoft Office 365)。意义阈值被设定gydF4y2BaP -gydF4y2Ba值< 0.05。所有的实验都是独立进行统计分析之前的三倍。gydF4y2Ba
报告总结gydF4y2Ba
进一步研究信息设计是可用的gydF4y2Ba自然投资组合报告总结gydF4y2Ba与这篇文章有关。gydF4y2Ba
数据可用性gydF4y2Ba
原始数据作为补充提供数据gydF4y2Ba1gydF4y2Ba,而原来uncropped屁股可以在图中找到。gydF4y2BaS9gydF4y2Ba。质谱的蛋白质组学数据被存入ProteomeXchange财团通过骄傲gydF4y2Ba102年gydF4y2Ba合作伙伴库与数据集标识符PXD039403和10.6019 / PXD039403 (gydF4y2Bahttps://www.ebi.ac.uk/pride/archive/projects/PXD039403gydF4y2Ba)。gydF4y2Ba
引用gydF4y2Ba
林德,p . & Jankowsky大肠解除把死盒RNA解旋酶家族。gydF4y2BaNat。启摩尔。细胞杂志。gydF4y2Ba12gydF4y2Ba,505 - 516 (2011)。gydF4y2Ba
Kukhanova m K。,Karpenko, I. L. & Ivanov, A. V. DEAD-box RNA helicase DDX3: functional properties and development of DDX3 inhibitors as antiviral and anticancer drugs.分子gydF4y2Ba25gydF4y2Ba1015 (2020)。gydF4y2Ba
赵,l . et al .多功能DDX3:双重角色在各种癌症的发展及其相关信号通路。gydF4y2Ba点。j .癌症Res。gydF4y2Ba6gydF4y2Ba,387 - 402 (2016)。gydF4y2Ba
施罗德,M。,Baran, M. & Bowie, A. G. Viral targeting of DEAD box protein 3 reveals its role in TBK1/IKKepsilon-mediated IRF activation.EMBO J。gydF4y2Ba27gydF4y2Ba,2147 - 2157 (2008)。gydF4y2Ba
Soulat, d . et al .出局区解旋酶DDX3X TANK-binding激酶是一个关键组成部分1-dependent先天免疫反应。gydF4y2BaEMBO J。gydF4y2Ba27gydF4y2Ba,2135 - 2146 (2008)。gydF4y2Ba
顾,L。,Fullam, A., Brennan, R. & Schroder, M. Human DEAD box helicase 3 couples IkappaB kinase epsilon to interferon regulatory factor 3 activation.摩尔。细胞杂志。gydF4y2Ba33gydF4y2Ba,2004 - 2015 (2013)。gydF4y2Ba
顾,L。,Fullam, A., McCormack, N., Hohn, Y. & Schroder, M. DDX3 directly regulates TRAF3 ubiquitination and acts as a scaffold to co-ordinate assembly of signalling complexes downstream from MAVS.生物化学J。gydF4y2Ba474年gydF4y2Ba,571 - 587 (2017)。gydF4y2Ba
萨米尔,p . et al . DDX3X充当是死是活检查点在强调细胞通过调节NLRP3 inflammasome。gydF4y2Ba自然gydF4y2Ba573年gydF4y2Ba,590 - 594 (2019)。gydF4y2Ba
Yedavalli, v . S。Neuveut C。气,y . H。,Kleiman, L. & Jeang, K. T. Requirement of DDX3 DEAD box RNA helicase for HIV-1 Rev-RRE export function.细胞gydF4y2Ba119年gydF4y2Ba,381 - 392 (2004)。gydF4y2Ba
赖,m . c . et al。人类DDX3与hiv - 1蛋白质交互促进病毒信使核糖核酸的翻译。gydF4y2Ba《公共科学图书馆•综合》gydF4y2Ba8gydF4y2Bae68665 (2013)。gydF4y2Ba
Ariumi, y . et al . DDX3出局区所需的RNA解旋酶是丙型肝炎病毒RNA复制。gydF4y2Baj .性研究。gydF4y2Ba81年gydF4y2Ba,13922 - 13926 (2007)。gydF4y2Ba
李,et al。细胞DDX3调节日本脑炎病毒复制的病毒相互作用un-translated地区。gydF4y2Ba病毒学gydF4y2Ba449年gydF4y2Ba,70 - 81 (2014)。gydF4y2Ba
Brai, a . et al . DDX3X解旋酶抑制剂作为一种新的策略来对抗西尼罗河病毒感染。gydF4y2Baj .地中海化学。gydF4y2Ba62年gydF4y2Ba,2333 - 2347 (2019)。gydF4y2Ba
苏,y s . et al .刺激内部核糖体进入位点(IRES)端依赖翻译肠病毒71年DDX3X RNA解旋酶和病毒2和3 c蛋白酶。gydF4y2Ba前面MicrobiolgydF4y2Ba9gydF4y2Ba1324 (2018)。gydF4y2Ba
Vashist, S。Urena, L。,Chaudhry, Y. & Goodfellow, I. Identification of RNA-protein interaction networks involved in the norovirus life cycle.j .性研究。gydF4y2Ba86年gydF4y2Ba,11977 - 11990 (2012)。gydF4y2Ba
李,G。,Feng, T., Pan, W., Shi, X. & Dai, J. DEAD-box RNA helicase DDX3X inhibits DENV replication via regulating type one interferon pathway.生物化学Biophys。Res Commun。gydF4y2Ba456年gydF4y2Ba,327 - 332 (2015)。gydF4y2Ba
Thulasi拉曼,s . n . et al . DDX3与甲型流感病毒NS1和NP蛋白和施加压力的抗病毒功能通过调节颗粒的形成。gydF4y2Baj .性研究。gydF4y2Ba90年gydF4y2Ba,3661 - 3675 (2016)。gydF4y2Ba
王,H。,Kim, S. & Ryu, W. S. DDX3 DEAD-Box RNA helicase inhibits hepatitis B virus reverse transcription by incorporation into nucleocapsids.j .性研究。gydF4y2Ba83年gydF4y2Ba,5815 - 5824 (2009)。gydF4y2Ba
Kalverda, a . p . et al .痘病毒K7 bcl - 2蛋白采用褶皱:生化映射的互动与人类死亡盒RNA解旋酶DDX3。gydF4y2Baj·摩尔,杂志。gydF4y2Ba385年gydF4y2Ba,843 - 853 (2009)。gydF4y2Ba
Varnum, s m . et al。人类巨细胞病毒()血巨细胞病毒粒子识别的蛋白质:蛋白质组血巨细胞病毒。gydF4y2Baj .性研究。gydF4y2Ba78年gydF4y2Ba,10960 - 10966 (2004)。gydF4y2Ba
罗兰转发,S。,Guay, G. & Lippe, R. Comprehensive characterization of extracellular herpes simplex virus type 1 virions.j .性研究。gydF4y2Ba82年gydF4y2Ba,8605 - 8618 (2008)。gydF4y2Ba
克莱默,T。,Greco, T. M., Enquist, L. W. & Cristea, I. M. Proteomic characterization of pseudorabies virus extracellular virions.j .性研究。gydF4y2Ba85年gydF4y2Ba,6427 - 6441 (2011)。gydF4y2Ba
Stegen, c . et al . virion-incorporated宿主蛋白质分析所需的单纯疱疹病毒1型感染通过RNA干扰屏幕。gydF4y2Ba《公共科学图书馆•综合》gydF4y2Ba8gydF4y2Bae53276 (2013)。gydF4y2Ba
Cavignac, y . et al .细胞蛋白质Grb2和DDX3增加人类巨细胞病毒感染和前病毒的方式行动。gydF4y2Ba《公共科学图书馆•综合》gydF4y2Ba10gydF4y2Bae0131614 (2015)。gydF4y2Ba
Khadivjam, b . et al . ATP-dependent RNA解旋酶DDX3X调节单纯疱疹病毒1基因表达。gydF4y2Baj .性研究。gydF4y2Ba91年gydF4y2Bae02411-e02416 (2017)。gydF4y2Ba
惠特利,r &贝恩斯,j .单纯疱疹病毒感染的临床管理:过去,现在和未来。gydF4y2BaF1000ResgydF4y2Ba7gydF4y2BaF1000 (2018)。gydF4y2Ba
Zarrouk, K。,Piret, J. & Boivin, G. Herpesvirus DNA polymerases: structures, functions and inhibitors.病毒ResgydF4y2Ba234年gydF4y2Ba,177 - 192 (2017)。gydF4y2Ba
赫明,j . D。,Conway, J. F. & Homa, F. L. Herpesvirus capsid assembly and DNA packaging.放置阿娜特。Embryol。细胞生物。gydF4y2Ba223年gydF4y2Ba,119 - 142 (2017)。gydF4y2Ba
Remillard-Labrosse G。,Guay, G. & Lippe, R. Reconstitution of herpes simplex virus type 1 nuclear capsid egress in vitro.j .性研究。gydF4y2Ba80年gydF4y2Ba,9741 - 9753 (2006)。gydF4y2Ba
约翰逊,d . c . &贝恩斯,j . d .疱疹病毒改造主机膜病毒出口。gydF4y2BaNat。启MicrobiolgydF4y2Ba9gydF4y2Ba,382 - 394 (2011)。gydF4y2Ba
Remillard-Labrosse, g . &利珀,r .体外核出口1型单纯疱疹病毒衣壳。gydF4y2Ba方法gydF4y2Ba55gydF4y2Ba,153 - 159 (2011)。gydF4y2Ba
Klupp, b, G。,Granzow, H. & Mettenleiter, T. C. Nuclear envelope breakdown can substitute for primary envelopment-mediated nuclear egress of herpesviruses.j .性研究。gydF4y2Ba85年gydF4y2Ba,8285 - 8292 (2011)。gydF4y2Ba
杨,k &贝恩斯,j . d .选择HSV衣壳的包包括pUL31衣壳表面组件之间的交互,pUL17, pUL25。gydF4y2BaProc。《科学。美国gydF4y2Ba108年gydF4y2Ba,14276 - 14281 (2011)。gydF4y2Ba
Cockrell美国K。,Huffman, J. B., Toropova, K., Conway, J. F. & Homa, F. L. Residues of the UL25 protein of herpes simplex virus that are required for its stable interaction with capsids.j .性研究。gydF4y2Ba85年gydF4y2Ba,4875 - 4887 (2011)。gydF4y2Ba
Draganova, e . B。张,J。,Zhou, Z. H. & Heldwein, E. E. Structural basis for capsid recruitment and coat formation during HSV-1 nuclear egress.ElifegydF4y2Ba9gydF4y2Bae56627 (2020)。gydF4y2Ba
El Bilali N。,Khadivjam B。,Bonneil, E., Thibault, P. & Lippé, R. Proteomics of Herpes simplex virus type 1 nuclear capsids.j .性研究。gydF4y2Ba95年gydF4y2Ba,19 (2021)。gydF4y2Ba
Henaff D。,Radtke, K. & Lippe, R. Herpesviruses exploit several host compartments for envelopment.交通gydF4y2Ba13gydF4y2Ba,1443 - 1449 (2012)。gydF4y2Ba
利珀,r .运输intracellulaire du单纯疱疹病毒1。gydF4y2BaVirologiegydF4y2Ba24gydF4y2Ba,210 - 230 (2020)。gydF4y2Ba
常,y E。,Van Sant, C., Krug, P. W., Sears, A. E. & Roizman, B. The null mutant of the U(L)31 gene of herpes simplex virus 1: construction and phenotype in infected cells.j .性研究。gydF4y2Ba71年gydF4y2Ba,8307 - 8315 (1997)。gydF4y2Ba
辊、r . J。周,y . P。,年代chnetzer, R., Ferguson, J. & DeSalvo, D. Herpes simplex virus type 1 U(L)34 gene product is required for viral envelopment.j .性研究。gydF4y2Ba74年gydF4y2Ba,117 - 129 (2000)。gydF4y2Ba
Klupp, b, G。,Granzow, H. & Mettenleiter, T. C. Primary envelopment of pseudorabies virus at the nuclear membrane requires the UL34 gene product.j .性研究。gydF4y2Ba74年gydF4y2Ba,10063 - 10073 (2000)。gydF4y2Ba
Klupp, b, G。,Granzow, H. & Mettenleiter, T. C. Effect of the pseudorabies virus US3 protein on nuclear membrane localization of the UL34 protein and virus egress from the nucleus.j .性研究。gydF4y2Ba82年gydF4y2Ba,2363 - 2371 (2001)。gydF4y2Ba
雷诺兹,a . e . et al . U (L) 31和U (L) 34蛋白质的单纯疱疹病毒1型形成一个复杂的积累需要核边缘和包络的核衣壳。gydF4y2Baj .性研究。gydF4y2Ba75年gydF4y2Ba,8803 - 8817 (2001)。gydF4y2Ba
福克斯,W。,Klupp, b, G。,Granzow, H., Osterrieder, N. & Mettenleiter, T. C. The interacting UL31 and UL34 gene products of pseudorabies virus are involved in egress from the host-cell nucleus and represent components of primary enveloped but not mature virions.j .性研究。gydF4y2Ba76年gydF4y2Ba,364 - 378 (2002)。gydF4y2Ba
雷诺兹,a E。遗嘱,e . G。,辊、r . J。,Ryckman, B. J. & Baines, J. D. Ultrastructural localization of the herpes simplex virus type 1 UL31, UL34, and US3 proteins suggests specific roles in primary envelopment and egress of nucleocapsids.j .性研究。gydF4y2Ba76年gydF4y2Ba,8939 - 8952 (2002)。gydF4y2Ba
Simpson-Holley, M。贝恩斯,J。,Roller, R. & Knipe, D. M. Herpes simplex virus 1 U(L)31 and U(L)34 gene products promote the late maturation of viral replication compartments to the nuclear periphery.j .性研究。gydF4y2Ba78年gydF4y2Ba,5591 - 5600 (2004)。gydF4y2Ba
辊、r . J。,Bjerke, S. L., Haugo, A. C. & Hanson, S. Analysis of a charge cluster mutation of herpes simplex virus type 1 UL34 and its extragenic suppressor suggests a novel interaction between pUL34 and pUL31 that is necessary for membrane curvature around capsids.j .性研究。gydF4y2Ba84年gydF4y2Ba,3921 - 3934 (2010)。gydF4y2Ba
Klupp, b . g . et al。从核膜囊泡的形成是由coexpression两个守恒的疱疹病毒的蛋白质。gydF4y2BaProc。《科学。美国gydF4y2Ba104年gydF4y2Ba,7241 - 7246 (2007)。gydF4y2Ba
Bigalke, j . M。处,T。,Nicastro, D. & Heldwein, E. E. Membrane deformation and scission by the HSV-1 nuclear egress complex.Commun Nat。gydF4y2Ba5gydF4y2Ba4131 (2014)。gydF4y2Ba
洛伦茨,m . et al。一个疱疹病毒蛋白质可以调解在核膜囊泡的形成。gydF4y2Ba生物。化学。gydF4y2Ba290年gydF4y2Ba,6962 - 6974 (2015)。gydF4y2Ba
哈根,et al。结构内核膜囊泡形成的基础。gydF4y2Ba细胞gydF4y2Ba163年gydF4y2Ba,1692 - 1701 (2015)。gydF4y2Ba
Zeev-Ben-Mordehai, t . et al .晶体结构的疱疹病毒核出口复杂提供iInsights内核膜重建。gydF4y2Ba细胞的代表。gydF4y2Ba13gydF4y2Ba,2645 - 2652 (2015)。gydF4y2Ba
Arii, j . et al .角色interhexamer接触网站的六角晶格形成的单纯疱疹病毒1核出口复杂病毒主要包络和复制。gydF4y2Baj .性研究。gydF4y2Ba93年gydF4y2Bae00498-19 (2019)。gydF4y2Ba
杨,K。,Wills, E., Lim, H. Y., Zhou, Z. H. & Baines, J. D. Association of herpes simplex virus pUL31 with capsid vertices and components of the capsid vertex-specific complex.j .性研究。gydF4y2Ba88年gydF4y2Ba,3815 - 3825 (2014)。gydF4y2Ba
恐慌,c . et al .单纯疱疹病毒蛋白pUL31护送核衣壳的核出口,一个过程协调n端结构域。gydF4y2Ba公共科学图书馆Pathog。gydF4y2Ba11gydF4y2Bae1004957 (2015)。gydF4y2Ba
竹岛,k . et al .识别衣壳结合位点的单纯疱疹病毒1核出口复杂及其在病毒作用主要包络和复制。gydF4y2Baj .性研究。gydF4y2Ba93年gydF4y2Bae01290-19 (2019)。gydF4y2Ba
Purves, f . C。,年代pector, D. & Roizman, B. The herpes simplex virus 1 protein kinase encoded by the US3 gene mediates posttranslational modification of the phosphoprotein encoded by the UL34 gene.j .性研究。gydF4y2Ba65年gydF4y2Ba,5757 - 5764 (1991)。gydF4y2Ba
Ryckman, b . j . &辊、r . j .单纯疱疹病毒1型主要包:UL34蛋白质改性和US3-UL34催化的关系。gydF4y2Baj .性研究。gydF4y2Ba78年gydF4y2Ba,399 - 412 (2004)。gydF4y2Ba
谅解备忘录,F。,Wills, E. & Baines, J. D. Phosphorylation of the U(L)31 protein of herpes simplex virus 1 by the U(S)3-encoded kinase regulates localization of the nuclear envelopment complex and egress of nucleocapsids.j .性研究。gydF4y2Ba83年gydF4y2Ba,5181 - 5191 (2009)。gydF4y2Ba
Muradov, j . H。,Finnen, R. L., Gulak, M. A., Hay, T. J. M. & Banfield, B. W. pUL21 regulation of pUs3 kinase activity influences the nature of nuclear envelope deformation by the HSV-2 nuclear egress complex.公共科学图书馆Pathog。gydF4y2Ba17gydF4y2Bae1009679 (2021)。gydF4y2Ba
于m . k . et al .高度基本集群在单纯疱疹病毒1核出口复杂驱动膜崭露头角的诱导脂质排序。gydF4y2BamBiogydF4y2Ba12gydF4y2Bae0154821 (2021)。gydF4y2Ba
Benedyk, t·h·等人pUL21是一种病毒磷酸酶适配器,促进单纯疱疹病毒复制和传播。gydF4y2Ba公共科学图书馆Pathog。gydF4y2Ba17gydF4y2Bae1009824 (2021)。gydF4y2Ba
瓦格纳博士,f . et al . US3-encoded蛋白激酶从假狂犬病病毒的病毒粒子影响出口核。gydF4y2Baj .性研究。gydF4y2Ba76年gydF4y2Ba,1851 - 1859 (1995)。gydF4y2Ba
公园,r &贝恩斯,j . d .单纯疱疹病毒1型感染诱发蛋白激酶C的激活和招聘核膜和B增加核纤层蛋白的磷酸化。gydF4y2Baj .性研究。gydF4y2Ba80年gydF4y2Ba,494 - 504 (2006)。gydF4y2Ba
•马里奇m . et al .功能性角色TorsinA单纯疱疹病毒1核出口。gydF4y2Baj .性研究。gydF4y2Ba85年gydF4y2Ba,9667 - 9679 (2011)。gydF4y2Ba
王,y等人第9 -是一种新型病毒蛋白的目标ICP34.5单纯疱疹病毒1型和促进病毒核出口。gydF4y2Ba生物。化学。gydF4y2Ba289年gydF4y2Ba,35795 - 35805 (2014)。gydF4y2Ba
刘,z . et al .宿主细胞的作用在单纯疱疹病毒1 de-envelopment第9 -病毒核出口。gydF4y2Baj .性研究。gydF4y2Ba89年gydF4y2Ba,8982 - 8998 (2015)。gydF4y2Ba
特纳,e . M。,Brown, R. S., Laudermilch, E., Tsai, P. L. & Schlieker, C. The torsin activator LULL1 is required for efficient growth of herpes simplex virus 1.j .性研究。gydF4y2Ba89年gydF4y2Ba,8444 - 8452 (2015)。gydF4y2Ba
Hirohata, y . et al .单纯疱疹病毒1新兵CD98重链和beta1病毒de-envelopment膜整合蛋白核。gydF4y2Baj .性研究。gydF4y2Ba89年gydF4y2Ba,7799 - 7812 (2015)。gydF4y2Ba
Klupp, b . g . et al . nucleoskeleton链接器的完整性和细胞骨架需要高效的疱疹病毒核出口。gydF4y2Baj .性研究。gydF4y2Ba91年gydF4y2Bae00330 - 00317 (2017)。gydF4y2Ba
Arii, j . et al . ESCRT-III介导崭露头角的跨内核膜和调节其完整性。gydF4y2BaCommun Nat。gydF4y2Ba9gydF4y2Ba3379 (2018)。gydF4y2Ba
Demircioglu, f . e . et al . a . a . a + atp酶TorsinA聚合为中空螺旋管每转8.5的子单元。gydF4y2BaCommun Nat。gydF4y2Ba10gydF4y2Ba3262 (2019)。gydF4y2Ba
Saiz-Ros: et al .主机囊泡融合蛋白VAPB导致的核出口阶段单纯疱疹病毒1型(1型单纯疱疹病毒)复制。gydF4y2Ba细胞gydF4y2Ba8gydF4y2Ba1 - 28 (2019)。gydF4y2Ba
Maeda, f . et al .角色的孤儿运输车SLC35E1核出口的单纯疱疹病毒1。gydF4y2Baj .性研究。gydF4y2Ba96年gydF4y2Bae0030622 (2022)。gydF4y2Ba
密苏里州,j . et al . DDX3X:结构、生理功能和癌症。gydF4y2Ba摩尔。癌症gydF4y2Ba20.gydF4y2Ba38岁(2021)。gydF4y2Ba
施,j . w . et al . RNA解旋酶的关键角色DDX3及其交互作用与eIF4E / PABP1压力颗粒组装和压力反应。gydF4y2Ba生物化学J。gydF4y2Ba441年gydF4y2Ba,119 - 129 (2012)。gydF4y2Ba
安格斯,a·g·等。要求丙型肝炎病毒复制的细胞DDX3无关与病毒核心蛋白的相互作用。gydF4y2Baj .性研究。gydF4y2Ba91年gydF4y2Ba,122 - 132 (2010)。gydF4y2Ba
Owsianka a . m . Patel & a h .丙型肝炎病毒核心蛋白与人类相互作用蛋白质DDX3死框。gydF4y2Ba病毒学gydF4y2Ba257年gydF4y2Ba,330 - 340 (1999)。gydF4y2Ba
拉,c . L。杨,J。,Turner, R. J. & Edwards, R. A. Visible fluorescent detection of proteins in polyacrylamide gels without staining.肛交。物化学gydF4y2Ba326年gydF4y2Ba13-20 (2004)。gydF4y2Ba
Chopra,。,Willmore, W. G. & Biggar, K. K. Protein quantification and visualization via ultraviolet-dependent labeling with 2,2,2-trichloroethanol.科学。代表。gydF4y2Ba9gydF4y2Ba13923 (2019)。gydF4y2Ba
Knipe, d . M。,年代enechek, D., Rice, S. A. & Smith, J. L. Stages in the nuclear association of the herpes simplex virus transcriptional activator protein ICP4.j .性研究。gydF4y2Ba61年gydF4y2Ba,276 - 284 (1987)。gydF4y2Ba
Cockrell美国K。,年代一个nchez, M. E., Erazo, A. & Homa, F. L. Role of the UL25 protein in herpes simplex virus DNA encapsidation.j .性研究。gydF4y2Ba83年gydF4y2Ba47-57 (2009)。gydF4y2Ba
奥哈拉,m . et al .单纯疱疹病毒1型的突变分析UL25 DNA包装蛋白质显示区域重要的病毒DNA后包装。gydF4y2Baj .性研究。gydF4y2Ba84年gydF4y2Ba,4252 - 4263 (2010)。gydF4y2Ba
德赛,P。,DeLuca, N. A., Glorioso, J. C. & Person, S. Mutations in herpes simplex virus type 1 genes encoding VP5 and VP23 abrogate capsid formation and cleavage of replicated DNA.j .性研究。gydF4y2Ba67年gydF4y2Ba,1357 - 1364 (1993)。gydF4y2Ba
罗兰转发,s &利珀r .感染细胞的生化分析多肽(ICP) 0, ICP4, UL7 UL23整合到细胞外的单纯疱疹病毒1型病毒粒子。gydF4y2Baj .性研究。gydF4y2Ba93年gydF4y2Ba,624 - 634 (2012)。gydF4y2Ba
Henaff D。,Remillard-Labrosse G。,罗兰转发,S。&lippe, R. Analysis of the early steps of herpes simplex virus 1 capsid tegumentation.j .性研究。gydF4y2Ba87年gydF4y2Ba,4895 - 4906 (2013)。gydF4y2Ba
Padula m E。,年代ydnor, M. L. & Wilson, D. W. Isolation and preliminary characterization of herpes simplex virus 1 primary enveloped virions from the perinuclear space.j .性研究。gydF4y2Ba83年gydF4y2Ba,4757 - 4765 (2009)。gydF4y2Ba
利珀,r .破译小说host-herpesvirus病毒粒子相互作用的蛋白质组学。gydF4y2Ba前面。MicrobiolgydF4y2Ba。gydF4y2Ba3gydF4y2Ba181 (2012)。gydF4y2Ba
刘,z . et al .单纯疱疹病毒1 UL47与病毒核出口因素UL31 UL34,卖价和调节病毒核出口。gydF4y2Baj .性研究。gydF4y2Ba88年gydF4y2Ba,4657 - 4667 (2014)。gydF4y2Ba
雷诺兹,a E。,梁,L。&Baines, J. D. Conformational changes in the nuclear lamina induced by herpes simplex virus type 1 require genes U(L)31 and U(L)34.j .性研究。gydF4y2Ba78年gydF4y2Ba,5564 - 5575 (2004)。gydF4y2Ba
山内,y . et al .单纯疱疹病毒2型UL34蛋白需要UL31蛋白因其搬迁内部在转染细胞核膜。gydF4y2Baj .性研究。gydF4y2Ba82年gydF4y2Ba,1423 - 1428 (2001)。gydF4y2Ba
梁,L。,T一个naka, M., Kawaguchi, Y. & Baines, J. D. Cell lines that support replication of a novel herpes simplex virus 1 UL31 deletion mutant can properly target UL34 protein to the nuclear rim in the absence of UL31.病毒学gydF4y2Ba329年gydF4y2Ba,68 - 76 (2004)。gydF4y2Ba
高,J。,Finnen, R. L., Sherry, M. R., Le Sage, V. & Banfield, B. W. Differentiating the roles of UL16, UL21, and Us3 in the nuclear egress of herpes simplex virus capsids.j .性研究。gydF4y2Ba94年gydF4y2Bae00738-20 (2020)。gydF4y2Ba
Blaho, j . A。,Mitchell, C. & Roizman, B. An amino acid sequence shared by the herpes simplex virus 1 alpha regulatory proteins 0, 4, 22, and 27 predicts the nucleotidylylation of the UL21, UL31, UL47, and UL49 gene products.生物。化学。gydF4y2Ba269年gydF4y2Ba,17401 - 17410 (1994)。gydF4y2Ba
唐纳利,m &艾略特、g .核本地化和单纯疱疹病毒内膜蛋白VP13/14穿梭。gydF4y2Baj .性研究。gydF4y2Ba75年gydF4y2Ba,2566 - 2574 (2001)。gydF4y2Ba
麦克莱恩,c . et al .单克隆抗体三non-glycosylated抗原的单纯疱疹病毒2型。gydF4y2Baj .性研究。gydF4y2Ba63年gydF4y2Ba,297 - 305 (1982)。gydF4y2Ba
芒格,J。,Chee, A. V. & Roizman, B. The U(S)3 protein kinase blocks apoptosis induced by the d120 mutant of herpes simplex virus 1 at a premitochondrial stage.j .性研究。gydF4y2Ba75年gydF4y2Ba,5491 - 5497 (2001)。gydF4y2Ba
Ojala, p . M。,Sodeik B。,Ebersold, M. W., Kutay, U. & Helenius, A. Herpes simplex virus type 1 entry into host cells: reconstitution of capsid binding and uncoating at the nuclear pore complex in vitro.摩尔。细胞杂志。gydF4y2Ba20.gydF4y2Ba,4922 - 4931 (2000)。gydF4y2Ba
Finnen r . l . & Banfield b . w .亚细胞定位卖价alphaherpesvirus丝氨酸/苏氨酸激酶的卖价的行列式函数。gydF4y2Ba毒性gydF4y2Ba1gydF4y2Ba,291 - 294 (2010)。gydF4y2Ba
Vu,。,Poyzer, C. & Roller, R. Extragenic suppression of a mutation in herpes simplex virus 1 UL34 that affects lamina disruption and nuclear egress.j .性研究。gydF4y2Ba90年gydF4y2Ba,10738 - 10751 (2016)。gydF4y2Ba
Khadivjam B。,El Bilali N。&lippe, R. Analysis and sorting of individual HSV-1 particles by flow virometry.摩尔。生物方法。gydF4y2Ba2060年gydF4y2Ba,289 - 303 (2020)。gydF4y2Ba
Perez-Riverol y . et al ., 2022年骄傲数据库资源:中心质量spectrometry-based蛋白质组学证据。gydF4y2Ba核酸Res。gydF4y2Ba50gydF4y2BaD543-d552 (2022)。gydF4y2Ba
歌,h &霁,x RNA双识别机制和解除出局区解旋酶DDX3X。gydF4y2BaCommun Nat。gydF4y2Ba10gydF4y2Ba3085 (2019)。gydF4y2Ba
确认gydF4y2Ba
我们的许多人提供病毒,抗体和质粒(Drs。乔尔·贝恩斯,海伦娜布朗,布鲁斯·班菲尔德Prashant德赛,吉尔艾略特,Ari Helenius,弗雷德·Homa Arvind Patel伯纳德•Roizman Beate Sodeik理查德•辊和杰森年轻)。我们也要感谢黛安娜Gingras(蒙特利尔大学)和Elke Kuster-Schock(成像平台圣贾斯汀研究中心)分别与电子和荧光显微镜的宝贵帮助。最后,我们要感谢马修Gastinger (bitplane)协助荧光图像分析和迈克尔,阿尔温德•帕特尔的批判阅读手稿,所有提供的帮助后者DDX3X专长。这项研究是可能由于从加拿大卫生研究院研究基金(CIHR;拖把82921 & pjt - 178115),圣贾斯汀基金会和过去的设备资金从加拿大创新基金会(CFI)和加拿大自然科学和工程研究理事会(NSERC;rgpin - 2016 - 04277)。免疫学研究和癌症研究所(IRIC)从IRICoR接收基础设施支持,加拿大创新基金会,昏聩de说是Quebec-Sante (FRQS)。IRIC蛋白质组学工具是一个基因组学技术平台资助部分基因组加拿大和魁北克基因组。B.K.的接受者博士从圣贾斯汀基金会奖。gydF4y2Ba
作者信息gydF4y2Ba
作者和联系gydF4y2Ba
贡献gydF4y2Ba
概念化,R.L.和手段;方法,手段,E.B.看法,和R.L.; formal analysis, B.K., E.B., P.T. and R.L.; investigation, B.K. and E.B.; resources, R.L., P.T.; writing—original draft, R.L. and B.K.; writing—review and editing, B.K., E.B. P.T., and R.L.; visualization, B.K.; supervision, R.L. and P.T.; project administration, R.L., E.B., and P.T.; funding acquisition, R.L. and P.T.
相应的作者gydF4y2Ba
道德声明gydF4y2Ba
相互竞争的利益gydF4y2Ba
作者宣称没有利益冲突。gydF4y2Ba
同行评审gydF4y2Ba
同行审查的信息gydF4y2Ba
通信生物学gydF4y2Ba谢谢小君Arii和其他匿名评论者对他们的贡献的同行评审工作。主要处理编辑:小君魏油漆和Zhijuan秋。gydF4y2Ba同行审查报告gydF4y2Ba是可用的。gydF4y2Ba
额外的信息gydF4y2Ba
出版商的注意gydF4y2Ba施普林格自然保持中立在发表关于司法主权地图和所属机构。gydF4y2Ba
权利和权限gydF4y2Ba
开放获取gydF4y2Ba本文是基于知识共享署名4.0国际许可,允许使用、共享、适应、分布和繁殖在任何媒介或格式,只要你给予适当的信贷原始作者(年代)和来源,提供一个链接到Creative Commons许可,并指出如果变化。本文中的图片或其他第三方材料都包含在本文的创作共用许可,除非另有说明在一个信用额度的材料。如果材料不包括在本文的创作共用许可证和用途是不允许按法定规定或超过允许的使用,您将需要获得直接从版权所有者的许可。查看本许可证的副本,访问gydF4y2Bahttp://creativecommons.org/licenses/by/4.0/gydF4y2Ba。gydF4y2Ba
关于这篇文章gydF4y2Ba
引用这篇文章gydF4y2Ba
Khadivjam B。Bonneil E。,Thibault, P.et al。gydF4y2BaRNA解旋酶DDX3X调节单纯疱疹病毒1核出口。gydF4y2BaCommun杂志gydF4y2Ba6gydF4y2Ba134 (2023)。https://doi.org/10.1038/s42003 - 023 - 04522 - wgydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/s42003 - 023 - 04522 - wgydF4y2Ba
评论gydF4y2Ba
通过提交评论你同意遵守我们的gydF4y2Ba条款gydF4y2Ba和gydF4y2Ba社区指导原则gydF4y2Ba。如果你发现一些滥用或不符合我们的条件或准则请国旗是不合适的。gydF4y2Ba