摘要gydF4y2Ba
脱氢螺旋烯具有独特的螺旋手性,是最具吸引力的手性材料之一。然而,据我们所知,之前没有关于用不对称方法直接构建它们的报道。在本工作中,序次合成氮氧脱氢[7]螺旋烯gydF4y2Ba通过gydF4y2Ba实现了3-羟基咔唑与2-萘酚的电化学氧化异质偶联、脱水环化和分子内C-C键的形成。此外,通过手性钒催化的异构偶联和电化学氧化转化,得到了不发生外消旋化的异质脱氢[7]螺旋烯。得到的脱水[7]螺旋烯表现出强烈的蓝色圆偏振发光(|gydF4y2BaggydF4y2Ba亮度gydF4y2Ba|≈2.5 × 10gydF4y2Ba−3gydF4y2Ba在433 nm处)。异质脱氢[7]螺旋烯的外消旋势垒的热力学和动力学研究表明ΔG具有显著的手性稳定性gydF4y2Ba‡gydF4y2Ba> 140 kJ molgydF4y2Ba−1gydF4y2Ba.gydF4y2Ba
简介gydF4y2Ba
异脱氢烯,又称具有螺旋手性的准异环烯,可归为多环异芳烃(PHAs)。gydF4y2Ba1gydF4y2Ba其中螺旋烯的两个螺旋末端由sigma键连接gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba.它们独特的螺旋手性导致了非凡的手性反应gydF4y2Ba11gydF4y2Ba可以在各种基于材料的应用中实现,如有机发光二极管(oled)和场效应晶体管(fet)。此外,异脱氢helicene优异的环二色性(CD)和圆偏振发光(CPL)为光学信息存储和传输的各种应用打开了大门,在这种情况下,CPL的水平可以促进光传输信息含量的进一步维度gydF4y2Ba12gydF4y2Ba.1969年,Zander和Franke首次报道了以相应的aza[6]螺旋烯为前体,通过金属(Al)介导的末端环闭合合成的aza-脱氢[6]螺旋烯gydF4y2Ba2gydF4y2Ba.类似的方法随后被应用于合成噻吩基脱氢[5]gydF4y2Ba3.gydF4y2Ba,[6](使用Al)gydF4y2Ba4gydF4y2Ba,[7]螺旋烯(使用Pd和Sn)gydF4y2Ba5gydF4y2Ba.Tanaka和Osuka用二(三氟乙酰氧基)碘苯(PIFA)合成了含氮-脱氢[7]的三吡咯环的螺旋烯衍生物;这些分子表现出有趣的光物理性质gydF4y2Ba6gydF4y2Ba.然而,由于这些异脱氢烯的外消旋化势垒低,因此很难分离成光学纯形式gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba4gydF4y2Ba,gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba.gydF4y2Ba
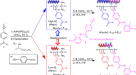
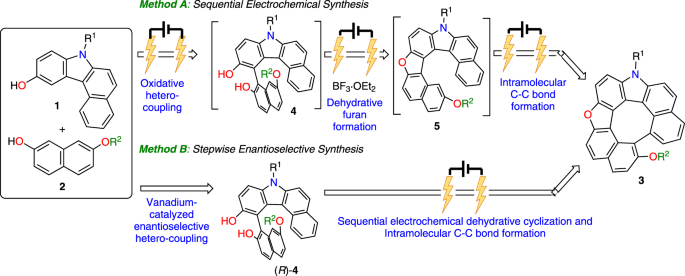
2017年,Itami和Segawa首次报道了thia-dehydro[6]螺旋烯作为鞍状螺旋分子gydF4y2Ba叔gydF4y2Ba末端芳香环上的-丁基取代阻止了外消旋;具有手性固定相的高效液相色谱法可用于对映体分离gydF4y2Ba7gydF4y2Ba.田中,OsukagydF4y2Ba8gydF4y2Ba和皮特尔科gydF4y2Ba9gydF4y2Ba也报道了异脱氢[7]螺旋烯修饰导致显著高外消旋化障碍。2021年,Maeda和Ema报道了一种具有强烈CPL和棉花效应的aza-dehydro[7]螺旋烯gydF4y2Ba10gydF4y2Ba.尽管异脱氢蒽表现出巨大的潜力,但据我们所知,目前还没有关于其直接结构的报道,包括不对称合成。这可能是由于与合成步骤相关的限制:总收率低,反应条件恶劣(如高温),容易外消旋化,和/或氧化剂的过度使用(官能基耐受范围窄)。2016年,我们报道了一种高效的钒催化合成oxa[9]螺旋烯gydF4y2Ba13gydF4y2Ba通过gydF4y2Ba烯醇类化合物的氧化偶联gydF4y2Ba14gydF4y2Ba然后是分子内脱水环化。最近,我们还利用手性钒配合物开发了芳香烃的催化对映选择性氧化异质偶联反应gydF4y2Ba15gydF4y2Ba.基于这些自由基-阴离子耦合机制,我们设想应用有机电化学方法来开发更环保的异脱氢螺旋烯的合成。电化学合成的优点是不需要氧化剂,在温和的反应条件下可以进行氧化转化gydF4y2Ba16gydF4y2Ba.事实上,许多无金属和无氧化剂的烯醇电化学氧化偶联反应已被报道gydF4y2Ba17gydF4y2Ba.此外,一些报告描述了级联电化学方法合成多环芳烃。gydF4y2Ba18gydF4y2Ba然而,据我们所知,在电化学条件下,尚无以芳香醇为起始原料合成异脱氢烯的报道。本文介绍了两种高效合成氮氧脱氢[7]螺旋烯的方法gydF4y2Ba3.gydF4y2Ba具有多个异芳环的;电化学顺序合成gydF4y2Ba3.gydF4y2Ba通过容易获得的烯醇的氧化异质偶联反应gydF4y2Ba1gydF4y2Ba而且gydF4y2Ba2gydF4y2Ba其次是脱水环化和分子内C-C键的形成,以及通过手性钒催化的异质偶联和电化学氧化转化的对映选择性方法(图。gydF4y2Ba1gydF4y2Ba).gydF4y2Ba
结果与讨论gydF4y2Ba
反应条件筛选及底物范围评价gydF4y2Ba
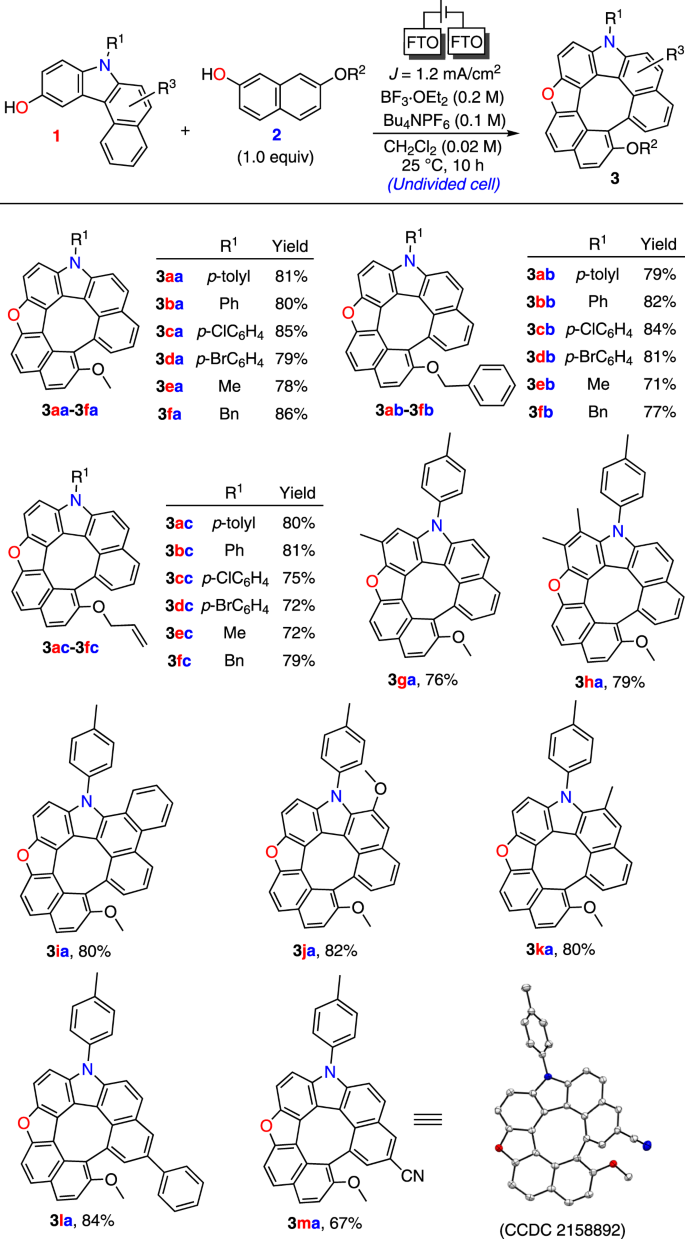
在考察了各种条件并进行了精心优化后(见表gydF4y2BaS1gydF4y2Ba- - - - - -gydF4y2BaS4gydF4y2Ba补充法gydF4y2Ba3.gydF4y2Ba),生成氮-氧-脱水[7]螺旋烯gydF4y2Ba3 aagydF4y2Ba收率为84%(孤立收率81%,电流效率= 30%);hydroxybenzo [gydF4y2BacgydF4y2Ba)咔唑gydF4y2Ba1gydF4y2Ba和7-methoxy-2-naphtholgydF4y2Ba2gydF4y2Ba被用作基于CV研究的模型底物(见图。gydF4y2BaS18gydF4y2Ba附注gydF4y2Ba6gydF4y2Ba),使用掺氟氧化锡(FTO)gydF4y2Ba19gydF4y2Ba电极和BugydF4y2Ba4gydF4y2BaNPFgydF4y2Ba6gydF4y2Ba作为电解液(0.1 M),在25°C,存在BFgydF4y2Ba3.gydF4y2Ba·诗人gydF4y2Ba2gydF4y2Ba(作为添加剂)在CHgydF4y2Ba2gydF4y2BaClgydF4y2Ba2gydF4y2Ba未观察到均偶联产物(表gydF4y2Ba1gydF4y2Ba,词条1)gydF4y2Ba20.gydF4y2Ba.的结构gydF4y2Ba3 aagydF4y2Ba经x射线晶体学证实(见补充注gydF4y2Ba7gydF4y2Ba).其他溶剂[THF, MeCN, MeOH (5 mL)]形成二醇gydF4y2Ba4节5号gydF4y2Ba作为主要副产物在9 - 22%的产量(条目2-4)。FTO电极显示底物的高转化率(条目1),而改变任何一个电极都会导致转化率降低(条目5-6)。当电流密度增加一倍时,产率降低gydF4y2Ba3 aagydF4y2Ba至65%(条目7);降低到0.8 mA/cmgydF4y2Ba2gydF4y2Ba对产率没有显著影响,但延长了反应时间(入口8)。高浓度的电解质,以及其他电解质,如LiClOgydF4y2Ba4gydF4y2Ba(0.1 M)形成二醇gydF4y2Ba4节5号gydF4y2Ba作为主要副产品(条目9-10)。减少BF量gydF4y2Ba3.gydF4y2Ba·诗人gydF4y2Ba2gydF4y2Ba或用其他Brønsted酸(作为酸性添加剂)替代,都产生低产量的氮氧脱氢[7]螺旋烯gydF4y2Ba3 aagydF4y2Ba(gydF4y2Ba4节5号gydF4y2Ba被分离出来作为5 - 20%产量的主要副产物)(条目11-13)。男朋友gydF4y2Ba3.gydF4y2Ba·诗人gydF4y2Ba2gydF4y2Ba改变二醇gydF4y2Ba4节5号gydF4y2Ba到螺旋烯中间体gydF4y2Ba5 aagydF4y2Ba,经过易阳极氧化形成gydF4y2Ba3 aagydF4y2Ba(见方案gydF4y2BaS1gydF4y2Ba附注gydF4y2Ba3.gydF4y2Ba).在没有电的情况下没有反应(条目14)。最后,为了推广这个协议,gydF4y2Ba3 aagydF4y2Ba使用ElectraSyn®2.0 (IKA设计)合成gydF4y2Ba21gydF4y2Ba;它展示了类似的结果(条目15)。gydF4y2Ba
随后,底物范围扩大到各种羟基咔唑gydF4y2Ba1gydF4y2Ba和2-naphtholsgydF4y2Ba2gydF4y2Ba在最佳反应条件下进行考察(图;gydF4y2Ba2gydF4y2Ba).gydF4y2BaNgydF4y2Ba芳基,gydF4y2BaNgydF4y2Ba-alkyl-substituted衍生品gydF4y2Ba1gydF4y2Ba- - - - - -gydF4y2Ba1gydF4y2BafgydF4y2Ba容易转化为氮氧脱氢[7]螺旋烯gydF4y2Ba3 aagydF4y2Ba- - - - - -gydF4y2Ba3 fagydF4y2Ba在78-86%的产量。不同的组合gydF4y2Ba2gydF4y2Ba有7-苄氧基或烯丙氧基gydF4y2Ba2 bgydF4y2Ba- - - - - -gydF4y2Ba2摄氏度gydF4y2Ba用来合成氮氧脱氢[7]螺旋烯gydF4y2Ba3 abgydF4y2Ba- - - - - -gydF4y2Ba3.gydF4y2Ba足球俱乐部gydF4y2Ba在71-84%的产量。一系列化合物gydF4y2Ba1gydF4y2Ba在芳香环的不同位置被Me、Ph和OMe取代,形成产物gydF4y2Ba3遗传算法gydF4y2Ba- - - - - -gydF4y2Ba3拉gydF4y2Ba在76-84%的产量。π扩大底物gydF4y2Ba1我gydF4y2Ba也有反应gydF4y2Ba2gydF4y2Ba形成gydF4y2Ba3 iagydF4y2Ba在80%的产量。HydroxycarbazolegydF4y2Ba1gydF4y2Ba米gydF4y2Ba有一个能吸电子的氰基gydF4y2Ba马3gydF4y2Ba在67%的产量。gydF4y2Ba
产品的双锅合成与转化gydF4y2Ba
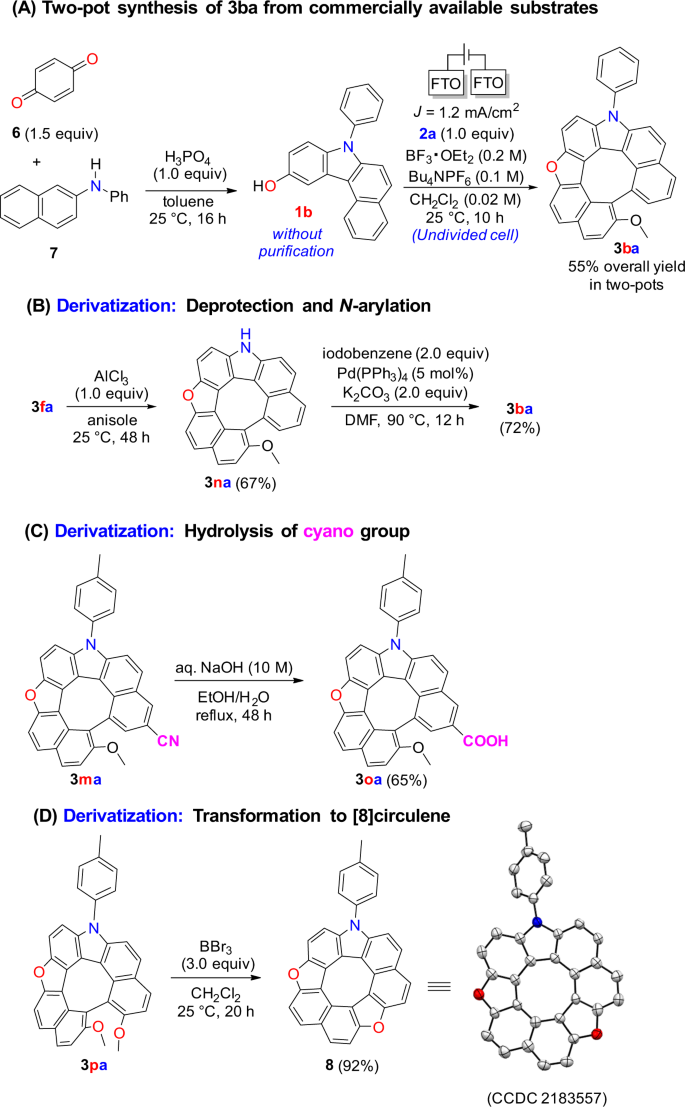
为了建立这种方法的适用性,简洁的合成,一个两锅协议使用市售底物gydF4y2BapgydF4y2Ba苯醌(gydF4y2Ba6gydF4y2Ba),gydF4y2BaNgydF4y2Ba-phenyl-2-naphthylamine (gydF4y2Ba7gydF4y2Ba)进行测试;生成氮氧脱氢[7]螺旋烯gydF4y2Ba3 bagydF4y2Ba55%的总产量(图;gydF4y2Ba3gydF4y2Ba).gydF4y2Ba
氮氧脱氢[7]螺旋烯的转化gydF4y2Ba3.gydF4y2Ba也进行了调查(见补充方法gydF4y2Ba6gydF4y2Ba).氮上的苄基gydF4y2Ba3 fagydF4y2Ba用AlClgydF4y2Ba3.gydF4y2Ba给gydF4y2Ba3 nagydF4y2Ba,经过pd催化gydF4y2BaNgydF4y2Ba-芳基化形成gydF4y2Ba3 bagydF4y2Ba(无花果。gydF4y2Ba3 bgydF4y2Ba).羧酸的导数gydF4y2Ba3办公自动化gydF4y2Ba水解后形成gydF4y2Ba马3gydF4y2Ba基本条件下(图;gydF4y2Ba3 cgydF4y2Ba).进一步,对gydF4y2Ba3 pagydF4y2Ba与BBrgydF4y2Ba3.gydF4y2Ba在25℃时得到相应的氮杂氧[8]环烯gydF4y2Ba8gydF4y2Ba92%产率(图;gydF4y2Ba3 dgydF4y2Ba).gydF4y2Ba
氮氧脱氢[7]螺旋烯的圆二色(CD)和圆偏振发光(CPL)分析gydF4y2Ba
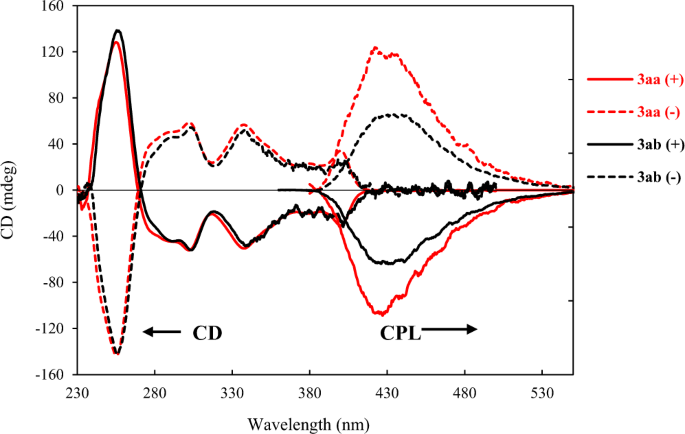
采用手性固定相(CHIRALPAK IC,己烷/gydF4y2Ba我gydF4y2Ba-PrOH=30:1),用于光学分辨率gydF4y2Ba3 aagydF4y2Ba,gydF4y2Ba3 cagydF4y2Ba而且gydF4y2Ba3 fagydF4y2Ba分析得到的aza- oxa-dehydro[7]螺旋烯的外消旋障碍,(见补充注gydF4y2Ba2gydF4y2Ba).光学纯的旋光值gydF4y2Ba3 aagydF4y2Ba第一个峰值(gydF4y2Ba米gydF4y2Ba)-gydF4y2Ba3 aagydF4y2Ba(α):gydF4y2BaDgydF4y2Ba24gydF4y2Ba= -1464 (gydF4y2BacgydF4y2Ba= 0.0175 g/mL),第二峰(gydF4y2BaPgydF4y2Ba)-gydF4y2Ba3 aagydF4y2Ba(α):gydF4y2BaDgydF4y2Ba24gydF4y2Ba= +1462 (gydF4y2BacgydF4y2Ba= 0.0173 g/mL)。(−)-的绝对配置gydF4y2Ba3 aagydF4y2Ba被确定为gydF4y2Ba米gydF4y2Ba对映体的第一个峰再结晶后,通过x射线结晶学分析gydF4y2Ba3 aagydF4y2Ba.Eyring图表明氮氧脱氢[7]螺旋烯具有明显的手性稳定性gydF4y2Ba3.gydF4y2Ba外消旋势垒>140 kJ molgydF4y2Ba−1gydF4y2Ba)(见图。gydF4y2BaS2gydF4y2Ba- - - - - -gydF4y2BaS10gydF4y2Ba附注gydF4y2Ba2gydF4y2Ba);tgydF4y2Ba1/2gydF4y2Ba复合gydF4y2Ba3 aagydF4y2Ba估计大于9.5 × 10gydF4y2Ba3.gydF4y2Ba年在25°C。Aza-oxa-dehydro[7]螺烯gydF4y2Ba3 aagydF4y2Ba表现出较高的手性稳定性,优于相应的aza-oxa[7]螺旋烯gydF4y2Ba5 aagydF4y2Ba(110 kJ molgydF4y2Ba−1gydF4y2Ba).随后,研究了光学纯氮氧脱氢[7]螺旋烯的手性。所有的螺旋染料gydF4y2Ba3.gydF4y2Ba在340 ~ 404 nm处有吸收,450 nm处荧光最大(见图)。gydF4y2BaS11gydF4y2Ba-gydF4y2Ba向gydF4y2Ba附注gydF4y2Ba4gydF4y2Ba);CD和CPLgydF4y2Ba11gydF4y2Ba在这些区域观察到信号(见图。gydF4y2BaS14系列gydF4y2Ba-gydF4y2Ba肌力gydF4y2Ba附注gydF4y2Ba5gydF4y2Ba).在合成的氮氧脱氢[7]螺旋烯中,gydF4y2Ba3 aagydF4y2Ba显示出中等量子产率Φ = 0.25, CPL活性显著gydF4y2BaggydF4y2Ba亮度gydF4y2Ba= 2.5 × 10gydF4y2Ba−3gydF4y2Ba在433 nm处(图;gydF4y2Ba4gydF4y2Ba).gydF4y2Ba
的手学特性gydF4y2Ba3 aagydF4y2Ba而且gydF4y2Ba3 abgydF4y2Ba(CD和CPL)在CHCl中进行了研究gydF4y2Ba3.gydF4y2Ba(2 × 10gydF4y2Ba−5gydF4y2Ba米)。gydF4y2Ba3 aagydF4y2Ba显示高CPL活性gydF4y2BaggydF4y2Ba亮度gydF4y2Ba= 2.5 × 10gydF4y2Ba−3gydF4y2Ba在433 nm和gydF4y2Ba3 abgydF4y2Ba显示gydF4y2BaggydF4y2Ba亮度gydF4y2Ba= 2.4 × 10gydF4y2Ba−3gydF4y2Ba在418纳米。gydF4y2Ba
异脱氢[7]螺旋烯的高效对映选择性合成gydF4y2Ba通过gydF4y2Ba手性钒配合物催化异质偶联和电化学氧化转化gydF4y2Ba
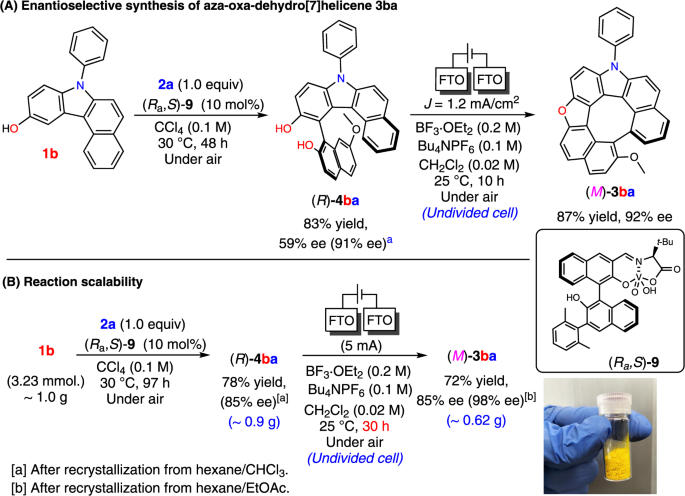
虽然有许多关于螺旋烯对映选择性合成的报道gydF4y2Ba22gydF4y2Ba,gydF4y2Ba23gydF4y2Ba,gydF4y2Ba24gydF4y2Ba,gydF4y2Ba25gydF4y2Ba,gydF4y2Ba26gydF4y2Ba据我们所知,没有关于异脱氢helicene的报道。一种有效的化学和对映选择性的方案,羟基咔唑和萘酚氧化杂偶联反应使用手性钒(v)配合物,产生轴手性联芳基衍生物,此前已报道gydF4y2Ba15gydF4y2Ba;在此基础上,对二醇进行了逐步对映选择性合成gydF4y2Ba4gydF4y2Ba进行电化学转化为相应的异脱氢helicene(见补充方法gydF4y2Ba7gydF4y2Ba).二醇(gydF4y2BaRgydF4y2Ba)-gydF4y2Ba4英航gydF4y2Ba采用单核钒配合物(gydF4y2BaRgydF4y2Ba一个gydF4y2Ba,年代gydF4y2Ba)-gydF4y2Ba9gydF4y2Ba.在电氧化条件下,(gydF4y2BaRgydF4y2Ba)-gydF4y2Ba4英航gydF4y2Ba经过连续的脱水呋喃环形成,然后两个螺旋末端耦合,得到相应的氮-氧-脱水[7]螺旋烯,(gydF4y2Ba米gydF4y2Ba)-gydF4y2Ba3 bagydF4y2Ba(见补充说明)gydF4y2Ba1gydF4y2Ba),在87%的产率下,光学纯度没有任何损失(图。gydF4y2Ba5gydF4y2Ba).值得注意的是,该协议被放大了,如图所示。gydF4y2Ba5 bgydF4y2Ba,形成0.62克(gydF4y2Ba米gydF4y2Ba)-gydF4y2Ba3 bagydF4y2Ba(电流效率= 48%)。gydF4y2Ba
综上所述,本文建立了一种在温和条件下电化学反应合成氮氧脱氢[7]螺旋烯的高效方法gydF4y2Ba3.gydF4y2Ba.本研究合成的异脱氢螺旋烯的外消旋化势垒明显高于相应的具有持续外消旋半衰期的螺旋烯。此外,本文首次报道了异脱氢helic烯的对映选择性合成,并将反应放大(达到克级)。目前正在研究其手学特性的应用。gydF4y2Ba
方法gydF4y2Ba
一般的方法gydF4y2Ba
所有反应起始材料的合成细节和分析数据gydF4y2Ba1gydF4y2Ba,参见补充方法gydF4y2Ba1gydF4y2Ba而且gydF4y2Ba2gydF4y2Ba.所有脱氢[7]螺旋烯的合成和分析细节gydF4y2Ba3.gydF4y2Ba,见补充方法gydF4y2Ba4gydF4y2Ba.脱氢[7]螺旋烯两锅法合成衍生化的一般步骤见补充方法gydF4y2Ba5gydF4y2Ba而且gydF4y2Ba6gydF4y2Ba.在补充法中重点介绍了对映选择性合成和放大的细节gydF4y2Ba7gydF4y2Ba.核磁共振谱见补充数据gydF4y2Ba1gydF4y2Ba.gydF4y2Ba
异脱氢螺旋烯序贯制备的一般步骤gydF4y2Ba
苯并溶液[gydF4y2BacgydF4y2Ba] carbazol-10-ol衍生品gydF4y2Ba1gydF4y2Ba(0.1 mmol), 2-萘酚gydF4y2Ba2gydF4y2Ba(0.1 mmol),六氟磷酸四丁基铵(V) (193.7 mg, 0.5 mmol)和BFgydF4y2Ba3.gydF4y2Ba・埃托奥gydF4y2Ba2gydF4y2Ba(0.2 MgydF4y2Ba2gydF4y2BaClgydF4y2Ba2gydF4y2Ba(5.0 mL)转入未分裂的电解池。该电池配备了两个FTO电极(1.0gydF4y2Ba×gydF4y2Ba2.5厘米gydF4y2Ba2gydF4y2Ba),连接直流电源(如图2所示)。gydF4y2BaS1gydF4y2Ba补充法gydF4y2Ba2gydF4y2Ba).在rt下,恒流电解,电流密度为1.20 mA/cmgydF4y2Ba2gydF4y2Ba是应用。搅拌10 h后,停止电解,用柱层析法(SiOgydF4y2Ba2gydF4y2Ba, EtOAc/己烷)提供所需的异氢[7]螺旋烯gydF4y2Ba3.gydF4y2Ba.gydF4y2Ba
数据可用性gydF4y2Ba
支持本手稿中描述的发现的其他数据可在gydF4y2Ba补充信息gydF4y2Ba及补充资料gydF4y2Ba1gydF4y2Ba.所有CIFs均在“补充数据”中提供gydF4y2Ba2gydF4y2Ba-gydF4y2Ba6gydF4y2Ba.本研究中报道的结构的x射线晶体学坐标已在剑桥晶体学数据中心(CCDC)沉积,沉积编号为CCDC-2091483 (gydF4y2Ba3 aagydF4y2Ba), ccdc-2128351 (gydF4y2Ba5 aagydF4y2Ba), ccdc-158892 (gydF4y2Ba马3gydF4y2Ba), ccdc-2183557 (gydF4y2Ba8gydF4y2Ba),及ccdc2057234 (gydF4y2Ba10 aagydF4y2Ba).这些数据可以从剑桥晶体学数据中心免费获得gydF4y2Ba通过gydF4y2Bawww.ccdc.cam.ac.uk data_request / cifgydF4y2Ba.作者声明,支持本研究结果的所有其他数据均可在文章中获得gydF4y2Ba补充信息gydF4y2Ba文件,也可以从相应的作者在合理的要求。gydF4y2Ba
参考文献gydF4y2Ba
Borissov, A.等人。杂环纳米石墨烯及其他多环杂芳烃化合物的研究进展。gydF4y2Ba化学。牧师。gydF4y2Ba122gydF4y2Ba, 565-788(2022)。gydF4y2Ba
Zander, M. & Franke, W. H. Über咔唑-咔唑。gydF4y2Ba化学。的误码率。gydF4y2Ba102gydF4y2Ba, 2728-2738(1969)。gydF4y2Ba
Wynberg, H., Groen, m.b. & Schadenberg, H.一些异螺旋烯的合成和分解。gydF4y2Baj . Org。化学。gydF4y2Ba36gydF4y2Ba, 2797-2809(1971)。gydF4y2Ba
杜珀,J. H.,奥德曼,D. &温伯格,H.异螺旋烯脱氢的肖勒型反应。dehydrohelicenes。gydF4y2Baj . Org。化学。gydF4y2Ba40gydF4y2Ba, 3398-3401(1975)。gydF4y2Ba
Rajca, A.等。噻吩基[7]螺旋烯分子内环化形成准[8]环烯。gydF4y2Baj . Org。化学。gydF4y2Ba74gydF4y2Ba, 9105-9111(2009)。gydF4y2Ba
陈芳,田中田,森,T. & Osuka, A.氮烯衍生物的合成、结构、光学性质及氮烯[8]环烯的意外形成。gydF4y2Ba化学。欧元。J。gydF4y2Ba24gydF4y2Ba, 7489-7497(2018)。gydF4y2Ba
Fujikawa, T., Segawa, Y. & Itami, K.具有七边子的横向π扩展双thia[6]螺旋烯:鞍状螺旋杂化分子。gydF4y2Baj . Org。化学。gydF4y2Ba82gydF4y2Ba, 7745-7749(2017)。gydF4y2Ba
陈芳,陈芳,田中平,田中平,大须贺。荧光异质[8]环烯类似物的光学性质和可溶性可调。gydF4y2Ba化学。科学。gydF4y2Ba10gydF4y2Ba, 11006-11012(2019)。gydF4y2Ba
Lousen, B.等人。将非平面芳香杂环[7]螺旋烯压缩成平面杂环[8]环烯。gydF4y2Ba化学。欧元。J。gydF4y2Ba26gydF4y2Ba, 4935-4940(2020)。gydF4y2Ba
Maeda, C., Nomoto, S., Akiyama, K., Tanaka, T. & Ema, T.通过分子内Scholl反应快速合成氮杂环烯和diaza[8]环烯。gydF4y2Ba化学。欧元。J。gydF4y2Ba27gydF4y2Ba, 15699-15705(2021)。gydF4y2Ba
对称双螺旋烯、三重螺旋烯和多重螺旋烯的手性。gydF4y2Ba化学。牧师。gydF4y2Ba121gydF4y2Ba, 2373-2412(2021)。gydF4y2Ba
彼得斯,E.等。聚合物发光二极管的圆极化电致发光。gydF4y2Baj。化学。Soc。gydF4y2Ba119gydF4y2Ba, 9909-9910(1997)。gydF4y2Ba
Sako, M.等。氧化还原/酸协同催化剂高效对映选择性合成恶蒽。gydF4y2Baj。化学。Soc。gydF4y2Ba138gydF4y2Ba, 11481-11484(2016)。gydF4y2Ba
佐科,M. Takizawa, S. & Sasai, H.手性钒配合物催化氧化偶联烯醇。gydF4y2BaTeterahedrongydF4y2Ba76gydF4y2Ba, 131645(2020)。gydF4y2Ba
Sako, M.等。手性钒配合物催化羟基咔唑的化学和对映选择性异质偶联反应。gydF4y2BaOrg。化学。前面。gydF4y2Ba8gydF4y2Ba, 4878-4885(2021)。gydF4y2Ba
程,X.等。均相催化在电化学有机合成中的最新应用。gydF4y2BaCCS化学。gydF4y2Ba4gydF4y2Ba, 1120-1152(2022)。gydF4y2Ba
Röckl, J. L., Pollok, D., Franke, F. & Waldvogel, S. R.芳基电化学脱氢C,C偶联的十年。gydF4y2BaAcc。化学。Res。gydF4y2Ba53gydF4y2Ba, 45-61(2020)。gydF4y2Ba
张磊,胡晓霞。镍催化聚合成对电解直接芳基化苄基C-H键。gydF4y2Ba化学。科学。gydF4y2Ba11gydF4y2Ba, 10786-10791(2020)。gydF4y2Ba
侯志伟,毛志勇,宋建军,徐海昌。多环化合物的电化学合成gydF4y2BaNgydF4y2Ba-二炔基级联环化异质芳烃。gydF4y2BaACS Catal。gydF4y2Ba7gydF4y2Ba, 5810-5813(2017)。gydF4y2Ba
金斯顿,C.等人。“电迷”的生存指南。gydF4y2BaAcc。化学。Res。gydF4y2Ba53gydF4y2Ba, 72-83(2020)。gydF4y2Ba
https://www.ika.com/en/Products-Lab-Eq/Electrochemistry-Kit-csp-516/ElectraSyn-20gydF4y2Ba- pro -包装- cpdt - 40003261 /gydF4y2Ba
Pelliccioli, V.等。[5]癸二烯的对映选择性合成及其合成后功能化以获得[9]癸二烯。gydF4y2BaAngew。化学。Int。艾德。gydF4y2Ba61gydF4y2Ba, e202114577(2022)。gydF4y2Ba
王强,张文文,郑春华,顾清泉,尤树林。铑催化碳氢环化合成偶氮芳烃的对映选择性。gydF4y2Baj。化学。Soc。gydF4y2Ba143gydF4y2Ba, 114-120(2020)。gydF4y2Ba
Stará, i.g. & Starý, I.螺旋手性芳烃:π-电子体系[2+2+2]环异构化合成螺旋烯。gydF4y2BaAcc。化学。ResgydF4y2Ba.gydF4y2Ba53gydF4y2Ba, 144-158(2020)。gydF4y2Ba
Yubuta, A.等。炔基芳炔与炔烃环三聚反应合成三重螺旋烯的对映选择性gydF4y2Ba通过gydF4y2Ba动态动力学分辨率。gydF4y2Baj。化学。Soc。gydF4y2Ba142gydF4y2Ba, 10025-10033(2020)。gydF4y2Ba
Dhbaibi, K., Favereau, L. & Crassous, J.含有主基元素(B, Si, N, P)的对反富集螺旋烯和螺旋烯。gydF4y2Ba化学。牧师。gydF4y2Ba119gydF4y2Ba, 8846-8953(2019)。gydF4y2Ba
确认gydF4y2Ba
在柴崎正松教授75岁生日之际,谨以此篇论文献给他。这项工作是由JSPS KAKENHI早期职业科学家(No.;日本文部科学省(MEXT)和日本科学促进会(JSPS)、JST CREST (No. JP20K15281)、变革性研究领域(A) 21A204数字化驱动的变革性有机合成(Digi-TOS)。JPMJCR20R1)、Masuyakinen基础研究基金会、Hoansha基金会。感谢大阪SANKEN综合分析中心的技术人员。大学(日本)。我们衷心感谢三浦正弘教授和中村正太郎先生对异脱氢helices的CPL分析。gydF4y2Ba
作者信息gydF4y2Ba
作者及隶属关系gydF4y2Ba
贡献gydF4y2Ba
m.i.k., m.s.h.s.:进行实验,分析数据,并撰写论文。S. M.和K. M.:设计实验。H. S.和S. T.:监督项目。gydF4y2Ba
相应的作者gydF4y2Ba
道德声明gydF4y2Ba
相互竞争的利益gydF4y2Ba
作者声明没有利益竞争。gydF4y2Ba
同行评审gydF4y2Ba
同行评审信息gydF4y2Ba
化学通讯gydF4y2Ba感谢田中孝之(Takayuki Tanaka)和其他匿名审稿人对这项工作的同行评议所做的贡献。gydF4y2Ba同行评审报告gydF4y2Ba是可用的。gydF4y2Ba
额外的信息gydF4y2Ba
出版商的注意gydF4y2Ba施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。gydF4y2Ba
权利和权限gydF4y2Ba
开放获取gydF4y2Ba本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问gydF4y2Bahttp://creativecommons.org/licenses/by/4.0/gydF4y2Ba.gydF4y2Ba
关于本文gydF4y2Ba
引用本文gydF4y2Ba
Khalid, m.i., Salem, m.s.h., Sako, m.s。gydF4y2Baet al。gydF4y2Ba异脱氢[7]螺旋烯的电化学合成。gydF4y2BaCommun化学gydF4y2Ba5gydF4y2Ba, 166(2022)。https://doi.org/10.1038/s42004-022-00780-7gydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/s42004-022-00780-7gydF4y2Ba
评论gydF4y2Ba
通过提交评论,您同意遵守我们的gydF4y2Ba条款gydF4y2Ba而且gydF4y2Ba社区指导原则gydF4y2Ba.如果您发现一些滥用或不符合我们的条款或指导方针,请标记为不适当。gydF4y2Ba