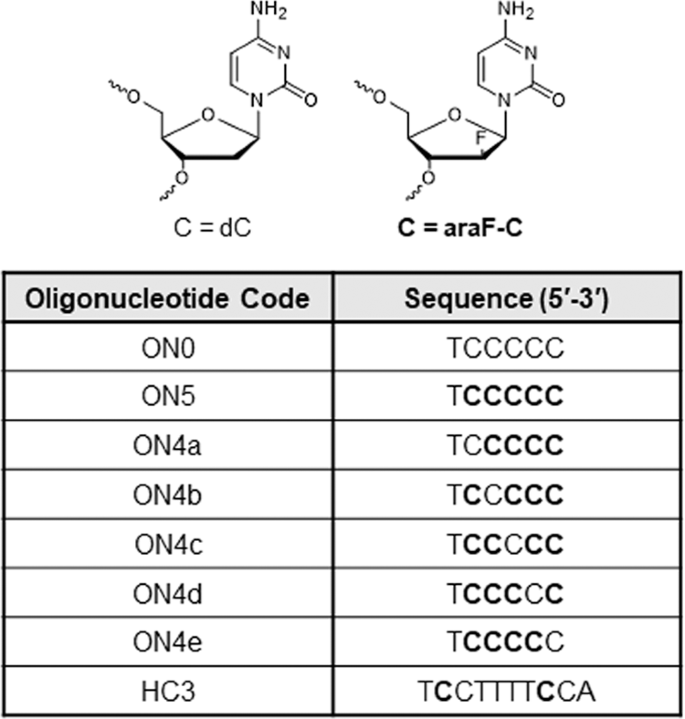
摘要
g -四重体和i-motif核酸结构被认为是通过动力学分配机制折叠的。这种机制解释了已被广泛报道的g -四元亚稳中间体的结构异质性。另一方面,i-motif折叠被认为是可预测的,对替代i-motif折叠的研究有限。在TC5通常在溶液中折叠成稳定的四聚体i-基序,我们报道了2 ' -脱氧-2 ' -氟阿拉伯半胱氨酸(阿拉法特- c)取代可提示TC5形成一种非路径的、动力学捕获的二聚i-motif,从而扩大i-motif折叠景观的范围。这个i-motif由两条链组成,头对头相连,并具有以前没有观察到的零核苷酸环。通过光谱和计算分析,我们还确定了二聚体i-motif是由氟和非氟氢键稳定的,从而解释了alac修饰的i-motif的最高稳定性。对比实验结果表明,这些相互作用的强度取决于alfa - c残基所采用的柔性糖皱褶。总的来说,这里报道的发现为i-motif在纳米技术中提供了新的作用,也提出了前所未有的i-motif折叠是否可能存在于体内的问题。
简介
动力学分配机制被认为控制着四重核酸结构的折叠。这些机制支持具有相同序列的多个共存构象的形成,但它们的热力学稳定性不同。特别是g -四重晶体,由于具有几个能量最小值的折叠景观而导致的结构多态性而臭名昭著1.另一方面,由胞嘧啶插层的两个平行双工组成的i-motif:胞嘧啶(C:C+)碱基对,似乎也通过动力学分配机制折叠2,3.,4,5,6,7,8但被认为结构上不那么异质9,10,11.除了结构未知的中间体或C:C不同的i基序构象外+堆垛顺序3.,4,5,6,7,12到目前为止,还没有其他替代i-motif折叠中间体被分离和表征。
在这里,我们报道了第一个亚稳二聚i-motif中间体的高分辨率结构,从而扩大了i-motif折叠景观的范围。这一发现是及时的,因为i-motif与疾病的相关性(调节DNA转录,原癌基因转录和端粒稳态)。13,14,15,16,17,18,19,以及它们的纳米技术应用(分子转子20.,蜂窝传感器21水凝胶成分22),它们依赖于ph值相关的折叠。
寡核苷酸d (TC5)在溶液中形成了表征良好的四聚体i-motif,这是迄今为止首次报道的i-motif结构23.研究表明,四聚体结构通过一种连续的折叠途径与逃避隔离的二聚体和三聚体中间体组装2.本文报道的非通路二聚体i-motif中间体的分离仅可能发生一次(图4)。1, ON4a-e)或全部五种(图。1, ON5) 2 ' -脱氧胞苷(dC)残基被2 ' -脱氧-2 ' -氟阿拉伯胞苷(alac)取代(图5)。1).我们之前已经证明,在i-motif形成序列中,用alac取代dC会显著减缓i-motif展开动力学24.与这些先前的发现一致,我们在这里表明,alac也可以稳定非原生结构,允许观察i-motif折叠中间体。我们还证明了,在酸性和中性pH下,alac的取代极大地提高了i-基序的热稳定性24,25,26.然而,由于缺乏基于量子力学的计算方法所需的具有足够高核磁共振分辨率的模型系统,因此无法阐明这种稳定的结构原因。因此,除了表征其折叠之外,我们还确定了内部残留的有机氟键和氢氧键有助于结构的稳定性,这种结构在溶液中可以持续数月。
结果
分离出二聚体ON5
样品制备影响了溶液中形成的alfa - c修饰的ON5物种的性质。非变性凝胶电泳显示,在较高的浓度(500 μM)下,缓慢退火(SA)(见方法)会导致低迁移率物种的形成,以前被表征为四聚体T(alfa - c)。5i-motif26和一个小种群的高流动性物种,我们在这里显示是一个非通路二聚体i-motif(图。2).有趣的是,快速(快速冷却)退火(RA)导致具有中等迁移率的带,可能对应于三聚体物种或结构较低的二聚体。当浓度低于200 μM时,SA作用下的ON5仍然形成多种物种的混合物,而RA作用下的ON5只形成高迁移率的二聚体(图2)。2).相比之下,未经修饰的TC5(ON0)无论采用何种退火方法都不能形成高迁移率的物种(补充图)1).不出所料,它在SA下形成了低迁移率的四聚体i-motif,令人惊讶的是,它在RA下形成了一个额外的中间迁移率物种,类似于高浓度ON5和RA中形成的(补充图)1).
确定二聚体ON5的结构
我们利用圆二色(CD)和核磁共振(NMR)对分离到的二聚体ON5的结构进行了表征。在不同的退火条件下,ON5的CD光谱(图2)2 b)分别在285 nm和265 nm附近显示相同的最大值和最小值,只是信号强度不同。这些光谱特征是i-motif的特征,与四聚体ON0 i-motif的特征相似(补充图)2)26.此外,RA和SA ON5都在15- 16ppm的区域显示信号1H NMR谱图2摄氏度),它们是C:C中亚诺质子的特征+碱基对。SA样品显示了多个重叠的信号,而RA样品显示了三个清晰且分散良好的信号,与单一物种的形成一致,并与非变性电泳实验的观察结果一致。类似地,RA ON5在11.3 ppm时显示一个单一的尖锐信号,这是T:T碱基对的特征,而SA ON5则显示多个。在评估二聚体RA ON5物种的稳定性时,我们发现大多数亚胺信号在pH值7.0时仍然可见(补充图3.),从而证明了由alc残基引起的稳定。
为了确定RA ON5的结构,采用了二维核磁共振波谱法。NOESY和TOCSY光谱(图。3)的研究证实了一种单一物种的存在,特别是通过观察残基T1的胸腺嘧啶的甲基质子与其芳香族质子之间的一个交叉峰,以及每个alfa - c (C2通过C6).而C:C只有三个亚氨基交叉峰+在15 - 16ppm之间观察到同碱基对。3)时,所有5个alfa - c残基的氨基质子均出现在质子化胞嘧啶特征的化学位移范围内(8.2-9.5 ppm)(补充表1),表明它们都参与了碱基配对。其他连续交叉峰的缺失和大量的糖-糖NOEs排除了平行双相形成的可能性。分配C3通过C6,我们录制了1D19F-NMR谱图3 b一系列寡核苷酸,ON4a-e(图;1),其原理是将ON5上的一个alc依次替换为一个dC残基。非变性凝胶电泳(补充图4), CD(补充图5),1H-NMR(补充图6)所有寡核苷酸的光谱表明,它们在RA作用下的构象与ON5相同。1 d19ON5的F-NMR谱在-188 ~ -202 ppm范围内显示了5个尖锐且分散的信号。3 b),分别对应五个19分子中的F个原子核。正如预期的那样,ON4a-e的光谱显示了四个信号,这意味着每个缺失的氟信号都可以被分配到被脱氧胞苷取代的ON5的alac残基上。在ON4b中,有两个19F信号在−193.10和−193.14 ppm时出现在一起,并在1H -19F-HOESY补充图7).在给每个氟信号赋值之后(补充表1),1H -19ON5的F-HOESY光谱(图;3 c)用于识别H2 '质子,通过它们的强内残馀交叉峰19F,从而便于完成,明确的赋值C3-C6残留。因此,我们确定了关键i-motif小槽NOE交叉峰(堆叠胞嘧啶之间的H1 ' -H1 '和堆叠胞嘧啶3 '边之间的互反H2 ' -H1 '),这是RA ON5按堆叠顺序折叠成二聚i-motif的决定性证据C2-C6-C3-C5-C4(从上到下)4).
二聚体ON5 i基序的结构特征
我们使用了50个与结构相关的距离限制(补充表2)来解析二聚i基序的结构。这些是从NOESY和1H -19通过对DQF-COSY的定性分析获得F-HOESY谱(见方法)和扭转角约束(补充图)8).
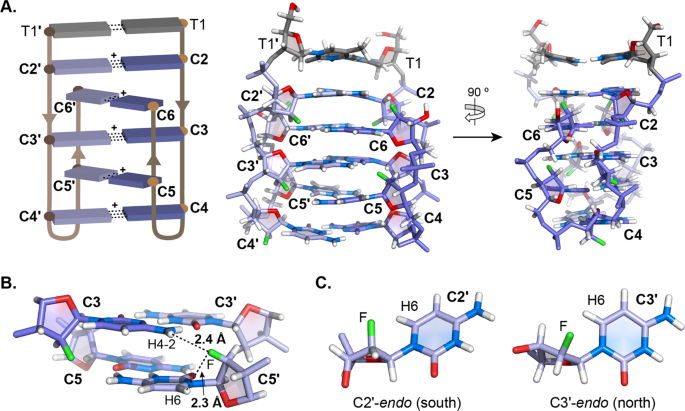
COSY谱中H2′-H1′的交叉峰强度表明C3而且C5采用北构象T1,C2而且C4一个南构象,和C6东北构象补充表3.显示了二聚体ON5 i-motif和补充表的平均伪旋转参数4显示其平均二面角和顺序参数。
二聚体i-motif由两条紧密转动的链组成,头对头相连,并由五个C:C稳定+和一个T:T链间同碱基对。在链方向的改变是通过一个前所未有的无核苷酸环在C4- p -C5步骤(图。4).有趣的是,T:T碱基对并不遵循C:C的交替插层模式+碱基对,所以结构的插层单元由五个C:C+碱基对C2:C2+而且C4:C4+成为最外部的人。重要的是,有可能检测到与氟原子相关的HOE交叉峰C3的氨基质子C5反之亦然(图;3 c).两者之间也存在同样的相关性C22 'f和C6氨基质子,但它们之间没有观察到C62 'f和C2氨基质子,可能是因为C2:C2+碱基对是最外部的,它的氨基质子与溶剂交换更快。我们还检测到所有alfa - c残基的2'F和H6芳香族质子之间存在强烈的HOE交叉峰(图1)。3 c).总的来说,这些HOE相关性的存在表明2'F原子与链间氨基质子或残留芳香族质子之间的距离很短(图2'F)。4 b).这些结果引导我们研究了2'F··H氢键的形成,我们之前假设这在alac稳定的i-motif中很重要24,25,26.
F··H键和O··H键有助于阿拉法特- c修饰的i-基序的稳定性
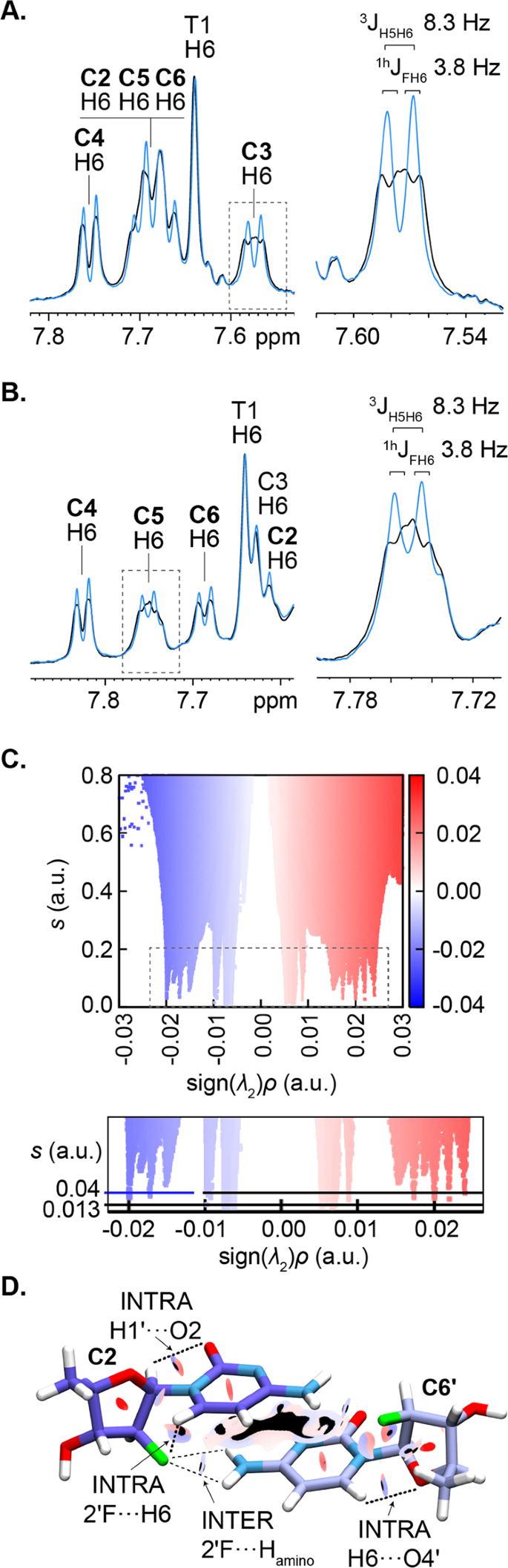
有机氟-氢键在核酸系统中的建立很少有定论,因此我们采用实验(NMR)和计算方法来确定它们在二聚体i-motif中的存在。我们发现RA ON5的所有alac芳香族质子(H6)信号都表现出明显的线宽展宽19f耦合谱(图;5).考虑到2'F和H6原子之间的长穿透键距离(5个键)(图。4 b),这种戏剧性的展宽无疑归因于这些原子之间发生的贯穿空间的标量耦合。C3特别是H6,在19F-coupled1H NMR谱和共振为双峰中的双峰,使我们能够估计的大小Jh键的耦合(≈3.8 Hz)5).
为了确定其他alac稳定的i-motif是否也具有残留的氟-氢键,我们进行了19f耦合和解耦的1SA ON4b的H-NMR(图;1;补充图9),在高浓度时只折叠成四聚体i-motif(补充图)4而且6).由于四聚体的尺寸较大,信号的线宽明显比二聚体宽。然而,在两个光谱之间检测到alac残基芳香族信号的精细结构的具体差异。同样,所有的-只有- α - c的芳香族质子信号在19启用f -耦合。结果相似(补充图9 b)得到了先前研究的HC3着丝粒序列(图。1),形成二聚体i-motif26,27.因此,我们推断残余的2'F···H6氢键有助于增强含alac的i-motif的稳定性。
接下来,我们试图了解alfa - c残基所采用的糖皱是否会影响贯穿空间的大小J常数,因此h键的强度。就像C3,C5采用北方(C3′-endo糖皱机(图。4摄氏度).然而,H6信号的C5与其他信号重叠19f耦合谱(图;5),对J常困难。这个障碍在1D中被克服1ON4b寡核苷酸的H-NMR谱图5 b),在RA上也折叠成相同的二聚体i-motif(补充图7).的H6信号C5出现孤立和分裂19的信号具有相同的3.8 Hz J耦合的f耦合频谱C3RA ON5样品中的H6。考虑到C3而且C5是唯一采用北(C3′-endo折糖机(补充图8及补充表3.),我们假设具有北构象的i-motif alac残基比具有其他构象的残基具有更高强度的残基内h键。
为了补充我们在2'F···H键上的实验发现,我们使用了NCI(非共价相互作用)计算方法,该方法可以有效地检测弱相互作用,如剩余氢键内28或者是氟受体29.NCI框架是基于对减少密度梯度(年代)穿过一个分子,它被绘制成符号(λ2)ρ,在那里ρ电子密度和λ2的第二个特征值ρ海赛。在氢键区域,标记(λ2)ρ会有较低的负值年代会接近0吗30.,31.据此,我们构建了NCI图(补充图)10- - - - - -13),共20个结构,由两个带帽胞嘧啶的模型组成(C2-C6的,C3-C5的,C6-C2的,C5-C3 ')(补充图14)从二聚体i基序的nmr约束分子动力学模拟中提取。为了将分子相互作用与NCI图中的峰值联系起来,我们为每一个双残基模型选择了一个具有代表性的结构,并报告了相对的NCI图(图2)。5度)和0.04年代分子表示中的等值面(图;5 d).此外,单残基模型的NCI图(补充图)15- - - - - -18)被用来辨别内部和内部的残差相互作用(详细的分配在补充信息).
使用NCI方法,我们检测到残留的氟-氢键涉及C2,C3,C5,C6残基及其质子化(')等价物(图。5 d),从而证实了我们基于nmr的结果,显示了alac - H6芳香信号的分裂19F耦合(图;5 a、B).在每对残基中,我们还检测到2'F与胞嘧啶H4氨基质子之间的残馀氟-氢键,以及残馀O2··H1 '和O4 '··H6氢键。检测到的氢键网络可能有助于用alfa - c修饰后i-motif的稳定。
二聚体ON5 i-motif是一个非通路动力学陷阱
我们用温控紫外光谱仪进行了热滞(TH)实验,以了解二聚体T(alac)的折叠。5I-motif,并将其与四聚体I-motif的折叠进行比较。在TH实验中,与样品的折叠和展开速率相比,温度斜坡速率较快,导致熔化和退火痕迹分别转移到较高和较低的温度。在50 μM和250 μM浓度下,对ON0和ON5样品进行了两种扫描速率,分别代表RA(5°C/min)和SA(0.5°C/min)。得到的TH廓线(图;6)表现出双相熔解曲线和明显的滞后现象,表明这两种寡核苷酸均可形成二聚体和四聚体物种,分别在低温和高温熔解转变26.
四聚体ON0 i-motif先前被提出通过连续的单体添加来折叠,通过二聚体和三聚体中间体进行折叠2.由于其折叠性质,我们假设我们分离的二聚体ON5 i-motif是一种非通路的动力学捕获中间体,是由通路上的二聚体中间体的结构重排引起的。为了验证这一假设,ON0和ON5的TH轨迹全局拟合了两种不同的组装路径(图5)。6 b(1)遵循有序的分子间组装机制;(2)允许出现非通路二聚体。二聚体光谱吸收系数假设为单体和四聚体光谱吸收系数的中间值,因为二聚体形成时原始吸光度变化幅度较小。与机制1相比,机制2所给出的RSS改善(说明了非通路二聚体的形成)使用f检验统计量计算32并且发现在某些水平上p≤10−2对于ON5,而ON0对机制2的RSS没有任何改善(补充表5).
此外,通过模拟TH实验中四聚体和二聚体i-motif的组装,我们可以提取样本中单个物种的种群信息。例如,RA ON0和ON5在低浓度(50 μM)下的等温动力学模拟表明,在4℃时,二聚体的组装程度很大(补充图)19),这与之前的实验表明ON0的四聚体组装的限速步骤是三聚体的形成相一致2.在ON0的情况下,这种二聚体中间体迅速转化为四聚体物种。相比之下,ON5通路上二聚体折叠成通路外二聚体i-motif,后者作为一个动力学陷阱,进一步减缓了四聚体物种的组装,并在低温下保持折叠数天。
讨论
我们之前已经证明,dc -to- alac取代导致i-motif在酸性和中性pH下的稳定性显著增强26.在这里,我们证明了阿拉法特- c取代也可以促进前所未有的二聚体T(阿拉法特- c)的形成。5i-motif由两条环链组成,由分子间C:C相关联+碱基对。有趣的是,连接每条链的两个反平行片段的环没有任何核苷酸,这反映了一个磷酸连接子的长度足以跨越异常狭窄的i-motif小槽。用dC取代第四个alc残基(如ON4d)降低了该序列折叠成二聚i基序的倾向(补充图)4)这表明,在3 ' -闭合转角位置存在的alac对结构的完整性很重要。据我们所知,这项研究首次报道了具有零核苷酸环的i-motifs,与其他非规范结构(如g -四环)相比,这一特征突出了i-motifs独特的折叠要求和能力。虽然尚不清楚这种循环是否可以在未经修改的i-motifs中形成,但研究人员发现1RA ON0的H NMR谱(补充图6)显示了一个小种的形成,我们假设这是与ON5相同的二聚i-motif。正在对其他富含胞嘧啶的序列进行额外的研究,以探索未经修饰的i-motif是否也可以形成零核苷酸环。
除了确定二聚体i-motif的结构外,我们还利用其核磁共振信号的质量(高色散,低重叠和高分辨率)来实验评估氟-氢键的存在。之前,我们根据取代四聚体TC的结构信息,将alfa - c诱导的i基序稳定性归因于良好的静电相互作用5i-motif26.然而,氟-氢键的潜在作用仍然是一个悬而未决的问题。有机氟作为氢键受体的能力一直存在争议,只有少数研究表明在核酸系统中形成氟-氢键。通常,F-H相互作用被认为是伪氢键,当唯一可用的实验证据包括短距离(或“接触”)和有利的角度(120-180°)时。33,34,35,36.这里,我们观察到19f诱导的H6芳香族质子信号在三种不同的i-motif上展宽,表明存在残余氢键。而通过连接2'F和芳香族质子的5个键可以发生耦合37,我们没有观察到距离2'F四个键的质子对应的信号分裂,例如C3H4”。这证实了我们的假设,即2'F和H6之间的耦合是通过空间转移的,本质上是氢键。在残留物的情况下C3而且C5ON5和ON4b为北构象,H6信号分裂,幅度为3.8 Hz(图;5 a、B).这J在g -四联体的alfa - g残基中,耦合显著高于2'F和H8之间的耦合(3.0 Hz)。38和在一个阿拉法特- n:RNA混合双工(2.7 Hz)39.类似地,J这里报道的耦合比在相同的阿拉法特- n:RNA杂化双工中阿拉法特- c (1.7 Hz)和阿拉法特- t (1.5 Hz)中相应残基的测量结果高两倍以上40.我们小组的另一项研究显示了2 ' f诱导的alaf - g H8质子在完全修饰的alaf - n双相(araF:araF)中分裂,但没有测量耦合常数41.基于芳香族信号的显著分裂C3而且C5残基中,我们假设alc的北皱有利于形成更强的残基内氟氢键。而araF核苷类则典型地向南(C2’-)endo)构象中,本文报道的二聚体i基序中alfa - c残基显示的皱折灵活性并不令人惊讶42.在alaf - n:RNA双工结构中,araF残基采用O4 ' -endo(东)皱口,它为有利的氟-氢相互作用提供了理想的几何形状,同时最大限度地减少空间应力33,43.由于这种几何结构和由此产生的相互作用,与其他杂化双工(包括DNA:RNA)相比,阿拉法特- n:RNA双工具有最高的稳定性43,44.同时,在g -四基团中采用南皱的alfa - g残基具有良好的2'F···H8距离和伪氢键的几何特征35.最后,在具有V-loop拓扑结构的g -四联体的北皱孔中也发现了alfa - g残基,从而形成了良好的2'F···H-N键45.据我们所知,本研究首次报道araF嘧啶残基方向为北,可以想象C3而且C5采用这样的几何优化二聚i-motif的稳定性。
在本研究中,我们还使用基于NCI分析的计算方法来验证我们的氟-氢键的实验证据。据我们所知,没有报道成功地协调实验和计算结果来描述核酸中的氟-氢键。最近的一项研究表明,在QTAIM-NBO(分子中原子的量子理论-自然成键轨道)水平上的计算没有提供2 ' -氟化核糖份中残留的2 ' f∙∙∙H6/8键的证据,尽管核磁共振检测到了标量耦合46.然而,这些计算分析被认为过于严格,仅限于描述强氢键,包括那些具有显著共价键的氢键28.这里使用的NCI分析(也基于QTAIM)更适合描述较弱的氟-氢键,包括分子内性质的氟-氢键28,47.与ON5的核磁共振数据一致,我们检测到残留的2'F···H6氢键。我们还发现2'F和胞嘧啶氨基质子之间的残余氟-氢键(图2'F)。4 b).与H6质子信号不同,这些氨基质子不表现出任何信号19f引起的增宽或分裂1H核磁共振谱(补充图20.).与此同时,19当alfa - g被并入g -四联体时,f诱导的剩余氨基质子分裂已经被观察到45.鉴于NCI分析是基于优化的结构,有可能检测到剩余的氟-氢键之间(图。5 d)在性质上非常弱,可能对二聚体i基序的稳定性没有显著贡献。NCI分析还揭示了非氟氢键。O2···H-C1 '键在核酸中未见报道;2'F的电负性可能使alac的H1 '具有更强的电正性,使其成为更好的氢键供体。有趣的是,NCI分析还揭示了O4 '···H6氢键;考虑到H6也在残基内与2'F形成氢键,我们假设这两种相互作用可以形成一个分叉的氢键体系48,49.总的来说,我们认为,通过灵活的折叠优化,阿拉法特- c残基所采用的几何结构有利于创建氟和非氟氢键网络,从而有助于阿拉法特修饰的i-motif无与伦比的稳定性。
除了研究alac修饰的i-motif的稳定性外,我们还利用TH分析研究了二聚体ON5 i-motif的折叠机制。一些研究表明,i-motif折叠遵循动力学分区模型4,5,6,7,8,12.这些研究大多是用单体i-motif进行的3.,4,5,7,8,12.对于四聚体TC5I-motif,折叠途径之前已经描述过通过寡核苷酸链的逐步结合2.而二聚体和三聚体的中间体已经被假定2在美国,它们从未被发现过。因此,除了C:C中的构象不同外+堆叠顺序(3e vs 5e)4,5,26在美国,从同一序列衍生出的i-motif折叠从未报道过。在这里,我们表明ON5折叠是由一个导致动力学捕获的非通路二聚体i-motif和一个更热力学稳定的四聚体i-motif的模型最好地描述的。6 b).这些结果有力地支持了i-motif折叠遵循动力学划分机制的假设。我们还证明了简单顺序折叠可以充分解释ON0折叠,但不能解释ON5折叠;当将非通路二聚体中间体引入模型时,后者明显更适合。因此,我们推断,alac修饰可以改变i-motif折叠景观,并可用于隔离原生序列中不被注意到的瞬态结构。
综上所述,我们证明了在TC中加入alac5i基序减缓了它们的折叠动力学,因此可以观察到亚稳折叠中间体。通过分离和测定二聚体T(alac)的结构5我们揭示了在原生和非原生i-motif中由alac取代引起的稳定性增强的根本原因。而i-motif因其pH敏感性而广泛应用于纳米技术20.,我们证明了i-motif分子可以通过温度变化率来调节和控制,这对于构建新型分子开关是有用的50,51,热可调水凝胶52,53,以及3D复杂度增加的DNA纳米结构54.这些i-motifs也有助于额外的链功能化(荧光团,货物…),这扩大了潜在的应用范围。最后,鉴于i-motifs最近在细胞中被检测到,而且它们的形成似乎是短暂的14这项研究的结果具体化了替代i-motif构象在体内折叠的可能性,并可能在没有阿拉法特- c取代的情况下,通过蛋白质结合或分子拥挤效应等因素促进。
方法
寡核苷酸的合成与纯化
寡核苷酸合成在ABI 3400 DNA合合器(Applied Biosystems)上以1 μmol尺度在Unylinker (Chemgenes) CPG固体载体上进行。胸苷(dT),脱氧胞苷(n -乙酰基)(dC)和脱氧腺苷(N-Bz) (dA)磷酸酰胺在0.1 M浓度的乙腈中使用,并偶联200 s。以0.1 M浓度使用alac,偶联600 s。寡核苷酸的去保护和从固体载体上的解理是用水溶液AMA(30%氢氧化铵/40%甲胺,1:1)在65℃下进行1小时。寡核苷酸序列用阴离子交换高效液相色谱法在Waters 1525仪器上纯化,使用Source 15Q树脂色谱柱(11.5 cm × 3 cm)。水缓冲体系由溶液A(25%乙腈,15 mM乙酸钠)和溶液B (0.5 M高氯酸锂,25%乙腈,15 mM乙酸钠)组成,流速为10 mL/min。梯度为0 ~ 100%高氯酸锂在60℃下50 min。在这些条件下,所需的峰在大约23分钟洗脱。使用Glen-pack脱盐柱(Glen Research)对纯化的寡核苷酸进行脱盐,并通过高分辨率LC-MS确认其质量。
退火条件下
快速或“快速冷却”退火(RA)包括将样品加热到90°C超过5分钟,然后立即将其放在冰上10分钟。
慢退火(SA)包括将样品加热到90°C超过5分钟,冷却超过3小时至室温,并将其放入冰箱过夜。
天然聚丙烯酰胺凝胶电泳(PAGE)
寡核苷酸样品使用由丙烯酰胺/双19:1(20%)、10 mM磷酸钠pH 5和1× TAE (Tris-Acetate-EDTA)组成的天然凝胶进行分析。浇注前将最终凝胶混合溶液调整到pH值5。
寡核苷酸样品(范围50-200 μM,如正文所述)在pH为5的10mm磷酸钠中退火,最终温度为5℃(通过快速冷却或缓慢退火方法)。在将它们装入凝胶之前,将它们与50%的甘油混合以获得~11.5%的最终甘油浓度。
浇注凝胶并加载样品后,以1× TAE pH 5作为运行缓冲液,在19 V/cm的温度下运行2 h,温度为7℃。凝胶结果通过紫外阴影可见。寡核苷酸对照为dT12和dT24链。用二甲苯氰醇和溴百里酚蓝染料监测电泳过程。
圆二色(CD)光谱学
CD研究在Chirascan VX光谱仪上进行,使用1毫米径长比色皿。使用仪器内的Peltier单元将温度保持在5°C(除非另有说明)。在320-220 nm范围内以100 nm/min的扫描速度记录光谱,每个光谱记录三次采集。从每个样品的光谱中减去缓冲光谱,然后使用Chirascan绘图软件中的Savitsky-Golay函数平滑样品光谱。用于CD测量的寡核苷酸溶液浓度为100 μM,在pH为5.0的10mm磷酸钠缓冲液中制备。在快速冷却或慢退火条件下进行采集。
核磁共振光谱学
用于核磁共振实验的样品溶解在含有10% D的10mm磷酸钠水缓冲液中2O.加入高浓度的HCl溶液,将样品的pH调至5。除SA ON4b和HC-3样品的寡核苷酸浓度为500 μM外,其余样品均为150 μM。所有核磁共振波谱都是在布鲁克光谱仪上获得的,操作频率为600 MHz,并配有冷冻探针1H和19F频道。使用TOPSPIN软件对核磁共振数据进行处理。一维1H-NMR是使用激发雕刻进行水抑制获得的。解耦的19一维中的F1H-NMR实验在与耦合相同的脉冲程序上进行,但在采集过程中应用180°射频脉冲。在混合时间为150和250 ms时获得NOESY光谱。NOESY和DQF-COSY实验使用激励雕刻进行水抑制,在采集过程中使用选择性脉冲19F解耦。用DIPSI-2序列记录TOCSY光谱,混合时间为80 ms。1H -19F-HOESY实验设置,检测在19F,在两个维度上解耦,混合时间为150毫秒。利用NMRFAM-Sparky软件对NOESY和HOESY交叉峰进行赋值,并对信号强度进行定量评价55.
用于结构确定的核磁共振约束
从NOESY和HOESY光谱中信号的强度得到距离约束。NOE和HOE强度分为很强、强、中等、弱或极弱,距离分别限制在3、3.5、4、4.5或5 Å。除了这些来自核磁共振谱的限制外,与碱基对中氢键相关的距离和角度的目标值被设置为由x射线晶体学确定的相关结构获得的值56.力常数设置为29 kcal/mol∙Å220 kcal/mol∙Å2分别为碱基对氢键和实验距离限制。通过定性分析DQF-COSY光谱中残基内H1 ' -H2 '(对于alac残基)和H1 ' -H2 '和H1 ' -H2 "(对于dT残基)交叉峰,得到了二面角的角约束。ν0的松散值,v1,v设置2个,将脱氧核糖和2 ' f -阿拉伯糖构象限制在南北结构域,相当于将糖伪旋转相位角北构象限制在0°到36°之间,南构象限制在144°到180°之间。残差的H6-F2′距离和C6-H6···F2′角C3而且C5分别设置为2.0 Å和高于100°。
结构测定
用CYANA 3.0程序初步计算了三种寡核苷酸结构57并使用分子动力学包AMBER 18的SANDER模块作为进一步细化的起点58.每个精细的结构被放置在一个立方水盒的中心,例如确保与任何溶质原子和盒子边缘的最小距离为8 Å。加入5个钠反离子来中和系统的总电荷。BSC1力场59并用合适的alac参数来描述寡核苷酸。采用TIP3P模型模拟水分子60.Hemiprotonated C: C+碱基对被建模为中性和质子化胞嘧啶之间的碱基对形成,其参数包括在BSC1力场中。
系统通过4000步最陡下降算法最小化,然后是16000步共轭梯度。应用100千卡/摩尔∙a的谐波势约束寡核苷酸的笛卡尔坐标−2.使用Berendsen恒温器在恒定体积下缓慢加热系统,从0到298.15 K61,并保持与最小化时相同的笛卡尔约束。因此,进行了5次20 ps的NPT平衡,在此期间对寡核苷酸原子的笛卡尔约束从100 kcal/mol∙A降低到5 kcal/mol∙A−2.最后,使用前一节中描述的NMR约束,进行了5 ns的约束分子动力学(rMD)。
在压力为1 bar、温度为298.15 K的条件下,应用Berendsen稳压和恒温算法模拟了平衡和rMD运行61.对于所有的模拟,使用了2 fs的积分步骤,并应用了SHAKE算法来约束涉及氢原子的键。采用粒子网格Ewald方法对远距离静电相互作用进行了评价62.从不同的CYANA结构开始,同样的协议应用于所有三个模拟。通过从rMD轨迹中提取10个结构,并在保持rMD模拟中使用的相同约束条件下进一步放松结构,得到最终结构。利用MOLMOL程序对典型结构进行了分析63, x3DNA64,和Pymol65.
量子力学(QM)计算
利用上述5种具有代表性的结构来评估2'F··H残馀氢键内和残馀氢键间的潜在存在。为了以可访问的计算成本做到这一点,我们为这五种结构中的每一种建立了两个模型系统:一个由阿拉法特胞嘧啶组成C2,C6,C2的,C6的(“'”表示含有质子化的阿拉法特-c链)和另一条包含阿拉法特-胞嘧啶C3,C5,C3 ',C5的.PO42 -4个核苷酸中3 '和5 '位置的磷酸基被移除了,糖3 '端被羟基覆盖,而5 '端被氢原子覆盖(补充图)14).C2-C2的,C6-C6的而且C3-C3 ',C5-C5的碱基对氢键,以及碱基叠加相互作用,有助于两个模型系统的稳定性。
T1和T1 '由于缺乏氟和氨基,不能形成2'F···H氢键内和间残馀,故不在QM计算范围内。C4而且C4的也排除了氟原子的位置,排除了任何残余的2'F··H氢键的形成。
所有模型系统均采用高斯16 Rev. B.01电子结构软件进行优化66.为此,M06-2X67函数和6-31 G(d)基集应用。在优化过程中,O3 '和C5 '原子的位置保持冻结状态。利用优化后的结构进行了非共价相互作用(NCI)分析,并检测了残留的2'F···H氢键内和间。NCI方法是一种源于“分子中的原子”(AIM)理论的方法,该理论根据分子的拓扑特征定义化学键ρ68.NCI分析评估的数量为年代,在那里
的数量年代将假设较大的值,密度尾巴远离原子核,在哪里ρ呈指数下降。另一方面,它将假设原子核附近的小值(大密度和接近于零的梯度)。最后,年代将在AIM临界点(CPs)消失,在哪里∇ρ= 0,但也在所谓的“非aim - cps”,其中∇ρ≈031.如果两个原子的密度重叠,例如,在共价键存在的情况下,总密度将呈现典型的AIM-CP。另一方面,如果密度在指数衰减渐近的区域重叠,则总密度可能具有非aim - cp特征,表明NCIs的存在31.
从先前优化的结构中提取了含有以下胞嘧啶的残基对:C2-C6的,C3-C5的,C6-C2的而且C5-C3 '.对于每一个,使用M06-2X泛函和6-311 + G(d)基集评估电子波函数。NCI图,报告密度梯度减小(年代)作为符号(λ2)*ρ(λ2的第二个特征值是ρ),用NCIPLOT4计算69.注意,符号(λ2)对吸引性相互作用是消极的,对排斥性相互作用是积极的。乘ρ通过符号(λ2)在氢键存在的情况下特别有用(符号(λ2) < 0),否则可能与排斥空间冲突重叠(符号(λ2) > 0)如果绘图年代只是作为的函数ρ.ρ接近零的值是典型的弱色散相互作用,而氢键通常以较大的值为特征47.
TH剖面的紫外-可见光谱及整体分析
在Cary 100紫外-可见分光光度计和Peltier温控仪上进行了紫外热变性实验。样品在10 mM磷酸钠缓冲液(pH为5)中以50或250 μM浓度制备,在265 nm和1 mM径长比色皿中进行采集。在5到85°C之间,以两种扫描速率获得吸光度值:0.5°C/min和5.0°C/min。吸光度的总变化取决于所应用的扫描速率,我们假设这是由于二聚体物种与四聚体物种具有不同的吸收系数,为了进行分析,我们假设二聚体的吸收系数等于四聚体物种的一半,而三聚体的吸收系数等于四聚体物种的四分之三。对于i-motif折叠路径的不同模型,TH剖面具有全局拟合性。所作的数学关系和假设在补充信息.从TH迹得到的动力学和热力学参数见补充表5.
报告总结
有关研究设计的进一步资料,请参阅自然组合报告摘要链接到这篇文章。
数据可用性
报道的核酸结构的原子坐标和结构因子已存入蛋白质数据库,登录号为7ZYX。
参考文献
Grün, J. T. & Schwalbe, H.多态g -四重结构的折叠动力学。生物聚合物113, e23477(2022)。
勒罗伊,J.-L。i基序四聚体的形成途径。核酸测定。37, 4127-4134(2009)。
Khamari, L. & Mukherjee, S.通过单分子förster共振能量转移破译c-MYC启动子基插层基序DNA折叠途径的纳米约束效应。期刊。化学。列托人。13, 8169-8176(2022)。
Lieblein, a.l., Buck, J., Schlepckow, K, Fürtig, B. & Schwalbe, H. DNA i-motif折叠的时间分辨NMR光谱研究揭示了动力学分区。Angew。化学。Int。艾德。51, 250-253(2012)。
Lieblein, a.l, Fürtig, B. & Schwalbe, H.优化DNA i-motif折叠的动力学和热力学。ChemBioChem14, 1226-1230(2013)。
曹毅,等。用电喷雾电离质谱监测序列d(XnC4Ym)的链间i基序的形成和解离。j。Soc。质量。范围。26, 994-1003(2015)。
Garabedian, A.等人。动力学捕获i-motif DNA中间产物的结构。理论物理。化学。化学。理论物理。18, 26691-26702(2016)。
达卡尔,S.等。在单分子水平上揭示了ILPR i基序和具有相当机械稳定性的部分折叠结构的共存。j。化学。Soc。132, 8991-8997(2010)。
Abou Assi, H., Garavís, M., González, C. & Damha, M. J. i-Motif DNA:结构特征和细胞生物学的意义。核酸测定。46, 8038-8056(2018)。
Benabou, S., Aviñó, A., Eritja, R., González, C. & Gargallo, R.核酸i-motif结构的基本方面。RSC睡觉。4, 26956-26980(2014)。
Day, H. A., Pavlou, P. & Waller, Z. A. E. i-Motif DNA:结构、稳定性和配体靶向。Biorg。地中海,化学。22, 4407-4418(2014)。
穆斯塔法等人。i-motif稳定性的单分子研究,折叠中间体,以及作为原位pH传感器的潜力。前面。摩尔。Biosci。9, 977113(2022)。
Dzatko, S.等。活哺乳动物细胞核中DNA i-motif稳定性的评价。Angew。化学。Int。艾德。57, 2165-2169(2018)。
泽拉提,M.等人。I-motif DNA结构是在人类细胞核中形成的。Nat,化学。10, 631-637(2018)。
金,J. J.等。在人类细胞中,DNA g -四重体和i-基序结构的形成是相互依赖的。j。化学。Soc。142, 20600-20604(2020)。
Kang周宏儒。,Kendrick, S., Hecht, S. M. & Hurley, L. H. The transcriptional complex between the BCL2 i-motif and hnRNP LL is a molecular switch for control of gene expression that can be modulated by small molecules.j。化学。Soc。136, 4172-4185(2014)。
高桥,S., Brazier, J. A. &杉本,N.非规范DNA结构对DNA聚合酶Klenow片段的拓扑影响。国家科学院学报美国114, 9605-9610(2017)。
陈,Y.等。深入了解羧化单壁碳纳米管对端粒酶和端粒的生物医学效应。Commun Nat。3., 1074(2012)。
Kendrick, S.等。BCL2启动子i-motif的动态特性提供了一种通过选择性结合到替代DNA发夹结构的化合物调节基因表达的机制。j。化学。Soc。136, 4161-4171(2014)。
董勇,杨志强,刘东。基于i-Motif结构的DNA纳米技术。Acc。化学。Res。47, 1853-1860(2014)。
莫迪等人。一种DNA纳米机器,可以绘制活细胞内的时空pH值变化。Nanotechnol Nat。4, 325-330(2009)。
Cheng, E.等。ph触发,快速反应的DNA水凝胶。Angew。化学。Int。艾德。48, 7660-7663(2009)。
葛林,K.,勒罗伊,j - l。& Guéron, M.具有质子化胞嘧啶-胞嘧啶碱基对的四聚体DNA结构。自然363, 561-565(1993)。
Abou Assi, H., El-Khoury, R, González, C. & Damha, M. J. 2 ' -氟阿拉伯核酸修饰捕获人类端粒DNA中的g -四重体和i-motif结构。核酸测定。45, 11535-11546(2017)。
Abou Assi, H., Lin, Y. C., Serrano, I., González, C. & Damha, M. J.探究DNA甲基化和2 ' -β-氟化对I -motif稳定性的协同作用。化学。欧元。J。24, 471-477(2018)。
Assi, H. A.等。DNA 2 ' -β-氟化稳定i-motif结构。核酸测定。44, 4998-5009(2016)。
Garavís, M., Escaja, N., Gabelica, V., Villasante, A. & González, C.着丝粒α -卫星DNA采用由AT hoogsteen碱基对覆盖的二聚i-motif结构。化学。欧元。J。21, 9816-9824(2015)。
莱恩,j.r., Contreras-García, J.,皮克马尔,j.p。,Miller, B. J. & Kjaergaard, H. G. Are bond critical points really critical for hydrogen bonding.j .化学。理论第一版。9, 3263-3266(2013)。
Mishra, S. K. & Suryaprakash, N.涉及有机氟的分子内氢键:由基于dft的理论计算证实的核磁共振调查。分子22, 423(2017)。
Narth, C.等人在分子化学中拓扑方法的应用(Remi Chauvin, Christine Lepetit, Bernard Silvi, & Esmail Alikhani) 491-527(施普林格国际出版,2016)。
拉普拉扎,R.等人。NCIPLOT和非共价相互作用的分析使用减少密度梯度。电线第一版。摩尔。科学。11, e1497(2021)。
贝文顿P. &罗宾逊,D. K.物理科学的数据缩减和误差分析。(麦格劳-希尔,2003)。
Anzahaee, M. Y., Watts, J. K.,真主安拉,N. R., Nicholson, A. W. & Damha, M. J.水中能量重要的C−H···F−C伪氢键:证据及其在高结合亲和力寡核苷酸合理设计中的应用。j。化学。Soc。133, 728-731(2011)。
Martin-Pintado, N.等。骨干FC•H⋅⋅⋅2 ' f取代核酸中的O氢键。Angew。化学。Int。艾德。52, 12065-12068(2013)。
Martín-Pintado, N.等。呋喃糖C2 '取代对结构和稳定性的显著影响:用单个氟原子指导人类端粒四重结构的折叠。j。化学。Soc。135, 5344-5347(2013)。
根据结构数据重新审视了DNA复制和氟氢键的立体假设。Acc。化学。Res。45, 1237-1246(2012)。
Bergstrom, D. E, Swartling, D. J., Wisar, A. & Hoffmann, M. R.通过MIND0/3技术评价胸苷、二脱氧胸苷和氟取代的脱氧核糖核苷几何结构氟取代对核苷几何结构和生物活性的影响。核苷核苷酸10, 693-697(1991)。
Dickerhoff, J. & Weisz, K.氟介导的g -四重结构折叠途径的编辑。ChemBioChem19, 927-930(2018)。
Trempe,肯尼迪。et al。具有2'F-ANA /RNA茎的寡核苷酸发夹的NMR溶液结构:RNase H对DNA/RNA杂化双工的特异性的影响。j。化学。Soc。123, 4896-4903(2001)。
杰尼索夫,A. Y.等。阿拉伯核酸(ANA)/RNA在嵌合发夹中的溶液结构:与2 ' -氟-ANA/RNA和DNA/RNA杂交的比较。核酸测定。29, 4284-4293(2001)。
Martín-Pintado, N.等。双螺旋阿拉伯核糖核酸(ANA和2'F-ANA)的溶液结构:阿拉伯核糖核酸在双发夹互转化中的作用。核酸测定。40, 9329-9339(2012)。
El-Khoury, R. & Damha, M. J. 2 ' -氟阿拉伯核酸(FANA):探测生物分子相互作用的多功能工具。Acc。化学。Res。54, 2287-2297(2021)。
瓦茨,J. K.等。2'F-ANA•RNA和ANA•RNA杂化双联体的差异稳定性:结构、假氢键、水化、离子摄取和灵活性的作用。核酸测定。38, 2498-2511(2010)。
Damha, m.j.等人。RNA和阿拉伯核酸的杂交产物(ANA和2'F-ANA)是核糖核酸酶H的底物。j。化学。Soc。120, 12976-12977(1998)。
Haase, L. & Weisz, K.通过改变氟的相互作用来切换糖修饰g -四聚体中的v -环类型。化学。Commun。56, 4539-4542(2020)。
奥莱利,D.等人。探讨非典型氟-氢键及其对核苷构象的影响。化学。欧元。J。24, 16432-16439(2018)。
Dalvit, C. Invernizzi, C. & Vulpetti, a .氟作为氢键受体:实验证据和计算计算。化学。欧元。J。20., 11058-11068(2014)。
杰弗里,G. A. &桑格,W.生物结构中的氢键。(斯普林格出版社,1994年版)。
Rozas, I., Alkorta, I. & Elguero, J.分叉氢键:三中心相互作用。期刊。化学。一个102, 9925-9932(1998)。
Ranallo, S., Porchetta, A. & Ricci, F.基于dna的传感应用支架。分析的化学。91, 44-59(2019)。
哈伦,S. G.等人。可编程DNA开关及其应用。纳米级10, 4607-4641(2018)。
koettting, m.c., Peters, j.t., Steichen, s.d. & Peppas, n.a.刺激反应水凝胶:理论,现代进展和应用。板牙。科学。Eng。:R: Rep.93, 1-49(2015)。
Morya, V., Walia, S., Mandal, b.b., Ghoroi, C. & Bhatia, D.功能性DNA基水凝胶:开发,性能和生物学应用。ACS Biomater。科学。Eng。6, 6021-6035(2020)。
罗鹏凯,梅特拉,K. L. & Sleiman, H. F.三维DNA纳米结构的自组装及其潜在的生物学应用。咕咕叫。当今。化学。医学杂志。14, 597-607(2010)。
Lee, W., Tonelli, M. & Markley, J. L. NMRFAM-SPARKY:生物分子核磁共振光谱的增强软件。生物信息学31, 1325-1327(2014)。
蔡,L.等。四膜虫端粒晶体结构中的插层胞嘧啶基序和新腺嘌呤簇。核酸测定。26, 4696-4705(1998)。
Güntert, P., Mumenthaler, C. & Wüthrich, K.用新程序Dyana11Edited进行核磁共振结构计算的扭转角动力学。J. Mol.生物学。273, 283-298(1997)。
AMBER(加州大学旧金山分校,2018)。
伊凡尼,我等人。Parmbsc1:用于DNA模拟的精细力场。Nat方法。13, 55-58(2016)。
乔根森,钱德拉塞卡,J.,马杜拉,J. D., Impey, R. W. & Klein, M. L.模拟液态水的简单势函数的比较。j .化学。理论物理。79, 926-935(1983)。
李文杰,李文杰,李文杰,李文杰,李文杰。分子动力学与外浴耦合研究。j .化学。理论物理。81, 3684-3690(1984)。
达顿,T.,约克,D. & Pedersen, L.粒子网格Ewald:一个N⋅大系统中Ewald和的log(N)方法。j .化学。理论物理。98, 10089-10092(1993)。
Koradi, R., Billeter, M. & Wüthrich, K. MOLMOL:显示和分析大分子结构的程序。J. Mol. Graph。14, 51-55(1996)。
陆,X.-J。& Olson, W. K. 3DNA:用于三维核酸结构分析、重建和可视化的多功能集成软件系统。Protoc Nat。3., 1213-1227(2008)。
Pymol分子图形系统v. 1.3版(Schrödinger, LLC)。
高斯16 Rev. C.01(沃灵福德,CT, 2016)。
Zhao, Y. & truhar, d.g.用于主要基团热化学、热化学动力学、非共价相互作用、激发态和过渡元素的M06密度泛函:两个新泛函和四个M06类泛函和其他12个泛函的系统测试。定理。化学。Acc。120, 215-241(2008)。
分子中的原子:量子理论。(克拉伦登出版社,1994)。
Boto, R. A.等。NCIPLOT4:非共价相互作用的快速、稳健和定量分析。j .化学。理论第一版。16, 4150-4158(2020)。
确认
我们感谢Javier López Prados博士,cicCartuja(塞维利亚,西班牙)生物分子相互作用平台核磁共振设施的经理,感谢他对获得高分辨率的贡献19F -和1氢谱数据。这项调查得到了西班牙“Ministerio de Ciencia e Innovación”[PID2020-116620GB-I00,给C.G., RTI2018-096704-B-100, PID2021-122478NB-I00给m.o]的研究资助,HPC H2020欧洲委员会卓越中心,“BioExcel-2计算生物分子研究卓越中心”[823830],加泰罗尼亚ERFD运行计划框架下的欧洲区域发展基金,加泰罗尼亚政府AGAUR [SGR2017-134],欧盟Marie Sklodowska Curie行动[799693,to M.G.],加拿大自然科学和工程研究委员会(发现补助金,to M.J.D.和A.K.M.),以及Fonds de Recherche du Québec-Nature等技术博士奖学金(de, to R.E.K)。巴塞罗那IRB是MINECO颁发的Severo Ochoa优秀奖的获得者。M.O.是ICREA学院的学者。
作者信息
作者及隶属关系
贡献
R.E.K.和M.G.设计了手稿的概念并撰写了手稿。R.E.K.制备了寡核苷酸样品,并用凝胶电泳、CD光谱和UV-vis光谱对其进行了表征。V.M.进行了计算计算,并参与了手稿的撰写和编辑。C.H.进行了热滞分析和动力学模拟,并对手稿的写作和编辑做出了贡献。T.M.监督热滞和动力学模拟分析,并有助于编辑手稿。M.O.监督了计算分析,并对手稿的编辑做出了贡献。C.G.监督了这个项目,并对编辑手稿做出了贡献。M.G.监督了该项目,并进行了核磁共振波谱和结构测定。M.J.D.监督了这个项目,并参与了手稿的编辑。
相应的作者
道德声明
相互竞争的利益
所有作者都声明没有竞争利益。
同行评审
同行评审信息
化学通讯感谢匿名审稿人对本工作的同行评议所作的贡献。同行评审报告是可用的。
额外的信息
出版商的注意施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议(Creative Commons Attribution 4.0 International License),允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可中,除非在材料的信用额度中另有说明。如果内容未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。要查看此许可证的副本,请访问http://creativecommons.org/licenses/by/4.0/.
关于本文
引用本文
El-Khoury, R., Macaluso, V., Hennecker, C.。et al。具有零核苷酸环的i-Motif折叠中间体被2 ' -氟阿拉伯胞苷通过F··H和O··H氢键捕获。Commun化学6, 31(2023)。https://doi.org/10.1038/s42004-023-00831-7
收到了:
接受:
发表:
DOI:https://doi.org/10.1038/s42004-023-00831-7